铁尾矿再选粗精矿深度还原含铁硅酸盐矿物的生成与还原
2015-10-12范敦城倪文李瑾李媛仇夏杰伏程红李德忠
范敦城,倪文,李瑾,李媛,仇夏杰,伏程红,李德忠
铁尾矿再选粗精矿深度还原含铁硅酸盐矿物的生成与还原
范敦城,倪文,李瑾,李媛,仇夏杰,伏程红,李德忠
(北京科技大学金属矿山高效开采与安全教育部重点实验室,北京,100083)
采用化学分析、XRD分析、SEM及EDS能谱分析方法,对齐大山铁尾矿再选粗精矿深度还原含铁硅酸盐矿物的生成与还原机理进行研究。研究结果表明:低温还原时,部分铁氧化物与脉石矿物发生固相反应,使含铁硅酸盐矿物中的铁(简称硅铁)占全铁的质量分数由未还原时的20.66%增加到720 ℃时的27.56%;当还原温度为770~930 ℃时,由于浮氏体大量生成和Na2CO3的加入,有大量低熔点富铁复杂硅酸盐矿物生成,使硅铁占全铁的质量分数由28.03%增加到53.18%;当升温到930 ℃时,大量钙铁辉石和少量铁橄榄石、钙铁橄榄石生成,由于CaO的碱性氧化物效应,铁橄榄石不能大量稳定存在而转化为还原性更好的钙铁辉石、钙铁橄榄石。在高温还原条件下,钙铁辉石及钙铁橄榄石中的铁离子进入复杂硅酸盐相中,并迁移到复杂硅酸盐相表面进行还原,还原得到的金属铁沿着复杂硅酸盐相表面聚集连晶,形成金属铁环边产物层;当升温到1 300 ℃时,硅铁占全铁的质量分数可降至9.13%。
铁尾矿;还原;钙铁辉石;硅酸盐相
深度还原是指将复杂难选含铁物料在低于其熔化温度下,用还原剂将含铁矿物还原成金属铁,并使金属铁长成为一定粒度铁颗粒的过程[1]。深度还原包括铁氧化物还原和铁颗粒长大2个过程[2],其中铁氧化物还原的越彻底越有利于铁金属化率的提高。由前人研究可知,铁氧化物的还原以Fe2O3→Fe3O4→FeO→ Fe方式逐级还原[3−5]。当复杂难选含铁物料脉石矿物含量较高时,铁氧化物由高价向低价还原过程中,低价铁氧化物易与SiO2和Al2O3等发生反应生成含铁硅酸盐矿物[6−9]。含铁硅酸盐矿物比铁氧化物更难还 原[10−11],其生成与还原会影响到还原铁产品质量。目前,对含铁硅酸盐矿物的生成与还原机理进行专门研究的文献比较少,因此,对其进行系统研究十分有必要。本文研究的原料为齐大山铁尾矿再磨再选得到的粗精矿。该粗精矿再进一步采用常规选矿方法进行选矿提纯已无法得到较高铁回收率且具有经济价值的铁精矿,因此,采用深度还原−磁选技术来提取金属铁微粉[12]。该粗精矿主要含铁矿物为赤铁矿、磁铁矿,脉石含量高且成分复杂。为实现粗精矿中含铁矿物的较好还原,添加CaO和Na2CO3进行试验研究,获得了比较理想的指标,但对其在深度还原过程中含铁硅酸盐矿物的生成与还原机理还不太清楚。因此,本文作者对粗精矿含铁硅酸盐矿物的生成与还原机理进行了较系统的研究,旨在揭示还原本质、改进工艺条件、调整试验方案,也为工业生产和技术的不断改进提供帮助。
1 材料与方法
1.1 试验原料
齐大山铁尾矿再磨再选粗精矿的主要化学成分见表1。由表1可以看出:粗精矿中TFe品位(质量分数,下同)为36.34%;SiO2为41.71%;Al2O3,CaO和MgO分别为1.82%,1.82%,1.69%,S和P品位较低。还原剂为粒度为小于1 mm的烟煤(固定碳质量分数为67.83%,挥发分质量分数为18.45%,灰分质量分数为12.02%,水分质量分数为1.48%,硫质量分数为0.028%),其主要化学成分见表2。
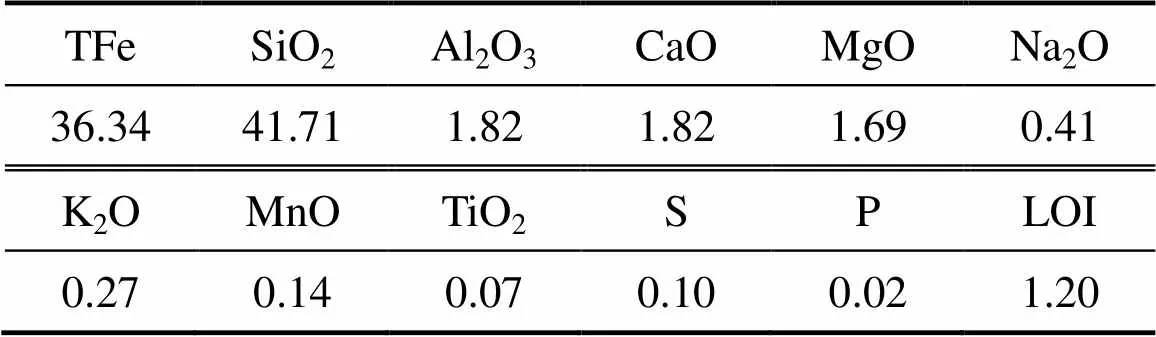
表1 再选粗精矿的主要化学成分(质量分数)
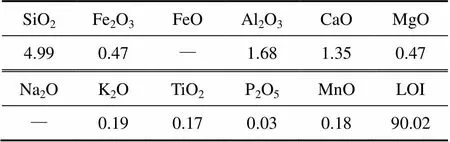
表2 烟煤的主要化学成分(质量分数)
1.2 试验方法
将再选粗精矿、烟煤、CaO和Na2CO3按质量比为100:17.5:15:6比例混合均匀,装入石墨坩埚中,并在物料表面铺适量烟煤。然后将装有物料的坩埚放入CD−1400X型马弗炉里以10 ℃/min随炉升温,达到设定温度点时将坩埚取出,自然冷却,还原后的物料称为还原产物。
1.3 测试方法
1) 化学分析。用化学分析研究不同温度条件下还原产物TFe,Fe3+,Fe2+,金属铁及含铁硅酸盐矿物中铁(硅铁)的质量分数变化。根据式(1)和(2)分别计算Fe3+的质量分数及铁的金属化率:
(Fe3+)=(Fe)−(金属铁)−(Fe2+) (1)
式中:(Fe3+)为Fe3+的质量分数,%;(Fe)为TFe质量分数,%;(金属铁)为金属铁质量分数,%;(Fe2+)为Fe2+质量分数,%;为铁的金属化率,%。
2) 硅铁含量测定。硅铁含量采用木炭磁化还原焙烧−磁选分离(磁场强度为(8.0~9.6)×104A/m)−钛(Ⅲ)还原重铬酸钾无汞滴定法测定[13−15]。主要步骤为:① 称取0.2 g试样(粒度小于0.038 mm)于30 mL瓷坩埚中,加0.5 g木炭粉混合均匀,并铺盖1.0 g炭粉,在550 ℃条件下磁化还原焙烧30 min;② 焙烧结束后,将瓷坩埚原封不动迅速移入干燥器中进行冷却至室温后,将试料转入250 mL烧杯用(8.0~9.6)×104A/m永磁铁进行磁选分离;③ 磁性部分移入250 mL锥形瓶并加适量盐酸,加热溶解至无磁性为止,过滤后所得液体用钛(Ⅲ)还原−重铬酸钾无汞滴定法测定其中的铁,全铁减去磁性部分铁质量分数即为硅铁质量分数。
3) XRD分析。用XRD分析研究不同温度条件下还原产物的物相变化,其分析采用日本理学Rigaku−RA 高功率旋转阳极X线衍射仪(12 kW),Cu靶,步长为0.02°,扫描范围为10°~90°,扫描速度为5°/min,电压为40 kV,电流为150 mA。
4) SEM及EDS能谱分析。用SEM及EDS能谱分析研究不同温度条件下矿物微观结构和成分变化,其分析采用德国卡尔蔡司EVO18 扫描电子显微镜及Bruke XFlash Detector 5010 能谱分析仪。
2 结果与讨论
2.1 化学分析
不同温度条件下还原产物各铁相占全铁的质量分数如图1所示。由图1可知:随着还原温度的升高,硅铁占全铁的质量分数与Fe2+占全铁的质量分数增加的趋势一致,表明在高价铁氧化物向低价铁氧化物还原的同时,部分铁氧化物与脉石矿物反应生成了含铁硅酸盐矿物;当还原温度小于770 ℃时,硅铁占全铁的质量分数增加较缓;当还原温度为770~930 ℃时,硅铁占全铁的质量分数快速增加,而Fe3+及Fe2+占全铁的质量分数分别快速下降和快速增加。分析原因是铁氧化物在小于770 ℃时主要发生Fe2O3转变为Fe3O4的反应,在大于770 ℃时主要发生Fe3O4转变为FeO的反应。Fe2O3及Fe3O4与脉石矿物反应速率慢,而FeO(浮氏体)与脉石矿物反应速率快,加之升温可加快反应速率,导致硅铁占全铁的质量分数在大于770 ℃时快速上升。当还原温度大于930 ℃时,硅铁占全铁的质量分数开始迅速下降,表明有大量硅铁还原出来。当升温到1 200 ℃时,Fe2+占全铁的质量分数为18.80%,硅铁占全铁的质量分数为17.32%,Fe3+占全铁的质量分数仅为1.25%,表明Fe2O3→Fe3O4→FeO→ Fe反应过程基本完成,继续升温及后续的保温阶段主要为硅铁的还原。当升温到1 300 ℃时,硅铁占全铁的质量分数仅为9.13%。

1—金属铁;2—含铁硅酸盐矿物中的铁;3—Fe2+;4—Fe3+
2.2 XRD分析
还原产物在不同还原温度条件下的XRD谱如图2所示。由图2可知:未还原时,还原物料主要矿物是赤铁矿、磁铁矿、石英、角闪石、绿泥石及石灰;当升温至570 ℃时,还原产物中角闪石的峰减弱、绿泥石的峰基本消失,出现了新物相堇青石的峰。杨雅 秀[16]研究得出:富铁绿泥石在550 ℃时脱羟基发生晶形转变,因此,绿泥石可能转变成了堇青石。当升温至720 ℃时,赤铁矿的峰显著减弱,石灰的峰有所减弱,而磁铁矿的峰增变化不明显。结合图1可以看出:硅铁占全铁的质量分数由未还原时的20.66%增加到720 ℃时的27.56%,说明赤铁矿或磁铁矿与石灰等脉石矿物发生了固相反应。据文献[17]报道:Fe2O3,CaO和SiO2等氧化物在400 ℃以上很容易发生固相反应(表3)。另外,再选粗精矿粒度细(小于0.074 mm颗粒质量分数>95%,小于0.038 mm颗粒质量分数>50%),与粉末状助剂均匀混合后,颗粒之间接触充分,有利于固相反应的进行。
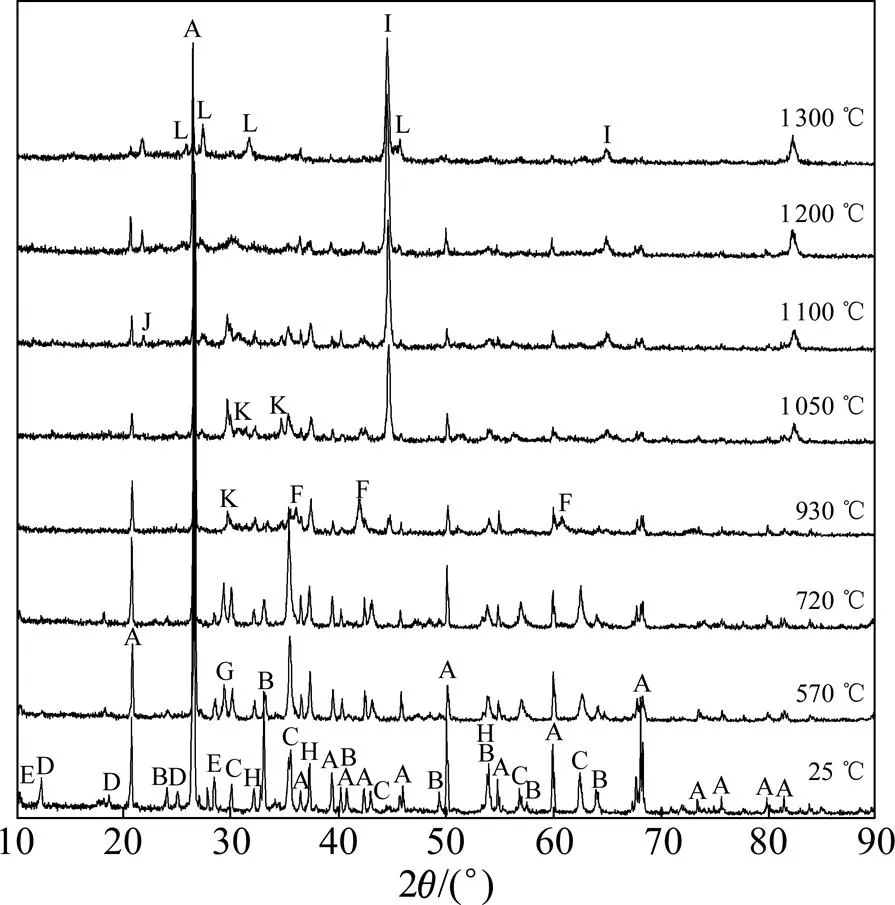
A—石英;B—赤铁矿;C—磁铁矿;D—绿泥石{(Mg,Al,Fe)6(Si,Al)4O10(OH)8};E—角闪石{Na3Mg2Fe2LiSi8O22(OH)2};F—浮氏体(FeO);G—堇青石{(Mg,Fe)2Al4Si5O18};H—石灰;I—金属铁;J—方石英;K—钙铁辉石{Ca(Fe,Mg)(SiO3)2};L—硅灰石(CaSiO3)

表3 固相反应产物开始出现的温度
当升温到930 ℃时,磁铁矿、石灰的峰明显减弱,出现了钙铁辉石、浮氏体和金属铁的峰;角闪石和堇青石的峰完全消失,可能是由于升温过程中生成其他复杂的化合物或者玻璃态物质,用XRD方法检测不出来。从720 ℃升到930 ℃,磁铁矿大量还原为浮氏体,其中部分浮氏体还原为金属铁,部分与SiO2和CaO反应生成钙铁辉石。另外,由于物料中添加Na2CO3后,Na2CO3可与SiO2发生反应形成一系列低熔点化合物如Na2SiO3- SiO2等[18]。此化合物和浮氏体等矿物反应,生成化学成分主要以CaO,NaO,FeO和SiO2为主的低熔点复杂含铁硅酸盐矿物,可消耗部分浮氏体。从930 ℃升到1 050 ℃时,浮氏体的峰显著减弱,钙铁辉石、金属铁的峰增强;从1 050 ℃升到1 300 ℃时,钙铁辉石的峰逐渐减弱,金属铁和硅灰石的峰逐渐增强,表明有大量钙铁辉石被还原,还原产物为硅灰石和金属铁。
2.3 SEM及EDS能谱分析
2.3.1 主要含铁硅酸盐矿物的生成
930 ℃时还原产物的SEM像及EDS能谱分析如图3所示。图3中白色区域为低价铁氧化物,灰白色区域靠近铁氧化物表面为铁橄榄石(点),灰白色区域在其他区域的为钙铁橄榄石(点),浅灰色区域为钙铁辉石(点),灰色区域为复杂硅酸盐相(点),深黑色区域为还原时留下的气孔。由图3可知:钙铁辉石在复杂硅酸盐相中大量结晶,形貌多为板状、棒状,晶粒粗大,粒度为10 μm左右;铁橄榄石在铁氧化物与复杂硅酸盐相界面处结晶,形貌多为粒状、菱形状,晶粒较小,粒度小于5 μm。铁橄榄石多在铁氧化物表面结晶且粒度普遍较小,而难以在复杂硅酸盐相中结晶,与其生成的环境有关。铁橄榄石在铁氧化物表面结晶长大过程中,会受到复杂硅酸盐相的熔蚀作用。Ca2+,Mg2+和Na+易进入铁橄榄石晶格中破坏Fe2+的连接(铁橄榄石为岛状硅酸盐矿物,硅氧四面体阴离子通过Fe2+连接),使其岛状结构解体。铁橄榄石在重结晶过程中与Ca2+及复杂硅氧四面体阴离子团作用转变成钙铁辉石并进一步结晶长大,由岛状硅酸盐矿物转变成链状硅酸盐矿物,晶体形态也从三向等长转变成一向延伸。另外,还原产物中几乎不存在纯的铁橄榄石,原因是其中的Fe2+位置可被Ca2+部分取代、Fe2+与Mg2+形成完全类质同相,形成含钙镁的铁橄榄石或钙铁橄榄石,且离铁氧化物表面越远的区域橄榄石中Ca和Mg元素含量越高。可见:铁橄榄石可沿着铁氧化物表面大量结晶但不能稳定存在,在CaO的碱性氧化物效应作用下转化为钙铁辉石和少量钙铁橄榄石。根据结晶化学原理[19],钙铁辉石、钙铁橄榄石比铁橄榄石的还原性好,形成更多的钙铁辉石、钙铁橄榄石对其还原有利,所以,加入CaO改善了硅铁的还原 条件。
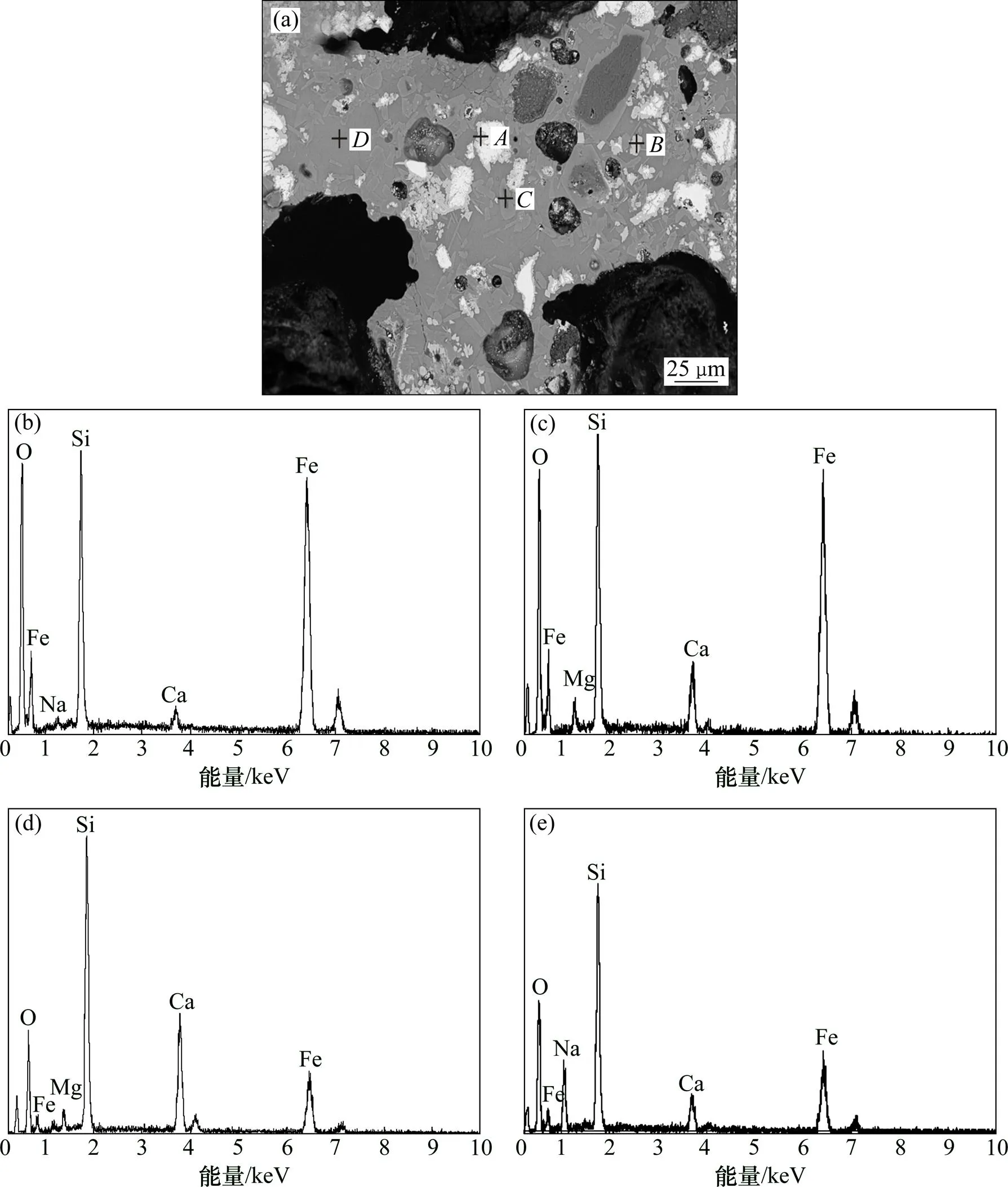
(a) SEM像;(b) A点;(c) B点;(d) C点;(e) D点
当升温到930 ℃时,还原生成大量低熔点复杂硅酸盐矿物,其具有较强的迁移能力,能够包裹和熔蚀石灰、石英、铁氧化物等矿物,使液相区域不断扩大。该矿物成分质量分数不定,没有明显的晶形,是一种富含铁的复杂硅酸盐相,其铁质量分数在20%~30%之间(图3(d))。这种富含铁的复杂硅酸盐液相的不断扩大促进了钙铁辉石等矿物的生成,使硅铁占全铁的质量分数由770 ℃时的28.03%增加到930 ℃时的53.18%(图1)。
2.3.2 主要含铁硅酸盐矿物的还原
由图1和图2可知:当还原温度为930~1050 ℃时,还原产物中既有大量硅铁还原为金属铁,也有大量钙铁辉石生成。钙铁辉石主要在复杂硅酸盐相中生成,其先还原可能性较小。复杂硅酸盐相表面还原气氛较强,CO可以顺利在其界面吸附、活化与脱附,因此,复杂硅酸盐相中的铁可在其表面还原为金属铁。
图4所示为1050~1300 ℃时还原产物的SEM像及EDS谱。由图4(a)~4(d)可知:钙铁辉石(~点)的形状由柱状、板状转变为羽毛状、麦穗状最后为纤维状、竹叶状。这种纤维状、竹叶状的物质钙硅质量比接近1:1,由XRD分析可知该物质为硅灰石;~点对应的EDS能谱显示钙铁辉石中的铁含量逐渐降低而钙含量逐渐增加,这表明钙铁辉石中的铁离子是逐渐迁移到复杂硅酸盐相中的。当钙铁辉石在复杂硅酸盐相中生成后,因复杂硅酸盐相较为密实而影响到还原气体在其内部的扩散,钙铁辉石在自身表面还原出金属铁较为困难。
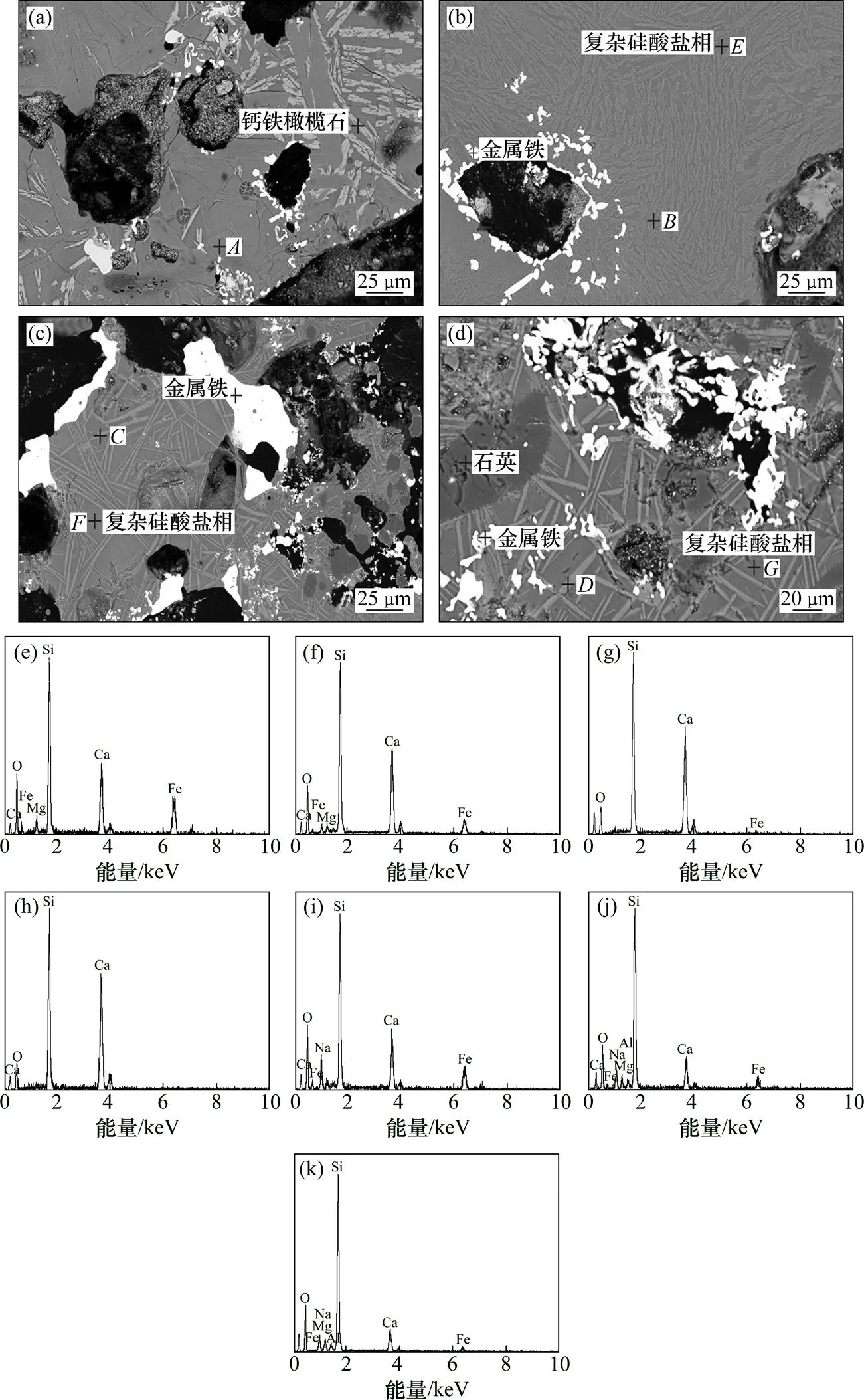
(a) 1 050 ℃;(b) 1 150 ℃;(c) 1 250 ℃;(d) 1 300 ℃;(e) A点;(f) B点;(g) C点;(h) D点;(i) E点;(j) F点;(k) G点
但是,在高温还原条件下,钙铁辉石可以通过间接方式进行还原,其间接还原过程:铁离子从钙铁辉石晶格中游离出来进入复杂硅酸盐相中,然后迁移到复杂硅酸盐相表面还原为金属铁;而钙铁辉石的晶体形貌和化学成分逐渐发生变化,最后转化为硅灰石。物料中配加CaO和Na2CO3后,Na2CO3在还原过程中首先离解出Na2O,Na2O主要存在于复杂硅酸盐相中,CaO主要存在于复杂硅酸盐相和钙铁辉石中。根据强碱性氧化物可置换复杂化合物中弱碱性氧化物的规律,Na2O可从FeO·CaO·2SiO2中取代出FeO,反应为
FeO·CaO·2SiO2+Na2O=CaO·SiO2+Na2O·SiO2+FeO
FeO从钙铁辉石中游离出来,成为自由状态FeO,进入复杂硅酸盐中后活性极高。Na2O·SiO2熔点低,可熔回复杂硅酸盐相中,而Na2O游离出来继续和其他钙铁辉石反应。
当还原温度大于1 150 ℃时,钙铁辉石(熔点1 150 ℃)开始熔入复杂硅酸盐液相中。随着钙铁辉石的还原和熔化,硅铁的还原实际主要是从更复杂的硅酸盐相中还原铁的过程。由图4(i)~4(k)可知:从1 150 ℃升到1 300 ℃时,复杂硅酸盐中铁含量逐渐减小。金属铁在复杂硅酸盐相表面、裂缝及由铁氧化物还原得到的铁晶粒表面聚集长大,而复杂硅酸盐相内结晶出大量硅灰石。
在高温还原条件下,复杂硅酸盐相中的组分Na2O和CaO电离得O2−,一方面,使复杂硅酸盐相中O2−浓度增大(O2−活度增大),由方程(Fe2+)+(O2−)+CO=CO2+[Fe]及其可知:提高了Fe2+还原反应活度[20]。另一方面,O2-可使复杂硅酸盐相中复杂的硅酸盐阴离子离解成简单的硅酸盐阴离子,使复杂硅酸盐相液相增多、质点迁移速度加快。这样,复杂硅酸盐相中的离子迁移阻力减少,Fe2+和O2−可克服长程迁移活化能由内部向界面迁移发生氧化还原反应,而Ca2+和Si4+等离子向相反方向迁 移[21−22],逐渐形成硅灰石、少含或不含铁的复杂硅酸盐矿物。
进入保温过程后,剩余硅铁的还原继续进行,而已还原出来的金属铁在铁相与硅酸盐矿物界面上进一步脱氧与除硅等杂质,并进行着小颗粒铁向大颗粒铁扩散、连晶、长大。
通过XRD分析、SEM及EDS能谱分析表明,这几种主要含铁硅酸盐矿物的还原互相关联,其还原过程大致可分为4步。
1) 铁橄榄石在铁氧化物表面结晶析出,在CaO碱性效应下转化为钙铁辉石及少量钙铁橄榄石。
SiO2+2FeO=2FeO·SiO2(3)
2FeO·SiO2+2CaO+4SiO2=2(FeO·CaO·2SiO2)(钙铁辉石) (4)
2FeO·SiO2+2CaO+SiO2=2(FeO·CaO·SiO2)(钙铁橄榄石) (5)
2) 在高温还原条件下,复杂硅酸盐相逐渐熔蚀钙铁辉石晶体表面,使铁离子从钙铁辉石晶体中游离出来进入复杂硅酸盐相中。同时,钙铁辉石的晶体形貌和成分也逐渐变化,最终钙铁辉石转化为硅灰石。
2(FeO·CaO·2SiO2)=2CaO·SiO2+2FeO+3SiO2(6)
2CaO·SiO2+SiO2=2(CaO·SiO2) (7)
FeO·CaO·SiO2=CaO·SiO2+FeO (8)
3) 复杂硅酸盐相中的铁离子通过长程或短程迁移到达复杂硅酸盐相表面进行直接还原和间接还原,还原引起复杂硅酸盐相中的铁离子浓度逐渐降低并产生浓度梯度。在浓度梯度的作用下,铁离子从复杂硅酸盐相内部向反应界面迁移。
FeO+C=Fe+CO (9)
FeO+CO=Fe+CO2(10)
4) 还原出来的金属铁沿着复杂硅酸盐表面聚集连晶,形成金属铁环边产物层。一部分碳通过金属铁环边产物层向内扩散,形成含碳的金属铁。在金属铁和复杂硅酸盐相接触界面上,被金属铁层覆盖的复杂硅酸盐相继续还原。
FeO+[C]金=Fe+CO (11)
3 结论
1) 在低温还原条件下,部分铁氧化物与脉石矿物发生固相反应,生成了早期的含铁硅酸盐矿物,使硅铁占全铁的质量分数由未还原时的20.66%增加到720 ℃时的27.56%。当还原温度升到770~930 ℃时,由于大量浮氏体生成和Na2CO3的加入,含铁硅酸盐矿物开始熔入到液相中形成低熔点富铁复杂硅酸盐矿物,使液相区域不断扩大,硅铁占全铁的质量分数由770 ℃时的28.03%增加到930 ℃时的53.18%。
2) 当还原温度升到930~1 050 ℃时,有大量钙铁辉石和少量铁橄榄石、钙铁橄榄石生成。由于CaO的碱性氧化物效应,铁橄榄石不能大量存在而转化为还原性更好的钙铁辉石及钙铁橄榄石。当还原温度大于930 ℃时,硅铁开始大量还原为金属铁,使硅铁占全铁的质量分数降低到1 300 ℃时的9.13%。
3) 主要含铁硅酸盐矿物的还原过程大致可分为4个阶段:①铁橄榄石转化为钙铁辉石及少量钙铁橄榄石;②钙铁辉石及少量钙铁橄榄石中的铁离子进入复杂硅酸盐相中;③铁离子迁移到复杂硅酸盐相表面或金属铁产物层进行还原;④金属铁沿着复杂硅酸盐表面聚集连晶,形成金属铁环边产物层。
[1] 韩跃新, 李艳军, 刘杰, 等. 难选铁矿石深度还原: 高效分选技术[J]. 金属矿山, 2011(11): 1−4. HAN Yuexin, LI Yanjun, LIU Jie, et al. Deep reduction-efficient separation technology applied to refractory iron ore[J]. Metal Mine, 2011 (11): 1−4.
[2] 韩跃新, 张成文, 孙永升, 等. Na2CO3促进复杂难选铁矿石深度还原的机理分析[J]. 东北大学学报(自然科学版), 2012, 33(11): 1633−1636. HAN Yuexin, ZHANG Chengwen, SUN Yongsheng, et al. Mechanism analysis on deep reduction of complex refractory iron ore promoted by Na2CO3[J]. Journal of Northeastern University (Science and Technology), 2012, 33(11): 1633−1636.
[3] LIU Guisu, Strezov V, Lucas J A, et al. Thermal investigations of direct iron ore reduction with coal[J]. Thermochemica Acta, 2004, 410(1/2): 133−140.
[4] SUN Yongsheng, GAO Peng, HAN Yuexin, et al. Reaction behavior of iron minerals and metallic iron particles growth in coal-based reduction of an oolitic Iron ore[J]. Industrial and Engineering Chemistry Research, 2013, 52(6): 2323−2329.
[5] Jozwiak W K, Kaczmarek E, Maniecki T P, et al. Reduction behavior of iron oxides in hydrogen and carbon monoxide atmospheres[J]. Applied Catalysis A: General, 2007, 326(1): 17−27.
[6] 魏玉霞, 孙体昌, 寇珏, 等. 内配煤用量对某难选铁矿石压块直接还原焙烧的影响[J]. 中南大学学报(自然科学版), 2013, 44(4): 1305−1311. WEI Yuxia, SUN Tichang, KOU Jue, et al. Effect of coal dosage on direct reduction roasting of refractory iron ore briquettes[J]. Journal of Central South University (Science and Technology), 2013, 44(4): 1305−1311.
[7] LI Yongli, SUN Tichang, KOU Jue, et al. Study on phosphorus removal of high-phosphorus oolitic hematite by coal-based direct reduction and magnetic separation[J]. Mineral Processing and Extractive Metallurgy Review, 2014, 35(1): 66−73.
[8] 梅贤功, 孙宗毅, 陈苕. 高铁赤泥煤基直接还原过程中固相反应的热力学分析[J]. 轻金属, 1994(7): 8−12. MEI Xiangong, SUN Zongyi, CHEN Tiao. Thermodynamic analysis of sloid-state reaction during the process of coal-based direct reduction on iron-rich red mud[J]. Light Metals, 1994(7): 8−12.
[9] 梅贤功, 袁明亮, 陈苕.难选贫铁矿煤基直接还原过程中固相反应特征[J].中国有色金属学报, 1995, 5(2): 42−46.MEI Xiangong, YUAN Mingliang, CHEN Tiao. Characteristics of solid-state reaction during the process of coal-based direct reduction on refractory iron ore[J]. The Chinese Journal of Nonferrous Metals, 1995, 5(2): 42−46.
[10] 刘牡丹. 基于还原法的高铝铁矿铁铝分离基础及新工艺研究[D]. 长沙: 中南大学资源加工与生物工程学院, 2010: 34−46. LIU Mudan. Studies on the foundamental and novel technology of Al-Fe separation of high-aluminium content iron ores based on the reduction method[D]. Changsha: Central South University. School of Minerals Processing and Bioengineering, 2010: 34−46.
[11] 贾岩. 拜耳法赤泥深度还原提铁及尾渣综合利用研究[D]. 北京: 北京科技大学土木与环境工程学院, 2011: 82−89. JIA Yan. The Comprehensive utilization of bayer red mud[D]. Beijing: University of Science and Technology Beijing. School of Civil and Environmental Engineering, 2011: 82−89.
[12] 倪文, 伏程红, 范敦城, 等. 一种铁矿尾矿强磁预富集深度还原提铁方法: 中国, 201210362689.3[P]. 2012−12−26. NI Wen, FU Chenghong, FAN Duncheng, et al. A method of extracting iron ore tailings by deep reduction after using strong magnetism to pre-concentrate the tailings: China, 201210362689.3[P]. 2012−12−26.
[13] 芮李竹. 一般铁矿石的物相分析[J]. 福建分析测试, 2010, 19(1): 64−67. RUI Lizhu. General phase analysis of iron ores[J]. Fujian Analysis and Testing, 2010, 19(1): 64−67.
[14] 黄宝贵. 铁矿石化学物相分析中硅酸铁的分离测定方法述评[J]. 岩矿测试, 2010, 29(2): 169−174. HUANG Baogui. Review on a seperation and testing method of iron silicate in iron ore chemical phase analysis[J]. Rock Ore Testing, 2010, 29(2): 169−174.
[15] 蒋月瑾. 炭粉磁化焙烧法测定铁矿石中硅酸铁[J]. 冶金分析, 1982 (2): 14−16. JIANG Yuejin. Testing method of iron silicate in iron ore by charcoal powder magnetization roasting method[J]. Metallurgical Analysis, 1982 (2): 14−16.
[16] 杨雅秀. 绿泥石族矿物热学性质的研究[J]. 矿物学报, 1992, 12(1): 36−44.YANG Yaxiu. A study on the thermal behavior of chlorite-group mingrals[J]. Acta Minalogica Sinica, 1992, 12(1): 36−44.
[17] 梁中渝. 炼铁学[M]. 1版. 北京: 冶金工业出版社, 2009: 59. LIANG Zhongyu. Ironmaking process[M]. 1st ed. Beijing: Metallurgical Industry Press, 2009: 59.
[18] 黄柱成, 蔡凌波, 张元波, 等. Na2CO3和CaF2强化赤泥铁氧化物还原研究[J]. 中南大学学报(自然科学版), 2010, 41(3): 838−844. HUANG Zhucheng, CAI Lingbo, ZHANG Yuanbo, et al. Reduction of iron oxides of red mud reinforced by Na2CO3and CaF2[J]. Journal of Central South University (Science and Technology), 2010, 41(3): 838−844.
[19] 陈耀铭, 陈跃. 烧结球团矿微观结构[M]. 1版. 长沙: 中南大学出版社, 2011: 85.CHEN Yingming, CHEN Yue. Microstructure of sintered pellets[M]. 1st ed. Changsha: Central South University Press, 2011: 85.
[20] 李磊, 胡建杭, 王华. 铜渣熔融还原炼铁过程反应热力学分析[J]. 材料导报B, 2011, 25(7): 114−117. LI Lei, HU Jianhang, WANG Hua. Thermodynamic analysis of iron smelting reduction from copper residue[J]. Materials Review B, 2011, 25(7): 114−117.
[21] 毛裕文. 冶金熔体[M]. 1版. 北京: 冶金工业出版社, 1993: 93. MAO Yuwen. Metallurgical melt[M]. 1st ed. Beijing: Metallurgical Industry Press, 1993: 93.
[22] Weissberger S, Zimmels Y, Lin I J. Mechanism of growth of met allic phase in direct reduction of iron bearing oolites[J]. Metall Mater Trans B, 1986, 17(3): 433−441.
(编辑 陈爱华)
Generation and reduction mechanism of silicate minerals containing iron in deep reduction of rough concentrate from iron tailings
FAN Duncheng, NI Wen, LI Jin, LI Yuan, QIU Xiajie, FU Chenghong, LI Dezhong
(Key Laboratory of the Ministry of Education of China for High-Efficient Mining and Safety of Metal Mines,University of Science and Technology Beijing, Beijing 100083, China)
Test methods including chemical analysis,X-ray diffraction, scanning electron microscope and X-ray energy spectrum analysis were used to study generation and reduction mechanism of silicate minerals containing iron in deep reduction of rough concentrate from Qidashan iron tailings. The results show that when the reduction temperature is lower than 720 ℃, some iron oxides react with gangue minerals in solid state which increases the iron mass fraction of silicate minerals containing iron from 20.66% to 27.56%. When the reduction temperature is between 770 ℃and 930 ℃, numerous complicated silicate minerals containing rich iron are generated due to the occurrence of a large number of wustite and the addition of Na2CO3which makes the iron content of silicate minerals containing iron increases from 28.03% to 53.18%. When reduction temperature is 930 ℃, a lot of hedenbergite and a small amount of fayalite and kirschsteinite are crystallized. Because of the effect of basic oxide (CaO), fayalite can not exist stably in large quantity and transform into hedenbergite and kirschsteinite with better reducibility. Under conditions of high temperature reduction, iron ions in hedenbergite and kirschsteinite get into complicated silicate phase and move to the surface where the reduction reaction occurs. Metallic iron gathers and forms crystal stock on the surface forming iron rim. When the reduction temperature is 1 300 ℃, the iron content of silicate minerals containing iron decreases to 9.13%.
iron tailings; reduction; hedenbergite; silicate phases
10.11817/j.issn.1672-7207.2015.06.001
TD951
A
1672−7207(2015)06−1973−08
2014−06−13;
2014−08−20
国家高技术研究发展计划(863计划)项目(2012AA062401)(Project (2012AA062401) supported by the National High Technology Research and Development Program (863 Program) of China)
倪文,教授,博士生导师,从事直接还原、矿物材料、保温耐火材料及固体废弃物资源化研究;E-mail:niwen@ces.ustb.edu.cn
