对铜与浓硫酸反应溶液呈绿色的实验探究
2015-10-08夏立先
夏立先
摘要:通过查阅资料、分析思考及实验探究,排除了多种可能,最后找到了铜与浓硫酸反应溶液呈绿色的原因,即铜表面含有氯元素。这个实验结果超出许多人的预料,它告诉我们不可忽视实验原料(试剂)的纯度对反应的影响。
关键词:铜;浓硫酸;绿色实验;实验探究
文章编号:1005–6629(2015)7–0064–02 中图分类号:G633.8 文献标识码:B
铜与浓硫酸反应实验,理论上溶液呈蓝色(反应后的混合液倒入水中溶液也呈蓝色),但实际上往往看到溶液呈绿色(反应后的混合液倒入水中溶液也呈绿色)。对这一异常现象至今未有合理解释。笔者对此进行了研究,下面将笔者的研究历程及结果介绍如下。
1 根据查阅的资料[1]得知:铜与浓硫酸在加热条件下发生多个反应,如生成硫酸铜、硫化铜、硫化亚铜、硫酸亚铜、硫等
1.1 溶液呈绿色会不会与硫有关
因为硫是黄色的、水合铜离子是蓝色的,胶体硫与水合铜离子形成的混合溶液呈绿色。这种解释从理论上看是合理的,但需要实验进一步确认。为此,笔者设计了如下实验:通过酒精溶解硫,取上层清液逐滴加入到硫酸铜溶液中并不断搅拌,发现溶液变浑浊,但溶液依旧是蓝色。该实验说明,溶液呈绿色并不是由硫和水合铜离子引起的。
1.2 溶液呈绿色会不会与黑色的胶体状的硫化铜、硫化亚铜有关
为此,设计了如下实验:通过蔗糖被浓硫酸炭化制得细碎的炭(由黑色的炭代替硫化铜、硫化亚铜进行实验),取少量细碎的炭加入到硫酸铜溶液中并不断搅拌,发现溶液变浑浊,但溶液是蓝黑色的,过滤后溶液依旧是蓝色。该实验说明,溶液呈绿色并不是由硫化铜、硫化亚铜和水合铜离子引起的。
2 根据查阅的资料[2]得知:亚硫酸亚铜可与水生成的Cu2SO3·0.5H2O呈黄色,Cu2+与水结合生成的水合铜离子呈蓝色,黄色与蓝色混合后,溶液呈绿色
这种解释似乎可以。仔细想想,又觉得不对:一则没有资料证明铜与浓硫酸在加热条件下发生反应生成亚硫酸亚铜,二则亚硫酸亚铜在硫酸过量且加热的条件下不可能存在。这种解释又被否定了。
3 试问:反应后的混合液中会不会有Fe3+(铜不纯,含有铁)?如果有的话,Fe3+呈黄色,与水合铜离子混合溶液呈绿色
为此,笔者进行了如下实验。
实验1 检验反应后的混合液中是否含有Fe3+。
取反应后的混合液2~3mL加入试管中,向其中加入3~5滴硫氰化钾溶液,溶液未变红色,说明溶液中没有Fe3+。
4 试问:反应后的混合液中会不会有Fe2+(铜不纯,含有铁)?如果有的话,Fe2+呈绿色,与水合铜离子混合溶液呈蓝绿色
笔者又进行了如下实验。
实验2 检验反应后的混合液中是否含有Fe2+。
取反应后的混合液2~3mL加入试管中,向其中加入3~5滴硫氰化钾溶液,溶液未变红色,再滴入1~2滴3%的H2O2,溶液仍未变红色,说明溶液中没有Fe2+。
5 试问:反应后的混合液中会不会有氯离子?如果有的话可形成CuCl42-(黄色),与水合铜离子混合溶液呈绿色
笔者再次进行了如下实验。
实验3 检验铜丝表面是否含有氯元素。
取一段表面光洁的粗铜丝,用镊子夹住,放在酒精灯火焰上灼烧,发现火焰呈绿色,初步证明铜丝表面含有氯元素[3]。
为什么表面看上去比较光洁的铜丝、铜片上会有氯元素呢?是不是表面沾附了含氯物质呢?为此,又进行了实验:
取一段表面光洁的粗铜丝,用蒸馏水反复冲洗后用滤纸吸干,用镊子夹住,放在酒精灯火焰上灼烧,发现火焰仍呈绿色,初步证明铜丝表面含有氯元素。
为什么用蒸馏水冲洗过的铜丝表面还会有氯元素呢?经百度搜索得知:为防止铜在空气中被腐蚀或增强铜的电绝缘性,厂家常在铜表面加一层聚氯乙烯的覆膜,这层覆膜肉眼是不易发现的,并且聚氯乙烯在加热条件下易分解,放出氯化氢气体。
实验4 做对比实验。
实验装置如图1所示。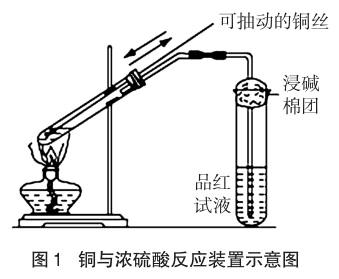
取一段螺旋状的粗铜丝放入较大试管中,然后加入浓硫酸5~8mL,将试管固定在铁架台上,用酒精灯加热,可观察到溶液慢慢变绿色、黑绿色。移开酒精灯,待溶液冷却后倒入5~8mL蒸馏水中,过滤,看到溶液呈绿色。
另取一段螺旋状的粗铜丝,用镊子夹住,在酒精灯上灼烧至火焰没有绿色,放入较大试管中,然后加入浓硫酸5~8mL,将试管固定在铁架台上,用酒精灯加热,可观察到溶液慢慢变蓝色、蓝黑色。移开酒精灯,待溶液冷却后倒入5~8mL蒸馏水,过滤,看到溶液呈蓝色。
通过以上对比实验可知,铜与浓硫酸反应溶液呈绿色,是由于铜表面沾附氯元素(聚氯乙烯)引起的。
除此之外,如果铜表面沾附无机含氯化合物;或者试管不干净,沾附无机含氯化合物;或者稀释硫酸铜时用自来水(含氯离子);或者用手(汗水)拿铜丝都有可能导致溶液呈绿色。
为保证实验成功(硫酸铜溶液呈蓝色),需做到:①对所用铜丝灼烧至火焰没有绿色后用。②试管要干净,多次用蒸馏水洗涤。③稀释硫酸铜时要用蒸馏水,不能用自来水(含氯离子)。④不要用手直接拿铜丝。
本次探究给我们的启示是:对于块状或丝状固体不能只凭外观干净就直接使用,使用前一定要打磨干净,能水洗的固体还要用蒸馏水把固体表面洗涤干净,然后才能使用。
参考文献:
[1]刘怀乐著.中学化学教学思维(第1版)[M].重庆:重庆出版社,2009:243~248.
[2]宋天佑等编.无机化学下册(第1版)[M].北京:高等教育出版社,2004:625.
[3]王祖浩主编.普通高中课程标准实验教科书·有机化学基础(第3版)[M].南京:江苏教育出版社,2010:7.
