主动脉夹层主动脉弓替换术后肾功能损伤分析
2015-09-15伍育旗李玉斌王清丽余旻张立伟杨晓玲俞彬
伍育旗 李玉斌 王清丽 余旻 张立伟 杨晓玲 俞彬
主动脉夹层主动脉弓替换术后肾功能损伤分析
伍育旗 李玉斌 王清丽 余旻 张立伟 杨晓玲 俞彬
目的 分析体外循环下主动脉弓替换术患者肾功能损害的原因及治疗方法。方法 回顾性分析2008年1月至2014年7月宜昌市第一人民医院22例体外循环下主动脉弓替换术的临床资料,其中男性17例、女性5例,年龄(49.53±9.64)岁。结果 术后血肌酐与术前相比有所增高,总体平均值之间的差别具有统计学意义[(174.00±111.61)μmol/L 比(87.90±43.44)μmol/L,t=4.137,P=0.000],提示手术加重肾功能损害。体外循环时间≥180 min与体外循环术时间<180 min相比,肾功能损害的差异有统计学意义(χ2=3.884,P=0.035),提示术中长时间体外循环加重肾功能损害。术后肾功能损害与术后无肾功能损害患者相比较,术前肾功能损害是术后肾功能损害的危险因素(χ2=7.246,P=0.011)。血液净化后血肌酐与血液净化前血肌酐相比有所降低,总体平均值间差别具有统计学意义[(84.00±113.62)μmol/L 比(174.00±111.00)μmol/L,t=6.335,P=0.000]。结论 主动脉夹层主动脉弓替换术后肾功能损伤与体外循环时间过长及术前肾功能损害有关。肾功能损伤患者在重症监护室进行血液净化治疗,疗效满意。
重症监护室; 深低温循环; 主动脉弓替换术; 肾功能损伤
体外循环下主动脉弓替换术是外科治疗主动脉夹层最有效的方法之一。2008年1月至2014年7月湖北宜昌市第一人民医院对22例主动脉夹层患者行体外循环下主动脉弓替换术,其中部分患者出现肾功能损害,经治疗,效果良好。现对其术后肾损害的相关因素及并发症进行分析,以总结治疗经验。
1 资料与方法
1.1 一般资料 本组共有22例患者,男性17例,女性5例,年龄(49.53±9.64)岁。围术期死亡2例,死亡原因夹层破裂,死亡率9.09%。术后病情好转转出ICU后,自动出院回当地治疗1例。所有患者均行CTA、主动脉超声检查、磁共振确诊主动脉夹层。将22例患者分为术后肾功能损害组和术后肾功能无损害组进行病例对照研究。
1.2 调查内容与方法 采用前瞻性调查方法,查阅病案资料并按统一表格逐项填写。参考国外及国内文献,术后肾功能衰竭定义为术后血肌酐升高>26.4 μmol/L 或术后尿量<0.5 ml·kg-1·h-1或血肌酐较前升高>50%,时间超过6 h;或术前肾功能正常术后急性肾功能衰竭需要血液透析。潜在的危险因素包括:年龄、性别、高血压、术前腹主动脉撕裂累及肾动脉(CTA或MRI、血管超声诊断)、肢体血压不对称、慢性阻塞性肺部疾病(COPD)、低蛋白血症、机械通气时间、住ICU时间、术前血糖、术前血红蛋白、术前血肌酐、术后血肌酐、术前肾功能损害(术前血肌酐高于正常)、凝血酶原时间、血清总胆红素、体外循环时间≥180 min、体外循环时间、主动脉阻断时间、急诊手术、再次手术、术中停循环时间、输血量、术前心功能(NYHA分级)不全≥Ⅲ级(轻度活动后胸闷气喘,或有咳嗽,或有夜间不能平卧,听诊肺部哮鸣音、湿啰音,心尖部奔马律等)、心律失常(由心电图、长程心电图、心电监测判读病态窦房结综合征、房室传导阻滞、房颤、阵发性室上性心动过速,交界性心动过速)、低心排(多巴胺用量>10 μg·kg-1·min-1)、延迟拔管(机械通气时间>2 d或拔管后再插管)等。在术前肾功能不全9例患者中,有6例患者有明确的腹主动脉撕裂累及肾动脉,1例患者肾结石,1例患者影像资料缺失,1例患者影像或超声未见明显原因。见表1。
1.3 手术方法 麻醉成功后,左桡动脉及左足背动脉置管测压,左侧腹股沟切口,游离右股动脉。胸骨正中切口,分别游离无名动脉、左颈总动脉、左锁骨下动脉。右股动脉插管,右房插入腔房管,建立体外循环,降温,右上肺静脉插入左心减压管,阻断升主动脉远端,切开升主动脉,自左右冠开口处灌血停搏液。褥式缝合两个撕脱的动脉交界,注水试验关闭满意,在近心端内膜和外膜间用生物胶固定粘连满意,再褥式缝合窦管交界一周,根部成形满意,26 mm人工血管与主动脉根部行端端吻合,降温至20℃,停循环,致无名动脉及左颈总动脉插入脑灌注血管,维持脑灌注,在降主动脉施放28 mm带膜支架,将人工血管远端与带膜支架做端端吻合,左锁骨下动脉及左颈总动脉与人工血管做端侧吻合,人工血管分支血管与无名动脉做端端吻合,升主动脉人工血管远端与主动脉弓人工血管做端端吻合,最后吻合前排气,以心包补片包绕人工血管。仔细检查吻合口,无明显出血,心腔排气,开放主动脉,心脏自动复跳为窦性心律后并行循环,继续复温,平衡容量,逐步停机拔去各插管,鱼精蛋白中和肝素,术野仔细止血,放置纵隔、心包引流管,钢丝缝合胸骨,逐层关胸,缝合股动脉,手术结束。
表1 术后肾损害组与术后无损害组的单因素分析[±s,例数及百分率(%)]
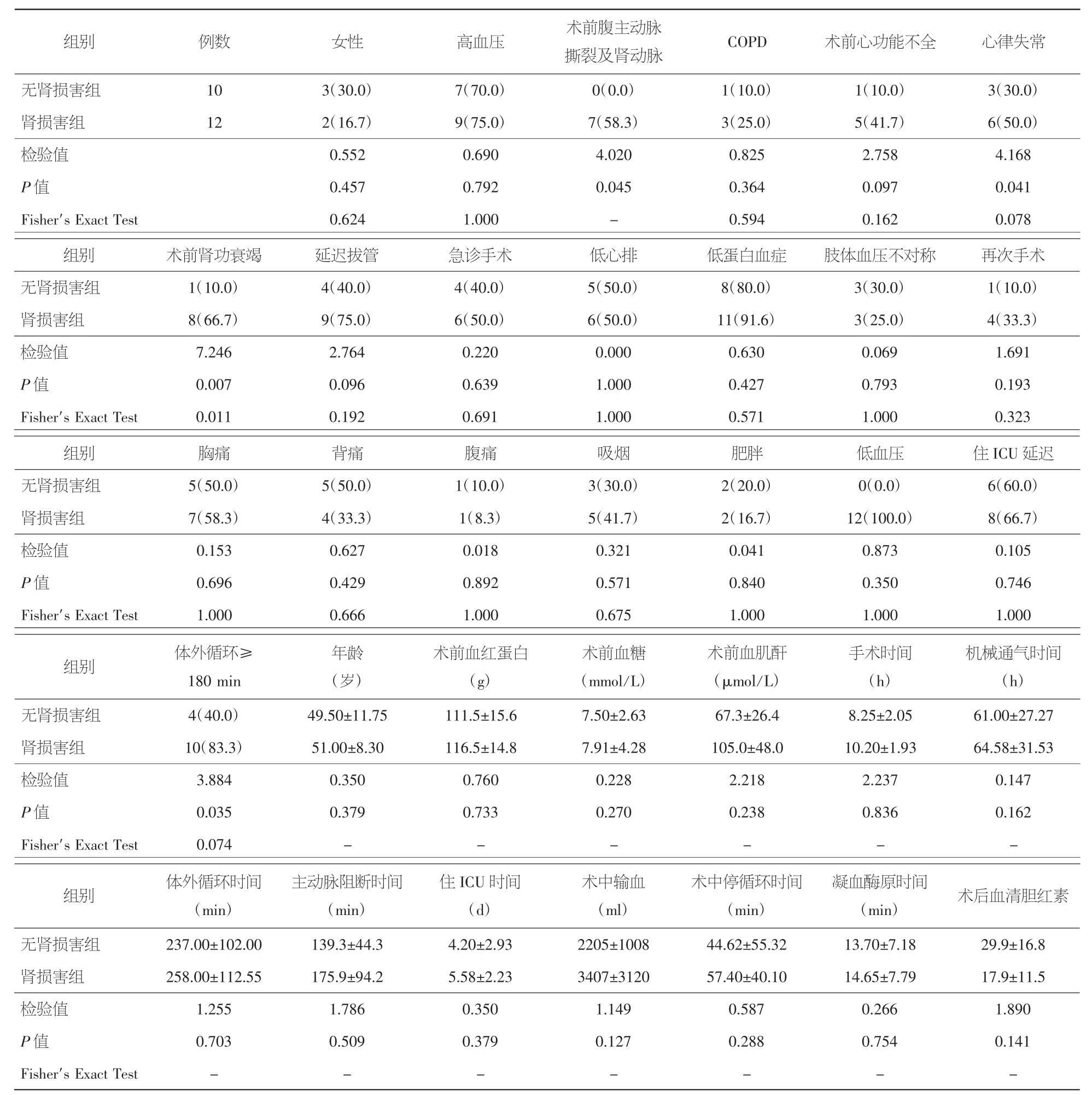
表1 术后肾损害组与术后无损害组的单因素分析[±s,例数及百分率(%)]
组别 例数 女性 高血压 术前腹主动脉撕裂及肾动脉 C O P D 术前心功能不全 心律失常无肾损害组 1 0 3(3 0.0) 7(7 0.0) 0(0.0) 1(1 0.0) 1(1 0.0) 3(3 0.0)肾损害组 1 2 2(1 6.7) 9(7 5.0) 7(5 8.3) 3(2 5.0) 5(4 1.7) 6(5 0.0)检验值 0.5 5 2 0.6 9 0 4.0 2 0 0.8 2 5 2.7 5 8 4.1 6 8 P值 0.4 5 7 0.7 9 2 0.0 4 5 0.3 6 4 0.0 9 7 0.0 4 1 F i s h e r′s E x a c t T e s t 0.6 2 4 1.0 0 0 - 0.5 9 4 0.1 6 2 0.0 7 8组别 术前肾功衰竭 延迟拔管 急诊手术 低心排 低蛋白血症 肢体血压不对称 再次手术无肾损害组 1(1 0.0) 4(4 0.0) 4(4 0.0) 5(5 0.0) 8(8 0.0) 3(3 0.0) 1(1 0.0)肾损害组 8(6 6.7) 9(7 5.0) 6(5 0.0) 6(5 0.0) 1 1(9 1.6) 3(2 5.0) 4(3 3.3)检验值 7.2 4 6 2.7 6 4 0.2 2 0 0.0 0 0 0.6 3 0 0.0 6 9 1.6 9 1 P值 0.0 0 7 0.0 9 6 0.6 3 9 1.0 0 0 0.4 2 7 0.7 9 3 0.1 9 3 F i s h e r′s E x a c t T e s t 0.0 1 1 0.1 9 2 0.6 9 1 1.0 0 0 0.5 7 1 1.0 0 0 0.3 2 3组别 胸痛 背痛 腹痛 吸烟 肥胖 低血压 住I C U延迟无肾损害组 5(5 0.0) 5(5 0.0) 1(1 0.0) 3(3 0.0) 2(2 0.0) 0(0.0) 6(6 0.0)肾损害组 7(5 8.3) 4(3 3.3) 1(8.3) 5(4 1.7) 2(1 6.7) 1 2(1 0 0.0) 8(6 6.7)检验值 0.1 5 3 0.6 2 7 0.0 1 8 0.3 2 1 0.0 4 1 0.8 7 3 0.1 0 5 P值 0.6 9 6 0.4 2 9 0.8 9 2 0.5 7 1 0.8 4 0 0.3 5 0 0.7 4 6 F i s h e r′s E x a c t T e s t 1.0 0 0 0.6 6 6 1.0 0 0 0.6 7 5 1.0 0 0 1.0 0 0 1.0 0 0组别 体外循环≥1 8 0 m i n机械通气时间(h)无肾损害组 4(4 0.0) 4 9.5 0±1 1.7 5 1 1 1.5±1 5.6 7.5 0±2.6 3 6 7.3±2 6.4 8.2 5±2.0 5 6 1.0 0±2 7.2 7肾损害组 1 0(8 3.3) 5 1.0 0±8.3 0 1 1 6.5±1 4.8 7.9 1±4.2 8 1 0 5.0±4 8.0 1 0.2 0±1.9 3 6 4.5 8±3 1.5 3检验值 3.8 8 4 0.3 5 0 0.7 6 0 0.2 2 8 2.2 1 8 2.2 3 7 0.1 4 7 P值 0.0 3 5 0.3 7 9 0.7 3 3 0.2 7 0 0.2 3 8 0.8 3 6 0.1 6 2 F i s h e r′s E x a c t T e s t 0.0 7 4 - - - - - -组别 体外循环时间(m i n)年龄(岁)术前血红蛋白(g)术前血糖(m m o l/L)术前血肌酐(μ m o l/L)手术时间(h)主动脉阻断时间(m i n)住I C U时间(d)术中输血(m l)术中停循环时间(m i n)凝血酶原时间(m i n) 术后血清胆红素无肾损害组 2 3 7.0 0±1 0 2.0 0 1 3 9.3±4 4.3 4.2 0±2.9 3 2 2 0 5±1 0 0 8 4 4.6 2±5 5.3 2 1 3.7 0±7.1 8 2 9.9±1 6.8肾损害组 2 5 8.0 0±1 1 2.5 5 1 7 5.9±9 4.2 5.5 8±2.2 3 3 4 0 7±3 1 2 0 5 7.4 0±4 0.1 0 1 4.6 5±7.7 9 1 7.9±1 1.5检验值 1.2 5 5 1.7 8 6 0.3 5 0 1.1 4 9 0.5 8 7 0.2 6 6 1.8 9 0 P值 0.7 0 3 0.5 0 9 0.3 7 9 0.1 2 7 0.2 8 8 0.7 5 4 0.1 4 1 F i s h e r′s E x a c t T e s t - - - - - - -
1.4 统计学方法 用SPSS 12.0统计软件进行统计处理。计量资料用±s表示,采用t检验;计数资料用卡方检验或Fisher精确检验。P<0.05为差异有统计学意义。
2 结果
术后患者血肌酐与术前相比有所增高,差异具有统计学意义[(174.00±111.61)μmol/L比(87.90±43.44)μmol/L,t=4.137,P=0.000]。血液净化后血肌酐与血液净化前血肌酐相比有所降低,差异有统计学意义[(84.00±113.62)μmol/L 比(174.00±111.00)μmol/L,t=6.335,P=0.000]。术后肾功能损害患者与术后无肾功能损害患者相比较,术前肾功能损害是术后肾功能损害的危险因素[8(66.7)比 4(40.0),χ2=7.246,P=0.007,Fisher精确检验 P=0.011]。体外循环时间≥180 min是术后肾功能损害的危险因素[10(83.3)比 1(10.0),χ2=3.884,P=0.035,Fisher 精确检验P=0.074]。分辨度检验:采用受试者工作特征曲线(ROC曲线)来评价分析结果的分辨度,术后肾功能损害曲线下面积(AUC)为 0.783,P=0.025,95%可信区间(95%CI)为 0.583,0.984,提示分辨度良好。见图1,表2。
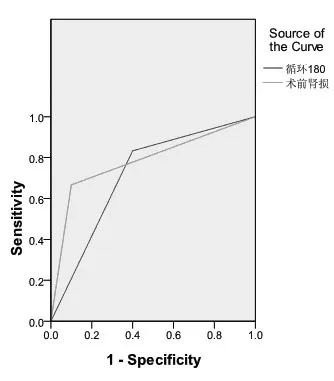
图1 术后肾功能损害的受试者工作特征曲线(ROC曲线)
表2 手术前后和血液净化前后血肌酐对照(±s)
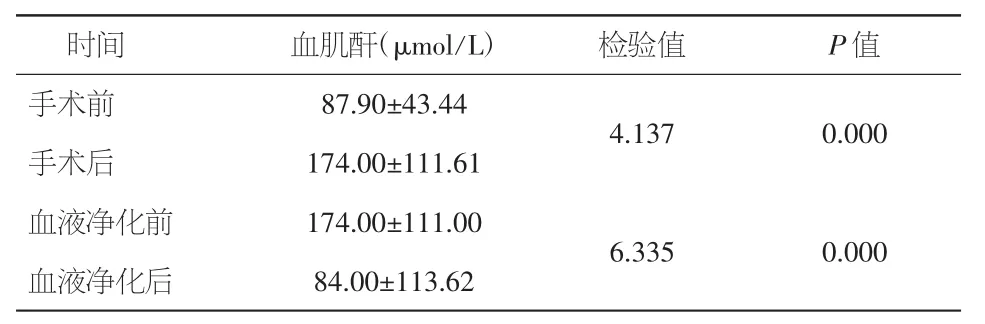
表2 手术前后和血液净化前后血肌酐对照(±s)
时间 血肌酐(μmol/L) 检验值 P值手术前 87.90±43.44 4.137 0.000手术后 174.00±111.61血液净化前 174.00±111.00 6.335 0.000血液净化后 84.00±113.62
上述发生并发症的患者均经相应的治疗治愈或好转。术后常规随访。随访17例,随访期2008年1月至2014年5月,随访时间为术后1、3、6个月和2年。随访结果:1~3个月常规行血管CTA检查,无主动脉夹层再发;2年随访均无复发。
3 讨论
主动脉弓替换术后肾功能损伤治疗主要有肾功能的维护及血液净化治疗。
研究表明,患者术后血肌酐与术前相比有所增高;术前肾功能不全、体外循环时间过长是术后发生肾功能损害的危险因素。本组病例中腹主动脉撕裂造成术前肾功能损害显著,术后均需血液净化治疗。原因是夹层病变可能已累及一侧甚至双侧肾动脉,造成肾脏供血障碍,即使术中维持了良好的血流动力学状况,但由于体外循环的副作用和术中肾脏灌注不足,大部分患者手术后肾脏功能会呈进行性恶化;且由于主动脉夹层手术的复杂性,患者术中通常需要更长时间的体外循环,甚至处于深低温停循环的状态,当肾脏再灌注时由于再灌注损伤,最终导致术后肾衰竭[1]。术中体外循环过程使肾脏灌注方式发生显著改变,灌注量明显减少,体外循环也参与了术后肾功能损害的形成[2,3]。肾功能损害的其他原因有:术中大量输血的患者肾功能衰竭的发生率明显增加;炎性产物、毒素可直接损害肾小管上皮细胞、肾小球基底膜;坏死的上皮细胞、血红蛋白、肌红蛋白和其他微栓可以直接堵塞肾小管,影响肾小球滤过[4]。因此,对于伴有术前肾功能不全的患者及长时间体外循环的患者应密切监测肾功能,并早期积极进行相应的血液净化治疗[1]。
炎症因子损害肾功能。Gormley等研究显示,体外循环炎性介质的肾小球滤过,导致肾小球受损。炎性介质可来源于组织损伤、血液与体外循环材料大面积的物理接触,以及大手术机体应激反应过度、大量输血等导致的白细胞、单核细胞、淋巴细胞激活致炎症因子分泌等。有人认为,主动脉夹层外科术后是更为复杂和严重的全身性炎症反应,主要包括:①深低温停体外循环手术的实施。②夹层本身即是一种炎症反应,强烈的血管内膜破裂,夹层进展至中层可激活细胞、体液的炎症反应系统包括白细胞、巨噬细胞及各种细胞因子。病理研究显示,夹层动脉中有巨噬细胞、白细胞浸润,并且炎性反应的相关基因如IL-6和IL-8均呈高表达。现在更多理论支持主动脉夹层是与手术无关的系统性炎症反应,主要表现为CRP升高,这种炎症反应可能是中性粒细胞激活释放弹性蛋白酶和其他朊酶类的结果[5]。为了避免脊髓和肾脏损伤,应尽量缩短停循环的时间,应在停循环之前先处理近心端,深低温停循环下进行四分支人造血管与降主动脉的吻合,吻合毕立即通过人造血管的灌注分支插入另一支灌注管,恢复胸降主动脉血液灌注,从而缩短脊髓和肾脏缺血时间[6]。术中密切观察尿量变化,若出现少尿或无尿,应该在提高下肢血液灌注压的基础上给予适量的呋塞米、小剂量多巴胺,维持尿量>1 ml·kg-1·h-1,减少对肾脏的进一步损伤。适量加用甘露醇。甘露醇有很强的渗透性利尿作用,可降低血液黏滞度,改善肾皮质血流量,有利于预防脑水肿;同时甘露醇有清除自由基功能,对减轻再灌注损伤有积极作用[7]。给予常规利尿保护肾功能,多数患者病情好转。术后如果肾功能损伤持续加重,应及时行血液净化治疗。本组共有7例患者行血液净化治疗,血液净化后血肌酐比血液净化前有所降低,其中只有1例经过血液净化后血肌酐无明显下降,转出ICU后给予常规血液透析,血肌酐明显下降。提示患者肾功能损害严重时给予血液净化或联合血液透析可显著改善肾功能。血液净化CVVHDF模式可清除血肌酐或其他对心肌有害的物质,增强心肌对血管活性药物的敏感性,保持血流动力学稳定。同时CVVHDF模式可以清除大量的炎症介质,包括肿瘤坏死因子α、白介素-6、白介素-8等,进而可以有效改善系统性炎症反应综合征患者的预后[8]。血液净化补充大量置换液和透析液,连续、缓慢清除溶质和水分,可保持足够的血容量和血流动力学平衡。在肢体肿胀明显时,适当减少容量负荷,以促进肢体消肿和伤口愈合,病情控制后可适当增加容量保证肾灌注。
综上所述,重症医学科对主动脉夹层换弓术后肾功能损伤患者进行血液净化治疗,技术成熟,疗效明显。
[1]王树伟,苏存华,阎岩,等.急性A型主动脉夹层术后肾衰竭的危险因素分析.第二军医大学学报,2014,35:136-140.
[2]伍育旗,余旻,杨卫东,等.体外循环下心脏瓣膜换瓣术后肾功能损害的危险因素分析.医学综述,2013,19:2432-2434.
[3]万彩红,董培青.体外循环与急性肾功能衰竭.心肺血管病杂志,2003,22:190-192.
[4]刘鲁祁,李培杰,李军,等.体外循环心脏直视手术后肾功能衰竭危险因素分析.中国体外循环杂志2004,2:139-142.
[5]Kurabayashi M,Okishige K,Azegami K,et al.Reduction of the PaO2/FiO2ratio in acute aortic dissection elationship between the extent of dissection and inflammation.Circ J,2010,74:2066-2073.
[6]孙永辉,邹承伟,李德才,等.Stanford A型主动脉夹层的外科治疗.山东大学学报(医学版),2011,49:71-73.
[7]程光存,严中亚,吴一军,等.大血管手术中的体外循环管理.心肺血管病杂志,2011,30:320-322.
[8]Nakae H,Asanuma Y,Tajimi K.Cytokine removal by plasma exchange with continuous hemodiafiltration in critically ill patients.Ther Apher,2002,6:419-424.
The renal injury analysis of aortic dissection after aortic arch replacement
WU Yu-qi*,LI Yu-bin,WANG Qing-li,et al.*Intensive Medical Unite,the Frist People′s Hospital,Yichang 443002,China
YANG Xiao-ling,E-mail:Dysyicu@163.com
ObjectiveTo analyze renal injury reason of patients with aortic arch replacement under extracorporeal circulation and give solution.MethodsThe clinical data of 22 patients with aortic arch replacement were analyzed retrospectively.From 2008 January to 2014 June in Yichang First People′s Hospital ICU,male 17 cases,female 5 cases,age(49.53±9.64)years old.ResultsThe postoperative serum creatinine was higher than preoperative,the difference was statistically significant [(174.00±111.61)μmol/L vs (87.90±43.44)μmol/L,t=4.137,P=0.000].The operation will aggravate renal injury.The renal injury of extracorporeal circulation time≥180 min compared with extracorporeal circulation time<180 min,the difference of renal injury was statistically significant(χ2=3.884,P=0.035),showed the long time extracorporeal circulation will aggravate renal injury.Preoperative renal injury compared with normal.Preoperative renal injury was the risk factor of postoperative renal failure (χ2=7.246,P=0.011).The serum creatinine after blood purification was lower than before,the difference was statistically significant [(84.00 ±113.62)μmol/L vs (174.00 ±111.00)μmol/L, t=6.335, P=0.000].ConclusionThe long time extracorporeal circulation and preoperative renal injury are the risk factor of postoperative renal failure.Under CPB aortic arch replacement patients with renal injury receives the satisfactory effect of CRRT in ICU.
ICU; Deep hypothermic circulatory; Aortic arch replacement; Renal injury
443002 湖北省宜昌市,宜昌市第一人民医院重症医学科(伍育旗、王清丽、余旻),肾内科(李玉斌),胸外科(张立伟),病案室(俞彬);湖北省当阳市人民医院重症医学科(杨晓玲)
杨晓玲,E-mail:Dysyicu@163.com
10.3969/j.issn.1672-5301.2015.10.011
R543.1
A
1672-5301(2015)10-0904-05
2015-04-03)
