VAP—1抑制剂及其应用领域的专利分析
2015-09-11焦士勇段洁王鑫等
焦士勇+段洁+王鑫等
[摘要] 血管黏附蛋白(VAP)与众多疾病的发生相关,是众多疾病治疗的靶点。本文通过运用CNABS,DWPI,Sipoabs数据库进行检索和分析,统计涉及VAP-1的专利申请,从专利的年申请量、申请人、技术领域、涉及的疾病治疗领域进行分析,供相关药物研发企业参考,统计结果显示目前涉及VAP-1的全球专利申请数量偏少,申请主要来源于欧美日等西方国家,涉及VAP-1的药物研发公司还没有完成相关专利的布局,这在一定程度上为我国申请人在相关领域的研发提供了机遇。
[关键词] 血管黏附蛋白;专利;统计分析;技术领域
[中图分类号] R977.6 [文献标识码] A [文章编号] 1674-4721(2015)07(b)-0012-04
[Abstract] Vascular adhesion protein-1(VAP-1) is related to the occurrence of numerous diseases and is target of many diseases.The information on annual application amount,applicant,technology and treatment field was analyzed by combinational utilization of CNABS,DWPI and Sipoabs databases,to provide research and development suggestions for related pharmaceutical companies.The results show that the number of global patent applications related to VAP-1 is quite small.The applications mainly come from western countries such as Europe,America and Japan.Companies involved in VAP-1 has not completed the layout of the relevant patents,which might provide an opportunity for Chinese applicants of in this relevant field.
[Key words] Vascular adhesion protein;Patent;Statistical analysis;Technical field
血管黏附蛋白-1(vascular adhesion protein-1,VAP-1)是一种内皮黏附分子,VAP-1具有双重功能,一方面是淋巴细胞的黏附分子,促进淋巴细胞黏附于血管内皮,另一方面VAP-1还具有酶的功效,能够催化伯胺为相应的醛[1-5]。VAP-1由定位于人17号染色体的AOC3基因编码,该基因全长6941 bp,编码序列全长2292 bp[6]。该蛋白可以以溶质的形式存在于血浆中,也可以膜结合形式存在于内皮细胞、脂肪细胞及平滑肌细胞的表面[7]。VAP-1在与炎性相关的疾病中发挥着重要作用,这些疾病包括心血管疾病、肝炎、皮肤病、癌症、炎性肠病等[8-11],因此,关于VAP-1的研究受到了科研机构的广泛重视。
目前,以VAP-1作为靶点开发的药物主要包括2类:一类为化学药物,主要涉及VAP-1抑制剂;另一类为生物类药物,主要涉及抗体类药物。2003年芬兰生物结治疗公司将正在开发的一种对VAP-1的抗炎单克隆抗体vapaliximab的独家开发权和商业化权利转让给了日本生物化学医疗保健公司,研究表明vapaliximab可阻断VAP-1介导的淋巴细胞进入炎性部位。
VAP-1在众多疾病中起着重要作用,药企已经开始围绕VAP-1抑制作用进行药物研发。鉴于VAP-1与较多的疾病存在明确的对应关系,相关专利申请通常以VAP-1的抑制作用限定到权利要求中,这类机制性限定的权利要求往往具有较大的保护范围,对于专利的保护以及布局具有深远的影响。专利是影响药物市场状况的重要因素,决定着企业的核心竞争力。为了全面了解目前涉及VAP-1专利的现状和发展趋势,选择恰当的研发突破点和市场竞争策略,本文就VAP-1抑制剂的基本状况以及专利情况进行检索、分析,以期了解该类药物专利申请的分布和发展趋势,并为相关药物的研究提供建议。
1 VAP-1专利信息统计与分析
1.1 研究方法
以中国专利文献检索系统为数据来源,对涉及VAP-1的发明专利进行统计分析,以关键词“血管黏附蛋白”、“血管黏着蛋白”、“VAP-1”在CNABS、DWPI、Sipoabs数据库中进行检索,上述检索系统能够总体反映世界范围内专利技术发展的现状与趋势,检索的时间截至日为2014年9月4日。通过初步阅读排除与VAP-1无关的专利,筛选出与VAP-1相关的药物领域专利,对各数据库中此时间段(2014年9月4日之前)内检索到的专利文献进行统计分析。
1.2 专利申请状况分析
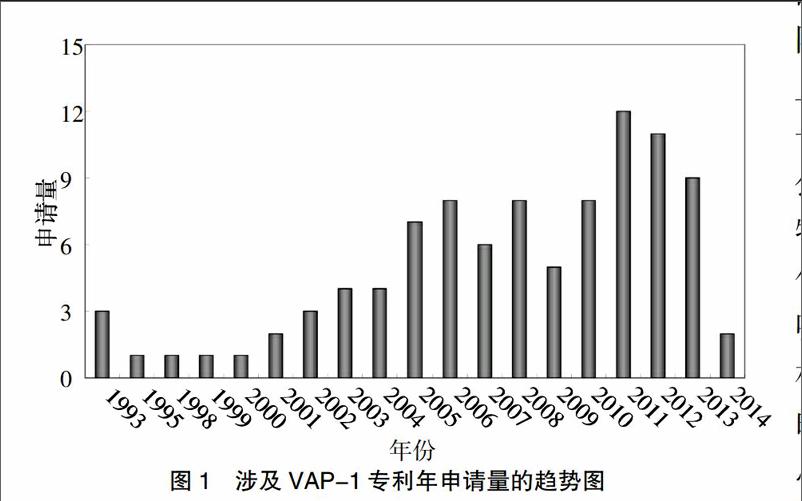
经统计,截至2014年9月,涉及VAP-1的药物和方法的专利申请共计96件,其年度申请量情况如图1所示。VAP-1发现于20世纪80年代,科研人员在关节炎病人的炎性部位分析到淋巴细胞,人们一度认为由于黏膜和外围寻址的作用导致了淋巴细胞的黏附。后来科研人员在风湿性关节炎患者的滑液腔中发现了一种单克隆抗体,这种单克隆抗体随后被确认为1B2,该抗体能够减少炎性滑膜血管上淋巴细胞的黏附,刺激该单克隆抗体产生的抗原不同于以往的其他细胞因子,人们便将这种新的抗原命名为血管黏附蛋白-1[12]。在90年代初,关于VAP-1的机理研究进一步深入,并于1993年出现了首个关于VAP-1抑制剂的专利申请,2003年以后相关专利申请的数量呈迅速增长趋势,2006年以后基本维持在年均10项。总体来说,涉及VAP-1专利的申请数量不是很多,表明VAP-1还是药物研发领域较新的靶点,考虑到部分专利申请公开的滞后性,2013年后的专利申请还会有进一步的增加。虽然申请量绝对数值还不高,但2011年后的申请量已经呈现增长趋势,提示涉及VAP-1的专利申请在药物开发领域受到了越来越多的关注。
2 VAP-1专利申请人分析
2.1 专利申请人类型分布
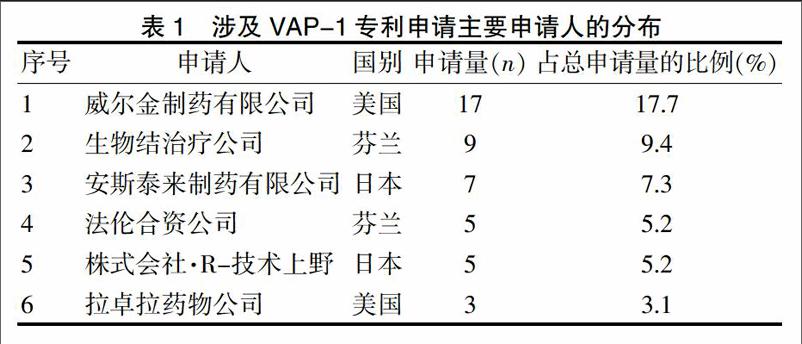
对VAP-1专利的申请,美国排在第1位,大约占总申请量比例的20.8%,其次为芬兰和日本(表1)。
2.2 申请人类型分析
对申请人的类型进行分析,发现企业申请量为72件,占75.8%;大学、研究所以及医院等科研机构的申请量为5件,占5.3%;个人申请量为18件,占18.9%。在专利申请所属国家分布中,中国国内申请量为5件,占总申请量的5.3%,由表1可知,排名前几位均为企业申请,均被欧美日等西方国家所占据,尤其是美国,其在有关VAP-1的申请中占据绝对优势。从上述申请量的比例可以看出,企业和个人的申请量占绝大多数,科研院所对VAP-1相关药物的研究关注度还不高,国内申请人对该领域药物研发的关注度低于国外申请人。
2.3 国内外重点申请人分析
对国内外申请人统计分析发现,国内申请量较少,并没有突出的申请人,且申请人主要以个人申请为主。5件国内申请中,陶英亮申请2件(专利公开号:CN101401802A;CN10249991A)、毛利真申请2件(专利公开号:CN101732712A;CN103933565A)、黄若磐和广州瑞博奥生物科技有限公司共同申请1件(专利公开号:CN102236015A)。所涉5件专利申请中,产品专利申请4件,主要涉及组合物,用于治疗脑率中等神经系统疾病;检测方法涉及1件,均未形成有效的保护体系。国外申请中,以美国药企威尔金制药有限公司申请量最多,共17件,占所有申请量的17.7%,且申请中主要涉及以马库什通式化合物为注,如公开号为WO2012082746A2的申请涉及三唑类化合物、公开号为WO2011082245A2的申请涉及四唑类化合物,公开号为WO2011133875A2的申请涉及吡啶类化合物,公开号为WO2012058529A2的申请涉及嘧啶类化合物,以上化合物均是用于治疗与VAP-1相关的疾病。其次是芬兰的生物结治疗公司以及日本的安斯泰来制药有限公司,申请量分别为9件和7件,占总申请量比例分别为9.4%和7.3%,生物结治疗公司以生物类制药为主,如公开号为WO9325582A1、WO0 3093319A1、WO2008129124A1的申请涉及人VAP-1抗体的制备及应用,公开号为CA2289903A1的申请主要涉及与VAP-1相关的核酸以及重组宿主细胞的构建;安斯泰来制药有限公司以化学类药物研究为主,如公开号为WO2004067521A1、WO2004087138A1、WO2 005089755A1、WO2006011631A2、WO2006028269A2的申请涉及噻唑类化合物,公开号为WO2011034078A1、WO2012124696A1的申请涉及嘧啶、哌嗪类化合物,以上申请均是其于VAP-1为靶点研发。从国外的申请量可以看出国外企业对于VAP-1相关药物研发具有较强的实力,相关企业已呈现了对VAP-1相关药物进行初步的专利布局的形势,不论是生物制剂还是化学制剂,相关企业已经专注研究近10年。然而,国内申请人特别是国内制药企业和科研院所对以VAP-1为靶点的药物开发的关注度不高,未以VAP-1为靶点进行相关研究。随着我国科研投入的不断提高,以VAP-1为靶点的药物研究必将更为深入,科技含量也会随之提升。从上述数据可以看出,相关药物开发公司并未对涉及VAP-1的专利进行广泛的专利布局,这给国内研究机构以及相关药物企业在VAP-1领域的药物研发以及进行专利布局提供了机遇。
3 VAP-1专利技术分析
3.1 专利技术领域分布
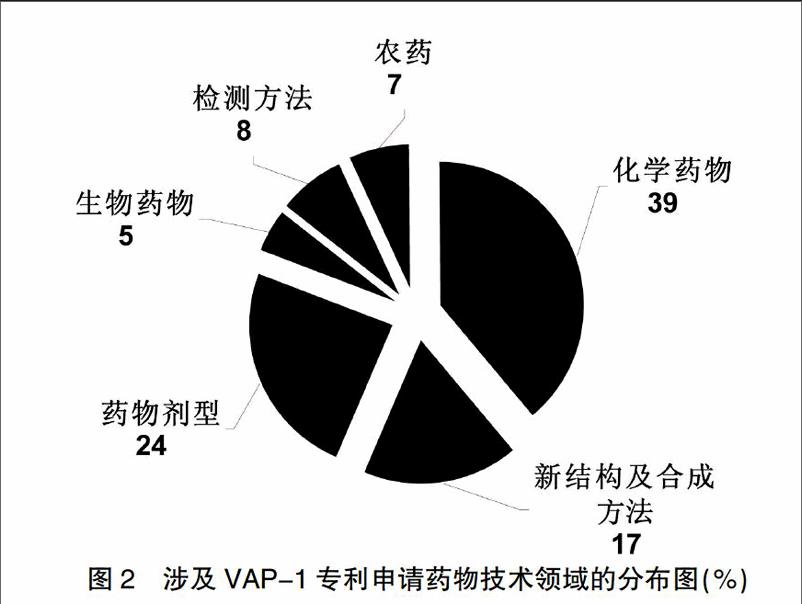
涉及VAP-1的专利申请研究以化学药物的申请量占据首位,达39%;药物剂型的改进占24%;其次是新结构及合成方法,占17%;生物制药领域所占比重较低,仅5%(图2)。在涉及的国内申请中未见化合物方面的申请,化合物的专利申请主要来自欧美等国,由此可知,化学药物、药物剂型以及新结构和合成方法是VAP-1靶点药物研发的重点。
3.2 化学药物专利分析
4 VAP-1涉及疾病治疗领域
对每篇专利申请的前3个分类号进行统计分析,相关专利中涉及的主要疾病类型如表2所示。由此可知,与VAP-1相关的专利申请所涉及的疾病广泛,VAP-1可作为不同疾病治疗的药物靶点。针对不同疾病进行分析,可以看出与VAP-1相关的神经系统疾病的申请占22件,居于首位,远超排在第2位的免疫或过敏性疾病,排在第3位的疾病为心血管疾病。神经系统疾病主要由感染、中毒、异常增生、免疫损伤等引起,且免疫或过敏性疾病以及心血管疾病等也经常伴有炎性改变,上述3种疾病通常会导致VAP-1的增加。VAP-1表达于活体的微血管内皮细胞上,其对淋巴细胞及中性粒细胞均有黏附作用[13-14]。在VAP-1介导的多性核白细胞(PMN)与内皮细胞黏附实验中发现,VAP-1通过其SSAO酶活性在黏附级联过程中的滚动及迁徙环节中发挥作用,用SSAO酶抑制剂阻止SSAO酶活性,可抑制PMN与内皮细胞黏附而有效缓解体内的炎性反应[15],因此,以VAP-1为靶点用于开发治疗神经系统疾病、免疫或过敏性疾病以及心血管系统疾病的药物研发受到广泛关注,也从侧面反映出涉及VAP-1的药物专利研发方向的重点主要集中于神经系统疾病、免疫或过敏性疾病以及心血管系统疾病、重症休克。
5 总结
总体而言,目前涉及VAP-1的全球专利申请数量偏少,其申请主要来源于欧美日等西方国家。由于目前还没有作为VAP-1抑制剂上市的药物,关于VAP-1相关药物的研发还是新的领域,且在本领域尚无系统的专利布局,因此,该领域的研究开发前景广阔。从上述分析可知,对于VAP-1相关药物研发的重点在于化合物以及药物剂型2个方面,主要申请人是美国、日本等发达国家的制药企业。
从本领域专利覆盖的范围来看,居于专利申请首位的威尔金制药有限公司的专利申请主要涉及化合物专利,而且是新结构的通式化合物,这些化合物涉及多种结构,保护范围广泛。相关药物研发公司通常以VAP-1的抑制作用对治疗的疾病进行机制性限定,同样造成保护范围广泛。国内申请人主要涉及的是组合物,活性组分仅为具体的一种化合物,疾病也仅为某一具体疾病,保护范围相对较小。相比较而言,我国药物企业、科研结构在新的化合物研究领域与国外药企相比还存在较大的差距。从申请所涉及的与VAP-1相关的疾病而言,国内申请人主要涉及脑中风等神经系统疾病,而国外申请人对与VAP-1相关的疾病的涵盖范围较广,说明国内相关科研机构对以VAP-1为靶点的疾病研究以及相关药物研究还不够系统。
涉及VAP-1的药物研发公司还没有完成相关专利的布局,在数量和技术上并不存在被国外企业所独占,因此,涉及VAP-1的药物研发仍然是开放和公平的,这在一定程度上为我国申请人在相关领域的研发提供了机遇。
[参考文献]
[1] Madej A,Reich A,Szepietowski J.Vascular adhesion protein-1:an unusual adhesion molecule[J].Postepy Hig Med Dosw(online),2005,59:172-179.
[2] Tohka S,Laukkanen M,Jalkanen S,et al.Vascular adhesion protein l(VAP-1) functions as a molecular brake during granulocyte rolling and mediatesrecruitment in vivo[J].FASEB J,2001,15(2):373-382.
[3] Airenne Tr,Nymalm Y,Kidron H,et al.Crystal structure of the human vascular adhesion protein-1:unique structural features with functionalimplications[J].Protein Sci,2005,14(8):1964-1974.
[4] Stolen CM,Marttila-Ichihara F,Koskinen K,et al.Absence of the endothelial oxidase AOC3 leads to abnormal leukocyte traffic in vivo[J].Immunity,2005,22(1):105-115.
[5] Lyles GA.Mammalian plasma and tissue-bound semiearbazide-sensitive amine oxidases:biochemical,pharmacologicaland toxicological aspects[J].Int J Biochem Cell Biol,1996,28(3):259-274.
[6] Ochiai Y,Itoh K,Sakurai E,et al.Molecular cloning and characterization of rat semicarbazide-sensitive amine oxidase[J].Biol Pharm Bull,2005,28(3):413-418.
[7] Schwelberger HG.The origin of mammalian plasma amine oxidase[J].J Neural Transm,2007,114(6):757-762.
[8] 赵德福,孙侃,常向云,等.可溶性血管黏附蛋白-1对2型糖尿病患者下肢大血管病变的影响[J].临床和实验医学杂志,2011,10(8):563-564.
[9] 严丽荣,蒋廷波,于焱,等.可溶性血管黏附蛋白、C反应蛋白在老年冠心病发病中的作用[J].江苏大学学报(医学版),2004,14(4):323-324.
[10] 张庆殷,侯桂华.内皮细胞黏附分子研究进展[J].国外医学:生理病理科学与临床分册,1995,15(4):226-229.
[11] 潘昌如,刘会怡.胃癌患者血清可溶性血管内皮黏附蛋白-1检测的临床意义[J].西南国防医药,2012,22(3):246-248.
[12] Salmi M,Jalkanen S.A 90-kilodalton endothelial cell molecule mediating lymphocyte binding in humans[J].Science,1992,257(5075):1407-1409.
[13] Yu PH.Deamination of methylamine and angiopathy;toxicity of formaldehyde,oxidative stress and relevance to protein glycoxidation in diabetes[J].J Neural Transm Suppl,1998,52:201-216.
[14] Gubisne-Haberle D,Hill W,Kazachkov M,et al. Protein cross-linkage induced by formaldehyde derived from semicarbazide-sensitive amine oxidase-mediated deamination of methylamine[J]. J Pharmacol Exp Ther,2004, 310(3):1125-1132.
[15] Jalkanen S,Karikoski M,Mercier N,et al.The oxidase activity of vascular adhesion protein-1(VAP-1) induces endothelial E- and P-selectins and leukocyte binding[J].Blood,2007,110(6):1864-1870.
(收稿日期:2015-06-01 本文编辑:李秋愿)
