超声激发碘自由基降解水中磺胺嘧啶
2015-08-25杨小雨李克斌西安理工大学西北旱区生态水利工程国家重点实验室培育基地陕西西安70048西北大学化学与材料科学学院合成与天然功能分子化学教育部重点实验室陕西西安70069
魏 红,杨小雨,闵 涛,李克斌(.西安理工大学,西北旱区生态水利工程国家重点实验室培育基地,陕西 西安 70048;.西北大学化学与材料科学学院,合成与天然功能分子化学教育部重点实验室,陕西 西安 70069)
超声激发碘自由基降解水中磺胺嘧啶
魏 红1*,杨小雨1,闵 涛1,李克斌2(1.西安理工大学,西北旱区生态水利工程国家重点实验室培育基地,陕西 西安 710048;2.西北大学化学与材料科学学院,合成与天然功能分子化学教育部重点实验室,陕西 西安 710069)
以H2O2和KI作为分子碘(I2)的来源,研究超声/H2O2/KI体系对磺胺嘧啶(SD)的降解效果.考察超声/H2O2/KI体系中溶液初始pH值、H2O2和KI添加浓度等因素的影响.采用碘自由基抑制剂甲硫咪唑对体系中的活性物质进行分析.结果表明,超声/H2O2/KI体系显著提高了磺胺嘧啶的降解效果,磺胺嘧啶的去除率随溶液初始pH值(2.6~5.2)的升高而降低; H2O2和KI的添加浓度对磺胺嘧啶的去除率影响较大,磺胺嘧啶的去除率随其初始浓度的增大而降低.碘自由基(I·和)是超声/H2O2/KI体系降解磺胺嘧啶的主要活性物质.HPLC图谱表明,磺胺嘧啶降解的同时生成4种产物,磺胺为降解产物之一.
碘;碘自由基;超声;磺胺嘧啶;甲硫咪唑
近年来的研究表明,国内外各种环境样品中均有抗生素类药物检出[1-3].虽残留量较低(ng~μg),但由于其分布广泛、成分复杂多样和持久性等特点,严重威胁人类健康及生态系统的安全[1,4].磺胺类药物是成功应用于人类传染性疾病治疗的第一类抗菌剂[5],其环境残留问题也越来越得到国内外学者的重视.目前,国内外用于磺胺类药物的去除技术主要有UV/H2O2、Fenton[7]、UV-A/TiO2、Fe3+[8]、γ射线/]等.
由于反应条件温和、效率高等优点,超声技术在抗生素降解方面受到广泛关注[10-15].超声主要通过空化效应使污染物在空化泡破裂所形成的高温、高压极端微环境中发生热解或被液相媒介中水分子裂解产生的自由基(HO·、H·)氧化而去除[10],但其处理效果受污染物特性、蒸汽压等条件制约[12].目前,超声与其他氧化剂联合是超声技术的研究热点之一,主要利用 HO·[E0= 2.80V][11,13-14]、·[E0= 2.01V][15]等活性物质氧化降解污染物质.
分子碘I2[E0(I2/I-)= 0.54V] 价廉易得、低毒,是一种温和的氧化剂,广泛用于有机物合成反应[16].有报道称I—I键在可见光(λ≥450nm)作用下断裂形成氧化性较强的 I·[E0(I·/I-)=1.33V],从而有效提高 2,4,6-三氯酚的去除效果[17].超声激发碘自由基在有机污染物的降解方面还鲜见报道.
本文首次将碘与超声联合,以H2O2和KI作为分子碘的来源,研究超声/H2O2/KI体系对磺胺类抗生素磺胺嘧啶(SD)的降解效果,考察溶液pH值、H2O2和KI添加浓度等因素的影响,分析体系中降解磺胺嘧啶的主要活性物质,旨在为磺胺类抗生素的去除提供新的方法.
1 材料与方法
1.1实验材料
碘化钾(分析纯,天津市福晨化学试剂厂);30%过氧化氢(优级纯,国药集团化学试剂有限公司);氢氧化钠、硫酸(分析纯,天津市天力化学试剂有限公司);磺胺(天津市福晨化学试剂厂,纯度大于99.5%);甲醇(分析纯,广东光华科技股份有限公司);甲硫咪唑(上海研臣实业有限公司,纯度大于98%);乙腈(色谱纯);超纯水.磺胺嘧啶(北京百灵威科技有限公司,纯度大于99%),分子式: C10H10N4O2S,结构如图1所示.
图1 磺胺嘧啶的结构式Fig.1 Chemical structure of sulfadiazine
1.2实验仪器
pHs-25数显酸度计(上海虹益仪器仪表有限公司)配E-201-C-9型pH复合电极(上海罗素科技);Hach DR5000紫外可见分光光度计(美国哈希公司);JY92-IIN超声波细胞粉碎机(配备直径 8mm的钛探头,宁波新芝仪器有限公司);Aglient 1200液相色谱仪,配备 G1311A四元泵,柱温箱30℃,G1314C XL可变波长紫外检测器.
1.3实验方法
1.3.1磺胺嘧啶的超声降解实验 准确移取一定浓度的磺胺嘧啶储备液于200mL容量瓶中,定容、摇匀、静置后转入250mL烧杯中,用1.0mol/L NaOH或H2SO4调节pH值,加入一定量KI后搅拌使其溶解,添加一定量 H2O2搅拌均匀.采用JY92-IIN超声波细胞粉碎机在标准大气压下进行超声处理,探针浸泡深度约1.0cm.每20min取样,过0.22µm滤膜后通过HPLC分析磺胺嘧啶的浓度,磺胺嘧啶的去除率按照式(1)计算:
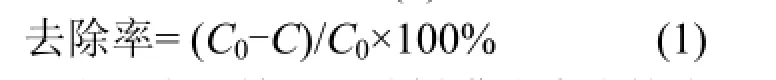
式中:C0和C分别为开始和t时刻磺胺嘧啶的浓度,mmol/L.
1.3.2磺胺嘧啶的 HPLC分析 磺胺嘧啶浓度通过 Agilent 1200高效液相色谱仪分析.色谱柱为Eclipse Plus C18(4.6×150mm;5µm);流动相为乙腈:超纯水=25:75(V:V);进样量为 10.0µL;流速为0.30mL/min;检测波长269nm;柱温为30℃.在此条件下,磺胺嘧啶的保留时间tR=8.408min.
2 结果与讨论
2.1比较不同反应体系中磺胺嘧啶的降解
实验研究了磺胺嘧啶初始浓度0.04mmol/L,超声功率195W, pH值为3.2, H2O2、KI添加浓度分别为120.0、3.2mmol/L时,单独超声(US)、单独H2O2氧化、US/H2O2、US/KI、H2O2/KI和US/ H2O2/KI六种反应体系对磺胺嘧啶的去除情况,结果如图2所示.
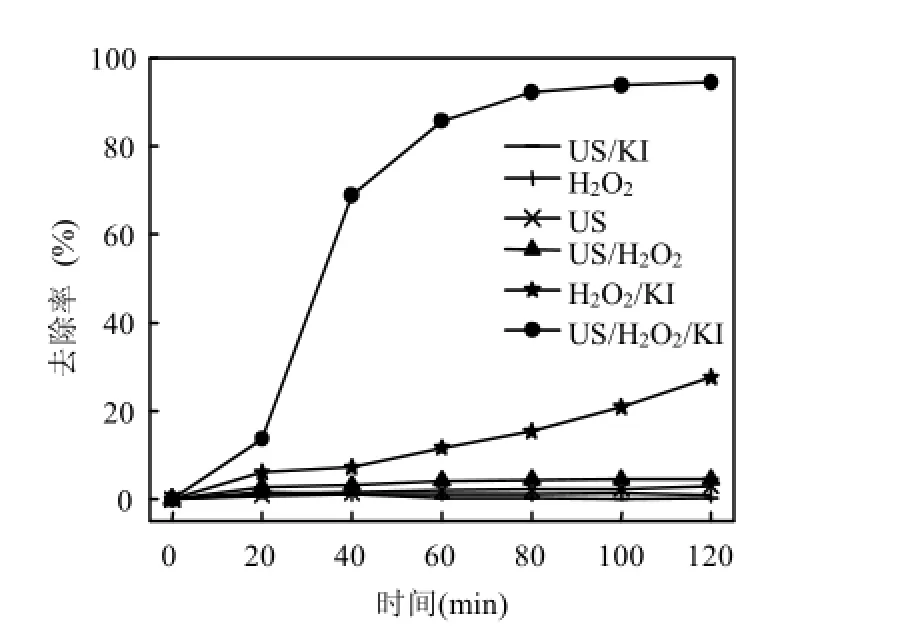
图2 不同反应体系中磺胺嘧啶的降解效果Fig.2 Sulfadiazine degradation under different systems
由图2可以看出,单独超声对磺胺嘧啶的去除效果不明显,120min的去除率仅为 3.0%.由于磺胺嘧啶的水溶性较高(logKow=0.826)[7],降解主要靠空化产生的HO·氧化,单独超声体系中水分子裂解产生的自由基非常有限.H2O2氧化条件下,磺胺嘧啶的去除率为1.3%,这主要是因为磺胺嘧啶同时含有氧化性基团(-SO2-)和还原性基团(-NH2,-NH-),限制了 H2O2的氧化作用[9].超声/H2O2一定程度上提高了磺胺嘧啶的去除率(4.5%),但效果不明显,类似结果也有报道[13-14].体系中HO·的产生量相对增加,但HO-OH的键能较大(207kJ/mol),限制了超声/H2O2降解磺胺嘧啶的效果.超声/KI体系中磺胺嘧啶120min的去除率仅为 0.2%,远低于直接超声去除率.这是由于 I-在超声作用下与磺胺嘧啶形成竞争,捕捉HO·而释放出碘[18].H2O2/KI体系中磺胺嘧啶的去除率为27.6%,超声/H2O2/KI体系中达到94.4%,表明它们之间存在协同效应,这可能与体系中分子碘和碘自由基的生成有关[17,19].
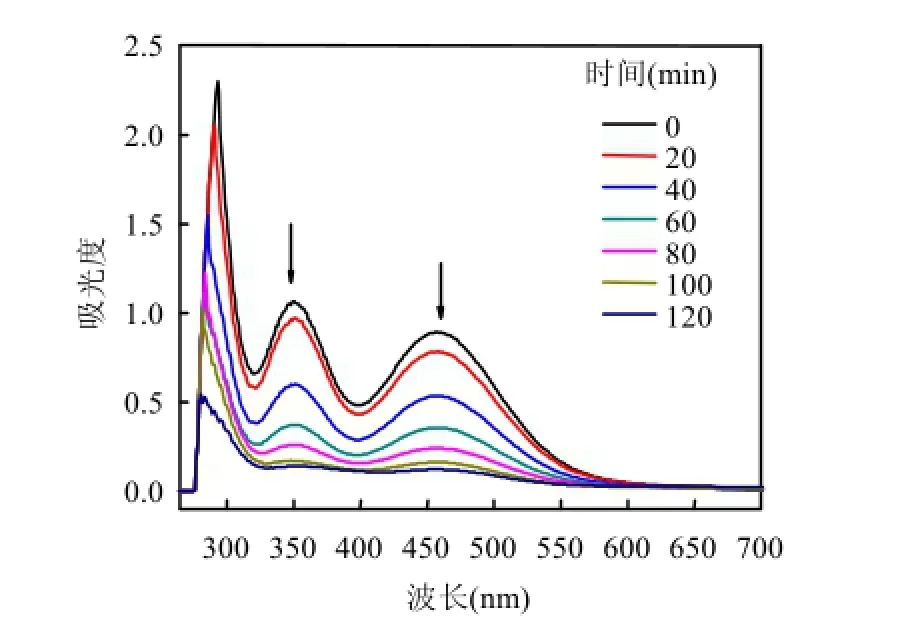
图3 超声/H2O2/KI体系降解磺胺嘧啶过程中的紫外吸收光谱Fig.3 UV-Vis spectra Changes recorded in US/H2O2/KI system at different reaction times
为此实验研究了超声/H2O2/KI体系降解磺胺嘧啶过程中的紫外吸收光谱变化(图3).磺胺嘧啶在285nm左右出现最大吸收峰(图4),随着反应的进行峰值不断降低,同时最大吸收波长向250nm移动,说明磺胺嘧啶发生降解的同时有其他产物生成.460nm和350nm分别为I2和的最大吸收波长[17],随着反应的进行, A460nm和A350nm降低,说明I2和I3-参与了磺胺嘧啶的降解反应.

图4 磺胺嘧啶溶液的吸收光谱Fig.4 UV-Vis spectra of SD
酸性条件下H2O2和KI为分子碘(I2)的来源,同时溶液中I-与I2结合成为[式(2)~(3)]能提高 I2在水中的溶解度[17,19].I2[E0(I2/I-)=0.54V]和[E0(I3-/I-)=0.53V]的氧化性较低,因此 H2O2/KI体系对磺胺嘧啶的降解效果较小.
超声/H2O2/KI体系降解磺胺嘧啶过程中的紫外吸收光谱变化与H2O2/KI体系的变化一致. 图5为H2O2/KI和超声/H2O2/KI两种体系中,反应液的A460nm和A350nm变化.
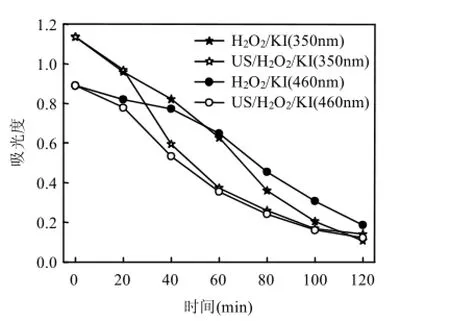
图5 超声/H2O2/KI、H2O2/KI体系中反应液的A460nm、A350nm变化Fig.5 Absorbance changes at 460nm and 350nm in US/H2O2/KI and H2O2/KI systems at different reaction times
由图5可以看出,与H2O2/KI体系相比,超声/H2O2/KI体系中,超声加快了 I2和的消耗. I2和的I—I键能较低(152.7kJ/mol),直接氧化磺胺嘧啶的同时,在超声作用下形成活性更高的和 I·[E0(I·/I-)=1.33V][式(4)~(5)],因此超声/H2O2/KI体系中,由于碘(I2、)及其自由基(I·和 ·)的共同作用, 磺胺嘧啶的去除效果显著提高.
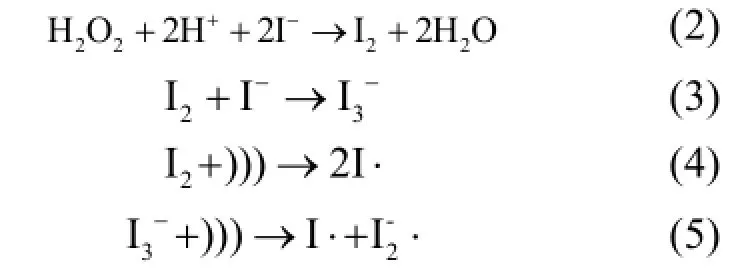
2.2超声/H2O2/KI体系降解磺胺嘧啶的影响因素
2.2.1溶液初始 pH值 磺胺嘧啶初始浓度为0.04mmol/L, H2O2、KI添加浓度分别为120.0、3.2mmol/L,超声功率 195W,采用 1.0mol/L的H2SO4和NaOH溶液调节体系初始pH值分别为2.6、3.2、4.2和5.2,磺胺嘧啶的去除情况如图6所示.
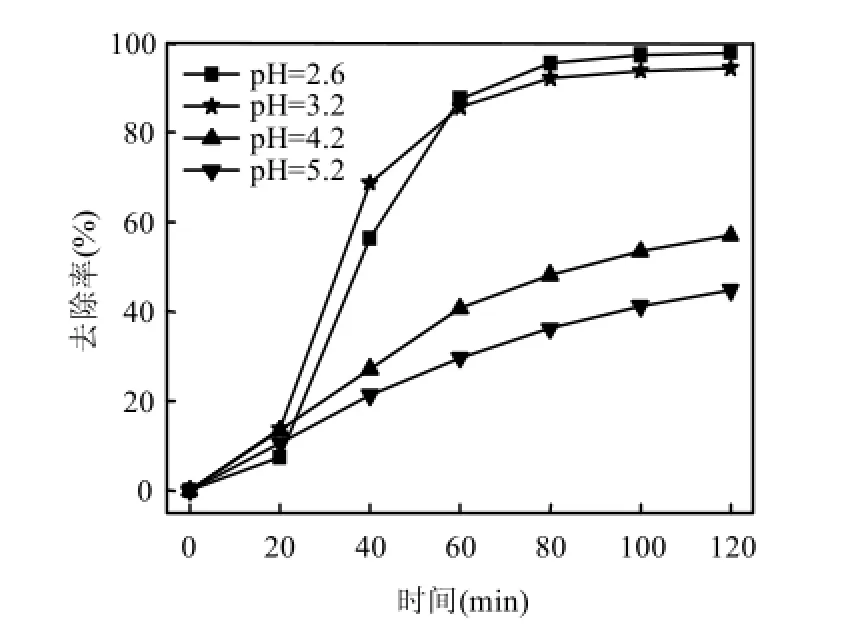
图6 溶液初始pH值对磺胺嘧啶降解的影响Fig.6 Effect of pH values on sulfadiazine degradation
由图6可以看出,初始pH值对磺胺嘧啶的去除效果影响非常明显.pH在2.6-5.2范围,磺胺嘧啶的去除率随溶液初始 pH值的升高而降低,溶液pH值依次为2.6、3.2、4.2和5.2时,120min,磺胺嘧啶的去除率分别为98.0%、94.4%、57.0% 和44.8%.
图7为不同初始pH值条件下,溶液的A460nm(即I2)随反应时间的变化,图8为对应A350nm(即)变化.
图7表明,初始pH值显著影响I2的产生量,I2的产生量随pH值的升高而降低.这是因为 H+能有效提高 H2O2的氧化性以促进反应(2)的进行[17],使得I2直接裂解产生的I·增大[式(4)];且由于更多I-氧化,降低了其对I2以及I·的捕捉[式(3),式(6)],即的产量减少(图8中A350nm随着pH值在 2.6~4.2范围内增加而降低),故一定程度上抑制了]的产生,而I·[E0(I·/I-) =1.33V]具有较高的氧化活性,使得磺胺嘧啶的去除效果随初始pH值的降低而显著增强.

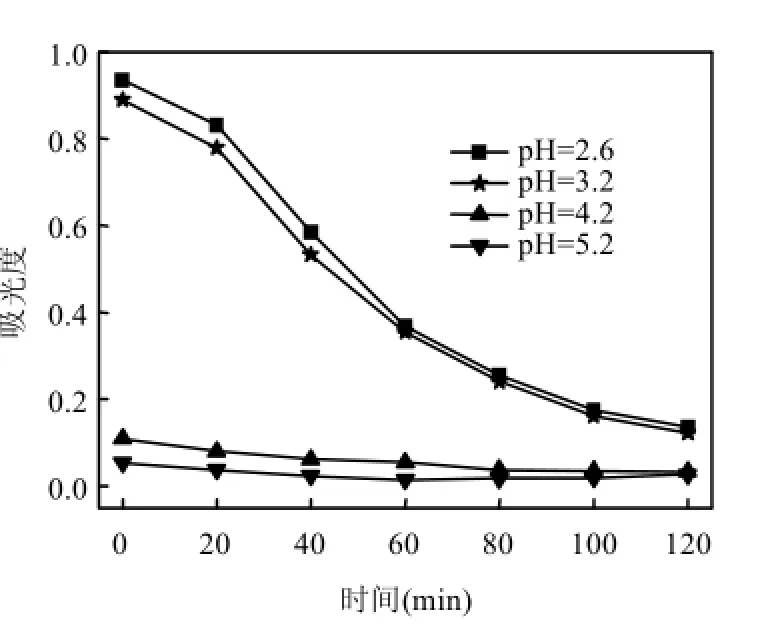
图7 不同初始pH值下反应液的A460nm变化Fig.7 Changes of A460nmat different pH values
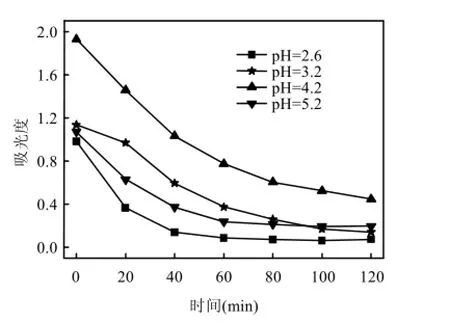
图8 不同初始pH值下反应液的A350nm变化Fig.8 Changes of A350nmat different pH values
2.2.2KI添加浓度 磺胺嘧啶初始浓度为0.04mmol/L, pH=3.2,超声功率195W, H2O2添加浓度为120.0mmol/ L, KI添加浓度分别为0.6、1.2、3.2和6.4mmol/L时,磺胺嘧啶的降解情况如图9所示.
由图9可以看出,一定范围内,磺胺嘧啶的去除率随KI添加浓度的增加而增大.KI添加量分别为0.6、1.2、3.2mmol/L,120min,磺胺嘧啶的去除率分别为79.0%、83.1%和94.4%;继续增加KI浓度到6.4mmol/L,去除率有所降低,为88.3%.
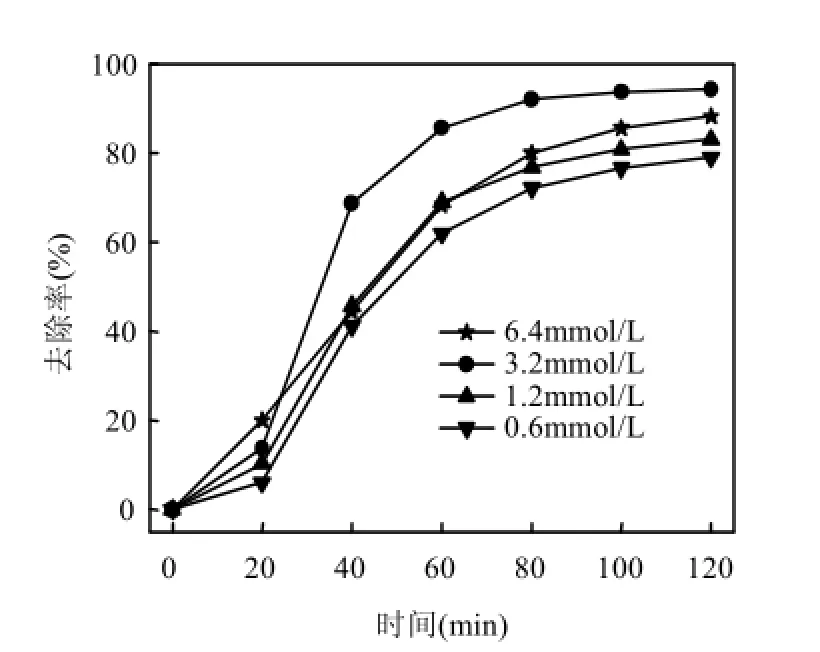
图9 KI添加浓度对磺胺嘧啶降解效果的影响Fig.9 Effect of KI concentrations on sulfadiazine degradation
图10为不同 KI添加浓度下,反应液的A460nm(即I2)变化,图11为对应A350nm(即)变化.
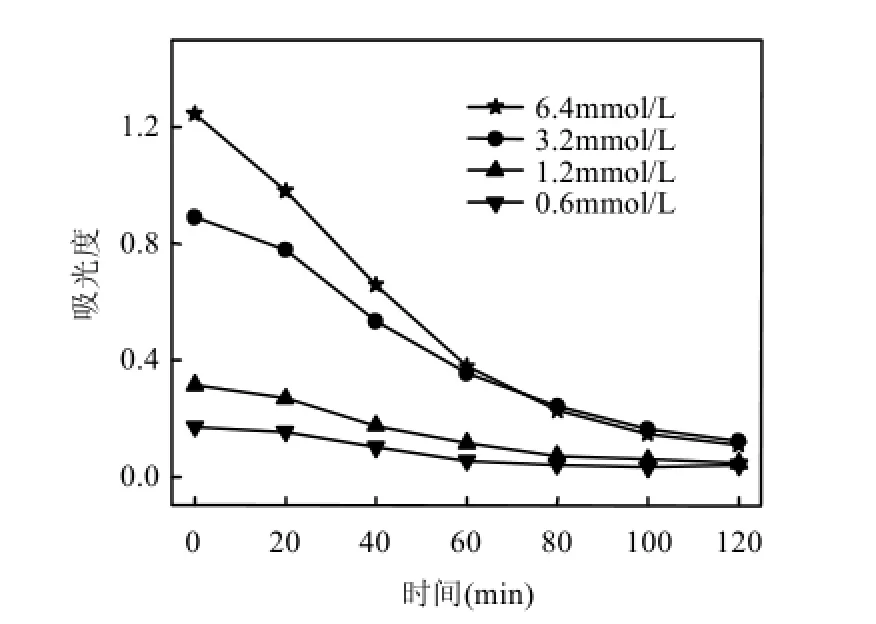
图10 不同KI添加浓度下反应液的A460nm变化Fig.10 Changes of A460nmat different KI concentrations
图10、11表明,KI添加浓度在 0.6~3.2mmol/L范围,0min时,A460nm和A350nm随KI添加浓度的增加而增大,即I-的增加促进了I2和的生成[式(2) ~(3)],I·以及·的产量随之增加[式(4)~(5)],磺胺嘧啶的去除率增加.但当KI添加量增加至6.4mmol/L,A350nm大幅度增加,且0~80min保持不变,这是由于过量I-与I2结合形成.一方面阻碍了I2的超声裂解,使成为体系中碘自由基(I·和·)的主要来源[式(5)],另一方面过量I-捕捉I·形成·[式(6)][17,19-20]·成为降解磺胺嘧啶的主要氧化剂.与 I·相比·的氧化活性较低,因此磺胺嘧啶的去除率有所降低.
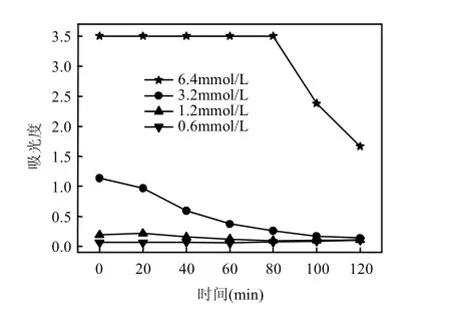
图11 不同KI添加浓度下反应液的A350nm变化Fig.11 Changes of A350nmat different KI concentrations
2.2.3H2O2添加浓度 磺胺嘧啶初始浓度0.04mmol/L, pH=3.2,超声功率 195W,KI添加浓度为3.2mmol/L, H2O2添加浓度在10.0~240.0mmol/L范围,磺胺嘧啶的降解情况如图12所示.

图12 H2O2添加浓度对磺胺嘧啶降解效果的影响Fig.12 Effect of H2O2concentrations on sulfadiazine degradation
由图12可以看出,H2O2添加浓度对超声/H2O2/KI体系降解磺胺嘧啶有一定的影响.H2O2添加量分别为10.0、60.0、120.0和240.0mmol/L,120min,磺胺嘧啶的去除率依次为 45.4%、91.7%、94.4%和94.3%.
图13为不同 H2O2添加浓度时,反应液的A460nm(即I2)变化,图14为对应A350nm(即)变化.
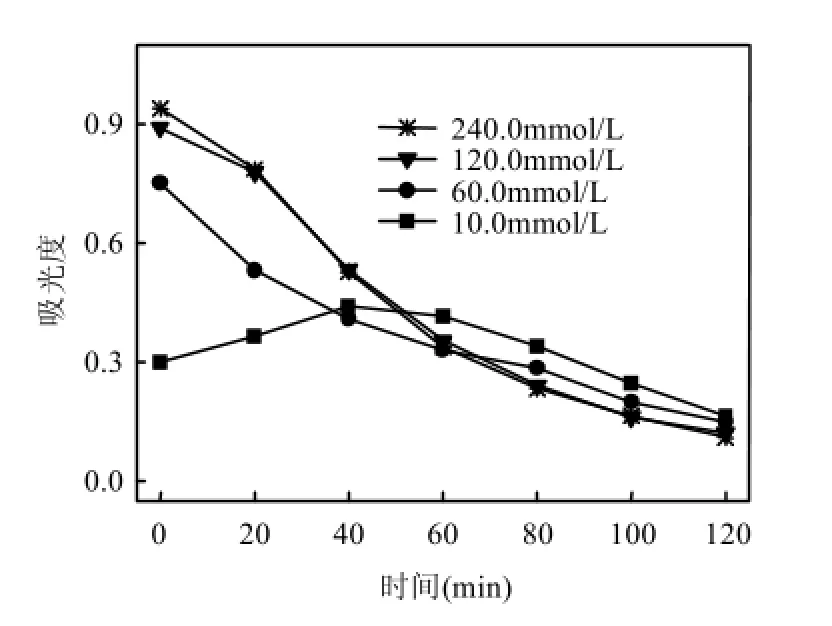
图13 不同H2O2添加浓度下反应液的A460nm变化Fig.13 Changes of A460nmat different H2O2concentrations
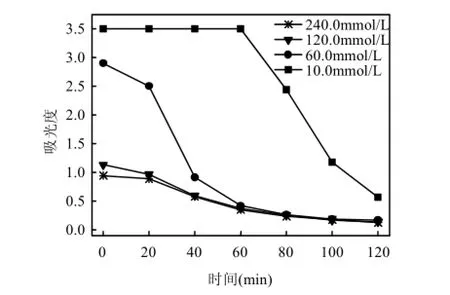
图14 不同H2O2添加浓度下反应液的A350nm变化Fig.14 Changes of A350nmat different H2O2concentrations
图13表明,0min,体系中I2产生量随着H2O2添加浓度的增加而增大,而随之降低.这是由于H2O2是超声/H2O2/KI体系中产生I2的重要氧化剂[式(2)],H2O2添加浓度在10.0~120.0mmol/L范围增加,更多 I-氧化,故超声作用下 I·自由基产生量增大,使得磺胺嘧啶的去除率增加.继续增大H2O2添加浓度至 240.0mmol/L,0min,A460nm无明显变化,即I2产生量无明显增加,且随着反应的进行,反应液的A350nm变化平缓(见图14),即体系中的消耗相对缓慢.由于酸性条件下H2O2与I-的反应较为复杂,一般先产生 HIO等中间氧化物,再进一步氧化I-形成当体系中H2O2添加浓度过大,HIO与过量H2O2反应产生I-[式(7)][21];同时H2O2可直接与反应[式(8)]产生I-[20].I-或与体系中产生的I2直接结合而使得到补充[式(3)],或与I·结合形成·[式(6)],故一定程度抑制了磺胺嘧啶的降解效果.

2.3自由基抑制
为确定超声/H2O2/KI体系降解磺胺嘧啶的活性自由基类型,对磺胺嘧啶初始浓度0.04mmol/L,pH=3.2,功率195W,H2O2、KI添加浓度分别为120.0、3.2mmol/L时,甲醇和甲硫咪唑(MMI)对磺胺嘧啶超声降解的抑制情况,结果如图15所示.
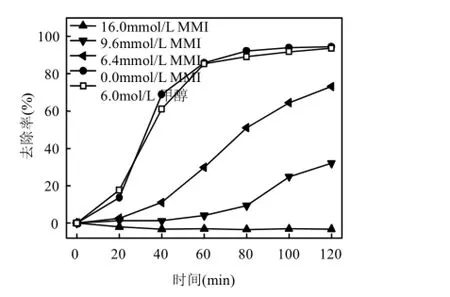
图15 甲醇、甲硫咪唑对超声/H2O2/KI降解磺胺嘧啶的抑制情况Fig.15 Inhibition effect of methanol, methimazole on sulfadiazine degradation in US/H2O2/KI system
图15表明,甲醇(HO·清除剂[20])对超声/ H2O2/KI降解磺胺嘧啶几乎没有影响,说明HO·不是该体系的主要活性物质.甲硫咪唑是碘自由基的清除剂[式(9)~(10)][24].当甲硫咪唑(MMI)的添加浓度分别为 0.0、6.4、9.6mmol/L时,120min,磺胺嘧啶的去除率分别为 94.4%、73.0%和 38.1%.继续增加甲硫咪唑的浓度至16.0mmol/L,磺胺嘧啶的降解完全抑制.因此碘自由基和I·)是超声/H2O2/KI体系降解磺胺嘧啶的主要活性物质.
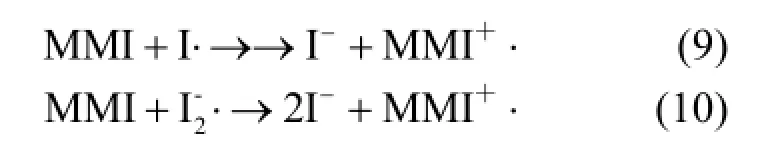
2.4HPLC谱图变化
磺胺嘧啶初始浓度0.04mmol/L, pH=3.2, 超声功率195W, KI、H2O2添加浓度分别为3.2、120.0mmol/L,磺胺嘧啶降解过程中的HPLC谱图变化如图16所示.
图16表明,磺胺嘧啶的保留时间 tR= 8.408min, 随着反应的进行,磺胺嘧啶的峰高不断降低,表明在超声/H2O2/KI体系中磺胺嘧啶发生了降解.同时有4种产物逐渐生成,对应的tR分别为 6.919、7.460、12.826和 15.147min. tR= 5.074min为H2O2的吸收峰.通过峰值增高法分析tR=7.026min为磺胺,表明磺胺为降解产物之一[5,25].其他产物及磺胺嘧啶的降解路径还有待于进一步研究.
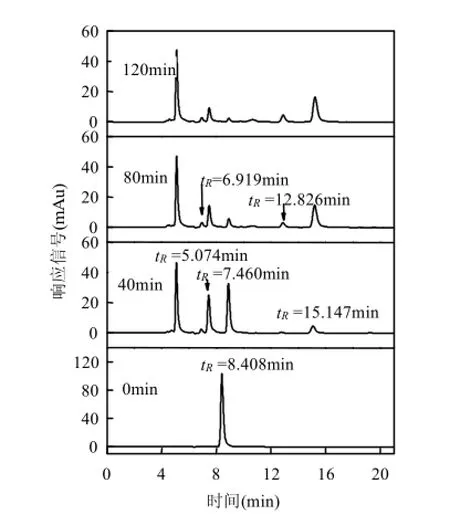
图16 不同时间超声/H2O2/KI体系降解磺胺嘧啶的HPLC图谱Fig.16 HPLC spectrum of sulfadiazine with reaction time in US/H2O2/KI system
3 结论
3.1与单独超声(US)、单独H2O2氧化、US/H2O2、 US/KI、H2O2/KI相比,US/H2O2/KI能够有效降解磺胺嘧啶,这主要是因为I2、在超声作用下迅速发生裂解而产生一系列具有较强活性的碘自由基I·、,在碘(I2、)及其自由基(I·、)共同作用下磺胺嘧啶的降解效果显著提高.
3.2超声/H2O2/KI降解磺胺嘧啶的影响因素表明,溶液初始pH值的影响较大,pH值在2.6~5.2范围,磺胺嘧啶的去除率随 pH值升高而降低;H2O2和KI添加浓度与体系中碘的生成有关.
Wojciech Baran, Ewa Adamek, Justyna Ziemianska, et al. Effects of the presence of sulfonamides in the environment and their influence on human health [J]. Journal of Hazardous Materials,2011,196:1-15.
汤薪瑶,左剑恶,余 忻,等.制药废水中头孢类抗生素残留检测方法及环境风险评估 [J]. 中国环境科学, 2014,34(9):2273- 2278.
薛保铭,杨惟薇,王英辉,等.钦州湾水体中磺胺类抗生素污染特征与生态风险 [J]. 中国环境科学, 2013,33(9):1664-1669.
张婉茹,那广水,陆紫皓,等.北黄海近岸海域磺胺类抗生素及其抗性Escherichiacoli分布 [J]. 应用与环境生物学报, 2014,20(3):401-406.
Garcia-Galan Jesus M, Diaz-Cruz Silvia M, Barcelo Damia. Identification and determination of metabolites and degradation products of sulfonamide antibiotics [J]. Trends in Analytical Chemistry, 2008,27(11):1008-1022.
Temesgen Garoma, Shyam K Umamaheshwar, Alison Mumper. Removal of sulfadiazine, sulfamethizole, sulfamethoxazole, and sulfathiazole from aqueous solution by ozonation [J]. Chemosphere, 2010,79:814-820.
Ana Paula S Batista, Flavio Chiquetto C Pires, Antonio Carlos S C Teixeira.Photochemicaldegradationofsulfadiazine,sulfamerazine and sulfamethazine: Relevance of concentration and heterocyclic aromatic groups to degradation kinetics [J]. Journal of Photochemistry and Photobiology A: Chemistry, 2014,28:640-46.
Wojciech Baran, Ewa Adamek, Andrzej Sobczak, et al. Photocatalytic degradation of sulfa drugs with TiO2, Fe salts and TiO2/FeCl3in aquatic environment—Kinetics and degradation pathway [J]. Applied Catalysis B: Environmental, 2009,90:516-525.
Guo Zhaobing, Zhou Fei, Zhao Yongfu, et al. Gamma irradiation-induced sulfadiazine degradation and its removal mechanisms [J]. Chemical Engineering Journal, 2012,191:256-262.
Evelien De Bel, Colin Janssen, Sanne De Smet, et al. Sonolysis of ciprofloxacin in aqueous solution: Influence of operational parameters [J]. Ultrasonics Sonochemistry, 2011,18:184-189.
魏 红,李 娟,李克斌,等.左氧氟沙星的超声/H2O2联合降解研究[J]. 中国环境科学, 2013,33(2):257-262.
魏 红,李 娟,李克斌,等.CCl4对左旋氧氟沙星超声降解的影响 [J].高等学校化学学报, 2012,33(7):1438-1443.
郭照冰,周 飞,张超智,等.超声降解水中的磺胺嘧啶 [J]. 环境工程学报, 2012,6(9):3143-3147.
Ma Ying-Shih, Sung Chi-Fanga, Lin Jih-Gaw. Degradation of carbofuran in aqueous solution by ultrasound and Fenton processes: Effect of system parameters and kinetic study [J]. Journal of Hazardous Materials, 2010,178:320-325.
Zou Xiaoli, Zhou Tao, Mao Juan, et al. Synergistic degradation of antibiotic sulfadiazine in a heterogeneous ultrasound-enhanced Fe0/persulfate Fenton-like system [J]. Chemical Engineering Journal, 2014,257:36-44.
任一鸣.分子碘催化和促进的有机合成反应研究 [D]. 南京:南京理工大学, 2009.
Hu Meiqin, Wang Yan, Xiong Zhigang, et al. Iodine-sensitized degradation of 2,4,6-trichlorophenol under visible light [J]. Environmental Science and Technology, 2012,46:9005-9011.
NestorJavierBejarano-perez,MarcoFidelSuarez-Herrera. Sonochemical and sonophotocatalytic degradation of malachite green: The effect of carbon tetrachloride on reaction rates [J]. Ultrasonics Sonochemistry, 2008,15:612-617.
John G Rowley, Byron H Farnum, Shane Ardo, et al. Iodide chemistry in dye-sensitized solar cells: Making and breaking I—I bonds for solar energy conversion [J]. The Journal of Physical Chemistry Letters, 2010,1:3132-3140.
Jiman Y, Wonyong C. Iodide-mediated photooxidation of arsenite under 254nm irradiation [J]. Environ. Sci. Technol, 2009,43:3784-3788.
Isao Matsuzaki, Radmilo Simic, Herman A. Liebhafsky. The mechanism of decomposition of hydrogen peroxide by iodine in acid solutions. The rates of associated reactions [J]. Bulletin of The Chemical Society of Japan, 1972,45:3367-3371.
陈肖虎,薛 安,杨善志,等.过氧化氢一硫酸氧化碘离子反应动力学研究 [J]. 过程工程学报, 2009,9(1):181-184.
Milan Melichercik, Anna Olexova, Ludovit Treindl. Kinetics of the oxidation of iodine by hydrogen peroxide catalyzed by MoO42-ions [J]. Journal of Molecular Catalysis A:Chemical,1997,127:143-47.
Taylor J J, Willson R L, Kendall-Taylor P. Evidence for direct interactions between methimazole and free radicals [J]. FEBS LETTERS, 1984,176(2):337-340.
Premasis Sukul, Marc Lamshoft, Sebastian Zuhlke, et al. Photolysis of14C-sulfadiazine in water and manure [J]. Chemosphere,2008,71:717-725.
Sulfadiazine degradation through iodine radicals excited by ultrasound.
WEI Hong1*, YANG Xiao-yu1, MIN Tao1,LI Ke-bin2(1.State Key Laboratory Base of Eco-Hydraulic Engineering in Arid Area, Xi'an University of Technology,Xi'an 710048, China;2.Key Laboratory of Synthetic and Natural Functional Molecule Chemistry of Ministry of Education, School of Chemistry and Material Science, Northwest University, Xi'an 710069, China).
China Environmental Science, 2015,35(11)Ţ 3288~3295
The ultra-degradation of sulfadiazine (Sulfadiazine, SD) enhanced by molecular iodine under ultrasound/ H2O2/KI system was investigated. The experimental parameters such as initial solution pH, KI and H2O2adding concentration were discussed. The main active species in ultrasound/H2O2/KI system were evaluated by adding methimazole, the scavenger of iodine radicals. The experimental results indicated that SD degradation was enhanced significantly under the ultrasound/H2O2/KI system. The SD removal efficiency decreased with the initial pH value, and was influenced considerably by the concentration of H2O2and KI. The radical inhibition experiments indicated that I· andwere the main active species contributed to SD degradation. HPLC analysis showed that four intermediate products formed during SD degradation under ultrasound/H2O2/KI system, and one was sulfanilamide.
iodine;iodine radicals;ultrasonic;sulfadiazine;methimazole
X52
A
1000-6923(2015)11-3288-08
2015-04-26
陕西省教育厅科学研究计划项目(2013JK0881);陕西省教育厅重点实验室项目(13JS067);陕西省水利科技项目(2013slkj-07);西安理工大学创新基金(106211302);环境工程国家重点学科培育学科项目(106-x12045)
* 责任作者, 副教授, weihong0921@163.com
魏 红(1977-),女,陕西大荔人,副教授,博士,主要从事有机污染治理及水资源保护方面的研究.发表论文20余篇.
