聚环氧琥珀酸及其衍生物的缓蚀性能及缓蚀机理
2015-08-22柳鑫华王文静赵新强佟欣佳丁云飞苏红
柳鑫华,王文静,赵新强,佟欣佳,丁云飞,苏红
(1河北工业大学化工学院,天津300130;2河北联合大学轻工学院,河北 唐山 063000; 3河北联合大学化工学院,河北 唐山 063009)
引 言
水是人类赖以生存的重要资源,而我国是世界上水资源严重缺乏的国家之一。水成了制约我国经济发展的一个瓶颈,为了实现国民经济的可持续发展必须合理节约用水,特别是合理节约工业用水。
工业用冷却水占工业总用水量的60%~80%,因此节约循环冷却水的用量,提高水的利用率,减少水的排放是节水的关键环节[1]。目前大多数工业循环冷却水是敞开式的系统,在冷却塔中的水随着循环使用、蒸发,矿物质浓度会逐渐增加,这样会加剧设备的结垢与腐蚀。而减少腐蚀与结垢的最简单方法就是绿色阻垢缓蚀剂的使用。
聚环氧琥珀酸(PESA)是国际公认的一种无磷、非氮且具有良好生物降解性的新型合成高分子水处理剂,兼有缓蚀、阻垢双重功能,同时不会引起水体的富营养化,是环境友好型绿色水处理剂,近年来备受关注[2]。而与传统的含磷缓蚀阻垢剂相比,药剂用量较大,增加了成本,从而影响了聚环氧琥珀酸的应用。为了拓宽聚环氧琥珀酸的应用范围,本研究就聚环氧琥珀酸及其硫脲改性的衍生物的缓蚀性能及其缓蚀机理进行了探讨。
1 实验部分
1.1 试剂、材料和仪器
试剂、材料:聚环氧琥珀酸(PESA),自制;聚环氧琥珀酸衍生物(CSN-PESA),自制;试片:标准A3碳钢挂片Ⅱ型,表面积20 cm2,高邮市秦邮仪器化工有限公司;腐蚀介质:自来水。
仪器:数显恒温水浴锅;S-250型扫描电子显微镜,CHI660D电化学工作站。
1.2 PESA与CSN-PESA的结构及制备
聚环氧琥珀酸及其衍生物的结构式为
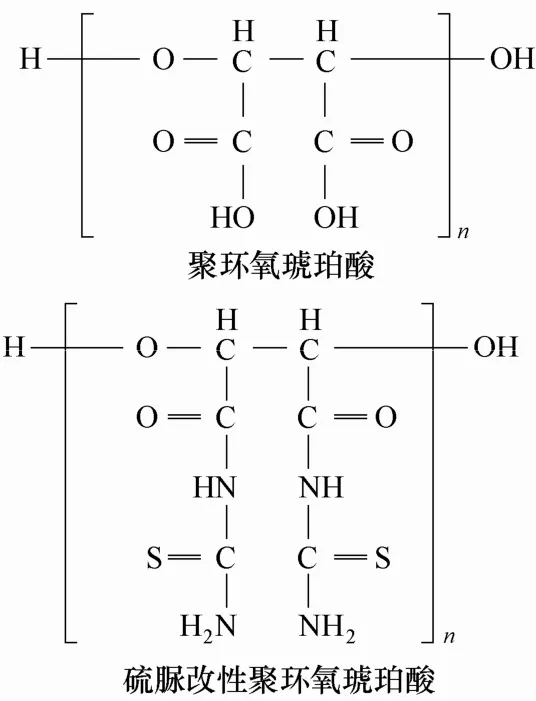
聚环氧琥珀酸及其硫脲改性的衍生物的制备:首先将马来酸酐通过环化,在温度70℃、时间1.5 h、pH=5、双氧水用量12 ml条件下制得环氧琥珀酸;其次通过聚合,在反应温度90℃、聚合时间2.5 h、引发剂用量0.8 g、pH=12条件下制得聚环氧琥珀酸;最后用硫脲改性,在pH=7、时间1.5 h、温度85℃、质量比r(M)=8:4条件下得到硫脲改性的聚环氧琥珀酸衍生物(CSN-PESA)。红外光谱和核磁共振谱证明了聚环氧琥珀酸及其硫脲改性的衍生物结构的存在,在PESA的红外谱图上存在波数分别为1115.37、1614.01 cm-1的醚键和羧基中的C—O—C开环对称伸缩振动,在CSN-PESA的红外谱图上还存在波数为3277.03 cm-1的酰胺键中的N—H伸缩振动;在PESA的核磁碳谱图上存在化学位移δ为170~180、81~83的羧基、开环醚键的碳;在CSN-PESA的核磁碳谱图上存在化学位移δ为170~180、81~83、181的羧基、开环醚键的碳和硫脲中的碳。通过黏度法[3]测出了聚环氧琥珀酸及其硫脲改性的衍生物的相对分子质量,MPESA=465.28, MCSN-PESA=581.02。
1.3 静态缓蚀实验
参照GB 10124—1998进行聚环氧琥珀酸(PESA)及其衍生物(CSN-PESA)失重腐蚀实验,其保护效率用腐蚀速率b和缓蚀效率W(质量分数)表示。
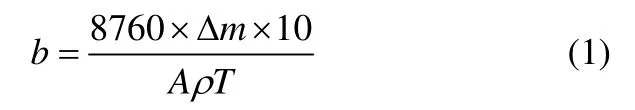
式中,b为腐蚀速率,Δm为腐蚀前后的质量差,A为试片面积,ρ为试片密度,T为实验时间。
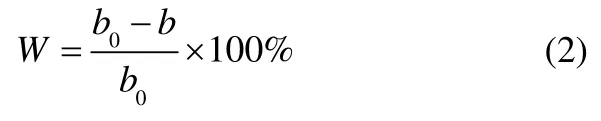
式中,b0为未加缓蚀剂时金属的腐蚀率,mm·a-1;b为加缓蚀剂后金属的腐蚀率,mm·a-1。
1.4 电化学测试
极化曲线和阻抗谱用电化学工作站CHI660D测试,测试装置:参比电极为饱和甘汞电极,辅助电极为铂电极,工作电极为A3碳钢。动电位扫描速率范围为-150~+150 mV(vsEcorr),扫描速率0.5 mV·s-1;电化学阻抗图谱测试采用频率为100 kHz~10 mHz、幅值为±5 mV的正弦波。
1.5 腐蚀试样的表征
采用S-250型扫描电子显微镜对腐蚀试样进行SEM表面分析。将腐蚀试样粘在贴有双面胶的试样台上,喷金后置于扫描电子显微镜下观察,加速电压为20 kV。
1.6 量子化学计算
聚环氧琥珀酸及其衍生物分子的构型由Material Studio4.0软件包中的Visualizer 模块构建,利用DMol3模块,使用密度泛函数理论(DFT)中的广义梯度近似法(GGA/PBE),在DND基组(双ξ数值基组,在非氢原子上加极化d函数)水平上对两种药剂分子进行优化电子计算,然后做频率分析,保证所得的结构都为势能面上的极小点(无虚频);在同一基组水平上计算药剂分子的最高和最低轨道分布情况以及量子化学参数,用于分析药剂分子结构与缓蚀机理之间的关系[4-7]。
2 结果与讨论
2.1 缓蚀性能
2.1.1 失重法 从表1中两种药剂的不同浓度的腐蚀速率和缓蚀速率可知:两种药剂随浓度的加大缓蚀性能增强。聚环氧琥珀酸衍生物的缓蚀速率比聚环氧琥珀酸大,而且当药剂浓度为150 mg·L-1时,CSN-PESA的腐蚀速率(0.1254 mm·a-1)基本上达到国家规定的腐蚀速率标准(0.125 mm·a-1),而PESA的腐蚀速率(0.1339 mm·a-1)与国家规定的标准相差很大。因此,聚环氧琥珀酸衍生物的缓蚀性能优于聚环氧琥珀酸。另外,与文献[3,8]相比,聚环氧琥珀酸衍生物无论是缓蚀性能还是缓蚀阻垢剂的绿色化都优于传统的缓蚀阻垢剂。
2.1.2 电化学法
(1)不同CSN-PESA浓度的极化曲线 图1和表2是A3碳钢在自来水中的动电位极化曲线及其电化学参数。从图1和表2可以看出,加入CSN- PESA药剂后,随着药剂浓度的加大,腐蚀电流密度(从0.02860 mA·cm-2到0.01876 mA·cm-2)明显减小,体系的自腐蚀电位(从-0.7520 V到-0.7910 V)发生负移,阴、阳极的塔菲尔斜率也显著发生变化,而且阳极变化较大,这证明在自来水 中硫脲改性的聚环氧琥珀酸抑制了碳钢的腐蚀,是以抑制阳极为主的混合型缓蚀剂[9]。而且随硫脲改性的聚环氧琥珀酸浓度的增大缓蚀率增加(从5.33%到37.90%),这与失重法是一致的。
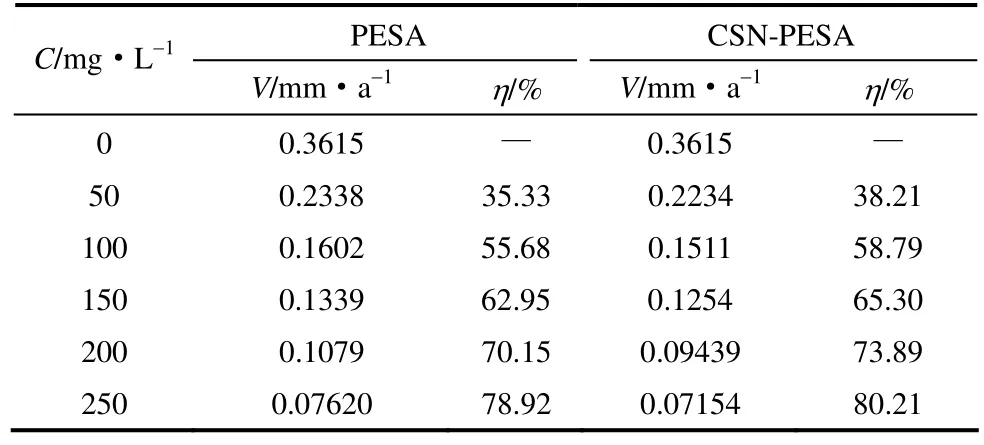
表1 聚环氧琥珀酸及其衍生物不同浓度时的 腐蚀速率和缓蚀效率 Table 1 Corrosion rate and inhibition rate of PESA and CSN-PESA in different concentrations
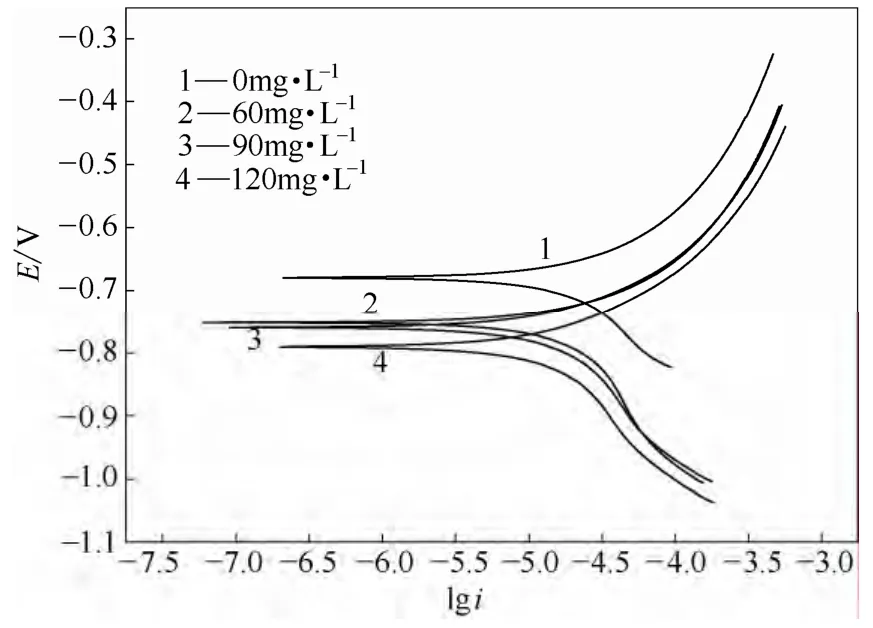
图1 碳钢在添加不同CSN-PESA 浓度的 自来水中的极化曲线 Fig.1 Potentiodynamic polarization curves for carbon steel in tap-water with various concentrations of CSN-PESA
(2)PESA与CSN-PESA的极化曲线 由图2和表3可知:加入PESA和CSN-PESA的极化曲线与空白体系相比,自腐蚀电流都减小,CSN-PESA的自腐蚀电位负移较大,PESA的自腐蚀电位变化较小;阳极和阴极的斜率都有一定程度的变化,PESA的阴极变化较大而阳极变化较小,CSN-PESA的阴极、阳极都有变化,但总的来说PESA和CSN-PESA对阴极、阳极都有一定程度的抑制作用,说明PESA为抑制阴极为主的缓蚀剂,CSN-PESA为混合型缓蚀剂[8]。总之,CSN-PESA的自腐蚀电流密度(0.01876 mA·cm-2)比PESA(0.02004 mA·cm-2)明显减小,自腐蚀电位明显负移,PESA和CSN-PESA的缓蚀效率分别为33.67%和37.90%,可以证明此改性产物比PESA的缓蚀性能增加,极化曲线的测试进一步证明硫脲改性的聚环氧琥珀酸衍生物拓宽了聚环氧琥珀酸的应用范围。

表2 极化曲线电化学参数 Table 2 Electrochemical parameters of polarization curve
(3)不同CSN-PESA浓度的阻抗图谱 图3为40℃下A3碳钢在加有不同浓度CSN-PESA缓蚀剂的自来水中的阻抗图谱,图4为阻抗图谱的对应等效电路。用阻抗图谱评价药剂的缓蚀能力通常用阻抗图中电荷传递电阻Rct、双电层电容Cdl以及弥散系数n参数描述,Rct值表示电化学反应的快慢,Cdl表示药剂分子在金属表面的吸附特性,n越趋近于1 双电层越接近理想电容。从图3和表4可知:随着 药剂浓度的增大,Rct增大,Cdl逐渐减小,n增加,说明腐蚀反应减慢,因此缓蚀率增大[9],这与失重法、极化曲线的结果一致。

图2 碳钢在添加PESA和CSN-PESA的 自来水中的极化曲线 Fig.2 Potentiodynamic polarization curves for carbon steel in tap-water with PESA and CSN-PESA
(4)PESA与CSN-PESA的阻抗图谱 40℃下A3碳钢在加有PESA和CSN-PESA缓蚀剂在自来水中的阻抗图谱如图5所示,交流阻抗的等效电路同图4。从图5、表5可知:硫脲改性的聚环氧琥珀酸衍生物的电层电容逐渐降低,弥散指数逐渐增大,双电层越来越接近理想电容;电荷传递电阻逐渐增大,在金属电极表面的腐蚀反应减慢。这都进一步 说明硫脲改性的聚环氧琥珀酸衍生物在A3碳钢表面的吸附膜比聚环氧琥珀酸在碳钢表面的吸附膜致密性增加,缓蚀效果增强。
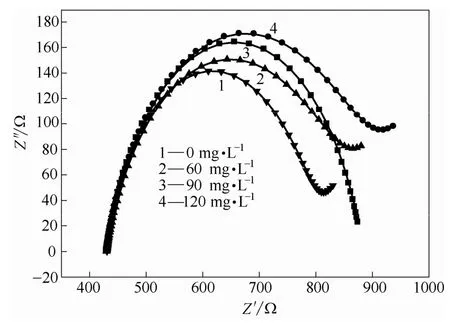
图3 改变CSN-PESA浓度时碳钢在 自来水中的Nyquist图谱 Fig.3 Nyquist plots of impedance spectra of carbon steel in tap-water with various concentrations of CSN-PESA

图4 等效电路 Fig.4 Equivalent circuit for EIS of carbon steel
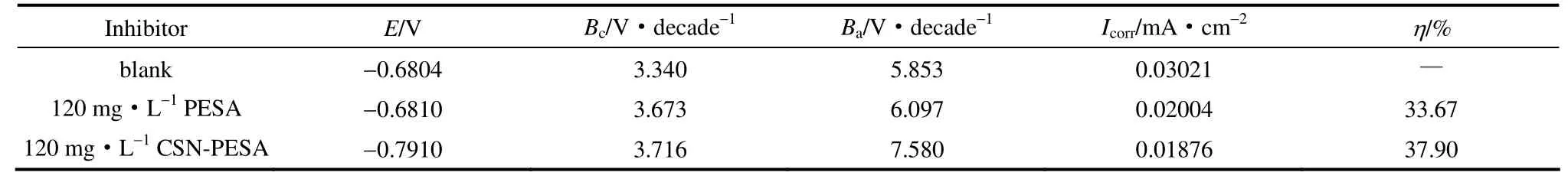
表3 极化曲线电化学参数 Table 3 Electrochemical parameters of polarization curve

表4 交流阻抗电化学参数 Table 4 Electrochemical parameters of Ac impedance

表5 交流阻抗电化学参数 Table 5 Electrochemical parameters of Ac impedance

图5 碳钢在添加 PESA 和 CSN-PESA 的 自来水中的 Nyquist 图谱 Fig.5 Nyquist plots of impedance spectra of carbon steel in tap-water with PESA and CSN-PESA
2.2 吸附性能
吸附热力学是研究缓蚀剂缓蚀性能的一种理论分析方法,可以通过Langmuir、Fremkin、Temkin和Freundlich等温式拟合吸附等温线,从而达到定量研究药剂在设备表面吸附达到平衡时药剂浓度与吸附量的关系,从中获得相关物理量,可以推测缓蚀剂缓蚀性能的大小。
缓蚀剂在设备表面的作用关系可表示如下

式中,Org(ads)和Org(sol)分别表示吸附在设备表面上和在溶液中的药剂分子,H2O(ads)和H2O(sol)分别表示吸附在设备表面上和在溶液中的水分子,x表示药剂分子取代水分子的比例数。
本研究利用失重法得出的数据计算缓蚀剂分子在设备表面覆盖率θ,将缓蚀率作为θ代入Langmuir吸附等温式进行拟合,发现吸附等温式与实验结果吻合较好。
其吸附等温式为

式中,C是缓蚀剂浓度,mol·L-1;θ是表面覆盖率;K是吸附平衡常数。
由式(3)可以看出,Langmuir吸附等温模型中C对C/θ作图呈直线关系。作C与C/θ的关系图(图6),通过计算机对缓蚀剂浓度和覆盖率进行线性回归,相关的参数列于表6。

图6 碳钢在不同浓度的CSN-PESA自来水中的 Langmuir吸附等温线 Fig.6 Langmuir adsorption isotherm on carbon steel in different concentrations of CSN-PESA in tap-water

表6 自来水中缓蚀剂在碳钢表面的热力学参数 Table 6 Thermodynamic parameters of inhibitor on carbon steel in tap-water environment
从图6和表6可知:硫脲改性的聚环氧琥珀酸衍生物在自来水中线性相关性较好,其线性相关系数接近1,直线的斜率有一定的偏差。这表明缓蚀剂分子在碳钢表面的吸附基本符合Langmuir吸附等温式,这与前面的阻抗模拟n值相符。
再根据式(4)[10]计算出吸附的Gibbs自由能ΔGads= -33.49 kJ·mol-1。

式中,55.5为水分子浓度,mol·L-1。
2.3 腐蚀动力学
为了进一步讨论缓蚀剂在自来水中对A3碳钢的缓蚀作用,对腐蚀反应的动力学进行研究。根据Arrhenius[13]方程式可得

式中,v为腐蚀速率,R为标准热力学常数,T为热力学温度,Ea为反应表观活化能,A为反应指前因子。
通过计算机对腐蚀速率的对数(lnv)和温度的倒数(1/T)进行线性回归,得到直线的斜率和截距,分别计算得到添加和不添加缓蚀剂时A3碳钢的溶解反应的活化能。
从图7可知:在自来水中lnv和1/T的线性相关性较好,线性相关系数都接近1。根据直线斜率求得表观活化能,列于表7。从表7可知,加入CSN-PESA缓蚀剂,腐蚀过程的反应活化能增大。这可能是在加入缓蚀剂后CSN-PESA分子吸附到钢表面反应的活性点上,增大了反应能垒,故活化能有所增大,降低了金属表面的腐蚀行为,从而缓蚀 率增大。
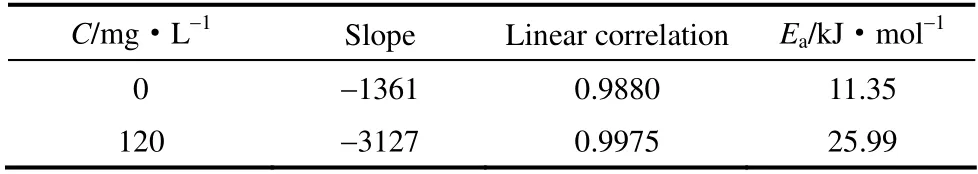
表7 碳钢在CSN-PESA溶液中的表观活化能 Table 7 Activation energies of carbon steel in solution of CSN-PESA of tap-water
2.4 缓蚀机理
2.4.1 分子轨道理论 前线轨道理论[14-16]指出:有机物的最高占有轨道(HOMO)和最低空轨道(LUMO)轨道密度分布决定着反应活性和反应机理。EHOMO表示分子供电子能力。最高占有轨道的最高能量值越大,电子越容易在金属表面发生作用;反之,最高占有轨道的最高能量值越小,电子越稳定,越不容易与金属发生作用。ELUMO表示分子接受电子的能力。最低空轨道的最高能量值越小,电子进入轨道后体系能量降低得越多,该分子接受电子的能力越强。二者的能量差可以证明药剂分子在金属表面化学反应的强弱。从表8和图8、图9可知:PESA和CSN-PESA的EHOMO分别为-0.2063 eV、-0.1862 eV,说明CSN-PESA的供电子能力比PESA增强;PESA和CSN-PESA的ELUMO分别为-0.0807 eV、-0.1324 eV,说明CSN-PESA的接受电子能力比PESA增强。ΔE为分子的最低轨道能量和最高轨道能量之差,表示缓蚀剂分子在金属表面的反应活性。PESA和CSN-PESA的ΔE值分别为0.1256 eV和0.0538 eV,表明CSN-PESA在金属表面的吸附能力比PESA增强,主要是因为CSN-PESA含有O、S、N等杂原子,而轨道密度主要分布在这些原子附近[17-20]。因此CSN-PESA的缓蚀性比PESA增强。

图7 加有CSN-PESA的溶液中腐蚀活化能的线性回归 Fig.7 Activation energy of carbon steel in different concentrations of CSN-PESA of tap-water

表8 聚环氧琥珀酸及其衍生物的最高占有轨道和 最低空轨道能量参数 Table 8 Energy parameter of HOMO and LUMO of PESA and CSN-PESA

图8 聚环氧琥珀酸及其衍生物最高空轨道分布 Fig.8 Distribution of HOMO on PESA and CSN-PESA
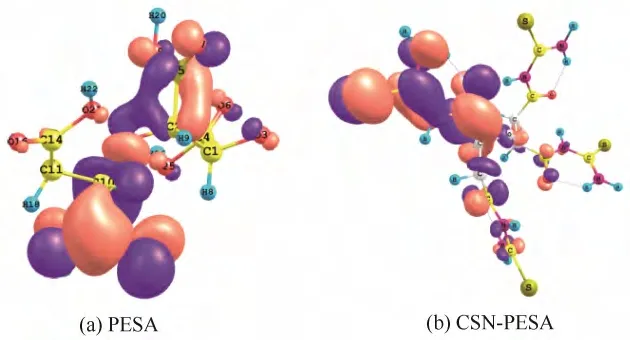
图9 聚环氧琥珀酸及其衍生物最低空轨道分布 Fig.9 Distribution of LUMO on PESA and CSN-PESA
2.4.2 试片的SEM的缓蚀分析结果 图10(a)为实验前的新碳钢腐蚀试片,试片表面可见明显的机械划痕;图10(b)是40℃空白水中碳钢腐蚀72 h后的碳钢试片的腐蚀照片。由SEM照片可以看出碳钢表面明显出现腐蚀坑,说明没加缓蚀剂的体系中的碳钢试片受到的腐蚀非常严重。图10(c)为 添加了PESA水对碳钢腐蚀72 h后的表面状态;图10(d)为添加了CSN-PESA水对碳钢腐蚀72 h后的表面状态。由图可以看出,经缓蚀剂处理后的试样表面原有的机械划痕纹变得模糊,碳钢表面腐蚀产物变少,整体表面腐蚀状况明显好于空白,加有CSN-PESA的碳钢表面形成的吸附膜比PESA均匀、致密,表明CSN-PESA缓蚀剂在金属表面形成了保护膜,对水中的碳钢进行了有效的保护[21]。
3 结 论
(1)PESA和CSN-PESA在自来水中很好地减缓了对A3碳钢的腐蚀,而且随着药剂浓度的增大,腐蚀速率逐渐减小,缓蚀保护作用逐渐增强,硫脲改性的聚环氧琥珀酸衍生物的缓蚀率大于聚环氧琥珀酸。

图10 40℃未加和加有阻垢缓蚀剂的碳钢试片形貌图 Fig.10 SEM micrograms of carbon steel in increasing scale inhibitor water or not
(2)电化学极化曲线和阻抗图谱进一步证明PESA和CSN-PESA对阳极、阴极有一定的抑制作用。
(3)PESA和CSN-PESA在自来水中对A3碳钢表面的缓蚀作用是物理吸附和化学吸附共同作用的结果,在A3碳钢表面的吸附作用基本符合Langmuir吸附等温式。加入CSN-PESA后的表观反应活化能是空白水的2倍。
(4)从量子化学计算可知:CSN-PESA最高占有轨道能量与PESA最高占有轨道能量相比降低,说明CSN-PESA的供电子能力增强;CSN-PESA最低空轨道能量与PESA最低空轨道能量相比升高,说明CSN-PESA的接受电子能力增强。这说明CSN-PESA的供电子能力、接受电子能力比PESA增强。ΔE的变化降低,说明CSN-PESA比PESA的缓蚀率增大。从电镜扫描的结果也可以得知:碳钢表面腐蚀孔变小,整体表面腐蚀状况明显好于空白,表明缓蚀剂在金属表面形成了保护膜。
[1] Wang Xuzhen(王旭珍), Meng Yanfeng (蒙延峰), Guo Zhenliang(郭振良), Tang Qinghua(唐清华).Progress on greening study of the corrosion and scale inhibitors for circulating cooling water [J].Techniques and Equipment for Environmental Pollution Control(环境污染治理技术与设备), 2003, 4(4): 50-54
[2] Lei Wu(雷武), Wang Fengyun(王风云), Xia Mingzhu(夏明珠), Wang Fenghe(王风贺).Synthesis and its scale inhibition effect of green scale inhibitor polyepoxysuccinic acid [J].Journal of Chemical Industry and Engineering (China) (化工学报), 2006, 57(9): 2207-2213
[3] Zhang Jian(张建).Research on synthesis of PESA and performance of its combinated scale inhibitors[D].Lanzhou: Lanzhou Jiaotong University, 2007
[4] Taner A, Kandemirli F, Ebenso E E, et al.Quantum chemical studies on the corrosion inhibition of some sulphonamides on mild steel in acidic medium [J].Corrosion Science, 2009, 51(1): 35-47
[5] Gómez B, Likhanova N V, Domínguez-Aguilar M A, et al.Quantum chemical study of the inhibitive properties of 2-pyridyl-azoles [J].Journal of Physical Chemistry B, 2006, 110(18): 8928-8934
[6] Costa J M, Lluch J M.The use of quantum mechanics calculations for the study of corrosion inhibitors [J].Corrosion Science, 1984, 24(11/12): 929-933
[7] Fang J, Li J.Quantum chemistry study on the relationship between molecular structure and corrosion inhibition efficiency of amides [J].Journal of Molecular Structure: TheoChem., 2002, 593(1/2/3): 179-185
[8] Jiang Shouhong(蒋守红), Xu Jiewu (徐杰武).Studies on the corrosion inhibition performance and mechanism of organic phosphonate on the carbon steel [J].Shandong Chemical Industry(山东化工), 2013, 12(42): 9-11
[9] Wang Qingyun(王清云), Tong Yongchun(佟永纯),Wang Yongsheng(王永生), Fu Rugang(付如刚), Zhen Wenlong(甄文龙).Inhibition effect of ciprofloxacin on low carbon steel in H2SO4solutions [J].Acta Hexi University(河西学院学报), 2012, 28(2): 77-82
[10] Zhang Shengtao (张胜涛), Tao Zhihua (陶志华), Li Weihua (李伟华), Deng Junying (邓俊英), Hou Baorong(侯保荣).A corrosion inhibition of mild steel by noveltriazole compound in 1 mol·L-1HCl solution [J].J.Chin.Soc.Corros.Prot.(中国腐蚀与防护学报), 2009, 29(6): 487-492
[11] Hu Songqing(胡松青), Hu Jianchun(胡建春), Gao Yuanjun(高元军), Jia Xiaolin(贾晓林), Guo Wenyue(郭文跃).Corrosion inhibition and adsorption of laury-l imidazolines for Q235 steel [J].CIESC Journal(化工学报), 2011, 62(1): 47-155
[12] Yurt A, Ulutas S, Dal H.Electrochemical and theoretical investigation on the corrosion of aluminium in acidic solution containing some Schiff bases [J].Applied Surface Science, 2006, 253(2): 919-925
[13] Wang Xianqun(王献群), Liu Ruiquan(刘瑞泉), Zhu Liqin(朱丽琴).Inhibition action and adsorption behaviors of BIT, BIOHT and BIM MT on copper in alkaline medium [J].Acta Phys.-Chin.Sin.(物理化学学报), 2007, 23(1): 21-26
[14] Bereket G, Hur E.Quantum chemical studies on some imidazole derivatives as corrosion inhibitors for iron in acidic medium [J].J.Mol.Struct.:Theochem., 2002, 578(1/2/3): 79-88
[15] Chu Yuting(褚玉婷), Chen Yu(陈 煜), Shi Wenyan(石文艳), Dai Linhong(戴林宏), Lü Zhimin(吕志敏), Xia Mingzhu(夏明珠), Lei Wu(雷武), Wang Fengyun(王风云).Quantum chemistry studies on mechanism of corrosion inhibition for amido phosphonic acids [J].Journal of Yancheng Institute of Technology: Natural Science Edition(盐城工学院学报:自然科学版), 2010, 23(1): 36-40
[16] Zhang Jun(张军), Hu Songqing(胡松青),Wang Yong(王勇).Theoretical investigation on inhibition, mechanism of l-(2-hydroxyethyl) -2- alkylimidazoline corrosion inhibitors [J].Acta Chim.Sin.(化学学报), 2008, 66(22): 2469-2475
[17] Hu Songqing(胡松青), Hu Jianchun(胡建春), Shi Xin(石鑫), Jia Xiaolin(贾晓林), Guo Wenyue(郭文跃).Corrosion inhibition and adsorption of 1-(2-phenylthioureaethyl)-2-phentadecylimidazoline for Q235 steel [J].Acta Petrolri Sinica: Petroleum Processing Section(石油学报:石油加工), 2011, 27(4): 593-600
[18] Chu Yuting(褚玉婷), Lü Zhimin(吕志敏), Xia Mingzhu(夏明珠), Lei Wu(雷武), Wang Fengyun(王风云).Quantum chemistry studies on amido-methylene inhibitors [J].Computers and Applied Chemistry(计算机科学与应用), 2008, 25(11): 1397-1400
[19] Zheng Xingwen(郑兴文), Gong Min(龚敏), Wang Ying(王莹), Jiang Chunmei(姜春梅).Corrosion inhibition of methionine for carbon steel in sulfuric acid solution [J].Chemical Research and Application (化学研究与应用), 2011, 23(12): 1589-1594
[20] Khalil N.Quantum chemical approach of corrosion inhibition [J].Electrochim.Acta, 2003, 48(18): 2635-2640
[21] Tao Zhihua(陶志华), Zhang Shengtao(张胜涛), Li Weihua(李伟华), Hou Baorong(侯保荣).Adsorption and corrosion inhibition behavior of mild steel by one derivative of triazole-phenylamide in acid solution [J].Journal of Chongqing University(重庆大学学报), 2010, 23(11): 89-95
