青防肿痛外敷散局部组织药动学研究
2015-08-21郭玉岩孟令超吕邵娃李永吉
郭玉岩,孟令超,吕邵娃,王 锐,李永吉
(黑龙江中医药大学药学院,哈尔滨150040)
盐酸青藤碱为防己科防己属植物青风藤主要成分-青藤碱的盐酸盐,具有显著的抗炎、镇痛、抗风湿等作用,主要用于风湿及类风湿性疾病的治疗[1].但由于其具有释放组胺作用而致皮疹、胃肠道不适等副作用,使其体内给药受到限制[2].本文以盐酸青藤碱为主要成分,加适宜辅料,制备成经皮给药制剂(盐酸青藤外敷散)[3-4],将本产品直接作用于患处,增加炎性关节局部药物质量浓度、提高疗效的同时,降低药物的毒副作用[5].由于局部给药制剂药物吸收入血量较少、且很难客观评价药物在局部病灶组织的吸收情况,为此本文对盐酸青藤外敷散局部贴敷给药后在局部炎性组织的吸收情况进行研究,总结盐酸青藤外敷散在局部病变部位局部药动学行为,用以评价盐酸青藤碱局部经皮给药制剂的性能.
1 实验材料
1.1 仪器与试剂
主要仪器有Waters 2690高效液相色谱仪(美国Waters公司);组织匀浆机 MINI-16(Bead Beater公司);D-37520超速低温离心机(德国Heraeus公司)
盐酸青藤外敷散(黑龙江中医药大学药剂学实验室自制);青藤碱对照品(中国药品生物制品检定所,批号:0774-201206);色谱纯甲醇、乙腈(美国,Dikma);角叉菜胶(美国,Sigma);其他试剂为市售分析纯.
1.2 实验动物
Wistar大鼠,雌雄各半,体重180~220 g,合格证号:P00102009,由黑龙江中医药大学实验动物中心提供,(生产许可证SCXK黑2008004).
2 方法与结果
2.1 色谱条件
Kromasil C18色谱柱(4.6 mm ×250 mm);流动相为磷酸缓冲盐(0.01 mol/L磷酸氢二钾溶液,加1‰三乙胺,磷酸调pH值3.0)-甲醇(80∶20);检测波长为265 nm;流速为1.0 mL/min,柱温30℃,进样量 10 μL.
2.2 对照品溶液制备
取经105℃干燥至恒重的青藤碱对照品约3.0 mg,精密称定 2.82 mg,置 100 mL 量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得.
2.3 组织样品的制备及处理
取健康的Wistar大鼠,左后足底皮下注射1%角叉菜胶(0.l mL/只),30 min后,将青防肿痛外敷散贴于造模足跖处,固定.24 h后,将其给药足剪下置于组织匀浆管中,依次加入氯化钠溶液3 mL及甲醇溶液2 mL匀浆3次,离心.取上清液置25 mL量瓶中,甲醇溶液定容,离心5 min(转速5 000 r/min),取上清液5 mL置10 mL量瓶中,用甲醇定容,离心,取上清液滤过,进样测定即可.
2.4 方法学验证
1)专属性考察
按比例加入有关组织及相关辅料,按“2.1.3”制成相当于供试品质量浓度的空白溶液,经高效液相色谱法测定,结果表明辅料、试剂均无干扰,专属性良好.
2)精密度试验
取对照品溶液10 μL连续进样6次,测定其峰面积,计算偏差.RSD为0.58%,精密度良好.
3)最低检测限、定量限
精密称取青藤碱对照品2.5 mg,甲醇定容至25 mL,取1 mL定容至10 mL逐级稀释,按照“2.1.1”项下色谱条件进样测定,得检测限为 0.8 μg/mL,定量限为 2.5 μg/mL.
4)标准曲线
精密称取青藤碱对照品7.05 mg,置25 mL量瓶中,加甲醇溶解并稀释至刻度,作为储备液(质量浓度为 0.282 mg/mL).取 1、2、4、8 mL 分别置100 mL量瓶中,同时再取1、2 mL置于10 mL量瓶中,加甲醇定容至刻度.得质量浓度分别为0.002 82、0.005 64、0.011 28、0.022 56、0.028 2、0.056 4 mg/mL的对照品溶液,按照1.2.1项下色谱条件进样10 μL,测定峰面积.以对照品质量浓度(x)对峰面积(y)进行线性回归,得回归方程为:y=8×106+1 315.4(R=0.999 9),结果表明在 0.002 82~0.056 4 mg/mL范围内,线性关系良好.
5)准确度
精密称取青藤碱对照品约7.1 mg,置10 mL量瓶中,加甲醇使其溶解并稀释至刻度,作为储备液.分别精密移取储备液各1 mL及称取适量供试品,共同放置于已有剪碎的大鼠足部的匀浆管中,共9份.按“2.1.3”项下方法处理,使质量浓度为测定质量浓度的80%、100%、120%各3份.进样测定,测得回收率为100.6%在98% ~102%范围内,RSD为1.9%,证明回收率良好.
6)样品稳定性
按“2.1.3”方法制备供试品,分别放置 0、2、4、8、10、12 h,测定其峰面积,计算标准偏差,结果RSD为1.25%,样品稳定性良好.
2.5 青防肿痛外敷散局部药动学研究
Wistar大鼠80只,体重180~220 g,雌雄各半,实验前 12 h禁食不禁水.将大鼠按“2.1.3”项下方法给药,每天换药1次,每天处死4只,连续定时取材20 d,测定每天药物的吸收情况.采用PKSolver药动学软件获得相关药代动力学参数及吸收曲线;AUC0-t为梯形法计算值,Cssmax、Cmin为实测值,平均稳态血药质量浓度(Cssav)为根据公式Cssav=AUC0-t/t计算所得,稳态谷质量浓度(Cssmin)为实测的4个谷质量浓度的平均值,波动度(DF)为根据公式DF(%)=(Cssmax- Cssmin)/Cssav×100%计算所得.用SPSS 18.0进行成组t检验的对照分析.研究结果见表1、2,图1、2.
表1 局部吸收药量测定结果(±S)
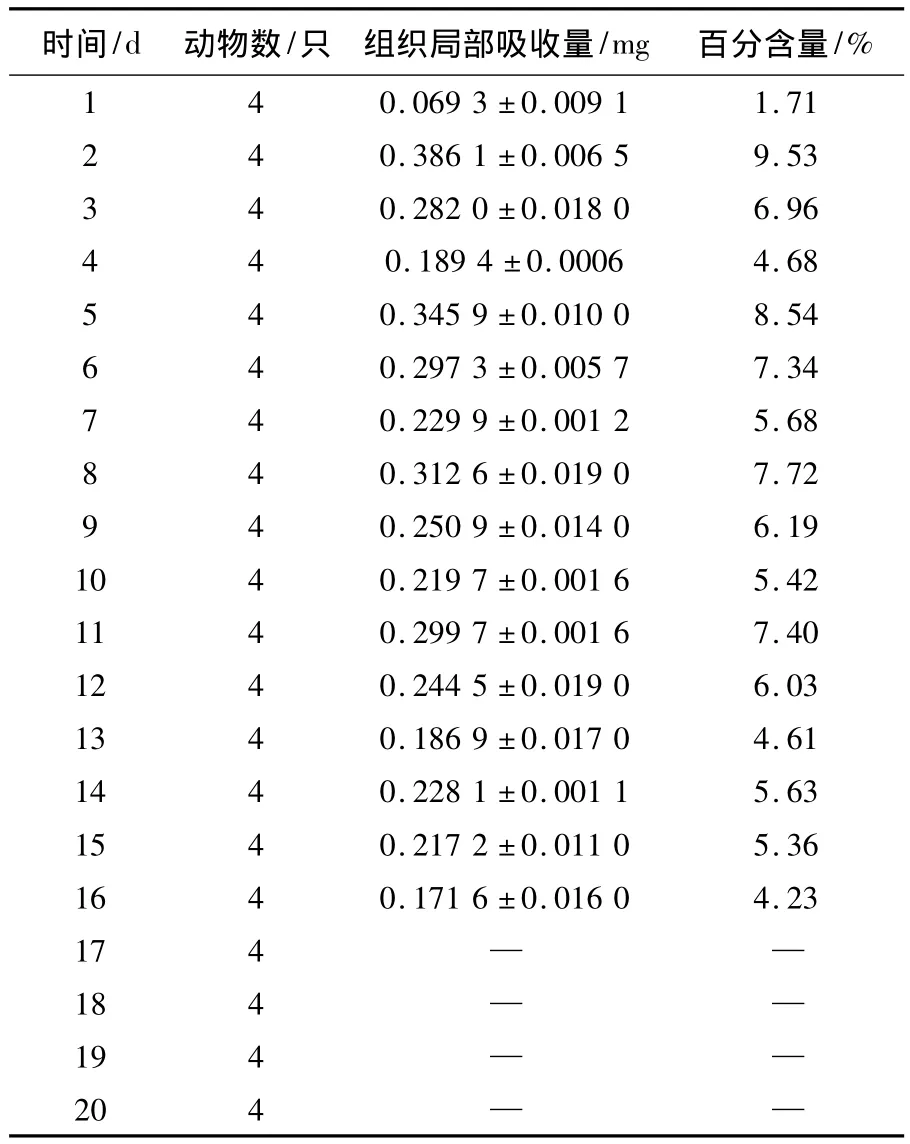
表1 局部吸收药量测定结果(±S)
注:“—”代表未检出
时间/d 动物数/只 组织局部吸收量/mg 百分含量/%4 0.069 3 ±0.009 1 1.71 2 4 0.386 1 ±0.006 5 9.53 3 4 0.282 0 ±0.018 0 6.96 4 4 0.189 4 ±0.0006 4.68 5 4 0.345 9 ±0.010 0 8.54 6 4 0.297 3 ±0.005 7 7.34 7 4 0.229 9 ±0.001 2 5.68 8 4 0.312 6 ±0.019 0 7.72 9 4 0.250 9 ±0.014 0 6.19 10 4 0.219 7 ±0.001 6 5.42 11 4 0.299 7 ±0.001 6 7.40 12 4 0.244 5 ±0.019 0 6.03 13 4 0.186 9 ±0.017 0 4.61 14 4 0.228 1 ±0.001 1 5.63 15 4 0.217 2 ±0.011 0 5.36 16 4 0.171 6 ±0.016 0 4.23 174——184——194——20 4 1——

图1 局部吸收药量曲线
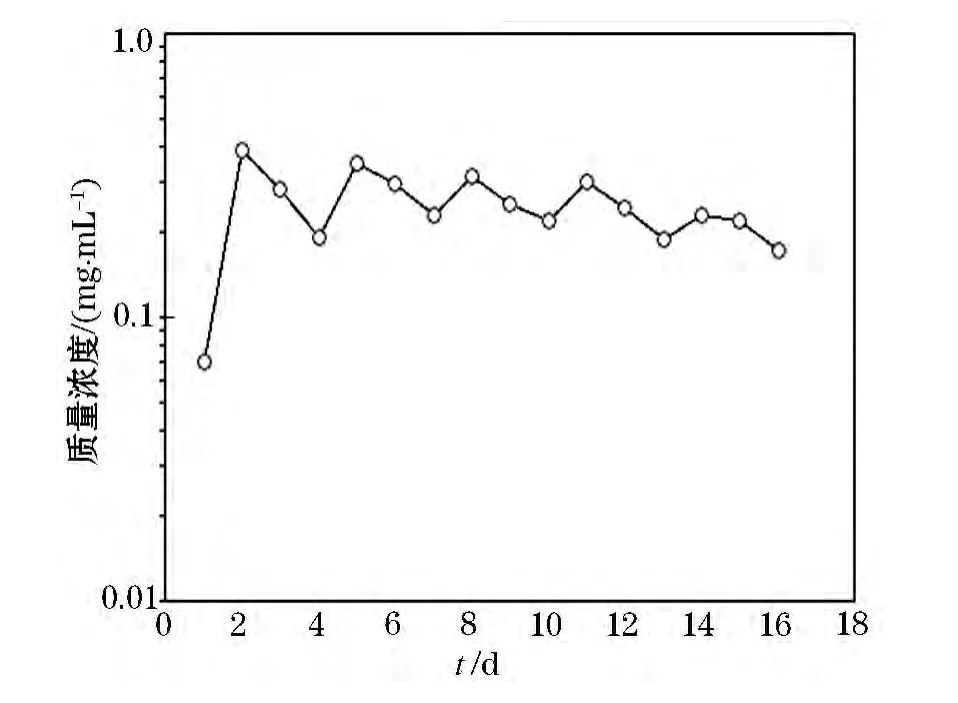
图2 局部吸收药量拟合曲线

表2 相关药动学参数
3 讨论
局部给药与口服给药相比,仅有少量的药物被吸收进入循环系统,而且由于消除与新陈代谢行为药物质量浓度下降很快[6],在局部给药系统中,血浆中药物质量浓度与药理效应没有直接关系,所以本文选择采用测定多次给药后局部病变部位全组织药物质量浓度,来评价外用给药在给药部位药物的动态行为.经数据拟合及药动学参数计算可知,药物稳态后的吸收质量浓度范围为0.21~0.39 mg/mL之间,平均稳态质量浓度为0.24 mg/mL.DF值为75%,波动度适宜,未超出治疗范围.
由实验结果可知,大鼠足部中盐酸青藤碱的吸收量3 d为一个波动期,13 d以后趋于平衡,至16 d后,实验动物足部吸收量较少,低于定量限以下.分析其原因可能是本品所用辅料中含有醋酸,长时间贴敷给药,醋酸可使皮肤组织蛋白凝固坏死,增加了皮肤的角质化,因此根据实验现象观察,在连续给药16 d后,实验动物给药部位已严重角质化,不能再继续吸收药物,导致检测量较低.
药物的透皮吸收不同于其他的吸收过程,药物从给药部位进入到体循环要经过一系列的动态过程,因此它的吸收不属于一级动力学,不会出现明显的“峰谷”现象[7-8].局部药动学研究显示,炎性部位吸收最高药量出现在给药后第2天.分析原因在于大部分药物透过皮肤去对抗炎性因子,只有少量的药物进入循环系统,这就证明了盐酸青藤碱等药物局部给药用于治疗关节炎等类疾病的优点.也就是说较少的药量在局部即可发挥较强的药效.此外,盐酸青藤碱局部给药的毒副作用在与口服给药对比时易被忽视,所以对于药物累计、质量浓度随时间变化等还需要进一步具体的研究.
[1]ZHAO X X,PENG C,ZHAN H,et al.Sinomenium acutum:A review of chemistry,pharmacology,pharmacokinetics,and clinical use[J].Pharmaceutical Biology,2012,50(8):1053 -1061.
[2]XU M,LIU L,QI C,et al.Sinomenine Versus NSAIDs for the Treatment of Rheumatoid Arthritis:A Systematic Review and Meta-Analysis[J].Planta Med,2008,74:1423-1429.
[3]孙 瑜.青藤祛湿外敷散的初步研究[D].哈尔滨:黑龙江中医药大学,2008.
[4]郭玉岩.盐酸青藤外敷散的研究(Ⅱ)[D].哈尔滨:黑龙江中医药大学,2009.
[5]LI X R,HUANG Y Q,LI X Y,et al.Preparation and evaluation of sinomenine hydrochloride patch[J].Journal Of Chinese Pharmaceutical Sciences,2010,19:110 -114.
[6]LI X R,LIXY ,ZHOU Y X,et al.Development of Patch and Spray Formulations for Enhancing Topical Delivery of Sinomenine Hydrochloride[J].Pharmaceutical Sciences,2010,99:1790-1799.
[7]LIU Z Q,CHAN K,ZHOU H,et al.The pharmacokinetics and tissue distribution of sinomenine in rats and its protein binding ability in vitro[J].Life Sciences,2005,77:3197 -3209.
[8]夏 畅,郭玉岩,吕邵娃,等.青藤祛湿外敷散对豚鼠的长期毒性研究[J].哈尔滨商业大学学报:自然科学版,2013,29(3):275 -279,291.
