电渗析技术在木糖醇酸水解法制备中的应用
2015-08-20汪耀明潘升东徐铜文
汪耀明,潘升东,徐铜文
(1 中国科学技术大学材料与化学工程学院,安徽 合肥 230026;2 合肥科佳高分子材料科技有限公司,安徽 合肥 230601)
引 言
木糖醇作为一种天然存在的稀有糖醇,其甜度与蔗糖相当,具有不刺激胰岛素分泌就能被人体吸收的功能,是糖尿病、肝炎等患者的理想甜味剂[1-2]。同时,木糖醇不被口腔类的细菌所利用,具有不致龋且有防龋齿的作用,可以适用于做口香糖、巧克力、硬糖等食品的甜味剂。此外,木糖醇具有和甘油等多元醇相类似的性质,在高分子材料、皮革制剂、涂料和医药化工等方面具有广泛的用途[3-4]。目前,工业上木糖醇的制备方法主要为酸水解法[5-6],一般是利用农业植物短纤维废料,如玉米芯、甘蔗渣、种壳等原料,在稀酸的作用下将植物纤维中的多缩戊糖水解得到木糖水解液,水解液经过中和脱酸、脱色、浓缩、离子交换得到较为纯净的木糖,木糖在镍催化剂的作用下催化加氢得到木糖醇,其大体的制备工艺流程如图1 所示。这种酸水解法制备木糖醇的工艺路线中,植物纤维水解液中一般含有0.6%~0.8%的稀硫酸,存在一个中和脱酸的工艺路线,一般是加入大量的饱和石灰水,充分搅拌中和沉淀后,去除水解液中的残酸。这种中和脱酸的方法存在几个明显的缺点。其一,消耗的大量的化工原料,其过程能耗比较大(中和过程温度维持在80~85℃)。其二,产生大量固体废渣(CaSO4)和废水,容易带来二次污染。以玉米芯制备木糖醇为例,每生产1 t 的木糖醇,可产生12~16 t 滤渣[7],需占用大量的空间。其三,工艺操作繁琐,劳动强度大,少量的硫酸钙残留会加重后续脱色、浓缩的工艺负担。特别是石膏沉积在蒸发器的管壁上会形成隔热层,降低浓缩过程中蒸汽效率及对蒸发设备造成腐蚀[8]。因此,如何选择一种更加清洁高效、绿色环保的技术应用于木糖醇的脱酸过程显得尤为迫切。
而基于离子交换膜电渗析的技术作为一种环境友好、方便快捷的新型分离技术得到了人们越来越普遍的关注[9-12],它的原理是利用离子的定向迁移和离子交换膜的选择透过性,因而可以实现电解质溶液的浓缩或淡化[13-16]。由于木糖呈电中性,而硫酸是强电解质,在电场的作用下,利用离子交换膜对离子的选择透过性,通过电渗析工艺可实现木糖水解液中残酸的选择性去除。目前,利用电渗析过程去除木糖水解液中的残留无机酸在文献中鲜见报道。因此,本文主要探讨了电渗析技术在木糖醇酸水解法制备过程中的可行性,并对整个分离过程的经济型进行评价。由于木糖醇作为众多生物糖产品中的一种,其制备方法与其他生物糖(如半乳糖、甘露糖和阿拉伯糖)比较类似,这类生物糖制备过程中均存在一个脱除残酸的工艺。因此,本文提供的电渗析分离法可为这类生物糖的清洁生产提供参照。
1 实验材料和方法
1.1 材料
含木糖的水解液由山东福田药业集团提供,以溶液形式存在,主要含有木糖和少量硫酸及胶体、蛋白、色素,其溶液pH 值为1.0 左右,电导率为13.5 mS·cm-1,糖含量为6.5%。均相阴、阳离子交换膜(CJ-MA-2、CJ-MC-2)由合肥科佳高分子材料科技有限公司提供,该型离子交换膜的主要材质为聚偏氟乙烯。其主要性能指标列于表1。

表1 膜的主要技术指标Table 1 Main characteristics of membranes used in experiments

图1 酸水解法制备木糖醇的工艺流程Fig.1 Schematic preparing route for production of xylitol byacid hydrolysis method
1.2 电渗析实验装置
CJ-ED-1 实验室普通电渗析脱盐系统,是由合肥科佳高分子材料科技有限公司自主设计产品,含有1 对电极和4 对阴离子交换膜,5 张阳离子交换膜组成,单张膜的有效面积为100 cm2,整个电渗析过程的原理如图2 所示。DDS-307A 型电导率测定仪(上海盛磁仪器有限公司)。手提式ATAGO PAL-1 折射计(日本,株式会社爱宕)。

图2 电渗析法去除木糖水解液中残酸的原理Fig.2 Principle for removal of residue acid in xylose hydrolyzedsolution by electrodialysis Note: Dotted box means repeating number of anion and cation exchange membrane is four.
1.3 电渗析实验过程
本实验所用的CJ-ED-1 实验室普通电渗析脱盐系统,由合肥科佳高分子材料科技有限公司自主设计产品,整个电渗析系统主要由4 部分构成:
(1)直流电源(WYL-605×2S,杭州余杭四岭有限公司),用于提供恒定的直流电场,提供的最大电压为60 V。
(2)烧杯,用于储存料液,根据膜池单元设计,此电渗析系统共分为3 个隔室,分别为极室、浓缩室和淡化室(料液室)。
(3)潜水泵(HJ-311,浙江森森有限公司),用于循环料液,最大流速300 L·h-1,3 台泵分别与3 个料液室通过硅胶管相连,形成3 个独立的闭合回路。
(4)电渗析膜堆。膜堆包括:①阳极和阴极,材质为钌铱电极;②带格网的有机复合垫片,厚度为0.08 cm,用于分隔相邻的离子交换膜同时提供液体流动的通道;③5 张CJMC-2 阳离子交换膜和4张CJMA-2 阴离子交换膜(合肥科佳高分子材料有限公司生产),单张膜有效面积为90 mm×110 mm,性质见表1;④支撑电解质:极室为400 ml、0.3 mol·L-1的硫酸钠溶液作为极室的支撑电解质;在淡化室注入400 ml木糖水解液,浓缩室注入400 ml,0.1 mol·L-1的硫酸溶液以降低溶液电阻。在接入直流电源之前,膜堆先行循环30 min,使料液得到充分的循环和稳定。
整个实验在室温下进行。
1.4 计算公式
脱盐率(Dr)的计算公式如下
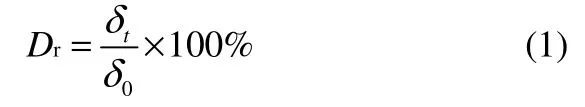
式中,δ0为电渗析前淡化室料液的电导率,μS·cm-1;δt为电渗析进行t 时,淡化室料液的电导率,μS·cm-1。
木糖的产品得率(η)的计算公式如下

式中,A 为电渗析实验结束时木糖水解液中木糖的含量;A0为实验开始时,木糖水解液中木糖的含量;V 为电渗析实验结束时电渗析淡化室的体积,ml;V0为电渗析中电渗析淡化室的体积,V0=400 ml。
电渗析过程中的能耗(E,kW·h·L-1)计算公式如下

式中,U 为膜堆的电压降,V;I 为施加的电流,A;V 为料液室的体积,L;t 为时间。
1.5 测定方法
电导率通过电导率仪直接测定;
pH 值由pH 计测定;
木糖的含量由手提式ATAGO PAL-1 折射计测定。
2 实验结果与讨论
2.1 电流电压-时间曲线
图3 所示为电渗析不同初始电流密度下的膜堆电流电压值随时间的变化情况图。从图3(a)中可以看出,在初始电流密度小于20 mA·cm-2时,膜堆的电流值在设定的电流密度上保持一段时间不变,随后随时间的增加而逐步下降。而在初始电流密度为25 mA·cm-2以上时,膜堆的电流值并没有出现一个明显的恒定值,其电流值随着电渗析实验的进行是逐步降低的。需要说明的是,本电渗析实验仪器选用的直流电源的最大电压值为60 V,实验中选择恒流操作是为了更好地控制电渗析的稳定运行,当整个膜堆的电压上升至直流电源的最大量程时,电渗析的运行模式将由恒流操作变为恒压操作。从图3(b)中可以看出,膜堆的电压值是随着电渗析实验的进行而快速上升的,并在接近60 V 时保持不变。这说明了在低电流密度下,电渗析实验在恒流模式下保持了一段时间,然后转为恒压操作。而在高电流密度下,电渗析实验始终是在恒压模式下运行的。如电流密度在40 mA·cm-2时,其膜堆的电压降在1 min 内便达到了直流电源的最大值,这也说明进一步加大初始电流密度对整个电渗析实验的运行没有意义,因此本论文并没有再考察更高的电流密度值。从图3 中电流电压随时间的变化来看,整个膜堆的电流值大体呈现逐步下降的趋势,这说明了整个膜堆的电阻逐步增加。结合电渗析实验中淡化室和浓缩室的物料特性,可以看出,随着电渗析实验的进行,木糖水解液中可导电的电解质(H2SO4)在电场的作用下不断地迁移出淡化室; 而木糖的导电性非常差,其在25℃下的当量电导在8.0 S·m2·mol-1左右,其值要远小于硫酸的当量电导66 S·m2·mol-1[17]。因此,随着电渗析实验的不断进行,淡化室中可导电的离子逐步减少,整个膜堆的电阻逐步增加。同时,随着电流密度的增加,离子迁移的电场也越大,离子迁移的速率也越快,因此电压上升的速率也是增大的,这与图3 所反映出的电压变化情况一致。

图3 不同初始电流密度下的膜堆电流电压随时间变化图Fig.3 Dependences of current and voltage drops in ED stack with time under different initial current density
2.2 电导-时间曲线
图4 所示为电渗析不同初始电流密度下的淡化室电导率随时间变化情况。需要说明的是,试验中测定的电导值是物料循环下在线测定的,由于木糖水解液不同批次间的差异性,导致其起始电导率略有波动,但是从图中电导率的变化趋势可以直观地看出,淡化室的电导随着时间逐步下降,实验结束时的电导率均在1000 μS·cm-1以下,这也说明了利用电渗析技术可以实现对木糖水解液中残酸的去除。同时,起始电流密度越大,离子迁移的推动力越大,其电导下降的速率也就越大,电渗析实验所需要的时间也就越短。但是,电流密度在30 和40 mA·cm-2下的电导变迁趋势基本一致,这主要是受实验过程中所选直流电源的限制,其电渗析过程并没有在其设定的电流条件下持续运行。电渗析过程对木糖水解液中残酸的去除率均达到99%以上,实现了很好的酸去除效果。
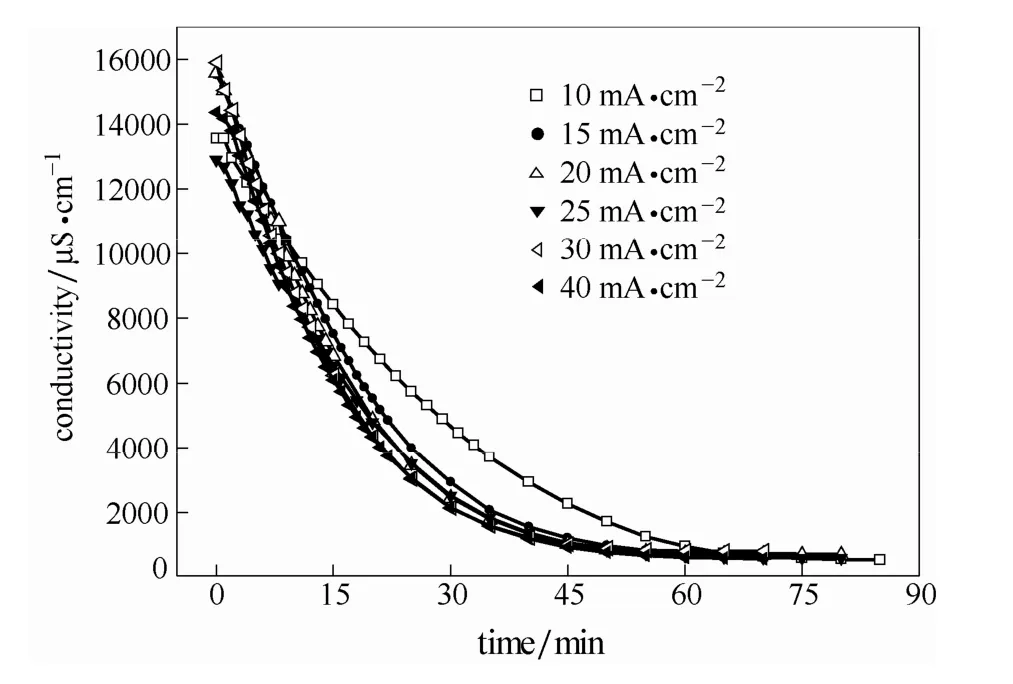
图4 不同初始电流密度下的淡化室电导率随时间变化图Fig.4 Dependences of conductivities in dilute compartment of ED stack under different initial current density
2.3 产品得率及过程能耗
图5 所示为电渗析不同初始电流密度下的木糖水解液中木糖产品得率情况。从图中可以看出,利用电渗析实现对木糖水解液中残酸去除的同时,其木糖的得率维持在78.4%~84.8%。在电渗析过程中,木糖产品有一定的损失,这主要是由于木糖分子为弱电解质,由于在淡化室中其含量较高,而浓缩室中含量较低,在浓度差的作用下,木糖分子会从淡化室中扩散至浓缩室,这种分子扩散[18]会导致产品中木糖的含量随电渗析过程有所下降。同时,随着电流密度的增加,木糖的得率有所提高。这主要是由于在高电流密度下,实验所需要的时间降低。因此,为了达到更高的处理效率并减少电渗析过程中木糖产品的损失,整个电渗析过程在较高的电流密度下较为合适,这时候可保持在较短的时间内实现残酸的去除,同时较少木糖分子扩散导致的产品损失。
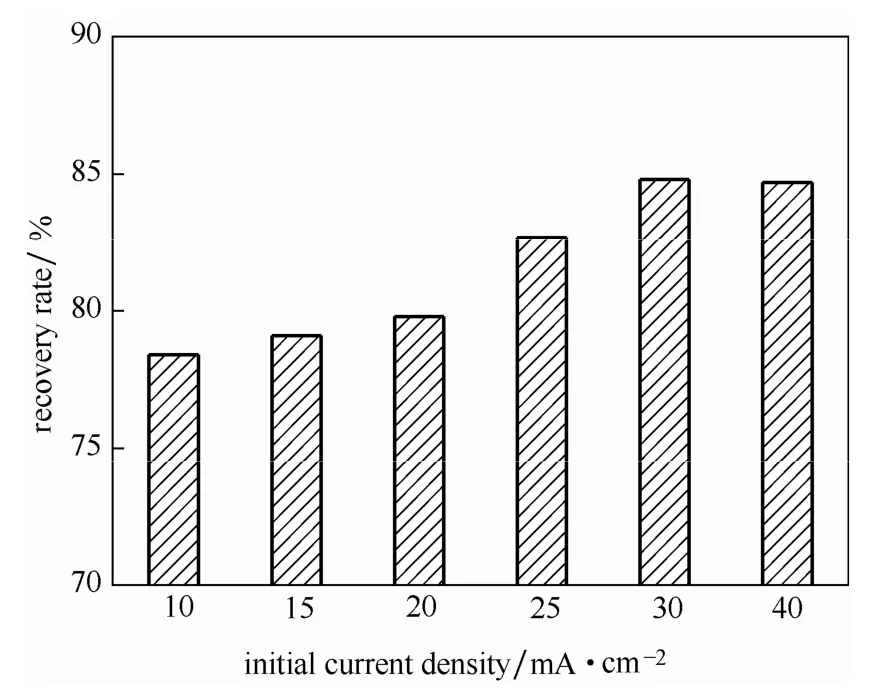
图5 不同初始电流密度下的木糖产品得率图Fig.5 Recovery ratio of xylose under different initial current density
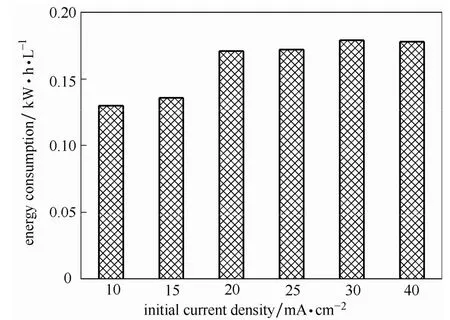
图6 不同初始电流密度下的电渗析过程能耗Fig.6 Energy consumption of electrodialysis process under different initial current density
图6 所示为不同电流下的电渗析处理木糖水解液的过程能耗图。从图中可以看出,随着电流密度的增加,电渗析过程处理木糖水解液的能耗逐渐增加,其过程能耗基本维持在 0.13~0.18 kW·h-1·L-1。电渗析过程的能耗随电流的增加基 本上呈线性上升,这种上升的趋势与欧姆定律相一致。事实上,在电渗析的实际应用过程中,电流密度的选择需要权衡考虑。过高的电流密度就意味着高的欧姆电阻,而过低的电流密度就以为需要更大的膜面积,这无疑会增加设备投资成本。综合考察木糖的产品得率和处理速率,操作电流密度选择为30 mA·cm-2时较为合适,此时处理木糖水解液的过程能耗仅为0.179 kW·h·L-1。
2.4 成本估算
通过对电渗析过程的能耗及成本进行评估[18-20],可为本技术的工业化应用前景提供参照。根据电渗析成本评估公式,对电流密度为30 mA·cm-2时,电渗析处理木糖水解液的成本进行了评价,结果见表2。

表2 电渗析处理木糖水解液的成本分析Table 2 Estimation of process cost for removal of residue acid in xylose hydrolyzed solution by electrodialysis
整个电渗析过程的成本包括能耗成本和投资成本。固定投资成本包括设备投资、利息以及设备维护费用;设备投资主要包含膜堆成本以及外辅成本;膜堆成本一般为膜成本的1.5 倍,而外辅成本为膜堆成本的1.5 倍;利息和维修费用按总投资的8%和1%进行计算。从表中可以看出,利用电渗析处理木糖水解液的能耗仅为179 kW·h·t-1,其脱酸工艺过程成本仅为139 ¥·t-1。考虑到木糖醇的市场价格在3 万~5 万元·t-1,其电渗析过程去除木糖水解液中的残酸是具有很好的经济性的。
3 结 论
(1)电渗析过程实现了木糖水解液中残酸的选择性去除,整个过程不添加额外化学试剂,不产生固体废渣,减轻了下游的工艺负担。
(2)电渗析过程对木糖水解液中残酸的去除率大于99%,其木糖的收率可达到84.8%。
(3)电渗析工艺处理木糖水解液的能耗为179 kW·h·t-1,电渗析技术处理木糖水解液脱酸工序的成本为每吨母液139 元,通过规模化生产,其处理费用有望进一步降低。
[1]Pepper T, Olinger P M.Xylitol in sugar-free confections [J].Food Technology, 1988, 42(10): 98-108.
[2]Trahan L.Xylitol: a review of its action on mutans streptococci and dental plaque-its clinical significance [J].International Dental Journal, 1995, 45(1): 77-92.
[3]Meyrial V, Delgenes J P, Moletta R, et al.Xylitol production from D-xylose by candida-guillermondii-fermentation behavior [J].Biotechnology Letters, 1991, 13(4): 281-286.
[4]Blair J B, Cook D E, Lardy H A.Influence of glucagon on metabolism of xylitol and dihydroxyacetone in isolated perfused rat-live [J].Journal of Biological Chemistry, 1973, 248(10): 3601-3607.
[5]Liu Chun(刘春), Fang Guigan(房桂干), Shi Yingqiao(施英乔), et al.Research progress on production and application of xylitol [J].Chemistry and Industry of Forest Product(林产化学与工业), 2010, 30 (10): 113-118.
[6]Lavarack B P, Griffin G J, Rodman D.The acid hydrolysisof sugarcane bagasse hemicellulose to produce xylose, arabinose, glucose and product [J].Biomass and Bioenergy, 2002, 23: 367- 380.
[7]Ma Weichao(马伟超), Li Yijing (李一婧), NianYanan (念亚男).Production of xylitol by fermentation of acid hydrolyzed corn stalk [J].Hunan Agriculture Sciences(湖南农业科学), 2011, 21: 76-78.
[8]Tan Shiyu (谭世语), Huang Cheng (黄诚).Research progress on extract technics of xylose [J].Food Science and Technology(食品科技), 2006, 12: 103-105.
[9]Xu Tongwen, Huang Chuanhui.Electrodialysis-based separation technologies: a critical review [J].AIChE J., 2008, 54(12): 3147- 3159.
[10]Strathmann H, Grabowski A, Eigenberger G.Ion-exchange membranes in the chemical process industry [J].Ind.Eng.Chem.Res., 2013, 52: 10364-10379.
[11]Zhang Y, Pinoy L, Meesschaert B, et al.Separation of small organic ions from salts by ion-exchange membrane in electrodialysis [J].AIChE J., 2011, 57: 2070-2078.
[12]Yuan Zhongwei (袁中伟), Zhong Yujiang (钟玉江), Yu Lixin(余立新).Separation of serine and proline by multistage electrodialysis [J].CIESC Journal(化工学报), 2009, 60 (5): 1199-1203.
[13]Readi O M K, Rolevink E, Nijmeijer K.Mixed matrix membranes for process intensification in electrodialysis of amino acids [J].J.Chem.Technol.Biotechnol., 2014, 89: 425-430.
[14]Xu Tongwen.Ion exchange membranes: state of their development and perspective [J].J.Membr.Sci., 2005, 263: 1-29.
[15]Strathmann H.Membrane separation process: current relevance and future opportunities [J].AIChE J., 2001, 47: 1077-1087.
[16]Cheng Qing (程清), Zhang Xiaosong (张小松).A new regeneration system for solar desiccant pre-treatment electrodialysis [J].CIESC Journal(化工学报), 2014, 65(3): 1018-1024.
[17]Ren Qiuhe(任秋鹤).Conductivities of saccharides in electrolytes solution and Debye-Huckel contribution [D].Zhengzhou: Henan Normal University, 2007.
[18]Jaime-Ferrer J S, Couallier E, Viers P, et al.Three-compartment bipolar membrane electrodialysis for splitting of sodium formate into formic acid and sodium hydroxide: role of diffusion of molecular acid [J].J.Membr.Sci., 2008, 325: 528-536.
[19]Wang Yaoming, Wang Anlei, Zhang Xu, Xu Tongwen.Simulation of electrodialysis with bipolar membranes: estimation of process performance and energy consumption [J].Ind.Eng.Chem.Res., 2011, 50(24): 13911-13921.
[20]Strathmann H, Koops G H.Process economics of electrodialytic water dissociation for the production of acid and base// Kemperman A J B.Handbook on Bipolar Membrane Technology [M].Enschede: Universiteit Twente Press, 2000: 191-220.
