糖尿病足与周围神经病变
2015-08-19刘芳上海交通大学附属第六人民医院内分泌代谢科
刘芳上海交通大学附属第六人民医院内分泌代谢科
糖尿病足与周围神经病变
刘芳
上海交通大学附属第六人民医院内分泌代谢科
doi:10.3969/j.issn.1672-7851.2015.05.009

刘 芳 教授,主任医师,博士生导师;上海交通大学附属第六人民医院内分泌代谢科副主任;中华医学会糖尿病学分会糖尿病足与周围血管病学组副组长、糖尿病神经并发症学组委员,中华医学会内科学分会青年委员兼秘书长,中国医师协会内分泌代谢科医师分会青年委员会副主任委员,上海医学会内分泌分会委员、糖尿病神经病变学组副组长,上海中西医结合学会内分泌代谢专业常务委员;主持国家卫计委行业专项子项目1项,国家自然科学基金项目2项,上海市科委和卫生局项目多项;发表学术论文90余篇,其中Diabetes等杂志第一/通讯作者SCI论文21篇。
什么是糖尿病周围神经病变?
糖尿病周围神经病变(Diabetic peripheral neuropathy,DPN)是指糖尿病患者出现周围神经功能异常的症状或体征,或检查发现周围神经传导功能异常,除外其它引起周围神经损伤的疾病。DPN是最常见的糖尿病慢性并发症,由于缺乏统一的诊断标准和检测方法,其患病率在10%~96%不等。随着糖尿病病程进展,30%~50%的患者会发生糖尿病神经病变。DPN的致残率高达46.6%。
DPN有什么临床表现?
DPN是临床表现最复杂的一种慢性并发症,从各种感觉异常的严重症状到感觉丧失而无症状不一而足。主要表现为:
1.感觉异常
肢体麻木、疼痛等感觉异常为DPN的常见主诉,最典型的是痛性神经病变(PDPN),表现为针刺、烧灼、刀割、虫咬或蚁行、钝痛等各种痛觉和痛觉过敏,对患者生活影响很大,常常不能忍受一条被单,夜不能寐,久之引起情绪异常(抑郁、焦虑等)甚至自杀倾向。更多的病人以感觉障碍为主要表现,初时肢端麻木、如穿了一层手套、袜子样,以后逐渐感觉减退乃至消失,尤其是保护性痛觉丧失,即为“无痛性神经病变”。
2.自主神经功能异常
薄髓的自主神经纤维受累时表现累及面最广,在手足表现为排汗异常、皮肤干燥,在躯干可出现局部出汗过多或无汗;在消化系统表现为腹泻、便秘、甚至恶心、呕吐等胃轻瘫症状;在生殖系统表现为女性性欲减退、阴道干涩,男性性欲下降、勃起功能障碍,不孕不育等;在泌尿系统表现为排尿淋漓不尽、排尿困难、尿潴留、尿失禁等。
3.运动异常
肢体肌肉无力和萎缩,足下垂,蹲下不能站起等,通常出现相对较晚。
DPN与糖尿病足病有什么关系?
DPN是糖尿病足发病的原因之一,也是诱发足皮肤损伤最常见的原因。糖尿病患者合并下肢周围神经病变,尤其是无痛性神经病变(painless neuropathy),因保护性感觉(痛觉、触觉、位置觉等)丧失(Loss of protective sensation,LOPS),往往因不易察觉的小的足部皮肤损伤,而致足溃疡的出现,加重而致截肢致残。因此,早期筛查和诊治糖尿病周围神经病变对预防足病发生和提高患者生活质量至关重要。

表1 下肢感觉筛查工具的对应神经功能
DPN多久筛查一次最好?
《中国糖尿病防治指南》、美国糖尿病协会糖尿病指南指出,对于DPN,筛查频率是:
1.2型糖尿病患者自疾病获得诊断之时进行第一次筛查,1型糖尿病患者糖尿病病程5年以上,都应每年筛查一次;对于糖尿病病程较长,或合并有眼底病变、肾病等微血管并发症、或筛查有神经病变的患者,应该每隔3~6个月进行复查。
2.筛查前了解患者的高危因素和足病相关病史,如下肢溃疡、疼痛和药物治疗史等。
如何筛查DPN?
DPN由于累及的神经众多,从有髓的Aα、β神经纤维,到薄髓的Aδ纤维,到无髓鞘的C纤维,单独靠一种工具是无法完整评价的,加之近2/3的患者并无明显神经病变症状,因此不能根据症状做出诊断,需要多种临床小工具联合进行筛查。各项神经感觉功能的筛查和评价方法如下:
1.足外观
下列体征提示下肢神经病变:(1)足底胼胝或足趾鸡眼;(2)足部皮温正常或者偏高;(3)足部皮肤干燥、汗液减少;(4)足畸形,如锤状趾、爪形趾、夏科氏关节等。
2.利用临床小工具,进行神经病变综合筛查和评价
(1)筛查工具
①大头针、10g尼龙丝、128Hz音叉、皮温计、叩诊锤等简单工具。②震动感觉阈值(VPT)测定:需要专用的测定仪器,有条件的开展。③肌电图:可进行四肢神经感觉性(SNCV)和运动性神经传导速度(MNCV)测定:并非筛查必须。需要专科医师做,有条件者做。
(2)每种筛查工具反映的神经功能
见表1。
(3)下肢神经病变筛查流程
见图1,摘自《中国糖尿病防治指南,2013版》。
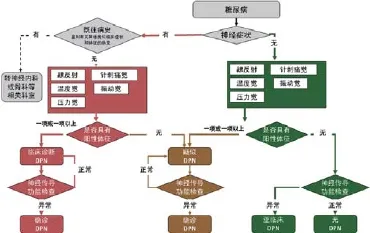
图1 糖尿病周围神经病变筛查流程
(4)下肢感觉的筛查方法及判断标准
【触觉】
① 检查时10g尼龙丝须和皮肤表面垂直放置。
② 常用位点,如图2A

图2 尼龙丝感觉检查部位及方法示意
③均匀用力使纤维变弯曲即可,如图2B。(此时单丝刚好对受检部位产生10g的压力)
④ 同一部位只重复2次,但是其中一次单丝勿接触皮肤,
⑤ 每个部位提问3次;检查的同时需要提问被检者,是否感觉到压力以及压力出现在左脚还是右脚。
⑥结果判断:
· 保护性感觉正常:每个部位能正确感知3次中的2次以上者。
· 保护性感觉缺失:每个部位错误感知3次中的2次以上。
【痛觉】
①方法:用大头针轻刺足底1、3、5足趾腹部及跖底皮肤(见图3),询问有无疼痛及疼痛程度。若无痛觉,再刺足外侧及足背皮肤。
②结果判断:
· 正常:各部位感觉到轻度疼痛,能忍受;
· 减退或消失:有感觉但感觉不到疼痛,完全无感觉;
· 过敏:轻触即感觉疼痛,难以忍受。
如果发现局部痛觉减退或过敏,嘱患者比较与正常区域差异的程度。
【温度觉】
①分别用盛冷水(5~10℃)和热水(40~45℃)的玻璃试管接触皮肤,嘱患者报告“冷”或“热”。无明显感觉及差异,为温度觉消失。
②用Tip-therm凉温觉检查仪(金属一头为凉觉,聚酯一头为温觉,左下图)置于足背皮肤(图4),询问其有无凉、温感觉。无感觉或比较不出差异,为消失。

图3 针刺痛觉检查示意

图4 温度觉检查示意
【震动觉】
①首先将128Hz音叉放在被检者手部(或肘部、或前额),让患者体会正常振动的感觉。
②敲击音叉使其振动,将音叉柄部放在大拇趾远端第一关节突起的上方进行双侧检查,同时病人闭起眼睛,询问患者有无震动感觉,并说出震动觉消失的时间,以判断震动感觉持续多长时间。
③同一部位重复检查二次,并增加一次静止音叉的检查(不振动)。
④如果被检者在大拇趾上感觉不到振动,就在其他就近部位重复检查(如:踝关节、胫骨粗隆)。
⑤结果判断:
· 震动觉正常:当患者不能感受到震动,而检查者把音叉放在自己示指上仍能感受到音叉振动小于10秒钟。
· 震动觉减退:当患者不能感受到震动,而检查者把音叉放在自己示指上仍能感受到音叉振动超过10秒钟。
· 震动觉缺失:患者未察觉到震动的存在。
【踝反射】
①病人脚放置平面上,足背屈30~45度。
②轻敲病人跟腱以造成踝反射。
③判断标准:一般轻叩即出现反射。若重扣出现,为减弱;重扣仍无反射出现,为消失。

周围神经病变的诊断标准是什么?
1.糖尿病远端对称性多发性神经病变(DSPN)诊断标准
(1)明确的糖尿病病史;
(2)诊断糖尿病时或之后出现的神经病变;
(3)临床症状和体征与糖尿病周围神经病变的表现相符;
(4)有临床症状(疼痛、麻木、感觉异常等)者,5项检查(针刺痛觉、震动觉、压力觉、温度觉、踝反射)中任1项异常;无临床症状者,5项检查中任2项异常,临床诊断为糖尿病周围神经病变。
2.DPN确诊标准
肌电图检查显示神经传导异常:上肢感觉性或运动性神经的传导速度(NCV)<50m/s,下肢感觉性或运动性神经传导速度<40m/s,且同时存在2支及以上的神经传导异常。
3.DSPN的分层诊断
(1)确诊:有DSPN的症状或体征,同时存在神经传导功能异常。
(2)临床诊断:有DSPN的症状及1项体征为阳性,或无症状但有2项以上(含2项)体征为阳性。
(3)疑似诊断:有DSPN的症状但无体征或无症状但有1项体征阳性。
(4)亚临床DPN:无症状和体征,仅存在神经传导功能异常。
怎么治疗糖尿病周围神经病变以预防足病?
1.治疗DPN的基础——代谢控制
(1)血糖控制
DCCT研究证实,强化血糖控制可减少1型糖尿病患者神经病变的发生;但VADT、ACCORD、ADVANCE、Steno-2、VA-CSDM等2型糖尿病患者大型临床研究表明,强化血糖控制对DPN进展无效,并不能减少新发DPN的出现。但一般情况下,血糖应该控制在理想范围,在合并感染的足病住院患者中,一般建议先应用胰岛素强化治疗方案(即三餐前短效胰岛素睡前中效或长效胰岛素皮下注射)或胰岛素静滴,将空腹和餐前血糖控制在4.4~8.0mmol/ L,餐后血糖控制在10.0mmol/L以下,但对有多种脏器功能问题和病重的患者,餐后血糖可以放宽在7.8~11.1mmol/L。血糖稳定后可以改用每日两次预混胰岛素的降糖方案。
(2)控制血压
应用血管紧张素转化酶抑制剂(ACEI)、血管紧张素受体拮抗剂(ARB)或钙离子拮抗剂(CCB)类,将血压控制在140/90mmHg以下。合并严重肾病血肌酐水平升高或肾小球滤过率低于60ml/ min/1.73m2者,则慎用ACEI和ARB类,且血压要控制在130/80mmHg以下。
(3)调节血脂
有报道,LDL-C升高,尤其是氧化的LDL-C参与了DPN发病。不同ApoE基因型的糖尿病患者患DPN的风险也不同。因此,应用他汀类等控制LDL-C水平可能对DPN有一定帮助,一般应控制在2.6mmol/L以下,有心血管危险因素者,LDL-C控制在1.9mmol/L以下。
(4)戒烟
2.DPN的对因治疗
DPN的发病机制复杂,涉及代谢紊乱(山梨醇途径、己糖胺途径、非酶糖基化及糖化终末产物形成)、微循环障碍引起的缺血缺氧及氧化应激损伤、同时伴有炎症和自身免疫因素、神经生长修复障碍和维生素营养障碍等的参与。
因此,治疗应针对发病机制的不同方面,目前的对因疗法包括以下几个方面:
(1)抗氧化应激
此类药物通过阻抑神经内氧化应激状态、增加营养神经血管的血流量、加快神经传导速度、增加神经Na+-K+-ATP酶活性等机制,改善糖尿病周围神经病变的症状。α-硫辛酸是丙酮酸脱氢酶系的辅助因子,也是目前临床应用最广的强抗氧化剂。
德国Ziegler D领衔的ALANDINⅠ、Ⅱ、Ⅲ研究以及Sydney等临床研究,证实以抗氧化应激为目的的抗氧化剂如α-硫辛酸可对DPN起到明确的改善神经感觉症状和神经传导速度等治疗作用。在亚洲糖尿病研究协会(AASD)的指南中,也推荐抗氧化剂α-硫辛酸治疗,其应用方法有α-硫辛酸针剂600mg/d,静滴*4周,和600mg一日三次,口服的方法。短期静滴和口服3个月以上的方法皆疗效确切。但其停药后仍会出现,故需要定期应用以巩固长期疗效。
(2)营养神经及神经修复
以前认为维生素B尤其是B12缺乏是DPN发病的原因之一,甲钴胺为蛋氨酸合成酶辅酶,该酶促进髓鞘的主要成分卵磷脂的合成,与髓鞘、核糖核体膜、线粒体膜、突触及受体等的功能有关,可促进核酸和蛋白质的合成,改善神经元和施旺氏细胞的代谢,促进轴索内输送和轴索的再生。在临床上应用活性B12制剂如甲基钴胺素,获得了一定效果。常用药物剂量是500ug每日三次口服,也可以500~1000ug/d静滴或肌注,连续使用1~2周,以获得更好疗效。荟萃分析显示,甲钴胺与改善循环药物前列腺素合用的疗效优于单用甲钴胺。
(3)改善神经微循环
基于DPN是一种糖尿病微血管病变,受损神经组织和神经元存在微循环障碍和缺血缺氧。血管扩张剂,如血管紧张素转化酶抑制剂(ACEI)、己酮可可碱;抑制血小板聚集药物如阿司匹林、西洛他唑;以及前列腺素E1、前列地尔、贝前列腺素钠等前列腺素制剂可扩血管,减轻血液粘稠度。尤其前列腺素E1针剂10~20μg/d静滴,2周为一疗程,对糖尿病神经病变的麻木、疼痛有缓解作用。
(4)改善糖代谢紊乱
醛糖还原酶抑制剂(ARIs)类药物通过抑制醛糖还原酶活性、恢复Na+-K+-ATP酶活性、减少山梨醇和果糖在周围神经组织的沉积,改善糖尿病神经病变。目前在日本、中国已上市的有依帕司他片,通常50mg每日三次,口服。长期应用可改善神经感觉症状,提高神经传导速度。
(5)其他
如,①神经营养,包括神经营养因子如神经生长因子(NGF)、肝细胞生长因子(HGF)、肌醇、神经节苷酯等;②糖基化终末产物形成抑制药如氨基胍等;③C肽;④蛋白激酶C抑制剂等,目前疗效有限或不确切而未在临床推广应用。
3.DPN的对症治疗
主要是改善疼痛症状。目前药物众多,但疗效因人而异。包括如下几种:
(1)三环类抗抑郁药物:阿米替林(Amitrip tyline)和丙米嗪(Berkomine)应用最为广泛。杜洛西汀是新一代药物,但疗效并不优于阿米替林。
(2)抗惊厥药物:老的有卡马西平,新一代的有普瑞巴林,目前RCT研究证实了其对DPN的有效性。
(3)抗癫痫药物:如老药卡马西平、苯妥英钠,研究证实可有效缓解痛性神经病变的疼痛症状,但副作用大,目前少用于临床。新一代的加巴喷丁(Gabapentin)是目前治疗糖尿病周围神经病变引起的疼痛的一线药物。
(4)阿片类镇痛药:阿片类麻醉镇痛药止痛的原理主要是作用于中枢痛觉传导通路阿片受体,提高痛觉阈值,使疼痛缓解。如硫酸吗啡、曲马多等。最常见的副作用是镇静、便秘、恶心和呕吐及成瘾。
(5)局部治疗药物:有的患者疼痛部位相对比较局限,可以采取局部用药。局部用药有全身副作用小、与其他药物相互作用少等优点。如已被FDA批准上市的利多卡因贴皮剂、辣椒素软膏、消心痛喷剂、硝酸甘油贴膜剂等,尚有人尝试过经皮神经电刺激方法,均有一定的缓解疼痛疗效。
1 Bril V. J Peripheral Nervous System,2012,17(suppl 2):22-27.
2 Callaghan, et al. Cochrane Review,6,2012.
3 许樟荣,王玉珍. 中华糖尿病杂志,2014,6(5):346-349.
4 Singh R, et al. Pharmacological Research, 2014,80:21-35..
5 Tesfaye S, et al. Diabetes Care,2010,33(10):2285-2293.
6 Asian Association for the Study of Diabetes(AASD). J Diabetes Invest,2011,2(1):33-42.
7 中华医学会神经病学分会. 糖尿病周围神经病诊断和治疗共识. 中华神经科杂志,2013,46(11):787-789.
8 Deng H, et al. Endocrine,2014,Feb.
9 Ziegler D, et al. Diabetes Care,2008,31(suppl 2):S255-261.
10 Hotta, et al. Diabetes Care,2006,29(7):1538-1544.
11 Han T, et al. Eur J Endocrinol,2012,167(4):465-471.
Diabetic Peripheral Neuropathy: Critical Triggering Factor and Aggravating Cause of Diabetic Foot Disorders
