HBSP抑制缺氧复氧心肌H9C2细胞Omi/HtrA2胞内转位及细胞凋亡
2015-07-31刘映峰张杰波林湧滦
游 伟,刘映峰,张杰波,林湧滦,缪 绯,刘 芃
(南方医科大学 珠江医院 心血管内科,广东 广州 510282)
HBSP抑制缺氧复氧心肌H9C2细胞Omi/HtrA2胞内转位及细胞凋亡
游 伟,刘映峰,张杰波,林湧滦,缪 绯,刘 芃*
(南方医科大学 珠江医院 心血管内科,广东 广州 510282)
目的探讨促红细胞生成素衍生肽(HBSP)对缺氧复氧心肌细胞Omi/HtrA2胞内转位及细胞凋亡的影响。方法将乳鼠心肌细胞(H9C2 细胞)分为对照(Ctrl)组、缺氧复氧(H/R)组、HBSP组和EPO组。培养结束后MTS法检测细胞存活率,酶标仪检测细胞上清液中LDH释放率,Western blot检测细胞内cleaved caspase- 3表达,TUNEL法检测心肌细胞凋亡;分离H9C2细胞胞质及线粒体,Western blot分别检测线粒体及细胞质Omi/HtrA2表达。结果与Ctrl组相比,H/R 组细胞存活率下降(P<0.05),LDH释放、cleaved caspase- 3表达、心肌细胞凋亡及Omi/HtrA2胞内转位均明显上升(P<0.05);与H/R组相比,EPO组的细胞存活率升高(P<0.05),LDH释放降低、cleaved caspase- 3表达减弱、心肌细胞凋亡减少、Omi/HtrA2线粒体转位明显减少(P<0.05);随着HBSP浓度的增加,各组细胞存活率逐渐上升,LDH释放、cleaved caspase- 3表达、心肌细胞凋亡及Omi/HtrA2胞内转位率逐渐下降 (P<0.05)。结论HBSP具有与EPO类似的保护作用,可抑制经H/R诱导的心肌细胞凋亡,其机制可能是通过减少Omi/HtrA2蛋白的胞内转位,抑制caspases通路激活,进而发挥细胞保护作用。
缺氧复氧;促红细胞生成素衍生肽;促红细胞生成素;细胞凋亡;Omi/HtrA2
在现阶段急性心肌梗死患者的再灌注治疗中,无论是溶栓还是冠脉介入治疗,心肌缺血/再灌注损伤(myocardial ischemia reperfusion injury,MIRI)都是临床医生无法回避的问题及难以攻克的治疗难点。然而缺血/再灌注(I/R)的机制至今仍未完全阐明,目前临床上尚无有效的治疗方法。近10年来,体内外大量的实验[1- 2]证实促红细胞生成素(erythropoietin,EPO)在心肌梗死、MIRI、心力衰竭等模型中起到良好的心肌保护作用。然而,近年来几个大型临床研究中[3- 6],EPO因血栓及高血压等不良反应,使其临床推广受到限制。HBSP是由EPO 3级结构衍生而来的具有11 个氨基酸(序列为QEQLERALNSS)的新型多肽,其生物多效性近年来被广泛证实。HBSP在缺血再灌注、炎性反应、神经创伤等多种生物模型中具有与EPO相似的组织保护作用,又无促红细胞生成的不良反应[7]。国外最新研究证实,在充血性心力衰竭及心肌梗死模型中,HBSP具有和EPO类似的心脏保护作用。然而HBSP对MIRI的影响鲜有报道。本研究细胞通过体外培养乳鼠心肌细胞,建立H/R细胞损伤模型,观察HBSP对心肌细胞凋亡及Omi/HtrA2转位率的影响,并探讨HBSP发挥心肌保护作用的分子机制。
1 材料与方法
1.1 材料与试剂
H9C2 细胞(南方医科大学珠江医院实验室)、胎牛血清、DMEM-高糖培养基、青霉素、PBS磷酸钾缓冲液和HBSP(上海科肽生物科技有限公司);重组EPO注射液(山东科兴生物制品有限公司);cellTiter96AQ单溶液细胞增殖检测试剂盒(Promega公司);乳酸脱氢酶细胞毒性检测试剂盒(赛默飞世尔科技公司);Cleaved caspase- 3多抗、GAPDH单抗、COX IV单抗、Omi/HtrA2单抗(Cell Signaling公司);Pluslight ECL kit (ECL发光试剂盒)(Forevergen Bioscience公司);原位缺口末端标记法(TUNEL)检测试剂盒(Roche公司);线粒体胞质分离试剂盒(Qiagen公司)。
1.2 实验方法
1.2.1 实验分组: 将H9C2细胞分为:1)对照组(Ctrl):细胞用DMEM-高糖培养基正常培养26 h,不作任何处理;2)缺氧复氧组(H/R):将待处理细胞、厌氧袋及氧气指示剂放入厌氧罐,将厌氧罐置于细胞培养箱,待氧气指示剂从浅紫色变成粉红色示无氧状态,开始计时缺氧时间,缺氧时间定为2 h,重新将细胞放置培养箱即为复氧状态,复氧24 h;3)HBSP组:同缺氧复氧组,在缺氧2 h加入不同浓度的HBSP(2.5、5和10 ng/mL)处理,然后复氧24 h。4)EPO组:同缺氧复氧组,在缺氧2 h后加入(40 IU/mL)的EPO,然后复氧24 h。
1.2.2 MTS法检测细胞存活率: 取指数增殖期细胞消化吹散并调整细胞至1×105/mL,按照实验分组进行处理,处理后的细胞加入cellTiter96AQ单溶液细胞增殖检测试剂,试剂与培养液比例为1∶10,孵育4 h后,酶标仪检测读取各样本AD490数据,得出的数据通过与对照组比较计算细胞存活率。
1.2.3 细胞上清液LDH浓度检测: 按实验设计培养结束后,提取上清液按照乳酸脱氢酶细胞毒性检测试剂盒说明书操作,测量细胞LDH释放率:

1.2.4 Western blot检测cleaved caspase- 3表达: 蛋白用Bradford法定量后,采用15%浓度的聚丙烯酰胺凝胶测cleaved caspase3,经SDS-PAGE电泳后将蛋白转至PVDF膜上,5%脱脂牛奶封闭后,将相应的一抗cleaved caspase- 3(Cell Signaling公司#9661,1∶1 000),4 ℃过夜后,用TBST每次7 min洗两次后,用相应的稀释好的二抗(HRP标记二抗,1∶5 000,Forevergen公司)室温下孵育1~2 h后,用TBST每次7 min洗3次后,进行化学发光显影(ECL,Forevergen公司)。用Image J分析目标条带的吸光度值,比较各组cleaved caspase3/GAPDH(HC301,1∶5 000)吸光度的差异。
1.2.5 TUNEL法检测心肌细胞凋亡: 根据TUNEL检测试剂盒进行检测,以LSM710型激光扫描共聚焦显微镜观察记录结果。每组细胞计数10个随机高倍视野中TUNEL阳性细胞核数和总细胞核数。计算TUNEL阳性细胞核数占总细胞核数的百分比即为凋亡率。
1.2.6 分离H9C2细胞胞质及线粒体,Western blot分别检测线粒体及细胞质Omi/HtrA2蛋白表达:选取10 ng/mL HBSP组细胞为实验对象,按照线粒体胞质分离试剂盒说明书分离线粒体蛋白及胞质蛋白,Western blot检测各组Omi/HtrA2蛋白表达,计算其转位率:

1.3 统计学分析

2 结果
2.1 心肌细胞存活率变化
与Ctrl组相比,H/R组细胞存活率明显下降(P<0.05),细胞上清液LDH浓度明显上升;与H/R组比较,HBSP的3个处理组细胞存活率逐渐升高, 各组细胞上清液LDH浓度逐渐回降(P<0.05)(表1)。
2.2 HBSP对细胞cleaved caspase- 3表达的影响
H/R组细胞cleaved caspase- 3表达较Ctrl组明显升高(P<0.05)。与H/R组相比,HBSP的2个处理组(5、10 ng/mL)的cleaved caspase- 3表达逐渐回降(P<0.05)(图1)。
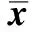
表1 心肌细胞存活率及LDH释放率的变化
*P<0.05 compared with Ctrl;#P<0.05 compared with H/R.
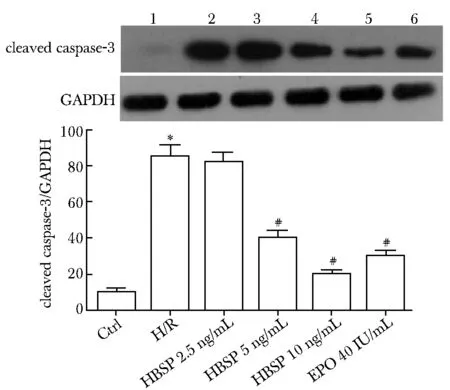
1.Ctrl;2.H/R;3.HBSP 2.5 ng/mL;4.HBSP 5 ng/mL;5.HBSP 10 ng/mL;6.EPO 40 IU/mL; *P<0.05 compared with Ctrl; #P<0.05 compared with H/R图1 各组细胞中cleaved caspase- 3的相对表达水平Fig 1 Western blot analysis of cleaved caspase- 3
2.3 各组心肌细胞凋亡率的比较
与Ctrl组相比,H/R组心肌细胞凋亡率明显升高(P<0.05);与H/R组相比,HBSP的2个处理组(5、10 ng/mL)及EPO组细胞凋亡率均明显回降(P<0.05)(图2)。2.4胞质及线粒体中Omi/HtrA2蛋白的表达情况
Ctrl组中Omi/HtrA2蛋白主要在线粒体内(mitochondrion,Mito)表达,在胞质(cytoplasma,Cyto)表达极少;H/R组中Omi/HtrA2蛋白在胞质中表达明显增加,在线粒体内表达减少,说明缺氧复氧诱导Omi/HtrA2蛋白由线粒体向胞质转位;而HBSP组和EPO组的Omi/HtrA2转位减少,说明HBSP和EPO均可抑制缺氧复氧诱导的Omi/HtrA2转位(P<0.05)(图3)。

*P<0.05 compared with ctrl group; #P<0.05 compared with H/R group图2 TUNEL法检测各组心肌细胞凋亡率Fig 2 The apoptosis of cardiomyocytes in different groups examined by TUNEL staining(×100)
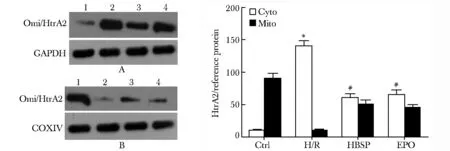
1.Ctrl;2.H/R;3.HBSP 10 ng/mL;4.EPO 40 IU/mL;A,B.expression of Omi/HtrA2 in Cyto(A) and Mito (B); GAPDH: Cyto marker; COXⅣ:Mito marker; *P<0.05 compared with Ctrl group; #P<0.05 compared with H/R group
3 讨论
在过去的10年里,EPO的生物多效性,尤其是对MIRI的保护作用被广泛证实[8]。由于EPO需要大剂量才能发挥组织保护作用,而大剂量EPO的不良反应(如高凝状态、血栓和高血压等)难以避免,EPO发挥组织保护效应在临床难以推广。HBSP是从EPO的三级结构helix B 段亲水表面中筛选合成而来,没有促红细胞生成的不良反应。通过扩张型心肌病仓鼠模拟充血性心力衰竭模型,发现HBSP可抑制TNF-α诱导的心肌细胞凋亡[9];有研究[10]通过大鼠心肌梗死模型发现HBSP能减小梗死面积,减少左室扩张,提高活性氧簇(reactive oxygen species,ROS)释放阈值,具有与EPO同样的保护效果;另有实验[11]证实HBSP抑制经C反应蛋白诱导的内皮细胞凋亡,降低经C反应蛋白诱导THP- 1细胞TNF-α和MM9的表达减轻巨噬细胞泡沫化,显著抑制心肌梗死兔子冠脉TNF-α表达和减少M1巨噬细胞;此外,在构建大鼠MIRI模型的实验中,发现HBSP 可显著抑制缺血再灌注诱导的大鼠心肌细胞凋亡,大鼠心肌梗死面积亦显著减少,心功能明显改善[12]。综上所述,目前HBSP对心脏保护作用逐渐被证实,然而在MIRI方面,HBSP能否像EPO一样减轻MIRI以及其具体保护机制尚不明确。本实验通过建立心肌细胞H/R模型,证实HBSP可抑制H/R诱导的心肌细胞LDH、caspase- 3表达增加,减少H/R诱导的心肌细胞凋亡率,同时观察到HBSP可抑制H/R心肌细胞Omi/HtrA2蛋白的胞质转位。
Omi/HtrA2蛋白是一种新近发现的促凋亡蛋白,在蛋白质修复和细胞凋亡中有重要作用。Omi/HtrA2在细胞正常生理情况下存在于线粒体膜间隙,当细胞受到凋亡信号刺激时完成自我加工,通过与X-连锁凋亡抑制蛋白(X-linked inhibitor of apoptosis protein,XIAP)结合,竞争性抑制XIAP与caspase- 9的结合,进而激活处于下游的caspase- 3蛋白表达,引起细胞凋亡。本实验结果显示,相比Ctrl组,H/R组Omi/HtrA2蛋白由线粒体转位至胞质中明显增多,而HBSP组随HBSP浓度增加Omi/HtrA2蛋白的转位率逐渐减少,提示HBSP可能是通过抑制Omi/HtrA2蛋白由线粒体转位至胞质,进而影响Omi/HtrA2对下游caspase- 9及caspase- 3通路激活作用, 最终减少细胞凋亡。诚然HBSP抑制细胞凋亡可能涉及多种因子,其具体的机制仍需进一步研究。本研究为HBSP的临床应用提供了一定的实验基础和理论依据。
[1] Bogoyevitch MA. An update on the cardiac effects of erythropoietin cardioprotection by erythropoietin and the lessons learnt from studies in neuroprotection[J]. Cardiovasc Res, 2004,63:208- 216.
[2] Riksen NP, Hausenloy DJ, Yellon DM. Erythropoietin: ready for prime- time cardioprotection[J]. Trends Pharmacol Sci, 2008,29:258- 267.
[3] Voors AA, Belonje AM, Zijlstra F,etal. A single dose of erythropoietin in ST-elevation myocardial infarction[J]. Eur Heart J, 2010,31:2593- 2600.
[4] Ludman AJ, Yellon DM, Hasleton J,etal. Effect of erythropoietin as an adjunct to primary percutaneous coronary intervention: a randomised controlled clinical trial[J]. Heart, 2011,97:1560- 1565.
[5] Ferrario M, Arbustini E, Massa M,etal. High-dose erythropoietin in patients with acute myocardial infarction: a pilot, randomised, placebo-controlled study[J]. Int J Cardiol, 2011,147:124- 131.
[6] Najjar SS, Rao SV, Melloni C,etal. Intravenous erythropoietin in patients with ST-segment elevation myocardial infarction: REVEAL: a randomized controlled trial[J]. JAMA, 2011,305:1863- 1872.
[7] Brines M, Patel NS, Villa P,etal. Nonerythropoietic, tissue-protective peptides derived from the tertiary structure of erythropoietin[J]. Proc Natl Acad Sci U S A, 2008,105:10925- 10930.
[8] 郭晋村, 黄卫斌, 王挹青, 等. 促红细胞生成素减轻大鼠心肌缺血再灌注损伤[J]. 基础医学与临床, 2010:289- 292.
[9] Patel NS, Nandra KK, Brines M,etal. A nonerythropoietic peptide that mimics the 3D structure of erythropoietin reduces organ injury/dysfunction and inflammation in experimental hemorrhagic shock[J]. Mol Med, 2011,17:883- 892.
[10] Ahmet I, Tae HJ, Juhaszova M,etal. A small nonerythropoietic helix B surface peptide based upon erythropoietin structure is cardioprotective against ischemic myocardial damage[J]. Mol Med, 2011,17:194- 200.
[11] Ueba H, Shiomi M, Brines M,etal. Suppression of coronary atherosclerosis by helix B surface Peptide, a nonerythropoietic, tissue-protective compound derived from erythropoietin[J]. Mol Med, 2013,19:195- 202.
[12] 蒋娜, 叶瑾, 党晶艺, 等. 促红细胞生成素衍生肽抑制缺血/再灌注损伤诱导的大鼠心肌细胞凋亡[J]. 心脏杂志, 2013:327- 332.
新闻点击
60岁以下女性患糖尿病恐将提高心脏病风险
据美国国家科学院院报(PNAS)网站2013-11-07报道,一般而言,在60岁以下患冠状动脉疾病的风险,同年龄层的女性比男性要低,但最近发表的一项美国研究却进一步发现,若本身有心脏病的风险因子之一“糖尿病”,将对这些女性产生与男性不同的影响。
目前约翰霍普金斯大学医学院针对3份研究中包含超过1万名男女参与者的数据进行分析,所有参与者都无心脏病病史。结果发现,60岁以下年轻与中年女性有2型糖尿病的话,她们患冠状动脉疾病的机会就大幅提高,风险增加了将近4倍之多,该风险数值已大致与男性心脏病风险相当。不过,糖尿病影响心脏病风险的情形却在相同年龄层的男性身上并不明显。
研究表示,其他风险因子如肥胖、高血压、糖尿病与吸烟对患心脏病的影响在研究中都未被发现有任何性别差异,唯独糖尿病对女性心脏病的影响远远超过男性。研究推测可能有不同的基因及激素因素影响着不同性别心脏病的发展过程,同时,不同性别对于医嘱与治疗的顺从程度也不一,这也可能是造成差异的原因之一,未来将需要更进一步的研究。
他汀类降血脂药物(Statins)恐提高患白内障风险
据美国国家科学院院报(PNAS)网站2013-11-08报道,过去针对降血脂药物Statins的讨论包括质疑该类药物对女性的效益不如男性,以及去年美国食品药物管理局要求该类药物应加注提高短暂性记忆认知受损、及血糖升高的警语。日前又有一项美国研究指出,使用Statins药物者比未使用者发生白内障眼疾的风险高,而这个争议性的发现早在1980年代药物出现时就曾被提出。
有关于Statins与白内障风险的关系,过去有些研究证实其中因果关系,但也有其他研究却发现该类药物对预防白内障具有保护作用,出现两种截然不同的结论。由于Statins类药物越来越常被用来作为初级预防用途,且白内障使生活质量受影响及造成美国健康照护支出的负担也非常大,因此这个问题相当重要。
这项回溯性研究针对过去两个共包含超过4万名参与者的研究进行分析,第一个研究参与者的平均年龄56岁,女性占46%;第2个研究参与者使用Statins的平均年龄为56岁、未使用者为46岁,两组中的女性各占40%和52%。
最后分析两个研究的结果显示,使用Statins药物都与发生白内障呈现显著的正向相关性,坏胆固醇(LDL)的数值愈低时,白内障风险反而愈高。其中一个计算出与未使用Statins相比的风险增加数据为9%(95% CI 1.02~1.17)。
白内障及青光眼主治医生Anurag Shrivastava评论此研究时表示,这项研究无法提供使用Statins药物的患者预防白内障的建议,但就一般而言,还是以维持均衡饮食、健康的生活形态、不抽烟及减少暴露于紫外线,并对糖尿病进行严格血糖控制为基本预防建议,同时,医生应小心Statins使用者有无并服类固醇,服用这些药物可能会增加白内障及青光眼的发生。
HBSP inhibits transposition of Omi/HtrA2 and apoptosis of myocardial cells induced by anoxia-reoxygenation
YOU Wei, LIU Ying-feng, ZHANG Jie-bo, LIN Yong-luan, MIAO Fei, LIU Peng*
(Dept. of Cardiovascular Medicine, Zhujiang Hospital, Southern Medical University, Guangzhou 510282,China)
ObjectiveTo investigate the effect of helix B surface peptide(HBSP) on transposition of Omi/HtrA2 and apoptosis of myocardial cells induced by anoxia-reoxygenation.MethodsNeonatal rat myocardial cells (H9C2 cells) were used to be research object, the cells were divideded into 4 groups:control group, H/R group, HBSP group and EPO group. The cell viability was measured by MTS assay, the concentration of LDH of cell supernatant was assessed by ELISA, the intracellular expression changes of cleaved caspase-3 was detected by Western blot. Apoptosis of cardiomyocytes was detected by TUNEL.Using mitochondria/cytosol isolation kit to isolate mitochondria from cytosol, Western blot was used to detect the expression of Omi/HtrA2 protein changes in the mitochondrial and cytosolic.ResultsCompared with the control group, H/R group cell survival rate decreased significantly(P<0.05), cell supernatant LDH concentration increased significantly,the expression of cleaved caspase- 3 increased, the cardiomyocyte
anoxia-reoxygenation; HBSP; EPO; apoptosis; Omi/HtrA2
2014- 11- 04
:2015- 01- 23
广东省自然科学基金(10151051501000038); 广东省科技计划(20130319c)
*通信作者(correspondingauthor):65473751@qq.com
1001-6325(2015)05-0615-06
研究论文
R541
:A
apoptosis and the expression of Omi/HtrA2 protein in the cytoplasm increased significantly (P<0.05). Compared with H/R group, EPO and HBSP group cell survival rate increased, cell supernatant concentrations of LDH, cleaved caspase- 3, cardiomyocyte apoptosis and the Omi/HtrA2 protein in the cytoplasm expression decreased significantly (P<0.05).ConclusionsH/R can induce apoptosis of myocardial cell,which can be reduced by EPO or HBSP,its mechanism may be related to the inhibition of Omi/HtrA2 protein in mitochondrial translocation, thus inhibiting the caspases pathway activation.
