1例泌尿系感染合并肾功能不全患者抗感染治疗的药学服务
2015-07-30刘慧敏夏晶李鹏朱雪松
刘慧敏,夏晶,李鹏,朱雪松
(1.湖北医药学院附属东风医院药学部,十堰 442008;2.武汉市第三医院临床药师培训基地,武汉 430060)
感染是重症监护病房患者(intensive care unit,ICU)的主要死亡原因之一,抗感染是重要治疗手段,是医师最关注的问题。肾功能不全合并感染治疗难度大,既需快速控制感染,又需避免蓄积中毒。这类患者如何用药值得深思。笔者通过对1例泌尿系感染并发肾功能不全老年患者使用替考拉宁的治疗过程,分析用药合理性,开展药学监护。
1 病例概况
患者,女,85岁,体质量65 kg。因突发头晕伴恶心、呕吐4 h余,于2014年2月14日入院,门诊以高血压3级(极高危)、颈椎病(椎基底动脉供血不足)收入心内科,给予降压、改善循环等相关治疗,逐渐出现嗜睡、血压下降、纳差、血尿、咯痰、昏迷,血氧饱和度降至85%,于2014年2月16日送入ICU治疗。既往有慢性支气管炎、脑梗死、慢性胃炎、胃溃疡、慢性肾功能不全病史。血常规:白细胞 8.8×109·L-1,中性粒细胞百分比 82.4%(↑);肾功能:尿素氮 12.5mmol·L-1(↑),血肌酐 220.0 μmol·L-1(↑);尿常规:白细胞152个·μL-1(↑),红细胞 3 156 个·μL-1(↑),尿蛋白+++(↑)。血气分析示pH 7.14(↓),二氧化碳分压 9.44 kPa(↑),氧分压 6.92 kPa(↓),血氧饱和度75% ,提示Ⅱ型呼吸衰竭,呼吸性酸中毒。主要诊断:①慢性阻塞性肺疾病,急性加重期,Ⅱ型呼吸衰竭;②高血压病3级(极高危);③急性多发性脑梗死;④肾功能不全;⑤血尿原因待查。
2 主要治疗经过和药学监护
2.1 抗感染主要治疗经过 2014年2月16日,患者意识下降,中度昏迷,经皮血氧饱和度71%,行气管插管,呼吸机辅助呼吸,导尿管中可见肉眼血尿、尿色浑浊,少尿,下肢水肿,间断发热,吸出中等量黄色粘痰,胸部X线片提示双肺感染,考虑肺部感染、泌尿系感染,给予头孢哌酮/他唑巴坦2 g+0.9%氯化钠注射液250mL,静脉滴注,q12 h。完善尿培养。2014年2月19日,肾功能恶化,降钙素原提示患者存在感染,尿培养示屎肠球菌感染,抗感染药物更换为比阿培南0.3 g+0.9%氯化钠注射液 100mL,静脉滴注,qd,加用替考拉宁(前3剂负荷量:0.4 g+0.9%氯化钠注射液100mL,静脉滴注,q12 h,维持量 0.4 g+0.9% 氯化钠注射液100mL,静脉滴注,q3 d)。2014年2月21日,患者神志好转,2次尿培养均为屎肠球菌,补充诊断泌尿系感染。2014年2月23日,患者尿色清亮,尿量增多,感染好转,停用比阿培南,换用头孢哌酮舒巴坦3 g+0.9%氯化钠注射液250mL,静脉滴注,q12 h,替考拉宁血药浓度46.56 mg·L-1。2014年2月28日,患者肢体水肿减轻,血压逐渐稳定,体温峰值有所下降,尿培养未见细菌生长,血替考拉宁浓度10.97 mg·L-1。2014年3月 4日,患者体温恢复正常,肾功能好转,血替考拉宁浓度 5.17 mg·L-1,将替考拉宁维持量增大至0.4 g+0.9%氯化钠注射液100mL,qd。2014年3月6日,考虑替考拉宁浓度低,重新给予负荷量(前3剂0.4 g+0.9%氯化钠注射液100mL,q12h),维持量 0.4 g+0.9% 氯化钠注射液100mL,qd。2014年3月8日,负荷量结束后血药浓度20.79 mg·L-1。2014年3月16日,患者自主呼吸好转,可脱离呼吸机8 h,考虑泌尿系感染控制较好、肺部感染也得到控制,停用替考拉宁。
2.2 实验室检查
2.2.1 血常规、降钙素原及肝肾功能检查结果 白细胞、中性粒细胞百分比、降钙素原及血小板、肌酐、肝功能指标见表1。
2.2.2 病原学相关检查报告 各体液细菌病原学培养和药敏试验报告见表2。2014年2月22日,将痰涂片革兰染色后发现白细胞10~20个,革兰阳性球菌>40个,革兰阴性双球菌>40个。多次检测,血清1,3-β-葡聚糖均为阴性,发热、呼吸道和泌尿道症状未见加重,暂不考虑真菌感染。
2.3 体温 每日体温峰值与替考拉宁血药浓度见如图1所示。
2.4 药物选择与初始剂量 患者入科后生命体征不稳定,感染严重,尿培养示屎肠球菌,痰涂片示革兰阳性菌较多。结合药敏试验结果,可选择对革兰阳性菌作用较强的万古霉素和利奈唑胺。而考虑万古霉素的肾毒性[1]和利奈唑胺对血小板影响明显[2],选择了抗革兰阳性球菌的有效药物替考拉宁,它对耐甲氧西林金黄色葡萄球菌(methicillin-resistantStaphylococcus aureus,MRSA)、屎肠球菌等多重耐药性的细菌具有良好的抗菌活性,耐受性良好。替考拉宁静脉给药的一般剂量为3 ~12 mg·kg-1,消除半衰期为155 ~188 h,血浆蛋白结合率为90% ~95%,体内代谢很少,97%的药物由肾脏从尿中以原形排出;肾功能障碍患者血浆半衰期明显延长,达 102 ~347 h[3]。
患者入科时存在肾功能不全,肌酐清除率仅为16.9mL·min-1,按照说明书使用:前 3 剂为负荷量为0.4 g,q12 h,然后给予维持量为 0.4 g ,q3 d。而《替考拉宁临床应用剂量中国专家共识(第二稿)》推荐“对于肌酐清除率10~50mL·min-1患者,负荷量为6~12 mg·kg-1,q12h,共 3 次,维持量为 6 ~12 mg·kg-1,q48h,该患者维持量为 0.4 ~ 0.8 g,q48 h,最大剂量高于说明书用量。目前普遍认为对于肾功能不全的患者建议监测替考拉宁血药浓度,特别是当肌酐清除率 <0.30mL·min-1·kg-1时,个体差异明显,必须监测,当血清谷浓度≥10 mg·L-1时为有效浓度[4],但高于60 mg·L-1时,血小板减少的发生率明显增高[5],故10 ~60 mg·L-1较合适。临床药师认为替考拉宁初始给药方案可行,建议医师监测血清谷浓度,若感染控制不佳、浓度偏低时可将维持量给药间隔缩短至2 d。按照初始给药方案,2014年2月23日,患者血药浓度46.56 mg·L-1,且尿路症状缓解,降钙素原降低,提示初始抗感染治疗有效。

表1 血常规中白细胞、中性粒细胞百分比、血小板、降钙素原、血肌酐及血清清蛋白检查结果

表2 体液细菌病原学培养和药敏试验检验报告
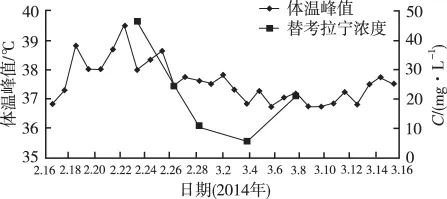
图1 体温峰值与替考拉宁血药浓度曲线
2.5 血药浓度监测与剂量调整 长期以来,很多文献认为替考拉宁血清谷浓度>10 mg·L-1对于多数感染有效,谷浓度>20 mg·L-1对于严重感染(如感染性心内膜炎、血行感染、肺炎、骨和假体感染)有效,新观点则认为>15 mg·L-1的血药浓度对常见感染的临床疗效更好[6]。2014年2月28日,患者血替考拉宁浓度为10.97 mg·L-1,肌酐清除率已上升至26.8 mg·min-1,推测半衰期较前缩短,根据《替考拉宁中国专家共识(第二稿)》的推荐意见,维持剂量应该0.4 ~0.8 g,q48 h,目前的剂量偏小,疗效难以保证,于是药师建议将给药间隔加至每2 d一次,但医师考虑患者当时体温峰值有所下降,感染好转趋势明显,未采纳。
2014年3月4日,血肌酐进一步恢复,肌酐清除率达 40.7mL·min-1,替考拉宁血药浓度仅为5.17 mg·L-1,医师将维持量增加至 0.4 g,qd。虽然当时患者体温开始恢复正常,但中性粒细胞比例仍高,提示感染仍然存在,但替考拉宁谷浓度已低于有效浓度,可能影响治疗效果,也易诱发细菌耐药,宜快速将谷浓度提升至有效浓度之上,药师建议重新负荷给药。医师于2014年3月6日采纳药师建议之后即达有效浓度,未见发热反复,说明感染得到控制。负荷给药的方式很多,患者2014年3月6日前3剂0.4 g,q12h的负荷方式与PEA[7]推荐的方式相同,在第3天达到了20.79 mg·L-1的谷浓度,此后按照 0.4 g,qd 维持,症状未见反复,且自主呼吸好转,肺部感染得到控制;BRINK 等[8]则推荐负荷量6 mg·kg-1,q12 h,2 d 后以6 mg·kg-1,qd 的剂量维持;UDEA[6]推荐对肾功能正常的患者可采用10~12 mg·kg-1,bid给药2 d,然后第3天给予10~12 mg·kg-1,qd后可达到15 ~30 mg·L-1的血药浓度等,剂量较大,而本病例中患者后期肌酐清除率仍属轻度异常可能不适用。由此可见,肾功能对于替考拉宁药动学影响较大,随肾功能的变化及时调整剂量才能保证疗效。
2.6 影响替考拉宁血药浓度的其他因素 研究发现[9],危重患者血流动力学紊乱、低蛋白血症或毛细管渗漏综合征等病理生理条件,均可影响抗菌药物在体内的代谢和排泄,从而改变药动学。因替考拉宁血清清蛋白结合率很高,低蛋白血症的患者中血药浓度会升高,YANO等提出了表现二者关系的公式“替考拉宁血药浓度=替考拉宁药量/[1+1.78×血清清蛋白浓度]”,但ROBERTS等[10]发现公式并不准确。本病例中药师根据此公式计算结果也与实测浓度不符,考虑血药浓度除与肾功能和血清清蛋白含量有关外,可能与肢体水肿改变了分布容积也有关,所以多种影响因素存在时,进行血药浓度监测更有必要。
2.7 监测替考拉宁的不良反应 替考拉宁可引起皮疹、肾毒性、肝功能异常与血小板减少等不良反应,但多发生于剂量高于临床常规用量或用药期较长时[5],药师对这些不良反应进行监测。如表1所示,用药期间患者血肌酐呈降低趋势,肾功能逐渐好转;血小板稳定在(194 ~249)×109·L-1范围内,未见皮疹发生,转氨酶无异常,安全性良好。
3 结束语
临床药师对替考拉宁的治疗方案进行分析,在建议临床监测血药浓度及重新负荷给药等方面提出建议并被采纳,并对肝、肾毒性,血小板减少和皮疹4类不良反应进行了监护,协助临床个体化治疗。危重患者的多种生理病理因素均能影响替考拉宁血药浓度,其中肾功能是主要影响因素,在患者肾功能不全的情况下,有必要监测血药浓度;当血药浓度低于有效浓度时,需重新给予负荷剂量;当肾功能变化时,应及时调整剂量或给药间隔,才能保证疗效,避免蓄积。通过参与上述抗感染病例的治疗。
[1]刘凌,方利洲,傅炜萍,等.替考拉宁治疗医院获得性肺炎伴肾功能不全的临床疗效和安全性评价[J].中华医院感染学杂志,2010,20(9):1307-1309.
[2]FALAGAS M E,SIEMPOS I I,VARDAKAS K Z.Linezolid versus a glycopeptides or lactam for treatment of Grampositive bacterial infection;a meta-analysis of randomized controlled trials[J].Lancet Infect Dis,2008,8(1):53-66.
[3]陆辉志,徐亮.替考拉宁在血药浓度监测下临床应用一例[J].中华危重症医学杂志(电子版),2013,6(4):245-246.
[4]胡萨萨,董亚琳.替考拉宁在不同人群中的药动学与给药方案分析[J].西北药学杂志,2009,24(3):232-234.
[5]李昊,田刚,王雪.肾功能不全患者替考拉宁药物浓度监测的研究进展[J].中国抗生素杂志,2010,35(11):815-839.
[6]UDEA T,TAKESUE Y,NAKAJIMA K,et al.High-dose regimen to achieve novel target trough concentration in teicoplanin[J].J Infec Chemother,2014,20(1):43-47.
[7]PEA F,BROLLO L,VIALE P,et al.Teicoplanin therapeutic drug monitoring in critically ill patients:a retrospective study emphasizing the importance of a loading dose[J].J Antimicrob Chemother,2003,51(4):971-975.
[8]BRINK A J,RICHARDS G A,CUMMINS R R,et al.Recommendations to achieve rapid therapeutic teicoplanin plasma concentrations in adult hospitalised patients treated for sepsis[J].Int J Antimicrob Agents,2008,32(5):455-458.
[9]王硕,吕凯,刘明亮.危重病患者抗生素治疗的剂量调节原则[J].国外医药抗生素分册,2011,32(2):65-71.
[10]ROBERTS J A,STOVE D,WAELE J J,et al.Variability in protein binding of teicoplanin and achievement of therapeutic drug monitoring targets in critically ill patients:lessons form the DALI Study[J].Int J Antimicrob Agents,2014,43(5):423-430.
