盐酸罗哌卡因的合成工艺研究
2015-07-12李玉双晗山东金诃药物研究开发有限公司山东济南250101
彭 坤 李玉双 李 晗山东金诃药物研究开发有限公司,山东济南250101
盐酸罗哌卡因的合成工艺研究
彭 坤 李玉双 李 晗
山东金诃药物研究开发有限公司,山东济南250101
[摘要]目的 探讨盐酸罗哌卡因的合成方法。 方法 本研究以2-哌啶甲酸为起始原料,与2,6-二甲基苯胺进行酰胺化反应得到N-(2,6-二甲基苯)-2-哌啶甲酰胺,与溴代正丙烷进行取代反应得到N-(2,6-二甲基苯基)-1-正丙基哌啶-2-甲酰胺,再通过与D-酒石酸在有机溶剂中拆分反应即可制得盐酸罗哌卡因。结果 所得盐酸罗哌卡因的光学纯度在99.5%以上,总收率约25%。 结论 本方法操作简便,所得产品光学纯度高,适合于药用,具有一定的商业化价值。
[关键词]盐酸罗哌卡因;酰胺类局麻药;合成;光学纯度
盐酸罗哌卡因(ropivacaine hydrochloride,化合物5),化学名为(-)-S)-N-(2,6-二甲基苯基)-1-正丙基哌啶-2-甲酰胺盐酸盐,分子式为C17H26N2O·HCl,是瑞典Astra制药公司1996年上市的新型纯左旋体长效酰胺类局麻药,具有镇痛和麻醉双重作用,广泛用于神经阻滞麻醉,局部浸润麻醉和硬膜外麻醉,与同类酰胺类局部麻醉药如布比卡因相比,使用时效更长,对心脏毒性更小。其药理学特点为心脏毒性低微,感觉阻滞与运动阻滞分离较明显,具有外周血管收缩作用。因此该药尤其适用于术后镇痛和产科麻醉[1-11]。
1 材料与仪器
1.1原理
盐酸罗哌卡因的合成方法报道较多[12-19],综合来看主要分以下两种。
(1)L-2-哌啶甲酰氯或L-2-哌啶甲酸为起始原料,经五氯化磷或氯化亚砜酰化,再与2,6-二甲基苯胺缩合,然后再与溴代正丙烷反应得到罗哌卡因。市售L-2-哌啶甲酸平均价格是消旋化2-哌啶甲酸的5~8倍,原料成本太高,不利于成本控制,且在后续反应过程中可能会出现消旋化现象,影响产品光学纯度,不利于产品质量控制[12-17]。
(2)以消旋化的2-哌啶甲酸为原料,经过酰胺化、烷基化反应,最后通过拆分反应制备盐酸罗哌卡因,该方法使用三光气制备酰氯,在贮存和后处理时存在危险性,同样不适合工业化生产。且拆分试验过于简单,在其试验条件下无法得到高光学纯度的罗哌卡因[18-19]。
本研究参照上述方法,对现有的盐酸罗哌卡因制备工艺进行改进,其合成路线见图1,以2-哌啶甲酸(化合物1)为原料,在氯化亚砜酰化作用下与2,6-二甲基苯胺缩合生成N-(2,6-二甲基苯)-2-哌啶甲酰胺(化合物2),再与溴代正丙烷取代反应得到N-(2,6-二甲基苯基)-1-正丙基哌啶-2-甲酰胺(化合物3),最后在钛酸四异丙酯和D-酒石酸的共同作用下拆分出罗哌卡因酒石酸盐,通入氯化氢气体成盐得到盐酸罗哌卡因粗品(化合物4),将粗品精制纯化即可得到盐酸罗哌卡因(化合物1)。
1.2 仪器与试剂
DF-101S集热式恒温加热磁力搅拌器(巩义市予华仪器有限公司);YP2102电子天平(上海光正医疗仪器有限公司);EYELA N-1100型旋转蒸发仪(日本东京理化);Agilent 1260型高效液相色谱仪(美国安捷伦),2020-2EBS电热恒温干燥箱(北京市永光明医疗仪器厂),SHZ-95B循环水式真空泵(巩义市予华仪器有限公司)。
2-哌啶甲酸(济南德信佳生物科技有限责任公司,化工品级,130426批);氯化亚砜(天津光复化学研究所,分析纯);2,6-二甲基苯胺(河北大鹏医药化工有限公司,化学纯,2,6-X130822批);溴代正丙烷(成都市科龙化工试剂厂,分析纯);钛酸四异丙酯(淄博日启橡塑助剂有限公司,化学纯);D-酒石酸(天津市光复精细化工研究所,分析纯);甲苯(莱阳经济开发区精细化工厂,分析纯);盐酸(莱阳经济开发区精细化工厂,分析纯);硫酸(莱阳经济开发区精细化工厂);氢氧化钠(天津市津科化工有限公司);无水硫酸钠(天津市光复精细化工研究所);二氯甲烷(天津百世化工有限公司);DMF(天津市富宇精细化工有限公司);异丙醇(天津市富宇精细化工有限公司);无水乙醇(天津市富宇精细化工有限公司)。
2 方法与结果
2.1合成路线图(图1)

图1 盐酸罗哌卡因的合成路线
2.2实验过程
2.2.1N-(2,6-二甲基苯)-2-哌啶甲酰胺的制备 将10.0g 2-哌啶甲酸、160mL甲苯加入500mL反应瓶中。通入HCl气体,至pH2~3,升温至45~50℃,加入1.5mL DMF,滴加9.3g(1.0当量)氯化亚砜与20mL甲苯混合液,滴毕,保温50~55℃反应3h。滴加2,6-二甲基苯胺与20mL甲苯混合液,保温55~60℃反应3h。过滤,得黄绿色湿品约65g,烘干得灰色固体56g,将固体加入280mL纯化水中,搅溶;将10% NaOH溶液缓慢滴加至反应液中,调pH至4.5~5.0,用100mL甲苯洗涤,分层,保留水层,继续用碱液调pH至9~10,加入100mL二氯甲烷。分层,取有机层,水层继续用50mL二氯甲烷萃取,合并有机层,无水硫酸钠干燥,40℃减压浓缩。浓缩毕,得淡黄色油状液体约14.8g,收率82.4%,即为中间体(Ⅰ)N-(2,6-二甲基苯)-2-哌啶甲酰胺。
2.2.2N-(2,6-二甲基苯基)-1-正丙基哌啶-2-甲酰胺的制备 将14.8g中间体(I)溶于60mL DMF中,加入8.5g K2CO3,滴加7.8g(1.0当量)溴代正丙烷,滴毕后升温至75~80℃,保温反应2h;降至室温,过滤,将滤液加入150mL冰水中,析出大量白色固体,过滤,烘干,得白色固体约16.6g,收率95%,即为中间体(Ⅱ)N-(2,6-二甲基苯基)-1-正丙基哌啶-2-甲酰胺。
2.2.3罗哌卡因酒石酸盐的制备 将16.6g中间体(Ⅱ)溶于100mL异丙醇中,升温40℃搅溶;待全溶,依次加入1.72g(0.1当量)钛酸四异丙酯、1.82g(0.2当量)D-酒石酸,升温至回流,溶清之后继续反应2h;降温,降至30 ~ 35℃析晶,过滤,75℃烘干,得白色固体8.3g,收率39.1%,即为罗哌卡因酒石酸盐。
2.2.4盐酸罗哌卡因的制备 将8.3g罗哌卡因酒石酸盐加入50mL异丙醇中,升温至50℃,滴加浓盐酸,测pH为1~2,保温反应2h。降温至0~5℃析晶,析出大量白色固体,过滤,烘干,得白色固体约6.3g,收率85.2%,即为盐酸罗哌卡因粗品。
将6.3g粗品和40mL无水乙醇-浓盐酸混合液(20∶1)加入反应瓶中,加热至50℃使溶解;全溶后,降温析晶,冰水浴降温至0~5℃,析晶2h;过滤,滤饼用少量冷的混合液洗涤,得到湿品,烘干,得白色固体5.8g,收率92.1%,即为盐酸罗哌卡因。mp144~146℃(文献[13]:143~146℃)。光学纯度≥99.5%[色谱条件:以α1-酸性糖蛋白(α1-acidglycoprotein)键合硅胶为填充剂的AGP手性色谱柱(100mm×4mm,ф5μm);以乙腈-磷酸盐缓冲液(pH 6.0)(每1L中含0.07mol磷酸二氢钠与0.01mol磷酸氢二钠的溶液100mL,加水稀释至400mL)(15:85)为流动相;流速为0.9mL/min;检测波长为302nm;柱温30℃;进样量20μL]。ES-MS(m/z):275[M+H]+;1H-NMR(DMSO-d6,300MHz)δ:0.89(t,3H),1.50~1.73(m,1H),1.80(m,2H),1.80(m,2H),1.80(m,2H),2.17(s,6H),2.95~3.08(m,3H),3.08~3.49(m,2H),4.45 (t,1H),7.11(m,3H),11.07(s,1H)。
2.3结果
依照上述方法,投入32.5g起始原料1 试验,制得48.1g中间体2,收率82.9%;反应制得中间体3 54.3g,收率95.3%;进而制得34.0g中间体4,收率40.5%;最后成盐酸盐生成5(盐酸罗哌卡因)并精制得产品19.7g,收率79.4%,总收率25.4%(以起始物料0.25mol计算),检测光学纯度为99.8%(中国药典2010年版第二增补本中盐酸罗哌卡因质量标准要求光学纯度≥99.5%),各步收率情况见表1。通过试验结果可以看出:本合成工艺操作简便,收率较高,关键质量标准指标光学纯度符合药典标准,质量可控。
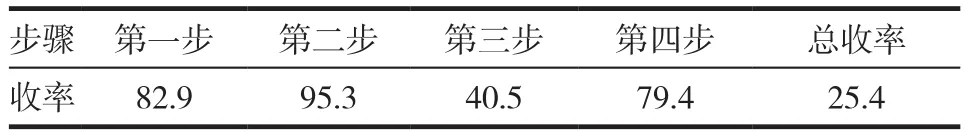
表1 各步反应收率汇总(%)
3 讨论
目前,盐酸罗哌卡因的合成方法主要存在产物光学纯度低、操作步骤繁琐的问题。参考文献[13]中所述一锅法制备盐酸罗哌卡因方法采用L-2-哌啶甲酸为起始原料,反应制得盐酸罗哌卡因。虽然简化了操作步骤,但市售L-2-哌啶甲酸作为起始原料成本太高,不利于成本控制;市售购得的L-2-哌啶甲酸其光学纯度仅98%以上,且在后续反应过程中可能会出现消旋化现象,影响产品光学纯度,产品质量难以满足药用标准(>99.5%)。参考文献[14]中使用L-2-哌啶甲酰氯为起始原料,同参考文献[13]存在类似的成本高、后续光学纯度不可控的问题。参考文献[17]以消旋化的2-哌啶甲酸为原料,经过酰胺化、烷基化反应,最后通过拆分反应制备盐酸罗哌卡因,该方法使用三光气制备酰氯,在贮存和后处理时存在危险性,同样不适合工业化生产;且拆分试验过于简单,在其试验条件下无法得到高光学纯度的罗哌卡因。
本研究在上述现有方法的基础上,通过大量试验,克服各方法中的缺点,摸索出一种盐酸罗哌卡因新的合成方法。本方法所采用的起始原料市售易得,价格低廉,通过后拆分,能够有效提高产物的光学纯度,将异构体杂质控制在较低的水平,光学纯度大于99.5%,适合于药用,具有一定的商业化价值。
罗哌卡因作为新型的长效酰胺类局部麻醉药,克服了传统长效局麻药的疗效短、可控性差以及可诱发心脏骤停的缺点,是一种脂溶性较低、更为安全的替代药品。其作用持续时间长,且具有麻醉和止痛的双重作用。其药理学特点为心脏毒性低微,感觉阻滞与运动阻滞分离较明显,具有外周血管收缩作用。该药尤其适用于术后镇痛和产科麻醉。该药具有很强的商业价值,本研究对原有的合成方法进行了改进,解决的有机试剂用量大、总体收率低、产品光学纯度低的缺点,提供了一种简洁实用、经济高效的盐酸罗哌卡因合成方法。但本研究提供的方法仍有一定的可优化空间,可以进一步改进。
[参考文献]
[1] 芮睿,程桥,凡浙录.罗哌卡因与舒芬太尼对创面愈合的影响[J].当代医学,2015,3,21(8):5-7.
[2] 周军.左布比卡因和罗哌卡因硬膜外麻醉效果比较[J].中国当代医药,2012,19(7):107-108.
[3] 黎笔熙,田玉科.罗哌卡因的基础研究与临床应用进展[J].华南国防医学杂志,2009,23(2):81-84.
[4] 梁健华,程平瑞,阮绪广,等.罗哌卡因复合喷他佐辛用于臂丛神经阻滞的效果观察[J].中国当代医药,2010,17(12):63-64.
[5] 张海生,张泳.吗啡复合罗哌卡因用于晚期癌痛患者硬膜外自控镇痛的疗效观察[J].中国医学创新,2013,10 (5):131-132.
[6] 李秀泽,谭玲.罗哌卡因的研究近况及临床应用[J].实用医药杂志,2004,21(6):554-555.
[7] 韦小友.甲磺酸罗哌卡因复合利多卡因在老年硬膜外麻醉中的应用[J].中国当代医药,2014,21(12):175-176.
[8] 徐露,李元海.舒芬太尼的药理作用和临床应用研究进展[J].安徽医药,2011,15(3):375-377.
[9] 赵波.不同浓度罗哌卡因复合利多卡因在臂丛肌间沟神经阻滞的应用[J].中国当代医药,2011,18(5):64-65.
[10] 方琴,赵正兰,祝燕琴.罗哌卡因应用于会阴侧切术的效果分析[J].中国医学创新,2012,9(14):22-23.
[11] 丁浩,王智珊,高其厚,陈刚.罗哌卡因局部浸润联合舒芬太尼静脉镇痛用于胸科术后镇痛[J].中国美容医学,2012(18):388-389.
[12] 薛克亮,黄明湖,江敏. 盐酸左布比卡因合成工艺改进[J].中国医药工业杂志,1990,21(6):250-251.
[13] 赵思太,任业明,沈乃涛,等.一种制备罗哌卡因的方法:中国,CN103086954 A[P].2013.05.08.
[14] Bo T.af Ekenstam,Hialteby,Christer Bovin,Frolunda,both of Sweden.L-N-N-propylpipecolic acid-2,6-xylidide:美国,US4695576[P].1987.09.22.
[15] Thuresson Af Ekenstam,Bovin Christer.L-N-n-Propylpipecolic Acid-2,6-xylidide and method for preparing the same:欧洲,EP0151110B1[P].1989.01.03. [16] 严波,张毅,徐华斌,等.富集哌啶-2-甲酰苯胺类旋光化合物的方法:中国,CN102093284 A[P]. 2011.06.15.
[17] 蒋瑶.盐酸罗哌卡因和盐酸布比卡因的合成工艺研究[D].长沙:湖南大学,2006:41-45.
[18] P·雅克斯赫.制备罗哌卡因盐酸盐一水合物的新方法:中国,CN1189822[P].1998.08.05.
[19] 马群立,黄庆云.罗哌卡因甲磺酸盐的制备方法及其化合物和制剂:中国,CN1517337[P].2004.08.04.
[中图分类号]TQ463.53
[文献标识码]B
[文章编号]2095-0616(2015)23-79-04
收稿日期:(2015-10-10)
Research on synthetic technology of ropivacaine hydrochloride
PENG Kun LI Yushuang LI Han
Shandong ARURA Pharmaceutical Research & Development CO., LTD. Ji'nan 250101, China
[Abstract]Objective To explore the synthetic method of ropivacaine hydrochloride. Methods 2-piperidinecarboxylic acid was starting material. N-(2, 6-dimethylphenyl)-2-pppiperidine amide was obtained by amidation reaction of 2-piperidinecarboxylic acid and 2, 6-dimethylaniline. N-(2, 6-dimethylphenyl)-1- n-propyl-2-piperidine formamide was obtained by substitution reaction of 1-bromopropane and N-(2, 6-dimethylphenyl)-2-pppiperidine amide. Then ropivacaine hydrochloride was obtained by resolution reaction in organic solvent of N-(2, 6-dimethylphenyl)-1- n-propyl-2-piperidine formamide and D-tartrate. Results Optical purity of the obtained ropivacaine hydrochloride was over 99.5% and total yield was about 25%. Conclusion This method is simple and convenient and the obtained products were of high optical purity. It is suitable for medicinal purposes, with certain commercial value.
[Key words]Ropivacaine hydrochloride; Local anesthetics of amide derivatives; Synthesis; Optical purity
