稀土-碱土金属异核配合物的合成及晶体结构
2015-07-04朱丽丽
徐 蕴,丁 芳,刘 东,朱丽丽
(淮北师范大学 化学与材料科学学院,安徽 淮北 235000)
金属有机框架配合物是配合物的一个研究分支,因其具有丰富多样的结构及在气体存储和分离、催化,磁性、光学及生物医学方面的潜在应用[1-4],受到广大研究者的青睐.目前研究的配合物大多集中在3d金属,4f 金属,3d-4f金属[5-7].稀土-碱土金属异核配合物具有稀土和碱土金属的特性,在发光及生物医学方面均有潜在应用价值,对于多功能配合物材料的开发将会有很大的帮助,但是相对于3d金属,4f金属,3d-4f金属配合物的研究来说,目前对稀土-碱土金属的研究不是太多[8-9],这方面还有很大的研究空间.鉴于以上所述,以及前期研究工作基础,我们利用氧二乙酸,硝酸镨及氧化镁,在溶剂热的条件下,成功合成一个新的稀土-碱土金属异核配合物,本文将报道该配合物的合成以及相关结构分析.
1 实验部分
1.1 仪器和试剂
所用试剂均为市售商品.C、H、N的含量是使用Perkin-Elmer 240型元素分析仪测定的,红外光谱是使用Nicolet FT-IR 傅里叶红外光谱测定的.
1.2 配合物{[Pr4(oda)12Mg4][Mg2(H2O)12]·6H2O}n(1)的合成
将 Pr(NO3)3·(H2O)6(0.5 mmol,0.22 g),MgO(1.5 mmol,0.06 g)和H2oda(3 mmol,0.40 g),加入8 mL H2O和2 mL C2H5OH的混合溶剂中,用三乙胺调节pH为4左右,充分搅拌均匀后将其转移至25 mL反应釜中,于160 °C恒温3 d,程序降温至室温,过滤,在空气中干燥,得到适合单晶衍射的浅绿色立方块状晶体.基于Pr 计算得产率为31%.元素分析结果C48Mg6O78Pr4H84:(实验值)C,21.09;H,3.18;(理论值)C,22.02;H,3.23.红外数据(KBr压片,υ/cm-1):3 552(w),2 920(w),2 357(w),1 629(s),1 437(s),1 356(s),1 310(s),1 245(w),1 127(s),1 058(m),937(m),728(w),575(m),405(m).
2 结果和讨论
选取具有一定尺寸的单晶体,在室温下用Rigaku R-axis Rapid IP 面探测器进行单晶衍射.用MoKα(λ=0.071 073 nm)射线,以ω-2θ扫描方式收集配合物的衍射数据,数据还原经RAPID AUTO系统自动完成.采用直接法进行晶体结构解析,用差值傅立叶合成法和最小二乘法确定非氢原子坐标,水上的氢原子的位置由理论加氢得到,并使用骑式换型位置参数和固定的各向异性热参数加入结构精修.所有的计算使用SHELXS-97和SHELXL-97程序包进行[10].
X-射线单晶结构解析表明配合物属于立方晶系,Fd3c空间群.如图1所示,Pr3+离子由9个分别来自3 个oda2-配体离子中的6 个羧基氧原子(O2)和3 个烷氧基氧原子(O3)(Pr-O2=0.245 93(3)nm,Pr-O3=0.250 77(2)nm)构成了九配位的三帽三棱柱结构,Mg12+离子由6个氧原子构成了六配位的八面体几何构型,其中 6 个氧原子分别来自相邻[Pr(oda)3]3-结构单元中的 6 个羧基氧原子(Mg1-O1=0.205 95(2)nm).每个[Pr(oda)3]3-周围同时有6个Mg12+离子(Pr-Mg1=0.649 2 nm);Mg22+离子由来自6个配位水中的6个氧原子构成六配位的八面体几何构型(Mg2-O4=0.207 16(2)nm,Mg1-Mg2=0.562 2 nm).Pr-O/Mg-O键长都在正常范围内.如图2a所示,[Pr(oda)3]3-和Mg12+离子连接起来,构成一个由[Pr(oda)3]3-和Mg2+两个模块组成的离子型3D 立方结构.该立方格子含有两种交替排列的孔洞构成,其中一种孔洞由[Mg(H2O)6]2+阳离子作为热力学稳定体填充着(其中镁离子为Mg22+),用来平衡骨架离子[Pr2(oda)6Mg2]2-阴离子,另一个孔洞中充填着自由水分子.由PLATON 软件计算得知[11],按体积计,一个结构单元含有13.0%的水分子(潜在溶剂体积为2.387 1 nm3,单位体积为 17.509 nm3).把Mg22+离子、配位水分子和自由水分子(O5)由氢键连接起来构成一个二重穿插的框架结构(O4…O5=0.323 61(4)nm,O4…O5=0.244 14(3)nm),该框架结构和由金属Pr3+和Mg12+离子构成的NaCl型骨架结合起来,构成一个三重自穿插框架(如图2b所示).此种结构对于离子交换,离子型的药物传输以及气体吸附都有着很好的潜在应用价值.
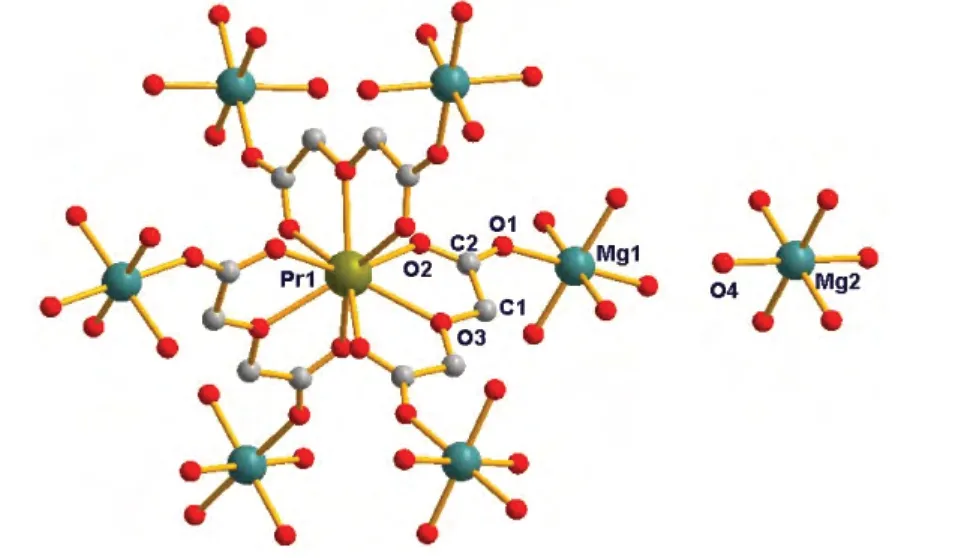
图1 配合物中镨及镁离子的配位模式图

图2 a 配合物的孔洞结构堆积图;b配合物的三重穿插结构示意图
[1]KIDO J,OKAMOTO Y.Organo lanthanide metal complexes for electroluminescent materials[J].Chem Rev,2002,102:2357-2368.
[2]ROWSELL J L C,YAGHI O M.Strategies for hydrogen storage in metal-organic frameworks[J].Angew Chem Int Ed,2005,44:4670-4679.
[3]LOMBARDI J R,DAVIS B.Periodic properties of force constants of small transition-metal and lanthanide clusters[J].Chem Rev,2002,102:2431-2436.
[4]TSUKUBE H,SHINODA S.Lanthanide complexes in molecular recognition and chirality sensing of biological substrates[J].Chem Rev,2002,102:2389-2403.
[5]EDDAOUDI M,MOLER D B,LI H,et al.Modular chemistry:secondary building units as a basis for the design of highly porous and robust metal-organic carboxylate frameworks[J].Acc Chem Res,2001,34:319-330.
[6]LI Ming,YUAN Liangjie,LI Hua,et al.A 3D heterometallic metal-organic framework constructed from luminescent build⁃ing blocks,exhibiting reversible dehydration and rehydration procedure[J].Inorg Chem Comm,2007,10:1281-1284.
[7]PRASADT K,RAJASEKHARAN M V,COSTES J P.A Cubic 3d–4f structure with only ferromagnetic Gd-Mn interac⁃tions[J].Angew Chem Int Ed,2007,46:2851-2854.
[8]XU Yun,CHE Yunxia,CHENG Fangyi,et al.Synthesis,structures,and adsorption properties of two new LaIII-MgIIhetero⁃metallic polymers[J].Eur J Inorg Chem,2011,34:5299–5304.
[9]CHANG Limei,ZHAO Xia,GU Zhigang,et al.Four LnIII-MgII metal organic frameworks containing fan-like helices and independent[Mg(H2O)6]2+units[J].Z Anorg Allg Chem,2012,638:652–657.
[10]SHELDRICK G M.Program for refinement of crystal structures[M].Germany:University of Göttingen,1997.
[11]SPEK A L.PLATON,Amultipurose crystallographic tool[M].Ultrecht:Utrecht University,2001.
