Ni2P催化剂加氢脱氧机理研究进展
2015-07-02宋华林
宋 华,宫 静,宋华林,李 锋
(1.东北石油大学 化学化工学院, 黑龙江 大庆 163318; 2.东北石油大学 石油与天然气化工省重点实验室, 黑龙江 大庆 163318;3. 黑龙江省高校肿瘤疾病防治重点实验室 牡丹江医学院,黑龙江 牡丹江 157011)
Ni2P催化剂加氢脱氧机理研究进展
宋 华1,2,宫 静1,宋华林3,李 锋1,2
(1.东北石油大学 化学化工学院, 黑龙江 大庆 163318; 2.东北石油大学 石油与天然气化工省重点实验室, 黑龙江 大庆 163318;3. 黑龙江省高校肿瘤疾病防治重点实验室 牡丹江医学院,黑龙江 牡丹江 157011)
介绍了Ni2P催化剂的结构特征、加氢脱氧(HDO)活性相及生物油中典型的含氧化合物,综述了具有代表性的典型含氧化合物呋喃类、酚类、醚类和酯类在Ni2P催化剂催化下的HDO机理方面的最新研究进展。HDO过程中,含氧化合物在催化剂作用下发生C—O键断裂,O主要通过加氢-氢解以H2O的形式脱除,其脱氧产物较为复杂。生物油中富含呋喃类和酚类化合物,因需要苛刻的脱氧反应条件,它们的脱氧难度最大。今后,需进一步深入开展HDO理论研究,探究Ni2P催化剂催化活性的调控机制,制备出性能更加优异的HDO催化剂。
Ni2P;加氢脱氧;生物油;机理;含氧化合物;活性相
随着世界经济的迅猛发展,能源的需求量急剧增加,石油储量逐年减少,全世界正面临着巨大的能源压力。因此,积极寻求替代能源,以缓解能源压力和环境问题至关重要。作为一种可再生能源,生物质能近年来备受关注[1-2]。目前,常采用快速热解的方法获得生物油。但所得生物油的组成复杂,其中含有大量的含氧化合物,包括呋喃、酚、酮、醛、醇、醚、酸、酯等,总含氧量高达50%[3-4]。大量的含氧化合物使生物油的热值(≈20 MJ/kg)和pH值降低,热稳定、化学稳定性以及油溶性变差,必须对其进行脱氧精制[5]。加氢脱氧(HDO)是生物油脱氧的重要手段,与加氢脱硫(HDS)和加氢脱氮(HDN)类似,HDO过程中,含氧化合物在催化剂作用下发生C—O键断裂,通过加氢-氢解,O以H2O的形式脱除[6]。近十年来,过渡金属磷化物,尤其是Ni2P,因其独特的金属性、半导体特性和优良的催化性能而成为新型HDO催化剂研究的热点[7-8]。但关于Ni2P催化剂对含氧模型化合物的加氢脱氧反应途径及相关理论研究不够完善,对具体反应途径方面的综述不够全面。制备具有高活性、高稳定性及反应选择性的加氢催化剂,需要有加氢机理等深层次的理论研究为指导。因此,了解生物油中含氧化合物的分类及其HDO机理的理论研究对制备高性能Ni2P加氢脱氧催化剂具有重要的意义。笔者介绍了Ni2P催化剂在HDO方面的应用,重点阐述Ni2P催化剂对典型氧化物HDO机理方面的最新研究进展。
1 Ni2P催化剂的结构特征及其在HDO反应中的活性相
Ni2P属于富金属磷化物。采用密度泛函理论(DFT)对Ni3P、Ni12P5、Ni2P、Ni5P4、NiP、NiP2、NiP3等Ni的磷化物进行的研究表明[9],Ni2P中Ni—P键的平均键长(0.220 nm)与其他的磷化镍化合物相似,Ni—Ni键长(0.261 nm)与金属Ni中的Ni—Ni键长(0.250 nm)类似,这种短的强金属键使Ni2P具有金属的性质。晶格能计算结果显示[9],热稳定性由大到小的磷化镍依次为Ni3P、Ni2P、Ni12P5、Ni5P4、NiP、NiP2、NiP3。Ni2P以三角棱柱体为结构单元,近似于球形。这种类似于球形的结构能够暴露更多配位不饱和表面原子,有更高的表面活性位密度,从而具有更好的催化活性。


图1 Ni2P晶体单元示意图[11]
Moon等[11]研究了Ni2P催化HDO反应的活性相结构性质,采用DFT方法计算了3种不同结构,即—OH、H2和H2O的解离吸附特性。图2为Ni2P(001)晶面上吸附的—OH,图3为Ni2P(001)晶面上吸附的—H。研究发现,—OH吸附在相邻的3个Ni(I)位上形成1个三重洞位(TFH),Ni—O键长为0.1776 nm,吸附能为-0.501 eV(见图2(b)),这比吸附在单个Ni(I)位上(Ni—O键长为0.1345 nm,吸附能-0.238 eV)的结构更稳定(如图2(a))。—OH吸附在Ni(II)和P(II)位上的吸附能分别为-0.163和0.303 eV,因此—OH更倾向于吸附TFH-Ni(I)位上。—H吸附在TFH(Ni(I)位上的吸附能为-0.637 eV,这种结构在Ni2P(001)晶面的吸附非常稳定(见图3)。

图2 Ni2P(001)晶面上吸附的-OH [11]
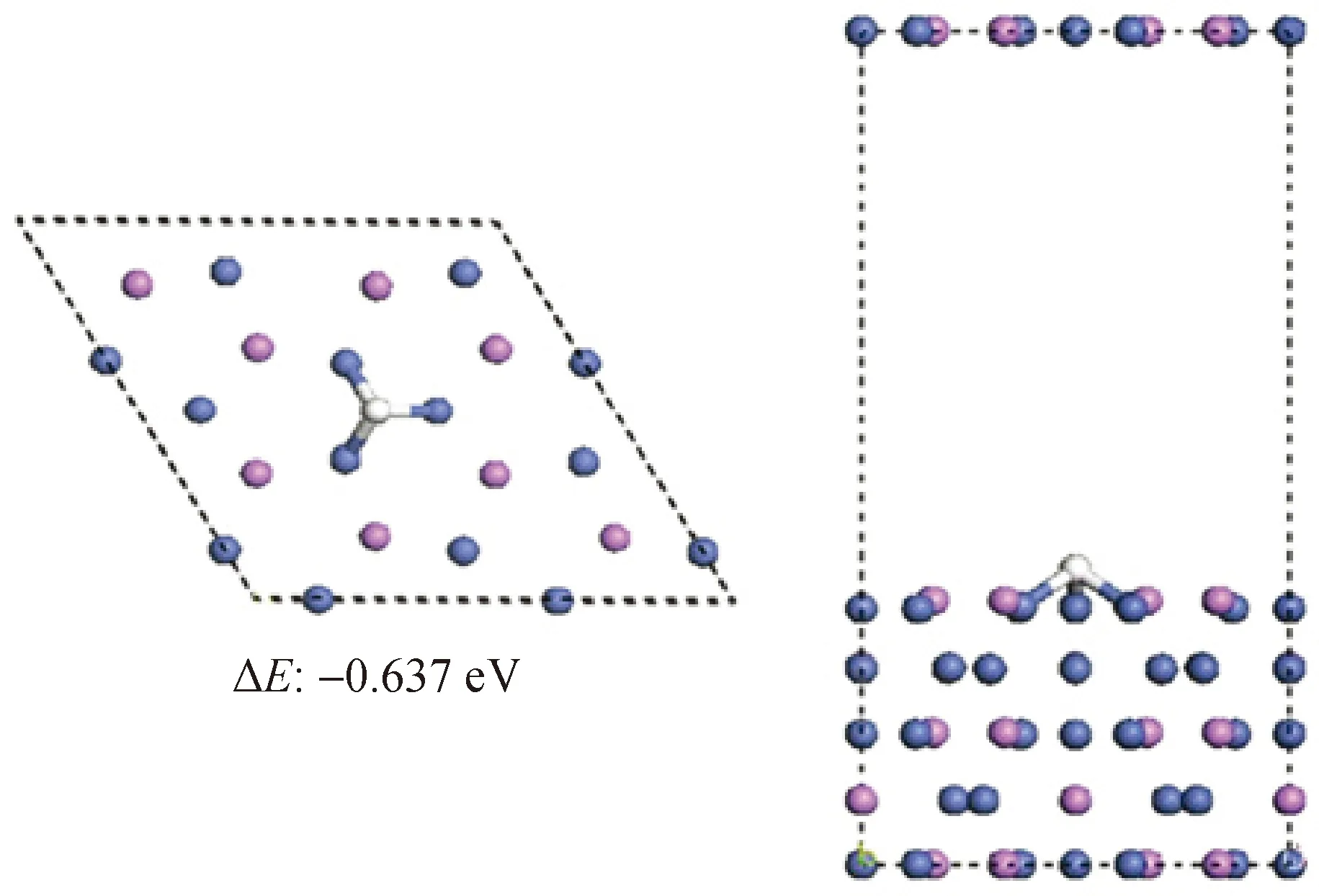
图3 Ni2P(001)晶面上吸附的-H [11]
图4为H2O解离吸附的结构和吸附能。Ni2P催化剂表面H2O解离吸附可能形成2种结构。第1种结构是—H吸附在TFH-Ni(I)位上,—OH吸附在由Ni(II)位包围的P(II)位上,如图4(a)所示,吸附能为-0.709 eV,P—OH键长和Ni—H键长分别为0.1718和0.1790 nm;第2种结构是—OH吸附在TFH-Ni(I)位上,—H吸附在由Ni(II)位包围的P(II)位上,如图4(b)所示,吸附能为-0.638 eV,Ni—OH键长和P—H键长分别为0.2025和0.1595 nm。相对于第1种结构,第2种结构不稳定,所以前者可能是Ni2P催化HDO反应所经历的结构。

图4 Ni2P(001)晶面上H2O解离吸附的结构和吸附能 [11]
Ni2P不仅具有普通过渡金属磷化物的强度大、硬度高、热电良导体等的特征,而且还有抗氧化、抗腐蚀的优点,不溶于水,能与具有强氧化性质的酸发生反应,但是可以稳定存在于稀酸、稀碱中。Ni2P因其独特的催化性能成为新型HDO催化剂研究的热点。
2 含氧化合物的分类
生物质油(Bio-oil)是水和复杂含氧有机物的混合物,即由纤维素、半纤维素和木质素的各种降解物所组成的一种混合物。图5给出了生物质油中含氧化合物的典型结构。这些含氧化合物主要由酚类组成,此外还包括酮、醛、酸、酯、醇、醚等物质,各类含氧化合物均以芳环类含氧化合物为主[12]。
原油、煤制油、页岩油以及生物质油的元素组成列于表1[13]。由表1可以看出,生物质油,特别是热解生物质油中S含量较低,但含有大量的O,其质量分数达到46.9%。因此,研究各类含氧化合物在HDO过程中发生的化学反应具有重要的意义。

图5 热解生物质油中含氧化合物的典型结构[12]
表1 不同原料油的元素组成[13]
Table 1 Elemental composition of the oils from different feeds[13]

Feedw/%CHSNOn(H)/n(C)Conventionalcrude85 212 81 80 10 11 8Coal⁃derivednaphtha85 19 60 10 54 71 4Oilshalecrude85 911 00 51 41 21 5Liquefiedbio⁃oils74 88 0<0 1<0 116 61 3Pyrolyzedbio⁃oils45 37 5<0 1<0 146 92 0
3 典型含氧化合物在Ni2P催化下的加氢脱氧反应机理
对加氢脱氧反应机理的研究多是以油品中的某一个或一类化合物的加氢反应为模型。呋喃类和酚类化合物在生物油中含量较多,并且酚类化合物也会在呋喃类化合物的加氢脱氧过程中以中间体形式存在,因此,模型化合物中最常用的是呋喃类与酚类化合物,此外还有苯甲醚、月桂酸甲酯、愈创木酚等。生物油中呋喃类和酚类的脱氧难度最大[14-15],因为这2类化合物的脱氧反应条件苛刻,且存在不稳定的含氧基团。
3.1 呋喃类
呋喃类化合物的脱氧一般分为3种形式[16]。(1)分子内的H原子迁移,脱水生成烯类;(2)C—O键先断裂,然后通过烃基-O-催化剂的模式经过C—C键断裂或者C—O键断裂进一步脱氧;(3)分子加氢氢解成为烃类、酚类和醇类,再进一步脱氧。
Cecilia等[17]研究了Ni2P/SiO2催化剂催化二苯并呋喃(DBF) HDO的活性,在300℃、3.0 MPa下DBF转化率高达99%。DBF的HDO反应除生成不含氧的最终产物环己烷(BCH)、环己基苯(CHB)、联苯(BP)和少量苯(B)和环己烷(CH)外,还生成了四氢呋喃(THDBF)、六氢苯并呋喃(HHDBF)和2-苯基-1-环己醇(2P-1CHol)等含氧中间产物。Ni2P催化DBF的HDO反应机理如图6所示。
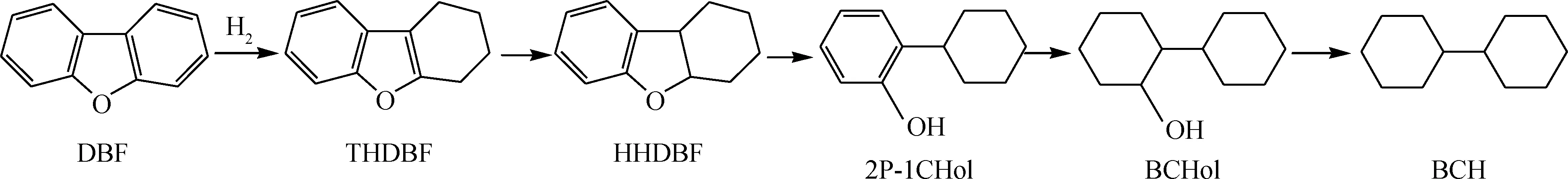
图6 Ni2P/SiO2催化DBF的HDO反应途径 [17]
Oyama等[18]制备了Ni2P负载量在6%~22%范围的Ni2P/SiO2催化剂,以苯并呋喃(500×10-6)、喹啉(2000×10-6)和二苯并噻吩(3000×10-6) 3种组分的混合物为模型化合物,在反应温度370℃、压力3.1 MPa下,在固定床反应器中考察了不同负载量的Ni2P/SiO2催化剂的催化性能。当Ni2P负载量为18%左右时,催化剂的加氢脱氧、加氢脱硫和加氢脱氮催化活性均达到最佳值,分别为80%、99%和91%。在370℃、3.1 MPa条件下,Oyama等[19]还研究了二苯并噻吩、喹啉、苯并呋喃和四氢萘共存时磷化物催化剂的HDO性能,结果表明,与CoP/SiO2相比,Ni2P/SiO2具有更高的HDO催化性能;降低Ni/P摩尔比有助于提高Ni2P催化剂的HDO催化性能,当Ni/P摩尔比为1/3时HDO催化性能最好,苯并呋喃转化率达到81%。在相同条件下,与Ni-Mo-S/Al2O3催化剂相比,Ni2P/SiO2能得到较高的转化率。Bui等[20]以2-甲基四氢呋喃(2-MTHF)为模型化合物,比较了2种P源(磷酸盐和次磷酸盐)制备的过渡金属磷化物的HDO催化活性。结果表明,在300℃、0.1 MPa条件下,催化活性由大到小的催化剂依次为Ni2P、WP、Co2P、FeP,并且均高于Pd/Al2O3;Ni2P和Co2P催化2-甲基四氢呋喃HDO反应的主产物是戊烷和丁烷,WP催化所得的主产物是戊烯和戊二烯,而催化活性较低的FeP和Pd/Al2O3催化所得产物为戊烯和C4的混合物;2种P源制备的Ni2P催化剂具有相似的产物选择性,选择性从高到低的产物依次为戊烯、2-戊酮、戊烷。Iino等[21]以2-甲基四氢呋喃为模型化合物,对比了SiO2负载的磷化镍催化剂和传统贵金属Ru/C、Pd/Al2O3催化剂的HDO催化活性。在0.5 MPa、350℃条件下,Ru/C、Pd/Al2O3催化HDO的转化率和正戊烷选择性分别为98.7%、71%和100%、0,而Ni2P/SiO2催化HDO的转化率和正戊烷选择性分别为100%和85%,HDO催化活性高于前二者。Ni2P催化2-甲基四氢呋喃的HDO的主反应分4步进行,如图7所示。(1)C—O键断裂生成2-戊酮或戊醛,形成有1个羰基的化合物;(2)通过氢化生成戊醇;(3)戊醇脱氢成戊烯;(4)戊烯氢化生成正戊烷。此外,戊醛还可以脱羰生成正丁烷和CO。各反应的速率常数列于表2。由表2可知,呋喃开环生成2-戊酮或戊醛的反应速率常数较小,分别为0.05 s-1和0.11 s-1,是反应控制步骤。

图7 Ni2P/SiO2催化2-MTHF HDO的反应途径 [21]
表2 2-MTHF加氢脱氧各步反应速率常数[21]
Table 2 The reaction rate constants for HDO of 2-MTHF[21]s-1

k1k2k3k4k5k6k7k8k90 052 20111000 11900300500300
3.2 酚类
表3给出了不同结构含氧化合物中C—O键的解离能[22]。Ar—OH和RO—Ar(Ar代表芳香环)中C—O键的键能比R—OH和RO—R的C—O键能高约83 kJ/mol,说明酚类和芳香醚类化合物中氧的脱除比醇类和脂肪醚类化合物困难。研究酚类的加氢脱氧反应一般以苯酚及其衍生物为模型化合物,其脱氧路径一般分为加氢-氢解路径和直接氢解路径两种。按照前者,芳环首先加氢,然后发生氢解反应除去氧;按照后者,则是C—O键直接断裂氢解除去氧[23]。

表3 不同结构含氧化合物中C—O键的解离能 [22]
Duan等[24-25]将Ni2P/MCM-41催化剂用于苯酚HDO反应中,在300℃、4 MPa条件下,该催化剂经过HDS反应后仍可得到接近100%的苯酚转化率和100 h的稳定性。他们采用程序升温还原法制备了Ni2P和MoP催化剂,并用H2S对其进行钝化,考察Ni2P上S原子与加氢脱硫(HDS)、加氢脱氮(HDN)和加氢脱氧(HDO)催化活性之间的关系。结果表明,Ni2P/MCM-41催化剂对苯酚HDO的催化活性非常高,并且在HDS-HDO-HDS过程中,O原子置换S原子的速率小于S原子置换O原子的速率。Whiffen等[26]研究了非负载的磷化物催化剂催化4-甲基苯酚的HDO反应,结果表明,在623 K、4.4 MPa条件下,添加柠檬酸后,非负载的Ni2P催化剂的活性是MoP催化剂的2~3倍,活性位数量是其6倍。Ni2P-CA催化剂催化4-甲基苯酚HDO反应主要沿着3条反应路径进行,即4-甲基苯酚通过氢解作用直接生成甲苯;通过加氢反应生成甲基环己烷;异构化反应生成1,3-二甲基环戊烷。与未添加柠檬酸的Ni2P催化剂相比,Ni2P-CA催化剂催化4-甲基苯酚的HDO反应产物中,甲基环己烷选择性大大增加。王洪岩[27]制备了Ni2P/MCM-41催化剂,并利用该催化剂对邻甲酚模型化合物进行HDO实验,发现Ni2P/MCM-41催化剂对邻甲酚有很高的HDO催化活性。在325~375℃范围内,邻甲酚的转化率随着反应温度升高而增加,含氧产物的选择性随温度的升高而减小;在375℃时,邻甲酚的转化率高达99.74%。图8为Ni2P催化剂催化邻甲酚HDO的反应路径。由图8看到,邻甲酚的HDO反应路径主要为2种。(l)苯环上的羟基直接脱除,形成甲苯;(2)苯环先进行加氢,形成邻甲基环己酮,H+与C=O键抢夺电子,迅速反应形成邻甲基环己醇,然后H+继续攻击C—O键致使羟基脱落变成H2O,另一部分变为3-甲基环己烯,C=C键继续加氢形成甲基环己烷。此外,随着反应温度升高,甲苯产量增加,说明温度升高有利于路径(1)反应。
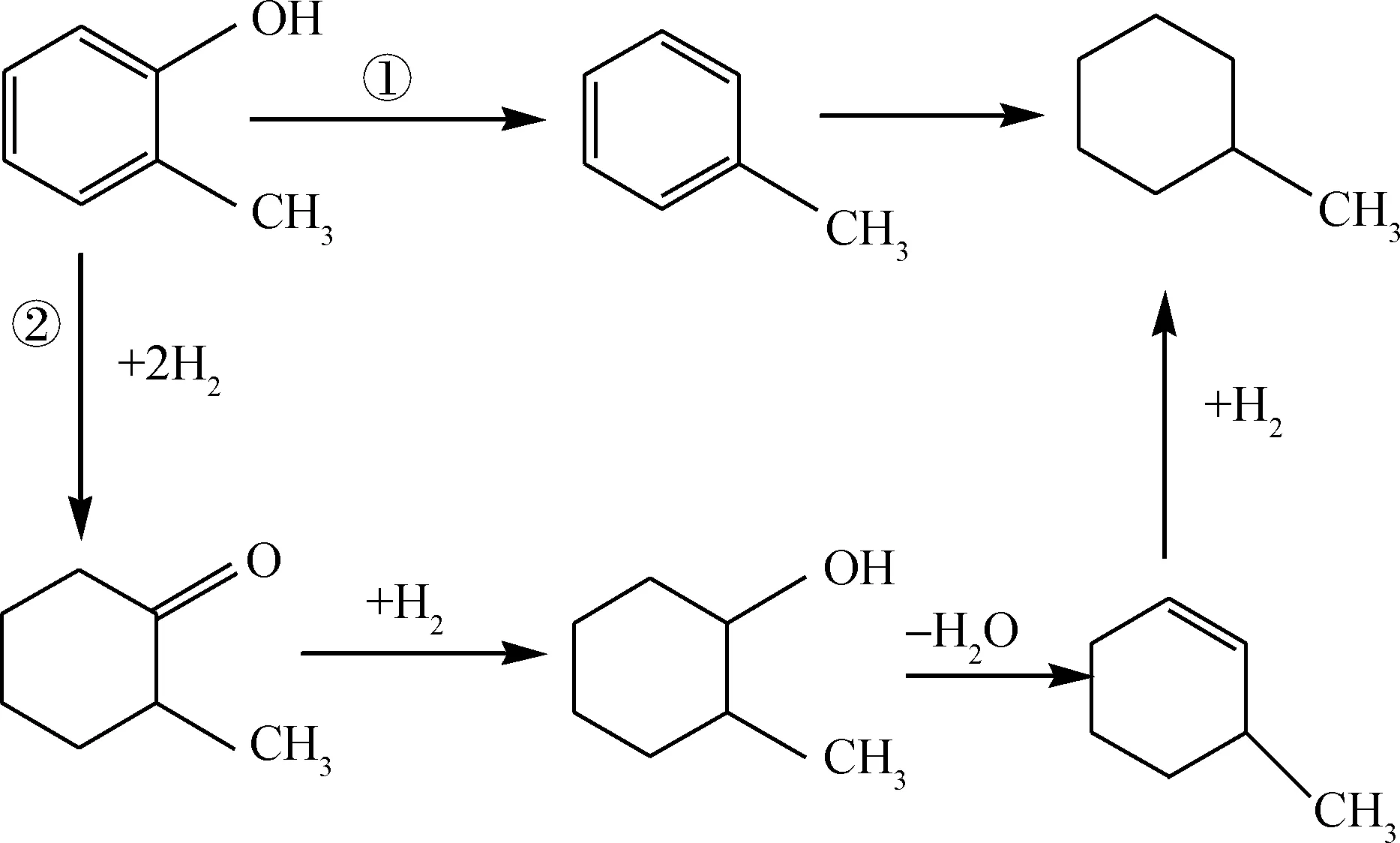
图8 邻甲酚的HDO反应路径 [27]
研究表明,苯酚和对甲酚的HDO表观活化能分别为102和135 kJ/mol,故对甲酚的HDO比苯酚更困难[28]。Wang等[29]采用热分解法从氯化镍和次磷酸钠的混合前驱物制备非负载的Ni-P催化剂,并用于催化对甲苯酚的HDO反应。Ni-P催化剂催化对甲苯酚的HDO反应存在2个平行的反应途径,一个是芳香环先预加氢脱H2O,随后氢化成脂族烃(HYD),另一个是C—O键直接断裂生成芳香制品(DDO)。DDO/HYD摩尔比随着催化剂前驱体中H2PO3/Ni2+的摩尔比和热分解温度的变化而变化。
3.3 醚类
苯甲醚(CAromOCH3)通过2种方式进行C—O键的断裂。(1)CAromO—CH3键(脱甲基)首先断裂,其ΔH=265.4 kJ/mol;(2)CArom—OCH3键(直接脱氧)首先断裂,其ΔH=422.9 kJ/mol[30]。很明显,路径(2)较路径(1)更为困难,因此苯的生成主要经过路径(1)。Li等[31-32]研究Ni2P/SiO2、MoP/SiO2和不同Ni/Mo摩尔比的NiMoP/SiO2催化剂在苯甲醚的HDO中的催化性能,结果表明,HDO过程中存在苯甲醚脱甲基(DME)生成苯酚、苯酚氢解和苯环加氢3种类型的反应。苯甲醚的HDO过程中,催化剂中的金属中心和P—OH均是脱甲基、加氢和脱氧的活性中心,其中Niδ+的活性最高。与传统的NiMoS/γ-Al2O3相比,Ni2P/SiO2具有较高的催化活性,其催化苯甲醚HDO的反应途径如图9所示。

图9 苯甲醚HDO反应网络 [31]
愈创木酚具有类似苯甲醚的芳环和甲氧基结构,因而具有相近的HDO反应途径。但愈创木酚具有2个不同的含氧官能团(酚基和甲氧基),是较难脱氧的化合物。Zhao等[33]研究了200~300℃、常压下不同磷化物催化剂对愈创木酚HDO反应的催化性能。与Co2P、Fe2P、WP和MoP催化剂相比,Ni2P催化剂能得到较高的转化率,并具有良好的稳定性。CoMoS/Al2O3催化剂的HDO活性很低,且很快失活。在300℃下,Ni2P/SiO2催化剂催化愈创木酚HDO反应能得到完全脱氧产物苯(摩尔分数为60%,以下同)、部分脱氧产物苯酚(30%)和甲氧基苯(10%)。Moon等[11]结合DFT和XAFS、FTIR表征手段,研究了愈创木酚在Ni2P/SiO2催化下的HDO反应。结果表明,Ni2P催化剂催化愈创木酚HDO的活性位可以用Ni2P表面Ni或P位上吸附的—H或—OH来表示,其相对量决定总反应的路径;在1×105Pa下,直接脱氧(DDO)占主导地位,HDO反应得到的产物为苯(62%)、苯甲醚(30%)、环己烷(7%)和苯酚(<1%);相反,在8×105Pa下,预加氢脱氧占主导地位,愈创木酚HDO反应的产物为环己烷(91%)、苯(8%)、茴香醚(1%)、苯酚(<1%)和少量的环己基和甲氧基环己烷(<0.1%),愈创木酚的转化率为100%。此外,高度分散的活性位对促进HDO的2个反应途径都非常重要。图10为愈创木酚HDO的反应网络。
Wu等[34]比较了负载在不同载体上(ZrO2、Al2O3、SiO2)的Ni2P对愈创木酚HDO反应的催化性能。结果表明,Ni2P/SiO2催化剂的活性最高;并提出了常压下愈创木酚HDO的反应途径,包括脱甲氧基化(DMO)、脱甲基化(DME)、直接脱氧(DDO)、预加氢脱氧(HYD)、烷基转移(TRA)、甲基化等过程。Ni2P/SiO2催化剂促进DMO和DDO反应路径,得到的产物主要为苯酚和苯,而Ni2P/ZrO2和Ni2P/Al2O3催化剂促进DME反应路径,主要生成邻苯二酚。这是因为Ni2P/SiO2催化剂中Ni2P的晶相尺寸小,分散度提高,Ni(II)位的数量增加。他们还研究了Ni2P催化剂的初始磷含量对其催化愈创木酚HDO反应性能的影响[35]。假一级动力学分析表明,随着Ni/P摩尔比降低,Ni2P催化剂催化HDO反应的活性降低。Ni2P/SiO2促进DMO和DDO途径生成苯酚和苯,而Ni12P5/SiO2和Ni3P/SiO2促进DME和TRA途径生成1,2-二甲氧基苯、3-甲基邻苯二酚和3-甲基愈创木酚。

图10 Ni2P/SiO2催化愈创木酚HDO的反应网络 [11]
3.4 酯类
采用磷化物催化剂时,月桂酸甲酯的脱氧产物包括C11和C12的烃(正构烷烃、异构烷烃和烯烃),它们分别通过加氢脱羰基和加氢脱氧的途径生成;含氧中间产物为月桂酸、十二烷醛、十二烷醇和月桂醇月桂酸酯[36]。573 K、2.0 MPa的条件下, 对月桂酸甲酯HDO反应的催化性能由高到低的磷化物催化剂依次为Ni2P/SiO2、MoP/SiO2、WP/SiO2、CoP/SiO2、FeP-Fe2P/SiO2;按目的产物C11和C12总选择性由高到低排列的催化剂顺序为Ni2P/SiO2、MoP/SiO2、CoP/SiO2、WP/SiO2、CoP/SiO2、FeP-Fe2P/SiO2;月桂酸甲酯在Ni2P/SiO2催化下的脱氧反应以加氢脱羰/脱羧途径为主[37]。脱氧途径受Brnsted酸和Ni2P晶粒尺寸的影响,尤其是受前者影响较大[38]。Shi等[39-40]比较了负载在不同载体上的磷化镍催化剂对月桂酸甲酯HDO的催化性能。在573~613 K、3.0 MPa条件下,按月桂酸甲酯转化率由大到小排列的催化剂顺序为Ni2P/SiO2、Ni3P-Ni12P5/Al2O3、Ni2P/TiO2、Ni2P/SAPO-11、Ni2P-Ni12P5/HY、Ni2P/CeO2,按目的产物C11和C12总选择性由高到低排列的催化剂顺序为Ni2P/CeO2、Ni3P-Ni12P5/Al2O3、Ni2P/SiO2、Ni2P/SAPO-11、Ni2P/TiO2、Ni2P-Ni12P5/H;催化剂的活性、产物选择性和脱氧途径受表面Ni位点密度、Ni电子密度、Ni2P晶粒尺寸、Ni位点和酸性部位或氧空位之间的协同作用影响。在573 K、2.0 MPa条件下,对一系列SiO2负载的金属(Ni、Co、Fe、Mo、W)磷化物催化剂催化月桂酸甲酯HDO的实验结果表明,Ni2P、MoP、CoP-Co2P、WP、Fe2P-FeP 对HDO反应的催化性能依次降低,而镍基催化剂对HDO反应催化性能按Ni≈Ni2P、Ni12P5、Ni3P的顺序降低;月桂酸甲酯的HDO反应包括氢解、水解、氢化、脱羰基化、脱氢、脱水、酯化、异构化、裂化以及聚合反应。月桂酸甲酯在Ni2P催化下的HDO反应有3种途径。(1)通过氢解或水解生成月桂酸,月桂酸可以进一步通过加氢生成十二醛或脱羰基生成十一碳烯;(2)通过加氢生成十二醛,十二醛很容易氢化生成十二醇,十二醇继续脱水形成十二碳烯或脱氢形成十二醛,十二碳烯氢化生成十二烷或异构化和裂解加氢生成异十二烷,十二醛通过脱羰基化途径生成十一烷或十一碳烯;(3)通过脱羰基生成十一碳烯。Yang等[41]研究Ni2P催化剂催化油酸甲酯HDO反应的实验结果表明,虽然与Ni/SBA-15相比,Ni2P/SBA-15的加氢脱氧活性较低,但目标产物n-C18对n-C17的摩尔比更大。
4 总结和展望
Ni2P具有较高的机械强度、热稳定性、导电性以及特殊的晶体结构,因而具有良好的HDO催化活性,成为HDO催化剂领域的研究热点。今后该类催化剂的研究重点主要有,(1)进一步借助有效表征手段深入开展Ni2P催化剂加氢脱氧反应的活性相以及相应催化理论的研究,为高活性、稳定性及产物选择性的HDO催化剂的制备提供理论依据;(2)开展不同类型含氧化合物在HDO反应过程中的相互作用方面的研究,为实际油品的HDO反应和工业化生产提供依据;(3)探究催化剂催化活性的调控机制,对催化剂的活性组分、载体进行改性,以及改进制备方法,以降低HDO反应温度,提高脱氧效率。
[1] HUBER G, IBORRA S,CORMA A. Synthesis of transportation fuels from biomass:Chemistry,catalysts,and engineering[J]. Chemical Reviews,2006,106(9):4044-4098.
[2] YANG G, PIDKO E A,HENSEN E J M. Mechanism of Brønsted acid-catalyzed conversion of carbohydrates[J]. Journal of Catalysis,2012,295(11):122-132.
[3] BRIDGWATER A V. Review of fast pyrolysis of biomass and product upgrading[J]. Biomass and Bioenergy,2012,38(3):68-94.
[4] MOHAN D, PITTMAN J C U,STEELE P H. Pyrolysis of wood/biomass for bio-oil:A critical review[J]. Energy & Fuels,2006,20(3):848-889.
[5] CZERNIK S,BRIDGWATER A V. Overview of applications of biomass fast pyrolysis oil[J]. Energy & Fuels,2004,18(2):590-598.
[6] 段艳,王欣, 张舜光,等. 溶胶-凝胶法制备非负载Ni-Mo复合氧化物加氢脱氧催化剂[J]. 石油学报(石油加工),2011,27(5):699-705.(DUAN Yan,WANG Xin,ZHANG Shunguang,et al. Unsupported Ni-Mo composite oxide catalysts prepared by sol-gel method for hydrodeoxygenation[J]. Acta Petrolei Sinica(Petroleum Processing Section),2011,27(5):699-705.)
[7] GAUDETTE A F, BURNS A W,HAYES J R,et al. Mössbauer spectroscopy investigation and hydrodesulfurization properties of iron-nickel phosphide catalysts[J]. Journal of Catalysis,2010,272(1):18-27.
[8] OYAMA S T, WANG X,LEE Y K,et al. Effect of phosphorus content in nickel phosphide catalysts studied by XAFS and other techniques[J].Journal of Catalysis,2002,210(1):207-217.
[9] REN J, WANG J G,LI J F,et al. Density functional theory study on crystal nickel phosphides[J]. Journal of Fuel Chemistry and Technology,2007,35(4):458-464.
[10] ANKUDINOV A L, RAVEL B,REHR J J,et al. Real-space multiple-scattering calculation and interpretation of X-ray-absorption near-edge structure[J]. Physical Review B: Condensed Matter,1998,58(2):7565-7576.
[11] MOON J S, KIM E G,LEE Y K. Active sites of Ni2P/SiO2catalyst for hydrodeoxygenation of guaiacol:A joint XAFS and DFT study[J]. Journal of Catalysis,2014,311(3):144-152.
[12] ANGELICI R J. An overview of modeling studies in HDS,HDN and HDO catalysis[J]. Polyhedron,1997,16(18):3073-3088.
[13] SAJKOWSKI D J, OYAMA S T. Catalytic hydrotreating by molybdenum carbide and nitride: Unsupported Mo2N and Mo2C/A12O3[J]. Applied Catalysis A:General,1996,134(2):339-349.
[14] GRANGE P, LAURENT E,MAGGI R,et al. Hydrotreatment of pyrolysis oils from biomass: Reactivity of the various categories of oxygenated compounds and preliminary techno-economical study[J].Catalysis Today,1996,29(1-4):297-301.
[15] FURIMSKY E. Catalytic hydrodeoxygenation[J] . Applied Catalysis A:General,2000,199(2):147-190.
[16] ABDU Y B, WANG X Q,UMIT S O. Hydrodeoxygenation of benzofuran over sulfided and reduced Ni-Mo/γ-Al2O3catalysts:Effect of H2S[J] . Journal of Molecular Catalysis A: Chemical,2007,270(1-2):264-272.
[17] CECILIA J A, INFANTES-MOLINA A,RODRGUEZ-CASTELLN E,et al. Oxygen-removal of dibenzofuran as a model compound in biomass derived bio-oil on nickel phosphide catalysts:Role of phosphorus[J] . Applied Catalysis B:Environmental,2013,136-137(6):140-149.
[18] OYAMA S T, WANG X,LEE Y K,et al. Active phase of Ni2P/SiO2in hydroprocessing reactions[J]. Journal of Catalysis,2004,221(2):263-273.
[19] OYAMA S T, WANG X,LEE Y K,et al. Effect of phosphorus content in nickel phosphide catalysts studied by XAFS and other techniques[J]. Journal of Catalysis,2002,210(1):207-217.
[20] BUI P, CECILIA J A,OYAMA S T,et al. Studies of the synthesis of transition metal phosphides and their activity in the hydrodeoxygenation of a biofuel model compound[J]. Journal of Catalysis,2012,294(10):184-198.
[21] IINO A, CHO A,TAKAGAKI A,et al. Kinetic studies of hydrodeoxygenation of 2-methyltetrahydrofuran on a Ni2P/SiO2catalyst at medium pressure[J]. Journal of Catalysis,2014,311(3):17-27.
[22] BENSON S W. Thermochemical Kinetics:Methods for the Estimation of Thermochemical Data and Rate Parameters[M]. New York:Wiley,1968.
[23] 何兵. 负载型非晶态催化剂的制备及其加氢脱氧性能的研究[D]. 湘潭:湘潭大学,2012.
[24] DUAN X P, TENG Y,WANG A J,et al. Role of sulfur in hydrotreating catalysis over nickel phosphide[J]. Journal of Catalysis,2009,261(2):232-240.
[25] 段新平. 磷化镍(铝)催化剂的制备改性以及加氢精制性能的研究[D]. 大连:大连理工大学,2009.
[26] WHIFFEN V M L, SMITH K J. A comparative study of 4-methylphenol hydrodeoxygenation over high surface area MoP and Ni2P[J]. Topics in Catalysis,2012,55(10):981-990.
[27] 王洪岩. 淮南煤多联产焦油催化加氢试验研究[D]. 杭州:浙江大学,2013.
[28] YANG Y Q, TYE C T,SMITH K J. Influence of MoS2catalyst morphology on the hydrodeoxygenation of phenols[J]. Catalysis Communications,2008,9(6):1364-1368.
[29] WANG W Y, ZHANG K,LIU H,et al. Hydrodeoxygenation ofp-cresol on unsupported Ni-P catalysts prepared by thermal decomposition method[J]. Catalysis Communications,2013,41(11):41-46.
[30] VILJAVA T R, SAARI E R M,KRAUSE A O I. Simultaneous hydrodesulfurization and hydrodeoxygenation: Interactions between mercapto and methoxy groups present in the same or in separate molecules[J]. Applied Catalysis A:General,2001,209(1-2):33-43.
[31] LI K, WANG R,CHEN J. Hydrodeoxygenation of anisole over silica-supported Ni2P,MoP and NiMoP catalysts[J]. Energy & Fuels,2011,25(3):854-863.
[32] 李克伦. 负载磷化物催化剂苯甲醚加氢脱氧性能研究[D]. 天津:天津大学,2012.
[33] ZHAO H Y, LI D,BUI P,et al. Hydrodeoxygenation of guaiacol as model compound for pyrolysis oil on transition metal phosphide hydroprocessing catalysts[J]. Applied Catalysis A:General,2011,391(1-2): 305-310.
[34] WU S K, LAI P C,LIN Y C,et al. Atmospheric hydrodeoxygenation of guaiacol over alumina, zirconia, and silica-supported nickel phosphide catalysts[J]. ACS Sustainable Chemistry & Engineering,2013,1(3):349-358.
[35] WU S K, LAI P C,LIN Y C. Atmospheric hydrodeoxygenation of guaiacol over nickel phosphide catalysts:Effect of phosphorus composition[J]. Catalysis Letters,2014,144(5):878-889.
[36] CHEN J X, YANG Y,SHI H,et al. Regulating product distribution in deoxygenation of methyl laurate on silica-supported Ni-Mo phosphides:Effect of Ni/Mo ratio[J].Fuel,2014,129(8):1-10.
[37] 李莉. SiO2负载过渡金属磷化物催化剂月桂酸甲酯加氢脱氧性能研究[D]. 天津:天津大学,2012.
[38] YANG Y, CHEN J X,SHI H. Deoxygenation of methyl laurate as a model compound to hydrocarbons on Ni2P/SiO2,Ni2P/MCM-41,and Ni2P/SBA-15 catalysts with different dispersions[J]. Energy & Fuels,2013,27(6):3400-3409.
[39] SHI H, CHEN J X,YANG Y,et al. Catalytic deoxygenation of methyl laurate as a model compound to hydrocarbons on nickel phosphide catalysts:Remarkable support effect[J]. Fuel Processing Technology,2014,118(2):161-170.
[40] CHEN J X, SHI H,LI L,et al. Deoxygenation of methyl laurate as a model compound to hydrocarbons on transition metal phosphide catalysts[J]. Applied Catalysis B:Environmental,2014,144(1):870-884.
[41] YANG Y X, HERNANDEZ C O,O’SHEA V A D L P, et al. Ni2P/SBA-15 as a hydrodeoxygenation catalyst with enhanced selectivity for the conversion of methyl oleate inton-octadecane[J]. ACS Catalysis,2012,2(4):592-598.
Advance in the Hydrodeoxygenation Mechanism on Ni2P Catalysts
SONG Hua1,2, GONG Jing1, SONG Hualin3, LI Feng1,2
(1.CollegeofChemistry&ChemicalEngineering,NortheastPetroleumUniversity,Daqing163318,China;2.ProvincialKeyLaboratoryofOil&GasChemicalTechnology,NortheastPetroleumUniversity,Daqing163318,China;3.KeyLaboratoryofCancerPreventionandTreatmentofHeilongjiangProvince,MudanjiangMedicalUniversity,Mudanjiang157011,China)
The structure and the active phase for hydrodeoxygenation (HDO) of Ni2P catalyst and the typical oxygen-containing compounds in bio-oil were introduced. The recent progress in the HDO mechanism over Ni2P catalysts based on representative oxygen-containing compounds, such as furans, phenols, ethers and esters, was reviewed. During HDO, C—O bonds of oxygen-containing compounds were cleaved under the action of catalysts, and then the oxygen was mainly removed by hydrogenation-hydrogenolysis in the form of H2O, by which complicated products were produced. Bio-oils were rich in furans and phenolic compounds, and the deoxidization of these compounds needed harsh reaction conditions, therefore, their HDO were of the most challenging. To prepare the catalysts with more excellent HDO performance, the HDO theoretical research and regulatory mechanism for HDO activity of the Ni2P catalyst were worthy of being further studied.
Ni2P; hydrodeoxygenation;bio-oil;mechanism;oxygen-containing compound;active phase
2014-07-21
国家自然科学基金项目(21276048)、黑龙江省科技厅项目(2009G0947-00)和研究生创新基金项目资助
宋华,女,教授,从事工业催化和绿色氧化方面的研究;E-mail: songhua2004@sina.com
宋华林,男,高级工程师,博士,从事催化材料及仪器分析方面的研究;Tel:0453-6984321;E-mail:songhualin401@126.com
1001-8719(2015)05-1232-10
O643.31; TE624.4
A
10.3969/j.issn.1001-8719.2015.05.028
