P促进Pd/C高效催化甲酸制氢的研究
2015-06-24焦晓新郑潇潇张鸿斌李海燕
焦晓新,郑潇潇,张鸿斌,李海燕
(厦门大学 化学化工学院,固体表面物理化学国家重点实验室,醇醚酯化工清洁生产国家工程实验室,福建厦门361005)

P促进Pd/C高效催化甲酸制氢的研究
焦晓新,郑潇潇,张鸿斌,李海燕*
(厦门大学 化学化工学院,固体表面物理化学国家重点实验室,醇醚酯化工清洁生产国家工程实验室,福建厦门361005)
以次亚磷酸钠(NaH2PO2)为还原剂,成功地制备出一种新型高效的Pd-P/C催化剂,其对甲酸-甲酸钠混合液分解制氢具有较高催化活性.经过优化后得到的3%Pd-P/C催化剂,在30 ℃,反应液甲酸和甲酸钠浓度比为1∶5,总浓度为4 mol/L条件下,前1 h平均转化频率可达565 h-1,该Pd-P/C催化剂的催化活性是传统的以NaBH4还原制得的Pd/C催化剂活性的3.5倍.联合谱学表征结果表明,在Pd粒子的形成生长过程中,P的掺入提高了Pd纳米粒子的分散性,减少了粒子的团聚,最终得到了粒径较小的Pd粒子,从而极大地提高了催化剂的活性.动力学研究表明Pd-P/C催化剂催化甲酸分解的反应活化能为18.63 kJ/mol,相比以NaBH4还原所得催化剂(反应活化能为26.69 kJ/mol),反应活化能更低.
甲酸;氢能源;NaH2PO2;Pd/C
工业革命以来,传统的化石能源日益枯竭,且引发了一系列资源与环境问题.人们迫切需要开发一种清洁廉价的新能源来逐步代替传统能源.而氢能以其清洁、可再生、化学活性高、资源丰富等优点引起了越来越多的关注[1].虽然氢能源有无可比拟的优点,但是实际开发应用中还有一些关键的技术问题,尤其是关于其制备与储备的问题尚待解决[2].
最近研究表明甲酸(FA)是潜在的再生能源[3],可由CO2加氢获得,它有较高的氢含量,使用简单、运输方便,被认为是最有前景的氢储存材料之一.FA分解有2种可能反应途径[4-6]:1) 脱氢,得到H2和CO2;2) 脱水,生成CO和H2;具体途径取决于所用催化剂、FA浓度以及反应温度.
目前,多相催化剂在催化FA分解上取得很大进展.其优点在于能使FA在较低温度下反应且容易分离和重复循环利用.目前,常见报道的为Pt、Au、Pd负载型多相催化剂,其中Pd最廉价,且Pt催化剂在反应中易产生大量CO,更容易使催化剂中毒[7-8],需进行表面改性处理.Pd基纳米催化剂是FA分解制氢反应最具潜力的金属催化剂[9-13].而目前报道的Pd基催化剂,大都局限于Pd和Au、Ag[9,12,14]的合金形式,因此开发低成本有效的Pd基催化剂对FA分解制氢的工业化应用更具现实性.
本文以NaH2PO2为还原剂,研发出一类新型高效的Pd-P/C催化剂,其对FA分解制氢具有较高催化活性.考察该催化剂对FA分解的反应活性,研究该反应的动力学过程的同时,联合利用X射线衍射(XRD)、扫描电子显微镜/能量色散光谱(SEM/EDX)等多种物理化学表征手段,进一步探讨了Pd-P/C高效催化FA分解的原因.
1 实验部分
1.1 试 剂
活性炭(AC)、PdCl2、NaH2PO2、NaBH4、NaOH、FA、甲酸钠(SF)、无水乙醇试剂均购买于国药集团化学试剂有限公司,均为分析纯.实验中所用蒸馏水皆为二次蒸馏水.
1.2 催化剂的制备
AC改性:实验对AC进行碱预处理,取2 g AC于10%(质量分数,下同)NaOH溶液中,超声0.5 h,90 ℃下搅拌1.5 h,冷却,洗涤至中性,80 ℃烘箱中干燥24 h.
催化剂制备:取200 mg处理后的AC,加入到10 mL 0.02 g/mL PdCl2溶液中,超声搅拌1 h,加5% NaOH溶液调节pH至9.5,后加入含0.38 g NaH2PO2(Pd和P原子比为1∶60)的水溶液,90 ℃下搅拌2 h,冷却后蒸馏水洗涤至Cl-全部去除,抽滤,烘干即得Pd-P/C催化剂.
作为比较,制备以NaBH4还原的Pd/C催化剂:取200 mg处理后的AC,加入到10 mL 0.02 g/mL PdCl2溶液中超声搅拌1 h,加5% NaOH溶液调混合液pH至9.5,加入含300 mg NaBH4的水溶液,于常温下搅拌2 h,洗涤,抽滤,烘干即得Pd/C催化剂.
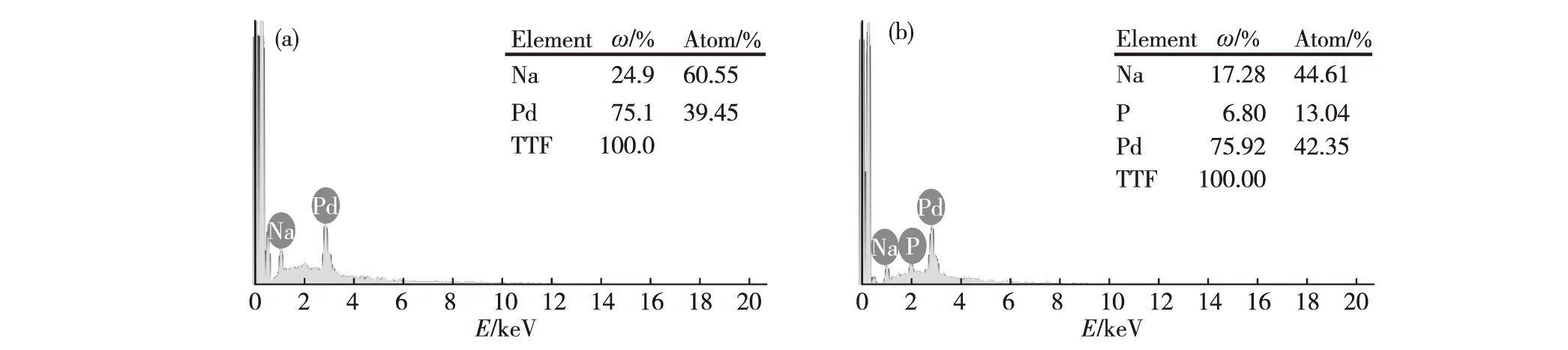
图2 Pd/C (a)和Pd-P/C (b)的EDX谱图
1.3 FA分解的评价和检测
将催化剂置于装有FA和SF的混合溶液(或纯FA和纯SF溶液)中,磁力搅拌,反应释放的气体通过导管引出,采用排液(饱和NaHCO3溶液)法测量一定时间内产生气体的体积,用转化频率(TOF)表示催化剂的催化活性,该TOF是基于催化剂总Pd原子数目,而不是催化剂活性中心数目进行计算,TOF计算公式为:
其中:patm为标准大气压力(101.325 kPa),VH2+CO2为反应液反应第一个小时内产生气体的体积,单位为L,R为理想气体常数(8.314 5 m3·Pa/(mol·K)),T为室温(298 K),nPd为催化剂所含Pd的物质的量,单位为mol,t为反应测试时间(1 h),文中的TOF均为反应第一个小时的平均TOF.
1.4 催化剂的物化性能表征
SEM测试于日本Hitachi公司的S-4800 SEM系统上进行,加速电压15 kV;样品的结构分析在Rigaku Ultima IV X射线衍射仪上完成,Cu靶材,Kα射线,管电压40 kV,管电流40 mA,扫描速率20 (°)/min,扫描范围10°~90°.
2 结果与讨论
2.1 还原方法的比较
本实验的创新性在于用NaH2PO2作为还原剂制备出Pd-P/C,并应用于催化FA分解的反应,为了突出该还原方法的优点,将其与传统NaBH4还原法制备的Pd/C催化剂的活性进行了对比.图1示出NaBH4还原所得催化剂Pd/C和NaH2PO2还原所得Pd-P/C催化剂催化FA分解反应活性的评价结果.从图中可以看出,在相同的反应条件下,由P促进的Pd-P/C催化剂催化FA分解的TOF可达473 h-1,是Pd/C催化剂(TOF为83 h-1)的5.7倍.
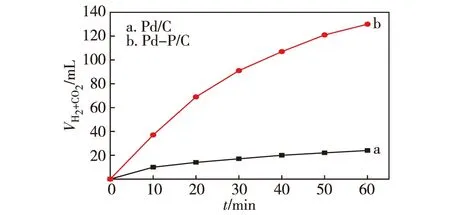
反应条件:20 mg 3%Pd-P/C或3%Pd/C催化剂,10 mL反应液(c(FA)∶c(SF)=1∶9,总浓度为2 mol/L),303 K.
图2(a)和(b)是Pd/C和Pd-P/C的EDX谱图.图2(a)的元素分析显示以NaBH4为还原剂时生成的Pd/C催化剂中并未检测到P元素的存在.而图2(b)显示NaH2PO2为还原剂时所得催化剂的组分为:Pd(质量分数75.92%),P(质量分数6.80%),有P的存在.该测试结果验证了Pd纳米粒子和P的共存关系,而Pd和P原子比为3.25∶1,说明大部分P已洗掉,只有少量的P与Pd共存,推测P的存在为该催化剂活性高的关键因素.
图3是Pd/C和Pd-P/C的XRD谱图.图中显示2种催化剂的C(002)晶面衍射峰都在25°,另外3个衍射峰40.15°,46.76°,和68.19°对应Pd晶面(111),(200),(220),说明此Pd纳米粒子在Pd-P/C和Pd/C 2种催化剂中都存在面心立方结构.对比图3-a和b可以看出,Pd-P/C的衍射图比Pd/C衍射图宽泛很多,Pd(200)的衍射峰据谢乐公式估算出Pd-P/C和Pd/C中Pd粒子的平均粒径分别为9和17 nm,说明Pd-P/C中Pd粒子的粒径更小.XRD图中并未观察到P的特征峰,说明P是以原子形式存在于Pd的晶格中.
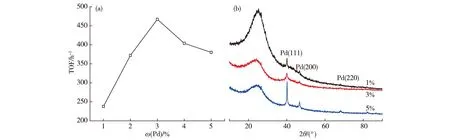
图5 不同Pd负载量的Pd-P/C活性对比(a)及XRD谱图(b)

图4 Pd/C (a)和 Pd-P/C (b)的SEM图
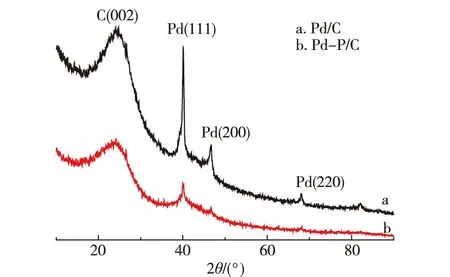
图3 Pd/C和Pd-P/C的XRD谱图
图4(a)和(b)为Pd/C和Pd-P/C的SEM图,图4(a)为存在于Pd/C催化剂表面团聚Pd颗粒的SEM图,而Pd-P/C催化剂表面未发现Pd团聚现象,均为图4(b)显示的均匀分布的细小Pd颗粒.可以看出Pd-P/C催化剂由于P的作用,减少了Pd粒子的团聚,得到分布均匀且粒径较小的Pd纳米粒子.
以上分析可得,在Pd的形成生长过程中,P的掺入使Pd纳米粒子分散良好,得到粒径较小的Pd粒子,为该催化剂高催化活性的主要原因.
2.2 Pd-P/C中Pd负载量的优化
催化剂的活性不仅与活性物种的大小、形貌有关,同时也与催化剂表面活性物种的数量有关,为此,进一步考察了Pd负载量对催化剂活性的影响(见图5).分别取含相同量Pd的100 mg 1%Pd-P/C,50 mg 2%Pd-P/C,33.3 mg 3%Pd-P/C,25 mg 4%Pd-P/C,20 mg 5%Pd-P/C 5组催化剂(1%,2%,3%,4%,5%均为Pd与催化剂的质量比,即Pd的负载量,制备时Pd和P原子比为1∶60保持不变),在10 mL反应液(c(FA)∶c(SF)=1∶9,总浓度为2 mol/L)中,30 ℃下进行反应.
图5(a)显示,随着Pd-P/C中Pd负载量的增加,催化剂的TOF逐渐增大,当Pd负载量为3%时,TOF达到471 h-1.随着Pd负载量进一步增加,TOF转而下降,这是因为在有限的载体表面,过多的Pd使部分粒子发生团聚,从而导致催化剂整体活性下降.图5(b)XRD表征显示,3种催化剂的衍射峰基本一致,随着Pd负载量增加,其衍射强度增加.
2.3 FA与SF浓度比的优化
为了探究SF对该反应的作用,本文考察了在Pd-P/C的催化作用下,保持FA与SF总浓度不变的前提下,FA与SF浓度比对反应速率的影响(见图6).取20 mg 3%Pd-P/C催化剂,加入到10 mL反应液(纯FA,c(FA)∶c(SF)=4∶1,1∶1,1∶4,1∶5,1∶9,纯SF,总浓度为2 mol/L),30 ℃下反应.
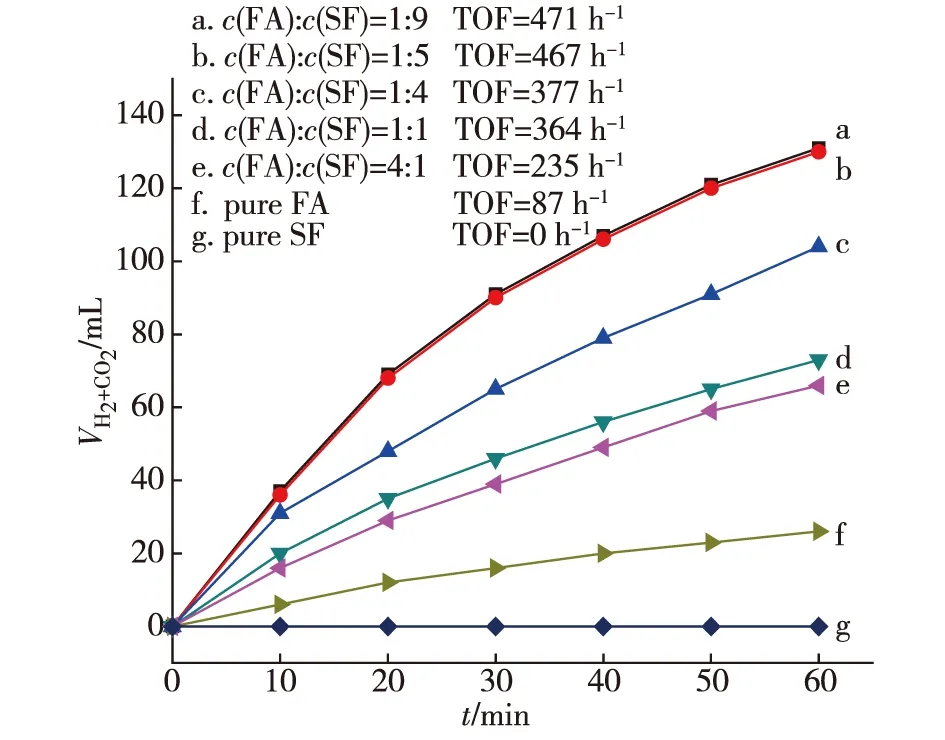
图6 催化剂催化不同浓度比的FA和SF反应液所产生气体的体积及对应TOF
从图6可看出FA存在的前提下,所含SF浓度越高,反应产生的气体量越多.然而当纯SF作为反应液时,相同实验条件基本无气体产生,纯FA反应有少量气体逸出.FA与SF浓度比为1∶5和1∶9时产生气体的量差别很小,出于FA量的考虑,取FA与SF浓度比为1∶5为最优比例.
为了考察SF的具体作用,在60 ℃下测定纯FA、纯SF及FA与SF浓度比1∶5时催化剂的反应活性.
由图7可以看出,60 ℃下纯FA、纯SF在Pd-P/C催化作用下都能分解放出气体.纯FA条件下,初始反应速度较快,但30 min时反应停止.纯SF反应速度最慢,却能持续反应近5 h.当FA与SF浓度比1∶5时,反应速度明显高于前两者,1 h后停止反应.可以看出SF的存在不仅提高了FA的分解速率,而且延缓了催化剂的失活.
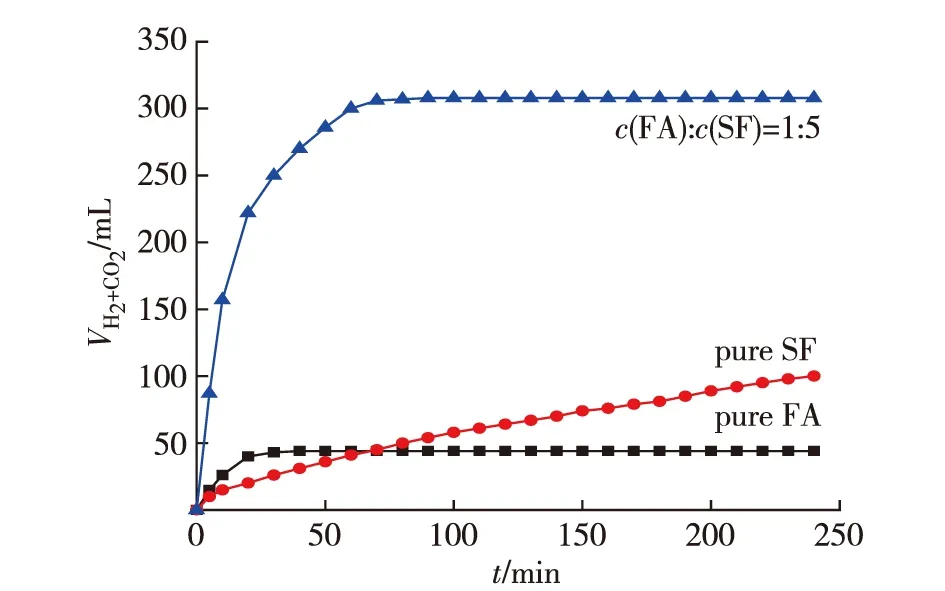
图7 60 ℃下催化剂催化不同浓度比的FA与SF所产生气体的体积
Pd-P/C催化剂可以催化分解FA和SF,溶液中FA分解存在2个竞争反应:
HCOOH→H2O+CO,
(1)
HCOOH→H2+CO2,
(2)
根据相关文献[15]报道,推测FA与SF混合液分解的反应途径为:
HCOO-+H2O→HCO3-+H2,
(3)
HCO3-+HCOOH→HCOO-+H2O+CO2,
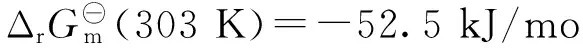
(4)
反应式(3)和(4)的总反应为式(2).
2.4 反应液总浓度的影响
此外,本实验还考察了反应液总浓度对反应速率的影响.取20 mg 3%Pd-P/C催化剂,加入到10 mL反应液中(c(FA)∶c(SF)=1∶5,FA和SF的总浓度分别为2,4,6,8 mol/L),在30 ℃下其催化反应的TOF分别为467,565,560,498 h-1.实验数据显示FA与SA总浓度为4 mol/L时,催化剂的TOF最高,过高的总浓度反而会导致TOF下降.推测可能是由于溶液过于黏稠,水的相对含量减少[16],使催化剂活性降低.
2.5 动力学研究
在研究其动力学过程时,考察了Pd-P/C和Pd/C催化剂在不同反应温度下对FA分解的催化活性.表1分别显示出2种催化剂在不同温度(303~333 K),c(FA)∶c(SF)=1∶5,总浓度为4 mol/L条件下催化FA分解的TOF.可以看出在303 K时,该Pd-P/C催化剂的催化活性是传统的以NaBH4还原制得的Pd/C催化剂活性的3.5倍.图8是各温度下TOF的自然对数值对温度倒数值的曲线图(lnTOF vsT-1).根据Arrhenius公式计算出Pd-P/C和Pd/C催化反应活化能分别为18.63和26.69 kJ/mol,说明相比Pd/C催化剂,Pd-P/C使FA分解反应的活化能降低.
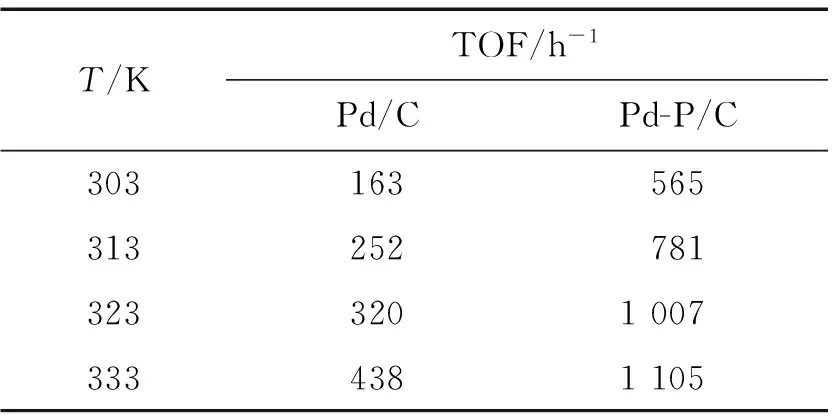
表1 不同温度下Pd-P/C和Pd/C催化剂催化反应液分解制氢的TOF

图8 Pd-P/C(a)和Pd/C(b)催化下甲酸分解反应的ln TOF对T-1曲线
3 结 论
本文以NaH2PO2为还原剂,制备出一种用于高效催化FA分解制氢的Pd-P/C催化剂,经过优化,在30 ℃,c(FA)∶c(SF)=1∶5,FA和SF的总浓度为4 mol/L条件下,反应第1小时的TOF可达565 h-1.对比近期相关文献报道的Pd基催化剂对FA分解的TOF值:Pd-NH2/MIL-125 (214 h-1,305 K)[17],Pd-Au-Dy/C[9](470 h-1,365 K),Pd9Ag1/rGO[18](526 h-1,298 K),显然,Pd-P/C反应速率有优势,且本催化剂为单金属催化剂,制备方法简单,NaH2PO2既为还原剂,又是添加剂P的来源.通过表征发现,相比于传统NaBH4还原法制备的Pd/C催化剂,P的掺入,一定程度上阻止了Pd纳米粒子的团聚,使Pd纳米粒子更均匀地分散于AC表面,得到了粒径较小的Pd纳米粒子.动力学研究表明,相比于Pd/C催化剂,Pd-P/C催化剂使FA分解反应的活化能得以降低.虽然Pd-P/C催化剂催化活性较高,但其稳定性却不理想,容易失活.查找催化剂失活的原因,提高Pd-P/C催化剂的实用性是本课题组今后需继续努力的方向.
[1] Weisz P B.Basic choices and constraints on long-term energy supplies[J] Physics Today,2004,57(7):47-52.
[2] von Helmolt R,Eberle U.Fuel cell vehicles:status 2007[J].Journal of Power Sources,2007,165(2):833-843.
[3] Enthaler S,von Langermann J,Schmidt T.Carbon dioxide and formic acid—the couple for environmental-friendly hydrogen storage?[J].Energy & Environmental Science,2010,3(9):1207-1217.
[4] Zhou X,Huang Y,Xing W,et al.High-quality hydrogen from the catalyzed decomposition of formic acid by Pd-Au/C and Pd-Ag/C[J].Chemical Communications,2008 (30):3540-3542.
[5] Metin Ö,Sun X,Sun S.Monodisperse gold-palladium alloy nanoparticles and their composition-controlled catalysis in formic acid dehydrogenation under mild conditions[J].Nanoscale,2013,5(3):910-912.
[6] Gan W,Snelders D J M,Dyson P J,et al.Ruthenium (II)-catalyzed hydrogen generation from formic acid using cationic,ammoniomethyl-substituted triarylphosphine ligands[J].ChemCatChem,2013,5(5):1126-1132.
[7] Chen A,Holt-Hindle P.Platinum-based nanostructured materials:synthesis,properties,and applications[J].Chem Rev,2010,110(6):3767-3804.
[8] Cuesta A,Cabello G,Osawa M,et al.Mechanism of the electrocatalytic oxidation of formic acid on metals[J].ACS Catalysis,2012,2(5):728-738.
[9] Zhou X,Huang Y,Liu C,et al.Available hydrogen from formic acid decomposed by rare earth elements promoted Pd-Au/C catalysts at low temperature[J].ChemSusChem,2010,3(12):1379-1382.
[10] Jia L,Bulushev D A,Podyacheva O Y,et al.Pt nanoclusters stabilized by N-doped carbon nanofibers for hydrogen production from formic acid[J].Journal of Catalysis,2013,307:94-102.
[11] Wang Z L,Yan J M,Wang H L,et al.Au@Pd core-shell nanoclusters growing on nitrogen-doped mildly reduced graphene oxide with enhanced catalytic performance for hydrogen generation from formic acid[J].Journal of Materials Chemistry A,2013,1(41):12721-12725.
[12] Wang Z L,Yan J M,Ping Y,et al.An efficient CoAuPd/C catalyst for hydrogen generation from formic acid at room temperature[J].Angewandte Chemie International Edition,2013,52(16):4406-4409.
[13] Mori K,Dojo M,Yamashita H.Pd and Pd-Ag nanoparticles within a macroreticular basic resin:an efficient catalyst for hydrogen production from formic acid decomposition[J].ACS Catalysis,2013,3(6):1114-1119.
[14] Huang Y,Zhou X,Yin M,et al.Novel PdAu@Au/C core-shell catalyst:superior activity and selectivity in formic acid decomposition for hydrogen generation[J].Chemistry of Materials,2010,22(18):5122-5128.
[15] Wang X,Qi G W,Tan C H,et al.Pd/C nanocatalyst with high turnover frequency for hydrogen generation from the formic acid-formate mixtures[J].International Journal of Hydrogen Energy,2014,39(2):837-843.
[16] Akiya N,Savage P E.Role of water in formic acid decomposition[J].AIChE Journal,1998,44(2):405-415.
[17] Martis M,Mori K,Fujiwara K,et al.Amine-functionalized MIL-125 with imbedded palladium nanoparticles as an efficient catalyst for dehydrogenation of formic acid at ambient temperature[J].The Journal of Physical Chemistry C,2013,117(44):22805-22810.
[18] Ping Y,Yan J M,Wang Z L,et al.Ag0.1-Pd0.9/rGO:an efficient catalyst for hydrogen generation from formic acid/sodium formate[J].Journal of Materials Chemistry A,2013,1(39):12188-12191.
Improved Highly Efficient Hydrogen Production from Formic Acid on a Pd/C Catalyst Doped by Phosphorus
JIAO Xiao-xin,ZHENG Xiao-xiao,ZHANG Hong-bin,LI Hai-yan*
(State Key Laboratory of Physical Chemistry of Solid Surfaces,National Engineering Laboratory for Green Chemical Productions of Alcohols-Ethers-Esters,College of Chemistry and Chemical Engineering,Xiamen University,Xiamen 361005,China)
A potent phosphorus-doped Pd nanocatalyst (Pd-P/C) for hydrogen generation from the formic acid (FA)-sodium formate (SF) mixtures has been successfully prepared via the reduction of NaH2PO2.Over this 3%Pd-P/C catalyst,the turn-over frequency (TOF) of 565 h-1was observed for a FA-SF mixture with a FA/SF concentration ratio of 1∶5 and the total concentration of 4 mol/L at 30 ℃.Compared with Pd/C synthesized with a NaBH4reduction method,the activity of Pd-P/C is 3.5 times as much.The results of the catalyst characterization demonstrated that the modification with P during the formation and growth of particles resulted in the well-dispersed fine Pd nanoparticles on carbon and enhanced the catalytic performance of the resulted catalyst.Kinetic studies showed that its reaction activation energy was 18.63 kJ/mol when utilizing Pd-P/C,much lower than utilizing Pd/C as a catalyst (reaction activation energy of 26.69 kJ/mol).
formic acid;hydrogen energy;NaH2PO2;Pd/C
2015-01-08 录用日期:2015-03-20
国家重点基础研究发展计划(973计划)(2011CBA00500);福建省自然科学基金 (E0510001)
焦晓新,郑潇潇,张鸿斌,等.P促进Pd/C高效催化甲酸制氢的研究[J].厦门大学学报:自然科学版,2015,54(5):707-712.
:Jiao Xiaoxin,Zheng Xiaoxiao,Zhang Hongbin,et al.Improved highly efficient hydrogen production from formic acid on a Pd/C catalyst doped by phosphorus[J].Journal of Xiamen University:Natural Science,2015,54(5):707-712.(in Chinese)
10.6043/j.issn.0438-0479.2015.05.014
新能源材料专题
O 641
A
0438-0479(2015)05-0707-06
* 通信作者:hyli@xmu.edu.cn
