紫外分光光度法测定吲哚美辛片含量及肠溶片的释放度*
2015-06-05吕倩李婷婷李珂
吕倩 李婷婷 李珂
(泰山医学院药学院,山东泰安271016)
紫外分光光度法测定吲哚美辛片含量及肠溶片的释放度*
吕倩 李婷婷 李珂
(泰山医学院药学院,山东泰安271016)
目的建立吲哚美辛的紫外分光光度法,并用于吲哚美辛片中吲哚美辛含量及肠溶片释放度的测定。方法采用紫外分光光度法,以磷酸盐缓冲液(pH7.2)—甲醇(1∶1)为溶剂,最大吸收波长320 nm。结果吲哚美辛标准品溶液在10~35 μg/ml的浓度范围内,A=0.0195C+0.0554(μg/ml)线性关系良好,相关系数为0.9995 (n=6);样品在7h内稳定,RSD%为0.25%;平均回收率分别为95.96%,96.85%,98.82%,RSD分别为0.31%,0.36%,0.15%。结论该含量测定方法准确,快速,简单,可靠,可用于吲哚美辛片含量及肠溶片释放度的测定,较适用于生产过程中的质量控制。
紫外分光光度法;吲哚美辛片;吲哚美辛肠溶片;含量测定
吲哚美辛片是常用的前列腺素合成酶抑制药之一,为非甾体消炎解热镇痛药,有显著的抗炎及解热作用,对炎性痛有明显的镇痛效果[1]。其作用机理为通过抑制环氧化酶,从而减少前列腺素的合成,制止炎症组织痛觉神经冲动的形成,抑制炎性反应。主要适用于:①关节炎,可缓解疼痛和肿胀;②软组织损伤和炎症;③解热;④其他:用于治疗偏头痛、痛经、手术后痛、创伤后痛等。了解药品中吲哚美辛的含量,能使我们能够安全合理的用药以及为生产过程的质量控制提供依据。用高效液相法[2-5]可测定吲哚美辛的含量,但用高效液相法测定其含量具有分析成本高、高效液相色谱仪价格及日常维护费用贵、分析时间比较长等缺点。
吲哚美辛在紫外光区有明显的特征吸收,因此本研究采用紫外分光光度法直接测定吲哚美辛片剂的含量,具有操作简便快捷、灵敏度高、精密度及重现性好、仪器设备简单等优点,尤其适用于生产过程中的质量控制。
1 仪器与试剂
1.1 仪器
岛津UV-2550紫外可见分光光度仪(日本岛津公司);电子分析天平(赛多利斯科学仪器北京有限公司);ZRS-8G智能溶出试验仪(天津市天大天发科技有限公司);KQ-500E型医用超声波清洗器(昆山超声仪器有限公司)。
1.2 药品及试剂
吲哚美辛原料药(浙江太仓制药有限公司,生产批号090807);吲哚美辛片(临汾奇林药业有限公司,产品批号1309151,规格为25 mg/片);吲哚美辛肠溶片(临汾宝珠制药有限公司,产品批号131001,规格为25 mg/片);吲哚美辛肠溶片(山西云鹏制药有限公司,产品批号A130702,规格为25 mg/片);纯净水(纯净水公司提供);甲醇(分析纯,天津市永大化学试剂有限公司);盐酸(分析纯,济南试剂总厂)。磷酸二氢钾(分析纯,天津市科密欧化学试剂开发中心);氢氧化钠(分析纯,天津市永大化学试剂有限公司)。
2 实验方法与结果
2.1 测定波长的确定
用移液管精密吸取对照品储备液5.0 ml,置100 ml容量瓶中,用磷酸盐缓冲液(pH7.2)—甲醇(1∶1)溶解,溶液稀释至刻度,摇匀,稀释成25 μg/ ml的溶液,在200~400 nm范围内进行紫外光谱扫描,得到吲哚美辛的紫外吸收光谱见图1,实验结果表明吲哚美辛片的紫外最大吸收波长为320 nm,因此本实验选择320 nm作为测定波长。
2.2 溶液的配制
2.2.1 稀盐酸溶液的配制0.1 mol/L的稀盐酸的配制:取36.5%的浓盐酸8.4 ml加991.6 ml纯净水。
2.2.2 磷酸盐缓冲液的配制pH7.2的磷酸盐缓冲液的配制[6]:精密称取0.7000 g氢氧化钠于烧杯中,加纯净水,搅拌溶解,再加入精密称取3.4000 g的磷酸二氢钾,搅拌溶解,用水稀释至500 ml,摇匀即得。
pH6.8的磷酸盐缓冲液的配制[6]:精密称取0.9440 g氢氧化钠于烧杯中,加纯净水,搅拌溶解,再加入精密称取6.8000 g的磷酸二氢钾,搅拌溶解,用水稀释至1000 ml,摇匀即得。
2.2.3 对照品储备液的配制取氢氯噻嗪原料药50.02 mg,精密称定置100 ml容量瓶中,加甲醇50 ml,振摇10 min使全部溶解,用磷酸盐缓冲液(pH7.2)稀释至刻度,摇匀,制成500 μg/ml吲哚美辛对照品储备液。
2.2.4 供试品溶液的配制取吲哚美辛片20片(临汾奇林药业有限公司,产品批号1309151),精密称定为1.2848 g,研细,精密称取片粉64.34 mg(约相当于吲哚美辛25 mg),置100 ml容量瓶中,加入甲醇70 ml,微温使吲哚美辛溶解,放冷至室温,加甲醇稀释至刻度,摇匀,滤过;精密量取续滤液1 ml,置10 ml量瓶中,加磷酸盐缓冲液(pH7.2)—甲醇(1∶1)至刻度,摇匀,作为供试品溶液。
2.3 方法学考察和样品测定
2.3.1 标准曲线的绘制精密吸取上述对照品储备液,配制浓度分别为10 μg/ml、15 μg/ml、20 μg/ ml、25 μg/ml、30 μg/ml、35 μg/ml的溶液,以溶剂做空白,照紫外分光光度法于320 nm波长处,测定各溶液的吸光度,以吲哚美辛浓度(C)为横坐标,吸收度(A)为纵坐标,进行线性回归,计算得回归方程为A=0.0195C+0.0554(μg/ml),结果显示氢氯噻嗪在10~35 μg/ml浓度范围内的吸光度有良好的线性关系,相关系数r=0.9995。
2.3.2 稳定性试验将上述配制的浓度为25 μg/ ml供试品溶液分别在0、1、2、3、4、5、6、7h测定溶液的吸光度。结果显示,溶液在7 h内稳定,平均值为0.5224,RSD为0.31%,表明溶液的稳定性良好。
2.3.3 重复性试验称取吲哚美辛片粉6份(临汾奇林药业有限公司,产品批号1309151),每份约64.24 mg(约相当于吲哚美辛25 mg),精密称定,分别置100 ml容量瓶中,加入甲醇70 ml,微温使吲哚美辛溶解,放冷至室温,加甲醇稀释至刻度,摇匀,过滤,弃去初滤液,取续滤液1.0 ml分别置6个10 ml容量瓶中,加磷酸盐缓冲液(pH7.2)—甲醇(1∶
1),稀释至刻度,摇匀,照紫外分光光度法于320 nm波长处测定吸光度,计算出样品中吲哚美辛的含量。结果表明此试验重复性良好。
2.3.4 回收率试验精密称取吲哚美辛片粉9份(临汾奇林药业有限公司,产品批号1309151),每份3.05 mg(约含吲哚美辛1 mg),每3份一组,分别置10 ml容量瓶中,用适量甲醇溶解,第一组加吲哚美辛标准品0.8 mg,第二组加吲哚美辛标准品1.0 mg,第三组加吲哚美辛标准品1.2 mg,分别用磷酸盐缓冲液(pH7.2)—甲醇(1∶1)定容至刻度,摇匀,过滤,弃去初滤液,分别精密移取续滤液1.0 ml至9个10 ml容量瓶中,加磷酸盐缓冲液(pH7.2)—甲醇(1∶1)稀释至刻度,照紫外-可见分光光度法(中国药典2010年版二部附录ⅣA)于320 nm波长处,测定溶液的吸光度,计算回收率。
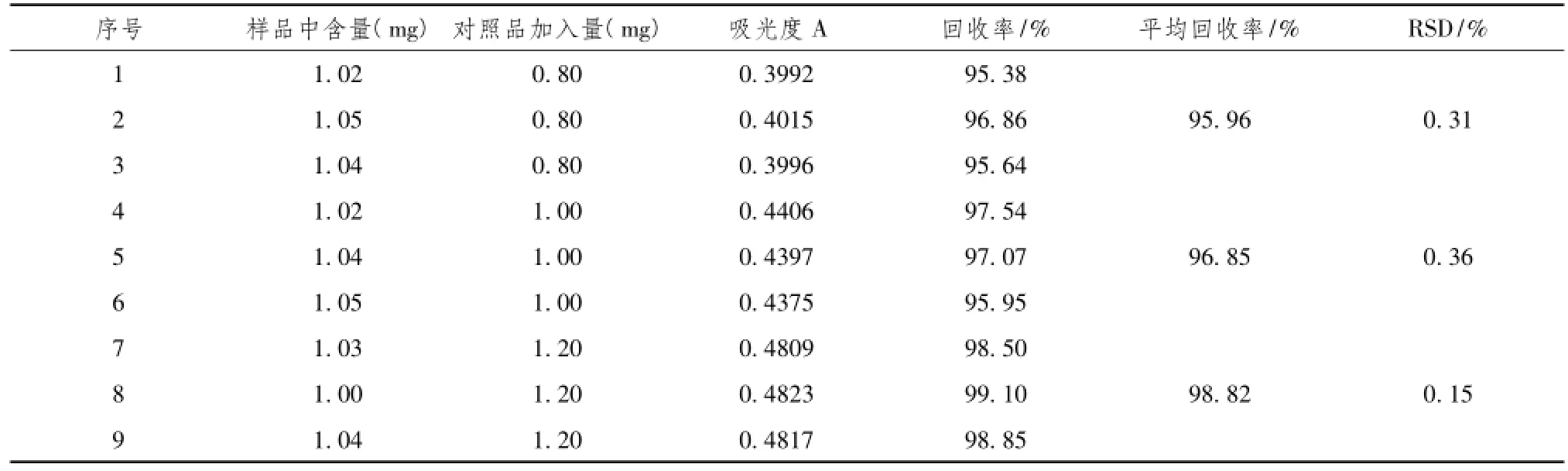
表2 回收率试验结果
2.3.5 含量测定取吲哚美辛片20片,精密称定,研细,精密称取片粉适量(约相当于吲哚美辛25 mg),精密称定,至100 ml量瓶中,加适量甲醇70 ml,微温使吲哚美辛溶解,放冷至室温,加甲醇稀释至刻度,摇匀,过滤,精密量取续滤液1.0 ml至10 ml量瓶中,加磷酸盐缓冲液(pH7.2)—甲醇(1∶1)稀释至刻度,摇匀,作为供试品溶液;另取其他规格吲哚美辛片,同法制成每1 ml中约含氢氯噻嗪25 μg的溶液,照紫外分光光度法(中国药典2010年版二部附录IVA)于320 nm波长处,测定溶液的吸收度,计算,即得本品3批样品测定结果。结果见表3。
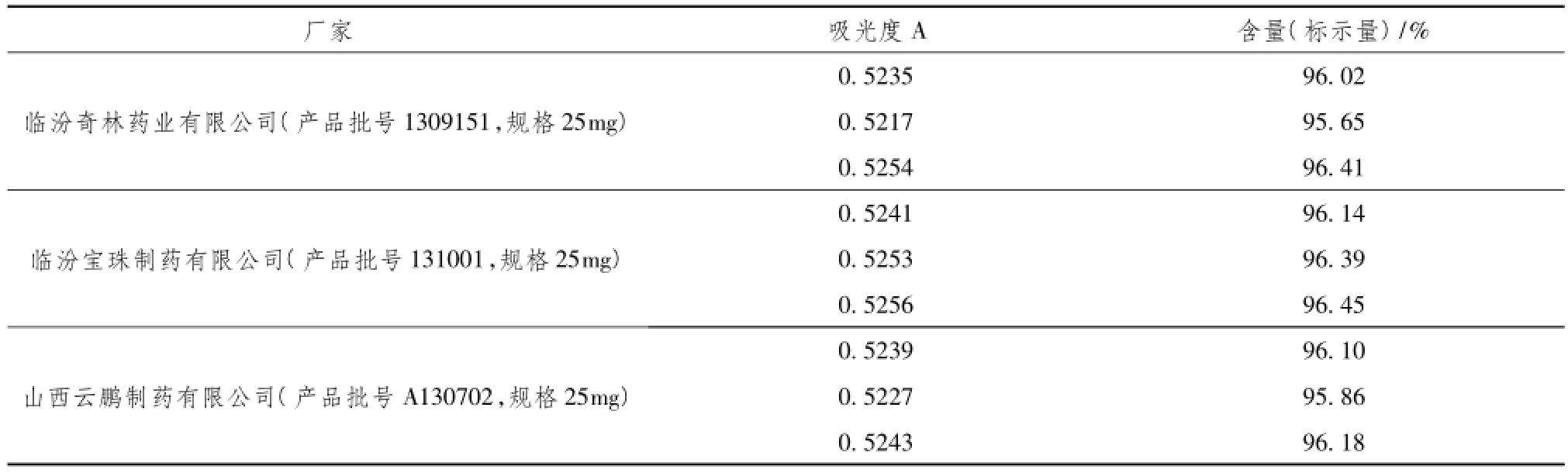
表3 吲哚美辛片含量测定结果
2.3.6 释放度的测定[7,8]酸中释放度:照释放度测定法(附录XD第二法),采用溶出度测定法第一法装置,加入1000 ml 0.1 mol/L盐酸溶液为释放介质注入每个溶出杯,实际量取的体积与规定体积的偏差应不超过±1%,待溶出介质温度恒定在37℃±0.5℃时,取吲哚美辛肠溶片6片分别投人ZRS-8G智能溶出仪的六个转篮中,注意供试品表面不要有气泡,转速为每分钟100转,依法操作,经2 h后,分别吸取溶液10 ml,滤过,自取样只滤过应在30秒内完成,照紫外-可见分光光度法(附录ⅣA),在320 nm的波长处测定吸光度,计算每片酸中的释放量。
缓冲液中释放度:经2 h时,立即将转篮升出液面,供试片均不得有裂缝或崩解等现象,随即将转篮浸入磷酸盐缓冲液(pH6.8)1000 ml释放介质中,转速为100转每分钟,继续依法操作,经45min时,取溶液滤过,自取样至滤过应在30 s内完成,照紫外—可见分光光度法(附录ⅣA),在320 nm的波长处测定吸光度,计算每片缓冲液中的释放量。
根据2010年版中国药典释放度测定法(附录XD第二法方法2),酸中释放量每片的释放量均不大于标示量的10%,结果见表4,从表中可以看出两厂家生产的吲哚美辛在酸中的释放度均不大于10%的要求,符合2010年版中国药典的规定,而且两个厂家的吲哚美辛肠溶片均未见裂片,符合中国药典对吲哚美辛肠溶片在酸性介质中的溶出规定,说明药品是合格的;根据2010年版中国药典释放度测定法(附录XD第二法方法2),缓冲液中释放量每片的释放量均不小于70%,结果见表5,从表中可以看出两厂家生产的吲哚美辛在酸中的释放度均不小于70%的要求,符合2010年版中国药典的规定,说明药品是合格的
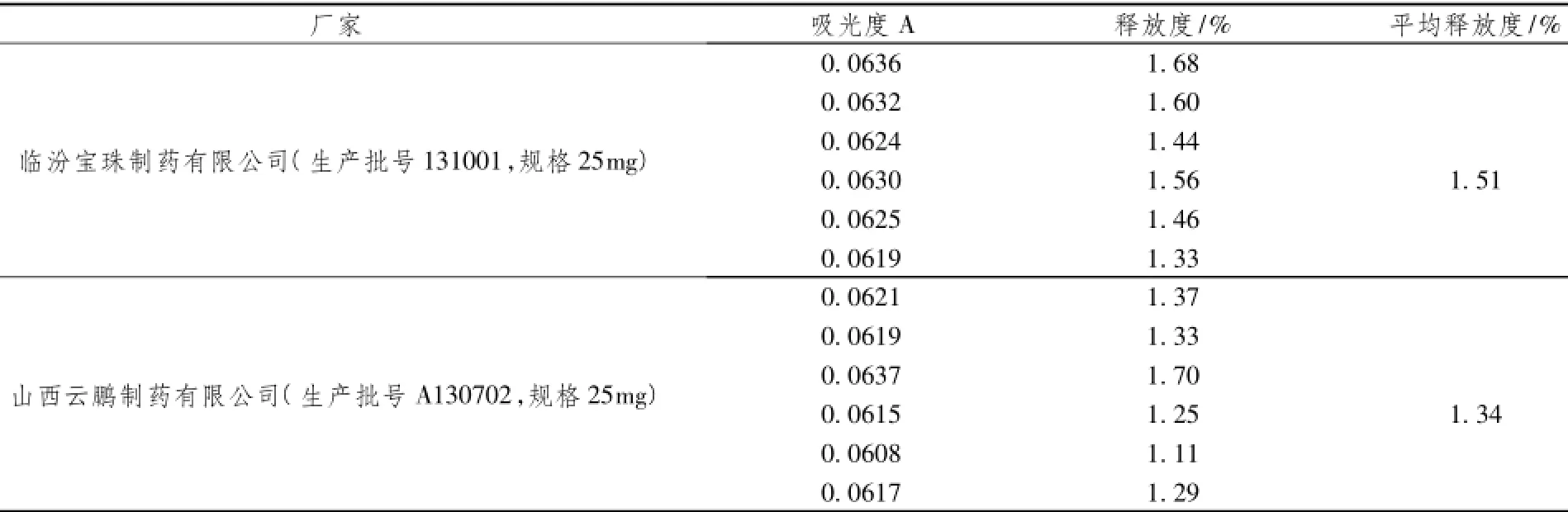
表4 吲哚美辛肠溶片酸中释放度测定结果
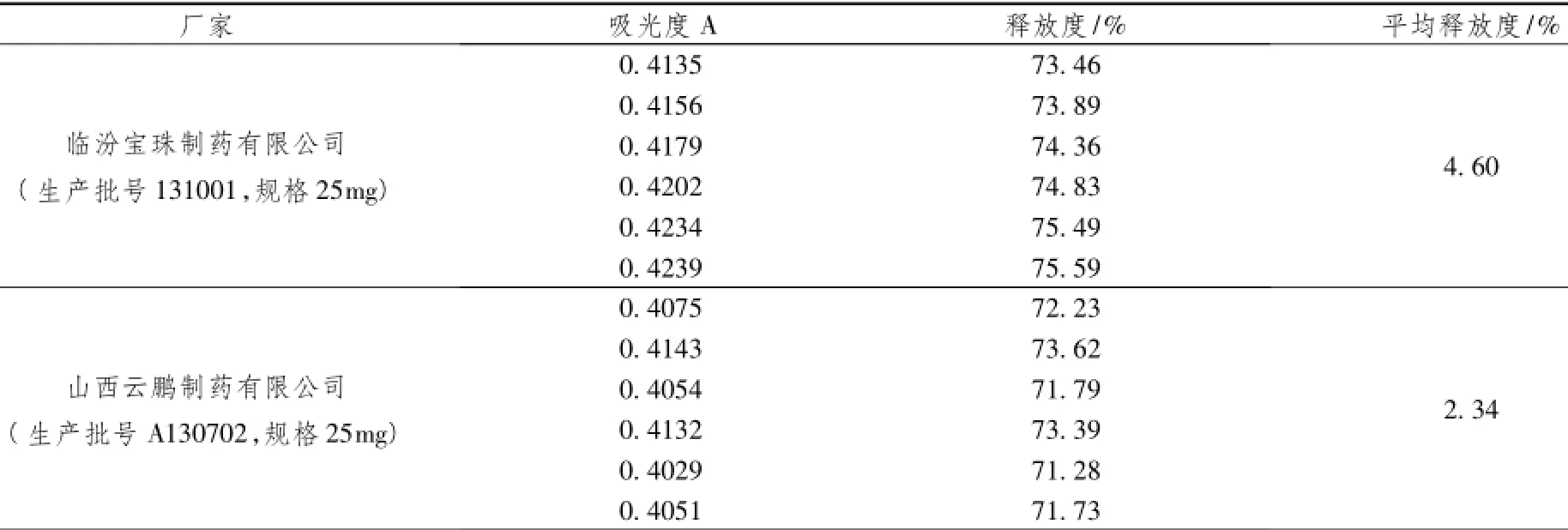
表5 吲哚美辛肠溶片在缓冲液中释放度测定结果
3 讨论
3.1 辅料的干扰[9]
本实验研究过程中,在确定最大吸收波长的同时对空白辅料(淀粉、胶化淀粉、聚乙烯比咯烷酮、硬脂酸、滑石粉等混合辅料)的吸收波长进行了测定,结果表明药品辅料在200-400nm波长范围内无吸收,不干扰样品的测定,故选择的波长范围在200~400 nm之间。
3.2 溶剂的选择
吲哚美辛在水中溶解性差,根据中国药典(2010年版),本研究采用甲醇作为溶剂,以磷酸盐缓冲溶液(pH7.2)-甲醇(1:1)稀释后测定。
3.3 影响因素
应用转篮实验时,应注意转篮的洁净程度,一般在阳光下观察转篮的空隙是否有堵塞,如有堵塞,可采用超声或在稀硝酸中煮沸、再在水中煮沸的办法进行,直至确认无任何堵塞物的存在,否则将会影响数据的准确性。实验前应注意外围水浴高度超过溶出杯里液面高度,否则将影响溶出杯中溶出液的温度,导致结果偏低。
[1]赵排风,郭重仪,陈天义等.不除肠溶衣测定吲哚美辛肠溶片的含量[J].中国药师,2002,5(10):634-635.
[2]孙银华.HPLC法测定吲哚美辛片含量及有关物质[J].中国药事,2012,26(2):172-177.
[3]高颖,吴艺君,金蓉蓉,等.高效液相法测定吲哚美辛缓释微球的含量[J].药物生物技术,2012,19(2):0150-0152.
[4]Wang HM,Zhang GY.Indomethacin suppresses growth of colon cancer via inhibition of angiogenesis in vivo[J].World J Gastroenterol.2005,11(3):340.
[5]Heller J.Ocular delivery using poly(ortho esters)[J].Adv Drug Deliv Rev.2005,57(14):2053.
[6]中华人民共和国药典,二部.2010:附录177.
[7]许善初,邢蓉,石庆平等.6厂家吲哚美辛肠溶片体外溶出试验比较[J].蚌埠医学院学报,2004,29(5):467-468.
[8]国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2000:296,附录75.
[9]辛俊衡.HPLC法测定吲哚美辛片剂的含量[J].中国药事,2004,18(4):238.
[10]国家药典委员会.中华人民共和国药典(二部)[S].2010版.北京:中国医药科技出版社,2010:附录XC:附录85-86.
Determination of the Indom -metacin content and release of Indom metacin Enteric -coated Tablets by Uv -vis method
LV Qian LI Ting-ting LI Ke
(Pharmacy Department,Taishan Medical University,Taian 271016,China)
Objective:To establish a Uv-vis method for Indom-metacin,and apply it into the determin of release ratel of Indom metacin Enteric-coated Tablets.Method:Adopting Uv-vis phosphate buffer solution(Ph7.2)-alcohl(1∶1) as dissolvant to determin its absorbance at the biggest assimilate wavelength.Results:Indom metacin’s standard substance dissolvent in the 10~35 μg/ml concentration renge,A=0.0195C+0.0554(μg/ml)(r=0.9995)good liner ralation.The sample will be stabilization in 7h(RSD=0.25%),the average of Indom metacin Enteric-coated Tablets(n=6)were 95.96%(RSD=0.31%),98.85%(RSD=0.36%),98.82%(RSD=0.15%).Conclusion:The method is accurate,convienent,sensitive and reliable with high reproducibility and used for content determination of release ratel of Indom metacin Enteric-coated Tablets and management control in the productive process.
Uv-vis;indom mectain;indom mecain;enteric-coated tablt;content determination
R917
A
1004-7115(2015)08-0884-04
10.3969/j.issn.1004-7115.2015.8.013
2015-5-28)
吕倩(1995—),女,山东济南人,泰山医学院药学院本科学生。
李珂,泰山医学院药学院副教授,E-mail:kli@tsmc.edu.cn。
