纤维素催化氢解制取多元醇的研究进展*
2015-06-01刘琪英廖玉河王铁军马隆龙
刘琪英,廖玉河,2,徐 莹,王铁军,张 琦,马隆龙†
(1. 中国科学院广州能源研究所,中国科学院可再生能源重点实验室,广州 510640;2. 中国科学院大学,北京 100049)
纤维素催化氢解制取多元醇的研究进展*
刘琪英1,廖玉河1,2,徐 莹1,王铁军1,张 琦1,马隆龙1†
(1. 中国科学院广州能源研究所,中国科学院可再生能源重点实验室,广州 510640;2. 中国科学院大学,北京 100049)
化石资源日益减少和使用化石资源带来的气候与环境问题促使人们将目光转向可再生的生物质资源。由生物质资源制备高附加值的化学品已成为国内外的研究热点。通过催化氢解将纤维素转化为多元醇化学品是一种可行的手段。本文总结了由纤维素氢解制备多元醇的最新研究进展,重点介绍了纤维素转化为山梨醇/甘露醇、异山梨醇和小分子多元醇(丙二醇和乙二醇)的催化剂体系以及可能的转化途径。最后分析了该领域存在的问题和今后的研究趋势。
纤维素;催化氢解;多元醇;反应机理
0 前 言
当今社会面临着化石燃料储量日趋枯竭、温室效应气体排放以及世界能源需求日益增加等问题。虽然化石燃料枯竭问题尚未有一个明确的时间表,但化石能源的时代终将结束[1]。基于太阳能、风能、水电能、地热能、生物质能等的可再生能源必占未来世界能源消耗的大部分。然而,目前使用的液体燃料和化学品几乎都来自煤、石油和天然气等化石资源,因此开发替代资源势在必行。纤维素由光合作用产生,是自然界储量丰富、来源稳定且廉价易得的一类可再生生物质资源。利用纤维素为原料生产高附加值的燃料和化学品,已经引起了国内外研究者的广泛关注[2]。由于纤维素生物质在生长与转化利用中的快速碳循环,生物基产品的生产可以延缓化石基产品生产中由碳排放引起的气候与环境问题。
纤维素高值化利用的有效途径之一是采取催化氢解手段,直接将其转化成包括山梨醇/甘露醇、异山梨醇和小分子多元醇如甘油、乙二醇、1,2-丙二醇和1,3-丙二醇等在内的多元醇。该类多元醇在精细化工、有机中间体、医药和聚酯材料等领域具有广泛的应用前景[3-5]。本文以自然界储量最为丰富的纤维素为原料直接制备糖醇和小分子多元醇,从催化剂体系、反应路径等方面进行了系统总结,并对未来该方向可能取得突破的重点进行了展望。
1 纤维素制山梨醇/甘露醇
1.1 催化体系
由纤维素制山梨醇/甘露醇的传统方法是一个两步反应过程:纤维素首先在酸作用下水解得到还原性单糖,然后对还原性单糖加氢到山梨醇和甘露醇。采用金属−酸双功能催化剂体系,可以耦合水解和加氢步骤,实现纤维素一步转化为山梨醇和甘露醇。目前的研究手段主要包括两种:(1)耦合水解/加氢反应制山梨醇和甘露醇;(2)直接催化氢解制山梨醇和甘露醇。
1.1.1 耦合水解/加氢制山梨醇和甘露醇
该体系和传统方法并无本质区别,只是耦合了纤维素水解反应和还原性糖加氢反应两个步骤。文献大多采用硫酸、磷酸、杂多酸及杂多酸盐等作为酸催化剂水解纤维素获得葡萄糖,利用对葡萄糖加氢效果较好的Ru/C催化剂进行加氢获得目标产物。
REGINA等使用无机酸(硫酸和磷酸)和碳负载的Pt、Pd、Ru催化剂在160℃、氢气压力5 MPa进行实验。研究发现加氢催化剂能够提高纤维素的转化率,不同金属的加氢和氢解能力不一样,使用Ru/C能够得到收率为59.9%的C4~C6醇[6]。虽然使用无机酸和Ru/C能够在比较温和的条件下制山梨醇和甘露醇,但鉴于无机酸不易回收的难题,近几年研究人员采用运用重结晶方法回收的杂多酸来水解纤维素。采用H3PW12O40或H4SiW12O40结合Ru/C 为催化剂,以α-纤维素为原料,在160℃、氢气压力5 MPa、反应7 h条件下C4~C6醇收率高达80.6%。如果以杉木为原料在相同条件下反应5 h,糖醇收率可以达到65%[7]。若以球磨微晶纤维素为原料在190℃和氢气压力5 MPa下还可以高浓度(279 g·L−1·H−1)制取C6醇,C6醇收率高达92%[8]。相对于无机酸,杂多酸虽然在回收和产物收率方面具有更大的优势,但系列实验证明杂多酸即使采用重结晶方法其回收率也只有50%左右。由于一些杂多酸盐不溶于水或者溶解度很小,经过一定的预处理后具有杂多酸的性质,所以可以使用杂多酸盐代替杂多酸。通过实验发现,经过不同焙烧温度和水热预处理的杂多酸铯盐,具有杂多酸的性质且催化性能也得到了改善:改变焙烧温度可以降低杂多酸铯盐在水相中的溶解度(有利于回收再利用),水热预处理能够增强活性和提高产物的选择性[9]。
球磨预处理可减小纤维素的结晶度,从而提高纤维素的可及率,但是球磨需要很长时间(约2天),因此通过球磨预处理的效率不高。SCHUTH等将纤维素浸泡在硫酸中,然后进行球磨得到可溶于水的低聚糖,使用Ru/C对低聚糖加氢即得到糖醇,整个过程只需4 h,效率比球磨预处理方法提高18~27倍,且降低了反应温度。如果对Ru/C催化剂进行水热预处理,反应温度可进一步降低[10]。由于水在高温下会自发产生H+,因此可以用高温水和Ru/C制取多元醇,反应产物主要得到山梨醇和甘露醇[11]。关于耦合水解/加氢反应制取多元醇的实验结果见表1。

表1 耦合水解/加氢反应制取山梨醇和甘露醇的不同实验结果Table 1 Results of sorbitol and mannitol production by coupling of hydrolysis and hydrogenation
1.1.2 纤维素直接氢解制山梨醇和甘露醇
由于耦合水解反应和加氢反应制山梨醇和甘露醇中使用的液体酸催化剂存在污染环境和催化剂回收难等问题,近年来研究人员研究了使用固体催化剂来制取山梨醇和甘露醇。直接催化氢解纤维素与耦合水解/加氢反应制山梨醇和甘露醇的不同在于,水解纤维素所需要的H+来源于高温水或H2在加氢活性组分表面的溢流效应,对水解得到的还原性糖进行加氢的活性组分多选用Pt、Ni、Ru等金属。FUKUOKA等以负载型Pt催化剂进行了纤维素和淀粉直接转化为山梨醇和甘露醇的研究,发现在所研究的催化剂中,山梨醇和甘露醇在Pt/γ-Al2O3的收率和选择性最高,山梨醇和甘露醇的最高总收率为31%(山梨醇为25%,甘露醇为6%)[12]。由于SnOx的电子和几何效应,在Pt/Al2O3中添加SnOx可以显著改善该类催化剂的性能。通过实验研究发现,Sn/Pt比在0.1~1范围存在SnOx向Pt的电子转移,这种电子转移效应是其具有优异加氢性能及山梨醇和甘露醇选择性高的原因。当Sn/Pt=0.5时,山梨醇和甘露醇的选择性为82.7%,是Pt/Al2O3在相同转化率(20%)下的两倍。如果Sn/Pt > 1.5,其主产物为C2和C3醇,主要原因是反应过程中形成了碱性的Sn(OH)2[13]。有研究表明,使用不同前驱体的Pt催化剂会导致催化剂上的差异。使用不含氯的Pt前驱体能提高山梨醇和甘露醇的选择性和收率;反之,氯离子的存在则加速C−C断裂、脱水等副反应获得小分子多元醇[14]。对于Ru催化剂,纳米团簇Ru在酸性溶液中能催化氢解纤维二糖制备山梨醇[15]。如果把纳米粒子Ru负载在CNTs(碳纳米管)和杂多酸铯盐上,则纤维二糖首先加氢的到3-β-D-吡喃葡萄糖基-D-山梨醇中间体,然后该中间体断裂β-1,4-糖苷键得到山梨醇[16-17]。杂多酸铯盐Cs3PW12O40在H2气氛下能氢溢流产生酸性[17]及CNTs的酸性功能团和表面上高浓度的吸附氢有均利于山梨醇和甘露醇的形成[18]。Ni也是催化该类反应的常用金属之一,以Ni/ZSM-5和Ni/CNFs(碳纳米纤维)催化剂得到的主产物是山梨醇和甘露醇。通过等体积浸渍法制备的Ni/ZSM-5(Si/Al=25)催化剂,其山梨醇和甘露醇的收率和选择性分别为48.6%、91.2%。运用TEM和XRD表征发现,此种方法制备的催化剂呈花瓣状,其花瓣上主要暴露Ni{111}晶面,该晶面加氢性能较好,同时抑制了C−C键断裂[19];Ni/CNFs催化剂中Ni粒子附着在CNFs的顶端,呈梨形的Ni粒子表面暴露较多{111}面[20]。Ni粒子暴露的高活性{111}晶面是其具有优异催化性能的原因。通过硝酸的氧化活化CNFs来改变酸性表面的氧基团数目,再通过等体积浸渍Ni,使Ni/CNFs的酸性位和金属位达到平衡,可以进一步提高山梨醇和甘露醇的收率[21]。除了使用单金属外,也有使用稳定性更高的双金属活性组分制取山梨醇和甘露醇的报道。例如,Ir-Ni/MC(MC为介孔碳)能重复使用4次,性能保持不改变,而不添加贵金属的Ni/MC催化剂只能重复使用两次。研究还发现,介孔碳比活性炭更有利于纤维素的水解及反应物的扩散,从而具有更优越的催化性能[22]。在过去几十年,过渡金属磷化物尤其是磷化镍在加氢脱氮和加氢脱硫反应中被广泛研究。对于Ni2P/AC催化剂,过量的P形成酸性位有利于纤维素的水解而Ni2P的金属位则有利于加氢。采用该类催化剂可使山梨醇的收率达48.4%[23]。进一步研究表明,随着温度的升高,Ni-P/AC催化剂中Ni-P的结构由晶型变成了无定型,而这种无定型结构导致了较高的山梨醇和甘露醇收率[24]。直接催化氢解纤维素制山梨醇和甘露醇的实验结果见表2。
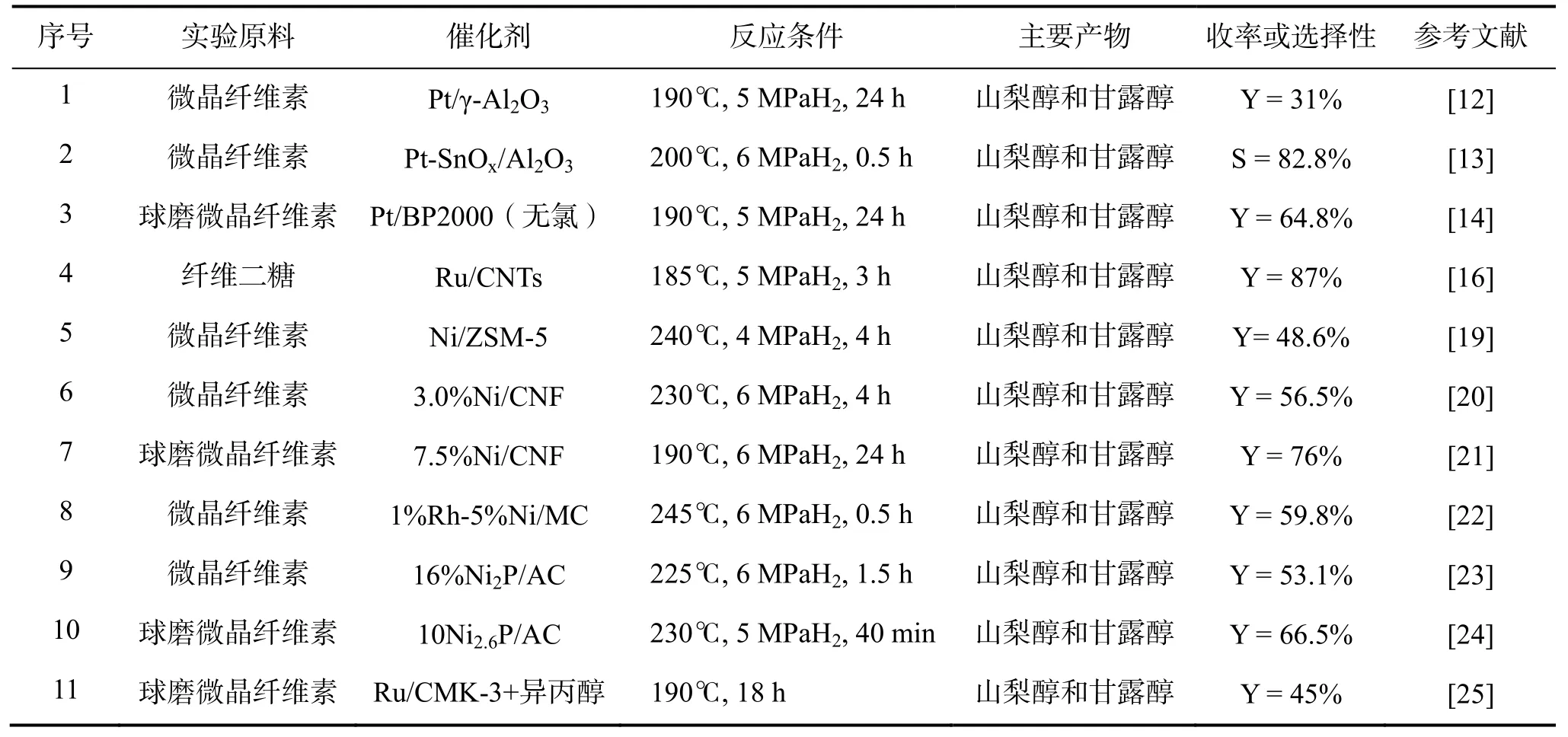
表2 直接催化氢解纤维素制山梨醇和甘露醇的实验结果Table 2 Sorbitol and mannitol production by hydrolytic hydrogenation of cellulose
除了使用外加氢源外,采用转移加氢和原位重整制氢/加氢方法也可以催化氢解纤维素制取山梨醇和甘露醇。有实验表明以异丙醇为氢源,发现只要在0.8 MPa时就可以得到山梨醇和甘露醇。通过XRD、H2-TPR和XPS研究发现,Ru在Ru/C中不是以零价金属形式存在,而是以阳离子形式存在,这是催化剂具有活性的原因[25]。其可能的反应路径如图1所示:异丙醇在金属中心脱氢为丙酮,同时产生的H2可作为氢源用于纤维素水解产物葡萄糖加氢得到山梨醇和甘露醇。

图1 H2转移氢解纤维素反应路径[38]Fig. 1 The hydrogenation transfer pathway in cellulose hydrogenolysis[38]
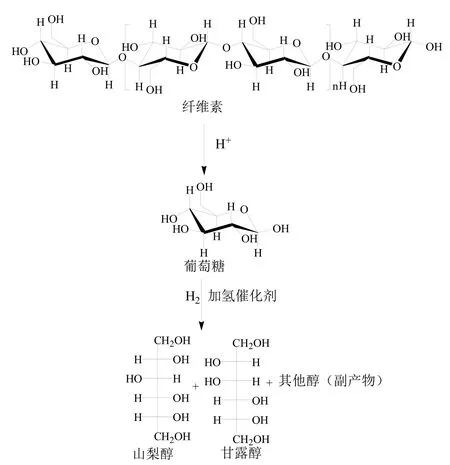
图2 纤维素制山梨醇和甘露醇的反应路径图Fig. 2 The reaction pathway in cellulose conversion to sorbitol and mannitol
1.2 反应路径
纤维素制山梨醇和甘露醇的反应路径如图2所示。溶液中的H+(来源于酸电离的H+、高温水和H2溢流)与水分子结合为H3O+,H3O+进攻纤维素分子中的β-1,4-糖苷键,从而诱使其断裂为葡萄糖,葡萄糖在加氢催化剂的作用下加氢得到山梨醇,其中少部分葡萄糖异构化为果糖,果糖加氢得到甘露醇。因此纤维素水解/加氢产物中往往为包括山梨醇和甘露醇在内的混合物,其中酸水解与金属加氢催化剂的匹配是获得高目标产物收率的关键。
2 纤维素制乙二醇和丙二醇
2.1 催化体系
由纤维素直接氢解制取包含乙二醇和丙二醇在内的小分子二元醇的反应步骤包括:纤维素的β-1,4糖苷键在酸性环境下断裂为葡萄糖,葡萄糖在氢气氛下和加氢/氢解催化剂上选择性断裂C−C键和C−O为最终产物,或者葡萄糖加氢为山梨醇,山梨醇再经氢解得到目标产物。V-IV族金属元素的碳化物在某些反应中具有类似铂族元素的性质,具有优异的加氢能力。ZHANG等首次报道采用W2C/AC(AC为活性炭)为催化剂氢解纤维素制取乙二醇,发现W2C活性相具有比贵金属铂、钌等更高的乙二醇收率。若在W2C中加入少量Ni,则能抑制W2C粒子的烧结,从而进一步提高催化剂的稳定性和乙二醇收率[29]。高分辨电子能量损失谱研究表明,乙二醇在2%Ni-30%W2C/AC催化剂表面较弱的键合作用可快速脱离催化剂表面,从而避免其继续反应,是其收率提高的主要原因[31]。如改变此催化剂的制备方法获得高度分散的负载型金属催化剂,则乙二醇的收率则可进一步提高[32]。在ZHANG的后续工作中研究了Ni-W2C/AC氢解菊芋[33]和木质纤维素[34-35]制取乙二醇和丙二醇。其中氢解菊芋时,其主要产物为1,2-丙二醇,收率达到38.5%)[33]。以不同预处理方法得到的玉米秸秆为原料进行氢解反应,发现木质素的存在阻碍了纤维素的降解,使得乙二醇和1,2-丙二醇的收率降低,而半纤维素可以直接降解为1,2-丙二醇和乙二醇,不影响纤维素的转化;另外纤维素的结晶度对乙二醇和1,2-丙二醇的收率似乎没有很大的影响[34]。直接氢解未经处理的木质纤维素时,其中的纤维素和半纤维素可降解为乙二醇和其他二元醇,总收率达到75.6%,木质素则选择性的降解为单酚,其收率为46.5%,如果使用小分子醇为溶剂可以获得更高的单酚收率[35]。Ni-W2C催化剂在纤维素和木质纤维素氢解制备小分子乙二醇和丙二醇中表现出来的优异催化性能被认为是由于Ni向W2C存在电子转移效应,该电子转移效应可协同催化反应物分在催化剂活性中心的吸附活化以及选择性断裂C-C键和C-O键,高收率得到目标产物。除了Ni-W2C外,Ni-WP和W-Pt(Pb、Ir)之间也存在类似的协同催化作用,在纤维素选择性氢解为小分子二元醇中表现了较好的活性和选择性[30,36]。虽然活性炭的比表面积较大,但它的微孔结构导致活性位分散性较差。相对于微孔结构的活性炭来说,介孔碳和SBA-15有利于分子的扩散和活性中心的分散,能提高催化剂活性和目标产物收率[36-37]。例如,在5%Ni-25%W/SBA-15催化剂中乙二醇收率达75.4%,为目前报道的最高值[36]。
由于碳化钨在水热条件下容易被氧化,使得Ni-W2C催化剂的稳定性较差。使用W的氧化态来代替W2C就可以避免这个问题。H2WO4在常温下不溶于水,当温度升高时开始溶于水,由黄色固体变成蓝色溶液,当温度降低的时候则以蓝色沉淀析出。XRD分析结果表明,蓝色沉淀是钨酸被氢气还原得到的HxWO3。如果将蓝色溶液暴露于空气中,溶液将慢慢变成无色,HxWO3被氧化成黄色沉淀H2WO4而析出。因此可利用具有相转移性质的钨酸和Ru/C为催化剂氢解纤维素制取小分子多元醇。经过优化催化剂用量、Ru的负载量等工艺参数,可以使得乙二醇的收率达到58.5%,且催化剂具有较好的稳定性,重复使用二十次未见明显失活[38]。此外还有使用WO3和Ru/C来氢解纤维素制小分子多元醇[39],同只用Ru/C的实验结果[14]相比较发现,高度分散的酸性WO3有利于纤维素的解聚,而晶态的WO3不仅有利于加速纤维素的水解,而且还能选择性断裂C−C键。关于纤维素制乙二醇和丙二醇的实验结果见表3。
此外,也有采用碱性载体ZnO、ZrO2、MgO等负载的金属Ni、Ni-Cu等为催化剂应用于纤维素氢解制小分子多元醇的报道[40-41]。例如,使用共沉淀法制备的20%Ni/ZnO,在优化条件下多元醇混合产物最高收率为70.4%。该催化剂的CO2-TPD分析结果表明,ZnO的碱性对纤维素的降解起了较大的促进作用。然而,碱性载体在水热环境通常不稳定,其水热稳定性还有待进一步改善,而且使用该类催化剂得到的产物均为小分子多元醇的混合物,对单一产物选择性还有待于进一步提高[40]。纤维素在碱性条件下水解可以得到葡萄糖,因此在碱性溶液中用负载的Ru催化剂也可以氢解纤维素制取多元醇,在这个体系下主要产物是乙二醇,1,2-丙二醇,1,2,5-戊三醇。纤维素的转化率和产物的分布受溶液的pH值和催化剂载体的影响[42]。碱性环境下纤维素转化的路径与酸性环境下的路径有所不同,其解聚有两种可能的途径(图3):(1)纤维素在碱的作用下首先解聚得到葡萄糖,葡萄糖选择性断裂C-C键然后经加氢得到C2和C3多元醇;(2)β-羟基羰基消去反应,这个反应从纤维素结构单元末端的还原性基团开始,一直到没有还原性基团时结束,这种途径能得到1,2,5-戊三醇。其大致的反应路径如图4所示。另外,还有在Al2O3中掺杂Si制备SiO2-Al2O3载体,通过改变载体的硅铝比来调变载体的酸性强弱,从而改善其催化性能。例如,在Ni/W/SiO2-Al2O3催化剂中,随着硅铝比的增加催化剂表面酸性位数目先增多后下降,催化剂载体的酸性越强,乙二醇的收率越高[43]。载体酸性质在纤维素氢解制小分子多元醇中的这种调控作用在Pt/Na-HZSM-5催化剂中也存在[44]。

表3 纤维素制乙二醇和丙二醇的实验结果Table 3 Ethylene glycol and propanediol production by cellulose hydrogenolysis

图3 碱性条件下纤维素氢解制取多元醇的可能反应途径[42]Fig. 3 The possible pathway for cellulose conversion to diols under base conditions[42]
2.2 反应路径
目前报道的纤维素高选择性和高收率制取乙二醇和丙二醇的催化剂体系均与W元素有关,而所有钨基催化剂在水热环境下都会形成HxWO3,HxWO3对断裂C−C键存在一定的促进作用,所以所有钨基催化剂的反应机理类似。目前对于这个机理尚不完全清楚,其反应的大致路径如图4所示。研究发现,以山梨醇为原料直接氢解往往得不到乙二醇和丙二醇;而当以葡萄糖为原料时,主要得到乙二醇,以果糖为原料则主要得到丙二醇。由此可以推断,葡 萄糖和果糖分别是乙二醇和丙二醇的前驱体。从糖的转化可以看出,C−C的断裂主要发生在羰基的β位置。从C5糖的转化也可以证明这一点,因为在相同的转化条件下得到等摩尔数的乙二醇和C3醇。但是如果以2-脱氧葡萄糖和2-脱氧核糖为原料时就否认这个断键模式,按上述这个模式应该得到乙二醇、乙醇和丙二醇,实际得到的却是2-脱氧山梨醇和 2-脱氧核糖醇,并没有C−C断裂的物质出现。综合以上结果可以推断,C6糖羰基的α-OH对C−C键的断裂也是必须的[39]。

图4 钨基催化剂氢解纤维素的反应路径图[39]Fig. 4 The possible reaction pathway for cellulose hydrogenolysis over tungsten based catalyst
3 纤维素制异山梨醇
3.1 催化体系
异山梨醇是山梨醇在H+的作用下,其分子内脱掉两分子水而形成的对称双环化合物,因此由纤维素制异山梨醇的催化体系与制山梨醇和甘露醇相似,反应步骤包含纤维素水解为葡萄糖,葡萄糖加氢为山梨醇,以及山梨醇脱水为异山梨醇。以水为反应介质,使用无机酸(盐酸和硫酸)和Ru/C为催化剂,在205℃、氢气压力6 Mpa、反应0.5 h的条件下,异山梨醇收率为50%[26]。而用H4SiW12O40和Ru/C为催化剂,在210℃、氢气压力5 Mpa、反应1 h下,异山梨醇收率则提高到52%,为目前报道的直接由纤维素制取异山梨醇的最高收率[27]。除了水作为反应介质外,还有以高浓度的ZnCl2溶液为反应介质,使用HCl和Ru/C为催化剂制取异山梨醇的文献报道[28]。
3.2 反应路径
由纤维素制异山梨醇的反应路径如图5所示。纤维素先水解、加氢到山梨醇,然后山梨醇在H+的作用下首先脱去一分子水得到1,4-失水山梨醇或者3,6-失水山梨醇,1,4-失水山梨醇和3,6-失水山梨醇在H+的作用下继续脱去第二分子水得到异山梨醇。纤维素水解−加氢−脱水转化中酸与金属催化剂的匹配是影响异山梨醇收率的主要因素。比较而言,采用酸性较强的矿物酸以显著提高纤维素的水解效率对提高异山梨醇的收率有利。

图5 纤维素制取异山梨醇的反应路径Fig. 5 The route for isosorbide production from cellulose
4 总结与展望
鉴于可再生的生物质资源转化利用的显著意义和多元醇的广泛应用性,近十几年来,研究人员对纤维素催化氢解制取多元醇的催化剂体系和反应途径等方面进行了不懈探索,已经取得了一些进展。例如,基于多年来催化剂和反应机理的研究积累,中科院大连化物所张涛课题组已将纤维素氢解制乙二醇工作由实验室研究推进到中试阶段。但纤维氢解制多元醇也存在反应温度高和单一产物选择性较差(往往只得到多元醇混合物)等问题,而且现有的催化剂体系中碱性载体水热稳定性较差,导致催化剂失活严重,或者添加的对环境不友好的液体酸导致腐蚀设备和环境污染。为了克服目前的困难,在今后的研究中应根据氢解反应的特点,控制催化剂的组成与结构,设计制备高效稳定的催化新体系,从而高效获得多元醇目的产物。导致目标产物选择性不高的另一原因是对氢解反应机理与转化途径认识较为肤浅,因此加强该类反应的机理研究可为提高单一目标产物选择性提供依据。另外采用纤维素预处理新技术,显著降低其结晶性以增加反应的可及性,从而提高反应效率,也是未来研究的重点。
[1] Statistical Review of World Energy[EB/OL]. BP, 2008.
[2] INDERWILDI O, KING D. Quo vadis biofuels?[J].Energy Environmental Science, 2009, 2: 343-346.
[3] 沈宜泓, 王帅, 罗琛, 等. 生物质利用新途径: 多元醇催化合成可再生燃料和化学品[J]. 化学进展, 2007, 19( 2/3): 431-436.
[4] RUPPERT A M, WEINBERG K, PALKOVITS R.Hydrogenolysis goes bio: from carbohydrates and sugar alcohols to platform chemicals[J]. Angewandte Chemie- International Edition, 2012, 51(11): 2564-2601.
[5] ROSE M, PALKOVITS R. Isosorbide as a renewable platform chemical for versatile applications--quo vadis?[J]. Chemsuschem, 2012, 5(1): 167-176.
[6] REGINA P, KAMEH T, JOANNA P, et al. Hydrogenolysis of cellulose combining mineral acids and hydrogenation catalysts[J]. Green Chemistry, 2010, 12: 972-978.
[7] PALKOVITS R, TAJVIDI K, RUPPERT A, et al. Heteropoly acids as efficient acid catalysts in the one-step conversion of cellulose to sugar alcohols[J]. Chemical Communications, 2011, 47(1): 576-578.
[8] GEBOERS J, VAN DE VYVER S, et al. Efficient catalytic conversion of concentrated cellulose feeds to hexitols with heteropoly acids and Ru on carbon[J]. Chemical Communications, 2010, 46(20): 3577-3579.
[9] JAN G, VAN DE VYVER S, CARPENTIER K, et al. Hydrolytic hydrogenation of cellulose with hydrotreated caesium salts of heteropoly acids and Ru/C[J]. Green Chemistry, 2011, 13: 2167-2174.
[10] HILGERT J, MEINE N, RINALDI R, et al. Mechanocatalytic depolymerization of cellulose combined with hydrogenolysis as a highly efficient pathway to sugar alcohols[J]. Energy & Environmental Science, 2013, 6(1): 92-96.
[11] LUO C, WANG S A, LIU H C. Cellulose conversion into polyols catalyzed by reversibly formed acids and supported ruthenium clusters in hot water[J]. Angewandte Chemie-International Edition, 2007, 46(40): 7636-7639.
[12] FUKUOKA A, DHEPE P L. Catalytic conversion of cellulose into sugar alcohols[J]. Angewandte Chemie- International Edition, 2006, 45(31): 5285-5287.
[13] DENG T, LIU H. Promoting effect of SnOxon selective conversion of cellulose to polyols over bimetallic Pt–SnOx/Al2O3catalysts[J]. Green Chemistry, 2013, 15(1): 116-124.
[14] HIROKAZU K, YUKIKO I, TASUKU K, et al. Synthesis of sugar alcohols by hydrolytic hydrogenation of cellulose over supported metal catalysts[J]. Green Chemistry, 2011, 13: 326-333.
[15] YAN N, ZHAO C, LUO C, et al. One-step conversion of cellobiose to C6-alcohols using a ruthenium nanocluster catalyst[J]. Journal of the American Chemical Society, 2006, 128: 8714-8715.
[16] DENG W P, LIU M, TAN X S, et al. Conversion of cellobiose into sorbitol in neutral water medium over carbon nanotube-supported ruthenium catalysts[J]. Journal of Catalysis, 2010, 271(1): 22-32.
[17] LIU M, DENG W, ZHANG Q, et al. Polyoxometalate- supported ruthenium nanoparticles as bifunctional heterogeneous catalysts for the conversions of cellobiose and cellulose into sorbitol under mild conditions[J]. Chemical Communications, 2011, 47: 9717-9719.
[18] DENG W P, TAN X S, FANG W H, et al. Conversion of Cellulose into Sorbitol over Carbon Nanotube-Supported Ruthenium Catalyst[J]. Catalysis Letters, 2009, 133(1/2): 167-174.
[19] LIANG G F, CHENG H Y, LI W, et al. Selective conversion of microcrystalline cellulose into hexitols on nickel particles encapsulated within ZSM-5 zeolite[J]. Green Chemistry, 2012, 14: 2146-2149.
[20] VAN DE VYVER S, GEBOERS J, DUSSELIER M, et al. Selective Bifunctional Catalytic Conversion of Cellulose over Reshaped Ni Particles at the Tip of Carbon Nanofibers[J]. Chemsuschem, 2010, 3(6): 698-701.
[21] VAN DE VYVER S, GEBOERS J, SCHUTYSER W, et al. Tuning the acid/metal balance of carbon nanofiber- supported nickel catalysts for hydrolytic hydrogenation of cellulose[J]. Chemsuschem, 2012, 5(8): 1549-1558.
[22] PANG J F, WANG A Q, ZHENG M Y, et al. Catalytic conversion of cellulose to hexitols with mesoporous carbon supported Ni-based bimetallic catalysts[J]. Green Chemistry, 2012, 14: 614-617.
[23] LI N, WANG A Q, ZHENG M Y, et al. Selective Transformation of Cellulose into Sorbitol by Using a Bifunctional Nickel Phosphide Catalyst[J]. Chemsuschem, 2010, 3: 818-821.
[24] YANG P F, KOBAYASHI H, HARA K, et al. Phase Change of Nickel Phosphide Catalysts in the Conversion of Cellulose into Sorbitol[J]. Chemsuschem, 2012, 5(5): 920-926.
[25] HIROKAZU K, YUKIKO I, TASUKU K, et al. Transfer hydrogenation of cellulose to sugar alcohols over supported ruthenium catalysts[J]. Chemical Communications, 2011, 47: 2366-2368.
[26] LIANG G, WU C, HE L, et al. Selective conversion of concentrated microcrystalline cellulose to isosorbide over Ru/C catalyst[J]. Green Chemistry, 2011, 13(4): 839-842.
[27] OP DE BEECK B, GEBOERS J, VAN DE VYVER S, et al. Conversion of (ligno)cellulose feeds to isosorbide with heteropoly acids and Ru on carbon[J]. Chemsuschem, 2013, 6(1): 199-208.
[28] DE ALMEIDA R M, LI J, NEDERLOF C, et al. Cellulose Conversion to Isosorbide in Molten Salt hydrate Media[J]. Chemsuschem, 2010, 3: 325-328.
[29] JI N, ZHANG T, ZHENG M Y, et al. Direct Catalytic Conversion of Cellulose into Ethylene Glycol Using Nickel-Promoted Tungsten Carbide Catalysts[J]. Angewandte Chemie-International Edition, 2008, 47(44): 8510-8513.
[30] ZHAO G H, ZHENG M Y, WANG A Q, et al. Catalytic Conversion of Cellulose to Ethylene Glycol over Tungsten Phosphide Catalysts[J]. Chinese Journal of Catalysis, 2010, 31(8): 928-932.
[31] JI N, ZHANG T, ZHENG M Y, et al. Catalytic conversion of cellulose into ethylene glycol over supported carbide catalysts[J]. Catalysis Today, 2009, 147(2): 77-85.
[32] JI N, ZHENG M Y, WANG A Q, et al. Nickel-Promoted Tungsten Carbide Catalysts for Cellulose Conversion: Effect of Preparation Methods[J]. Chemsuschem, 2012, 5(5): 939-944.
[33] ZHOU L K, WANG A Q, LI C Z, et al. Selective Production of 1,2-Propylene Glycol from Jerusalem Artichoke Tuber using Ni-W2C/AC Catalysts[J]. Chemsuschem, 2012, 5(5): 932-938.
[34] PANG J F, ZHENG M Y, WANG A Q, et al. Catalytic Hydrogenation of Corn Stalk to Ethylene Glycol and1,2-Propylene Glycol[J]. Industrial& Engineering Chemistry Research, 2011, 50(11): 6601-6608.
[35] LI C Z, ZHENG M Y, WANG A Q, et al. One-pot catalytic hydrocracking of raw woody biomass into chemicals over supported carbide catalysts: simultaneous conversion of cellulose,hemicellulose and lignin[J]. Energy & Environmental Science, 2012, 5(4): 6383-6390.
[36] ZHANG M Y, WANG A Q, JI N, et al. Metal Tungsten Bimetallic Catalysts for the Conversion of Cellulose into Ethylene Glycol[J]. Chemical Communications, 2010, 3: 63-66.
[37] ZHANG Y H, WANG A Q, ZHANG T. A new 3D mesoporous carbon replicated from commercial silica as a catalyst support for direct conversion of cellulose into ethylene glycol[J]. Chemical Communications, 2010, 46(6): 862-864.
[38] TAI Z J, ZHANG J Y, WANG A Q, et al. Temperature- controlled phase-transfer catalysis for ethylene glycol production from cellulose[J]. Chemical Communications, 2012, 48(56): 7052-7054.
[39] LIU Y, LUO C, LIU H C. Tungsten Trioxide Promoted Selective Conversion of Cellulose into Propylene Glycol and Ethylene Glycol on a Ruthenium Catalyst[J]. Angewandte Chemie-International Edition, 2012, 51(13): 3249-3253.
[40] WANG X C, MENG L Q, WU F, et al. Efficient conversion of microcrystalline cellulose to 1,2-alkanediols over supported Ni catalysts[J]. Green Chemistry, 2012a,14(3): 758-765.
[41] WANG X C, WU F, YAO S X, et al. Ni-Cu/ZnO-catalyzed Hydrogenolysis of Cellulose for the Production of 1,2-Alkanediols in Hot Compressed Water[J]. Chemistry Letters, 2012b, 41(5): 476-478.
[42] DENG T, SUN J, LIU H. Cellulose conversion to polyols on supported Ru catalysts in aqueous basic solution[J]. Science China Chemistry, 2010, 53(7): 1476-1480.
[43] BAEK I G, SU J Y, PARK E D. Direct conversion of cellulose into polyols over Ni/W/SiO2-Al2O3[J]. Bioresource Technology, 2012, 114: 684-690.
[44] SU J Y, BAEK I G, Kim Y T, et al. Direct conversion of cellulose into polyols or H2over Pt/Na(H)-ZSM-5[J]. Korean J. Chem. Eng., 2011, 228(3): 744-750.
Advances in Polyols Production by Catalytic Hydrogenolysis of Cellulose
LIU Qi-ying1, LIAO Yu-he1,2, XU Ying1, WANG Tie-jun1, ZHANG Qi1, MA Long-long1
(1. CAS Key Laboratory of Renewable Energy, Guangzhou Institute of Energy Conversion, Chinese Academy of Sciences, Guangzhou 510640, China; 2. University of Chinese Academy of Sciences, Beijing 100049, China)
Due to climate and environment problems posed by use of fossil resources, developing advanced technologies for sustainable production of value added chemicals from renewable biomass is of scientific and practical importance. Among those, polyols production from cellulose by catalytic hydrogenolysis has attracted more and more attention during the last decade. In this review, we summarized the state-of-art technologies in such area with the aims to the products of sorbitol/mannitol, isosorbide and small molecular polyols (ethylene glycol and propylene glycol), the employed catalysts and the possible reaction pathways. Finally, we analyzed the present problems and the possible trends in the future.
cellulose; catalytic hydrogenolysis; polyol; reaction pathway
TK6;TQ211
A
10.3969/j.issn.2095-560X.2015.06.001
2095-560X(2015)06-0405-010
刘琪英(1975-),男,博士,副研究员,主要从事生物质催化转化为燃料和化学品研究。
2015-09-28
2015-10-19
国家自然科学基金(51376185);国家重点基础研究发展计划(国家973 计划,2012CB215304);国家高技术研究发展计划(863计划,2012AA101806);广东省自然科学基金(S2013010011612)
† 通信作者:马隆龙,E-mail:mall@ms.giec.ac.cn
马隆龙(1964-),男,博士,研究员,主要从事生物质高值化转化利用研究。
