纳米石墨颗粒对气体水合物生成诱导时间的影响
2015-06-01周诗岽余益松甘作全王树立
周诗岽,余益松,甘作全,张 锦,王 密,徐 涛,王树立,李 辉
(1.常州大学油气储运技术省重点实验室,江苏 常州 213016;2.苏州苏净保护气氛有限公司,江苏 苏州 215122)
纳米石墨颗粒对气体水合物生成诱导时间的影响
周诗岽1,余益松1,甘作全1,张 锦1,王 密1,徐 涛1,王树立1,李 辉2
(1.常州大学油气储运技术省重点实验室,江苏 常州 213016;2.苏州苏净保护气氛有限公司,江苏 苏州 215122)
分析和比较了纯水及浓度为0.4%的纳米石墨悬浮液体系中的CO2水合物生成过程。采用观察法测定了二种溶液体系在不同温度和压力条件下的水合物生成诱导时间,并研究了其随温度、压力的变化规律。结果表明,纳米石墨颗粒的引入能够加快体系的传热效率及成核速率,较大程度减少水合物生成的诱导时间,同等条件下,相较于纯水体系诱导时间平均下降了80.6%。此外,二种体系中水合物生成的诱导时间随着温度及压力的升高均分别呈增大和减少的趋势。然而,纳米石墨悬浮液体系中的水合物生成诱导时间受温压的变化影响较小。因此,纳米颗粒能够加速水合物的成核过程,且鉴于其巨大的比表面对传质过程的影响,实验结果也从侧面证明了水合物的成核速率主要受气液传质过程控制的结论。
气体水合物;二氧化碳;纳米石墨;诱导时间;成核;温度;压力;传质;控制
水合物是一种由水分子与气体分子在一定的温度和压力条件下相互结合而形成的一种非化学计量的笼形络合物[1]。当前,基于水合物的理化性质而开发出了包括天然气水合物储运技术[2]、海水淡化技术[3],二氧化碳封存与捕集技术[4]等在内的一系列应用技术。这些技术在各自领域都具有很好发展前景,如分离后的CO2不仅能够提供大量的气驱原料用于提高大型油气田以及煤层气等的采收率,而且能够实现气体的循环利用等。然而,由于水合物具有生成时间长、效率低、条件苛刻等缺点。如何高效快速的生成水合物是这些技术大规模工业化应用亟需解决的难题。
水合物的生成过程实质上是一个传热传质控制的过程。基于此,当前用于加快水合物生成的方法主要有以下三种[5]:
(1)装置本体的设计:其主要设计方向是增加换热面积,如日本开发出的盘管式水合物合成装置等,但所取得的效果并不理想。
(2)机械强化方式:包括搅拌、鼓泡、喷淋等促进气液传质过程的一系列强化方式。这种方式对水合物的生成促进作用明显,但存在着一个非常大的缺点:需要外力作驱动,运行成本高。
(3)化学强化:该强化方式的原理主要是通过添加表面活性剂来降低气液界面的表面张力,以使得气体分子更容易被捕获。从目前的研究结果来看,这种方法是解决水合物技术工业化应用甁颈的最有效手段。然而,一种高效促进剂的开发是这种方法必须解决的难题。纳米流体是20世纪末提出的一种高传热传质工质[6],Li[7]首次提出采用纳米流体促进水合物的生成的设想并进行了相关的研究,此外李娜等[8]在此基础上进行了相关拓展。但由于二者所选的纳米颗粒市场价格昂贵,且均为金属或其氧化物,容易引起化学反应,不利于水合物的大规模工业化应用。石墨的理化性能稳定,采用纳米石墨粉作为此次研究的材料能够很好的避免这些缺点。鉴于高纯度甲烷气体的价格昂贵,通过研究石墨纳米流体对CO2水合物生成诱导时间的影响来反映其强化效果是研究的主要目的。
1 实验部分
1.1 实验装置
水合物生成实验所采用的装置流程如图1所示,其主要由进气系统、进液系统、光线摄像系统、制冷系统以及数字数据采集系统五部分组成。前二者主要为水合物反应提供物料支持,光纤摄像系统主要用于观察水合物的生成过程,制冷系统主要用于控制水合物反应的温度,数据采集系统能够实时地将水合物反应过程中釜内的温压数据记录下来,并存储在计算机当中,用于分析。反应釜的形状为球形,设计压力和容积分别为30MPa和500mL,并采用磁力搅拌器进行搅拌,有效工作温度为 0~15℃;循环槽制冷器是由宁波天宇仪器厂生产,型号为 THD-2030型,温度控制范围为 258.15K~268.15K,精度设置±0.01K;进气过程的增压过程采用先进的气驱气的增压方式。测温元件为Pt100铂电阻,测量范围为253.15K~293.15K,控制精度为± 0.1K;压力传感器的量程为0~10MPa,控制精度为± 5%。
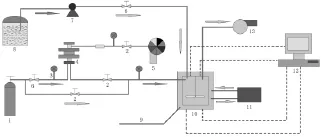
图1 水合物生成装置流程图
1.2 实验材料
蒸馏水,实验室自制,经检测各项指标均符合要求;纳米石墨颗粒,w=99.9%,平均细度50nm,江苏徐州捷创新材料科技有限公司;CO2气体,φ= 99.8%,江苏常州京华工业气体有限公司;电子天平,型号FA2104B,标准偏差±0.0002g,上海越平科学仪器有限公司。
1.3 实验步骤
首先用电子天平秤取一定量的纳米石墨颗粒,并与蒸馏水以一定的比例配制成w为0.4%的纳米颗粒悬浮液;在确定装置的气密性之后,将反应釜用蒸馏水清洗3次,后向反应釜中注入200mL的目标溶液;进液完成后,打开真空泵,以排除釜内的“杂质”气体。在打开真空泵的同时开启制冷系统,将釜内的温度控制在所设定的温度;上述步骤完成后,通过气体压缩机和增压泵向釜内缓慢注入CO2气体,直至釜内压力达到设定值。进气结束后,开启釜内磁力搅拌器,并将转速控制在300r/min,进行水合物的生成实验。实验过程中通过光纤摄像系统和数据采集系统实时观察水合物的生成情况和记录釜内的温压数据。
2 结果与讨论
水合物生成的诱导时间是表征水合物生成快慢的一个重要参数,当前对水合物生成诱导时间的定义主要有2种[9-10]:①系统由初始平衡状态到晶体成核阶段结束所需要的时间;②系统由初始平衡状态到可视晶体阶段这一过程所需要的时间。二者的定义在本质上是一致的,只是落脚点不同。在本文研究中,诱导时间采用第二种定义。由于水合物在生成过程中形成具有临界尺寸的晶核到可见晶体出现的时间非常短,因此,实验通过在同一温压条件下3次观察可视晶体出现的时间,并取其平均值作为这一条件下水合物生成的诱导时间。所得的结果与实验系统中的温压参数出现相对应的急剧升高和降低的时间与系统初始稳定状态的时间差进行相互印证。
2.1 纳米石墨颗粒对水合物生成的影响
石墨纳米颗粒作为一种添加剂用于促进水合物的生成,其与SDS、SDBS、APG等[11-13]促进剂对水合物的促进原理不同。后者主要从改变水合物生成液的表面张力来提高气液间的传质效率促进水合物的生成,其选用的出发点来自于气液间反应的传质控制过程,而对石墨纳米颗粒促进水合物生成的研究,则更加倾向于从水合物生成的传热及传质二个控制过程来研究。
图2和图3分别为水合物在277.15K、3.5MPa的设定条件下,200min内纯水以及纳米石墨悬浮液中水合物生成的温压变化曲线。可以看出,二种体系内水合物的生成过程中,温度和压力随着时间的推移,宏观上呈整体下降趋势。这主要是由于进气过程结束后,体系的温度有所升高,而随着时间的推移,在制冷循环系统的作用下温度逐渐降低;然而,对于纯水体系中水合物的生成,温度由初始的277.75K在经过200min后下降为277.22K,同等情况下的纳米石墨悬浮液体系中,温度在50min后便下降为277.15K,达到设定温度。因此,纳米石墨颗粒的存在能够极大地强化体系的传热过程。这主要是因为固体材料的导热系数相较于液体要大2个数量级左右。它的引入能够极大地增强水合物反应液体系的综合导热系数。使得体系内的热量能够及时地移除。此外,图2的温降曲线表明,在保持整体下降的趋势下,水合物生成体系的温降幅度在35min左右开始减缓,40min左右开始看到明显的局部上升趋势。而在图3中这种趋势并不明显,只在最初的 5min左右可以看见一个高点。这与Arjang[14]、Mohammadi等[15]在纳米银离子悬浮液体系中进行水合物生成实验所得的温降曲线相比,升高幅度较小。这主要是由于水合物反应是一个放热反应,体系在经过一定的诱导时间后开始进入大量生成的阶段,从而导致单位时间内所放出的热量增加,体系温度上升,而反应釜内的搅拌使得水合物生成过程中所放出的热量能够及时地被制冷循环系统所带走,且纳米石墨本身所具有的导热强化特性,使得这种趋势更加不明显。

图2 纯水中水合物生成的温压曲线

图3 纳米石墨悬浮液中水合物生成的温压曲线
水合物生成过程的压降变化是衡量水合物生成速率的重要参数。图2中的压降曲线表明,水合物在纯水体系中生成时,压力宏观上呈下降趋势,200min后釜内的压力为2.09MPa,且在40min左右时,压力有一个突然增大的趋势,这与局部的温升时间大体相同。这一现象与我们通过观察法所得出的诱导时间相近,这进一步表明出现这一现象的原因是由于诱导期结束后水合物晶核大量生成的缘故。而图3曲线表明,纳米石墨颗粒存在的情况下,水合物生成系统内的压力在 200min后降为1.82MPa,其压降相较于纯水有了大幅度的降低,但未观察到压力的局部增大趋势。这主要是由于水合物在纳米石墨悬浮液体系中的诱导时间非常短,容易受“初始端部效应”影响的缘故。
因此,得益于纳米石墨颗粒本身所具有的良好的导热特性,水合物生成体系的传热效率以及水合物的生成速率都大大提高,水合物的成核过程也更加容易。
2.2 压力对诱导时间的影响

图4 诱导时间随压力的变化曲线

图5 3.5MPa、277.15K下水合物生成过程
实验通过直接观察法测定了277.15K时纯水和纳米石墨悬浮液在不同压力(2.5MPa,3.5MPa,4.5MPa,5.5MPa和6.5MPa)下水合物生成的诱导时间,结果如图4所示。相较于纯水,纳米石墨悬浮液中水合物生成的诱导时间有了大幅度的降低。如4.5MPa时,水合物的生成诱导时间在纯水中为32min,而在纳米悬浮液体系中为6.1min,下降幅度达80.9%。计算结果表明:在这5种压力条件下,由于纳米石墨颗粒的作用而造成的诱导时间平均下降幅度为80.6%。这主要是由于一方面石墨纳米颗粒具有巨大的比表面积,能够为气液反应提供更大的接触面积,使得传质效率大幅度提高,晶体成核速率加快。另一方面,晶体的成核分为同相成核和异相成核二种,相较于同相成核,异相成核对于体系的过饱和度及过冷度的要求大大降低,纳米石墨颗粒的引入提供了异相成核的环境要求,使得水合物成核过程更加容易进行。此外,纳米石墨颗粒的引入能够极大地强化体系的传热效率,使得水合物生成过程中的反应热能够及时移除,体系内部的温度也更加均匀等也导致了纳米石墨悬浮液体系中水合物生成诱导时间的减少。图4表明二种体系中的水合物生成诱导时间随着压力的升高都呈下降趋势,且纯水体系中的下降幅度随压力的变化较大。这从侧面说明了水合物的生成主要受传质过程控制的结论。图5为3.5MPa、277.15K时的水合物生成过程变化图,ti为水合物生成的诱导时间。晶体从大量成核到可见的时间非常短,一般在1min之内就能够完成。因此,通过观察可视晶体来确定水合物生成的诱导时间能够满足一般的工程要求。测定过程中一般采用取3次平均值作为所测条件下的诱导时间来减少实验误差。
2.3 温度对诱导时间的影响
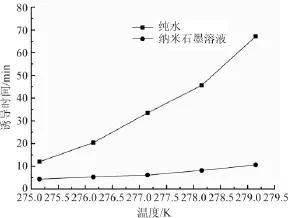
图6 诱导时间随温度的变化曲线
实验测定了 4.5MPa,不同温度(275.15K,276.15K,277.15K,278.15K和279.15K)条件下二种体系中的水合物生成诱导时间,结果如图6所示。可以看出,随着温度的升高,水合物的生成诱导时间越长,且其对温度的响应也越来越敏感。纯水中的水合物诱导时间由275.15K时的12min增加到279.15K时的67.2min,而纳米石墨悬浮液中水合物生成的诱导时间则由4.3min增加到10.6min,这是由于水合物成核过程中的驱动力—过冷度随着温度的升高而减小,进而导致其成核速率的降低,延长了诱导时间。此外,从图6中可以看出,纯水中水合物生成的诱导时间随着温度的升高而增大的幅度比纳米悬浮液中水合物生成诱导时间的变化幅度要大得多,且随着温度的升高,二种水合物生成体系中诱导时间的绝对差值也越来越大。这主要得益于纳米石墨颗粒对水合物成核的综合促进作用,其使得温度对水合物成核的影响力减弱。纳米石墨颗粒巨大的比表面积在气液界面传质过程中的影响,从另一面证明了水合物的成核速率主要受气液间传质过程控制的结论。
3 结论
通过研究不同温度及压力条件下,w为0.4%的纳米石墨悬浮液体系中CO2水合物生成过程,重点考察了纳米石墨颗粒对水合物生成诱导时间的影响,并分析了其相关的影响因素及机理。得到如下结论:
(1)纳米石墨颗粒的存在能够加快体系的传热效率及成核速率,减少水合物生成时间。
(2)水合物生成的诱导时间随着压力的升高而减小,且受压力的影响小。所引入的纳米石墨颗粒使得所测条件下水合物生成的诱导时间相较于纯水平均下降了80.6%。
(3)二种体系中水合物生成的诱导时间都随温度的升高而增高,且纳米石墨悬浮液对温度的“适应性”要好得多。这也从侧面验证了水合物的成核速率主要受气液传质过程控制的结论。
(4)纳米石墨颗粒能够减少水合物生成的诱导时间,加快晶体的成核速率主要得益于三方面的原因:①石墨纳米颗粒具有巨大的比表面积,能够为气液反应提供更大的接触面积,使得传质效率大幅度提高;②晶体的成核分为二种,同相成核和异相成核,相较于同相成核,异相成核对于体系的过饱和度及过冷度的要求大大降低,纳米石墨颗粒的引入提供了异相成核的环境要求,使得水合物成核过程更加容易进行;③纳米石墨颗粒的引入能够极大地强化体系的传热效率,使得水合物生成过程中的反应热能够及时移除,体系内部的温度也更加均匀。
总之,纳米石墨颗粒的引入能够极大地强化CO2水合物的生成过程。有理由认为,其对甲烷水合物的生成强化研究也具有重要的指导作用。相关的研究有待进一步开展。
[1]周诗岽,余益松,王树立,等.管道流动体系下天然气水合物生成模型的研究现状与进展[J].天然气工业,2014,34 (2):92-98.
[2]Javanmardi J,Nasrifar K,Najibi S H,et al.Economic evaluation of natural gas hydrate as an alternative for natural gas transportation[J].Appl Therm Eng,2005,25 (11-12):1708-1723.
[3]Khawaji A D,Kutubkhanah I K,Wie J M.Advances in seawaterdesalination technologies [J].Desalination, 2008,221(1-3):47-69.
[4]Li X S,Zhan H,Xu C G,et al.Effects of tetrabutyl-(ammonium/phosphonium)salts on clathrate hydrate capture of CO2from simulated flue gas[J].Energy Fuels, 2012,26(4):2518-2527.
[5]周诗岽,余益松,赵苗苗,等.管道流动体系下气体水合物促进技术研究进展 [J].天然气化工 (C1化学与化工), 2014,39(1):34-41.
[6]Khaleduzzaman S S,Mahbubul I M,Shahrul I M,et al. Effect of particle concentration, temperature and surfactant on surface tension of nanofluids[J].Int Commun Heat Mass,2013,49:110-114.
[7]Li J P,Liang D Q,Guo K H.Formation and dissociation of HFC134a gas hydrate in nano-copper suspension[J]. Energy Conv Manage,2006,47(2):201-210.
[8]李娜,马振魁.利用纳米粒子强化微乳液体系HCFC141b水合物的生成[J].科学通报,2011,56(22):1846-1853.
[9]Kashchiev D,Firoozabadi A.Driving force for crystallization of gas hydrates[J].J Cryst Growth,2002,241(2):220-230.
[10]Kashchiev D,Firoozabadi A.Nucleation of gas hydrates [J].J Cryst Growth,2002,243(7):476-489.
[11]Lirio C F S,Pessoa F L P,Uller A M C.Storage capacity of carbon dioxide hydrates in the presence of sodium dodecyl sulfate(SDS)and tetrahydrofuran(THF)[J].Chem Eng Sci,2013,96:118-123.
[12]Fazlali A,Kazemi S A,Keshavarz M M,et al.Impact of differentsurfactantsand theirmixtureson methane hydrate formation[J].Energy Technol,2013,1:471-477.
[13]Karimi R,Varaminian F,Izadpanah A A,et al.Effects of different surfactants on ethane hydrate formation kinetics: Experimental and modeling studies[J].Energy Technol, 2013,1/9:530-536.
[14]Arjang S,Manteghian M,Mohammadi A.Effect of synthesized silver nanoparticles in promoting methane hydrate formation at 4.7 MPa and 5.7 MPa[J].Chem Eng Res Des,2013,91(6):1050-1045.
[15]Mohammadi A,Manteghian M,Haghtalab A,et al.Kinetic study of carbon dioxide hydrate formation in presence of silver nanoparticles and SDS[J].Chem Eng J,2014,237: 387-395.
Effect of graphite nanoparticles on induction time of gas hydrate formation
ZHOU Shi-dong1,YU Yi-song1,GAN Zuo-quan1,ZHANG Jin1,WANG Mi1,XU Tao1,WANG Shu-li1,LI Hui2
(1.Jiangsu Key Laboratory of Oil and Gas Storage and Transportation Technology,Changzhou University,Changzhou 213016,China; 2.Suzhou Sujing Protective Atmosphere Co.,Ltd.,Suzhou 215122,China)
The processes of CO2hydrate formation in the pure water and the aqueous suspension containing graphite nanoparticles of 0.4%by mass were studied experimentally.The induction times of hydrate formation which occurred in two kinds of solution under different conditions of temperature and pressure were determined by observational method,and the rules of temperature and pressure affecting the induction time were investigated.The result showed that in presence of graphite nanoparticles, the efficiency of heat transfer and the rate of nucleation increased,and the induction time of hydrate formation decreased sharply by an average of 80.6%.In addition,the induction time of hydrate formation increased with temperature and decreased with pressure. However,in the aqueous suspension containing graphite nanoparticles,the induction time of hydrate formation had smaller change with pressure and temperature.Thus,graphite nanoparticles had a positive effect on hydrate formation.Besides,the conclusion of the rate of hydrate nucleation is mainly controlled by gas-liquid mass transfer was proved by the fact that the great surface area of graphite nanoparticles could accelerate the mass transfer.
gas hydrate;carbon dioxide;nanographite;induction time;nucleation;temperature;pressure;heat transfer;control
TQ013;TE8
:A
:1001-9219(2015)01-60-05
2014-05-08;
:国家自然科学基金(51176015),常州市工业支撑项目(CE20140055),江苏省研究生培养创新工程项目 (CXZZ13_0735);
:周诗岽(1978-),男,副教授,电话 0519-83290280,电邮 zsd@cczu.edu. cn。
