纳米SnO2光催化剂的制备及其在养殖废水处理中的应用
2015-05-22金晓杰于晓彩吴云英尚晓琳尹丹妮薛冠华
金晓杰,于晓彩,吴云英,尚晓琳,尹丹妮,薛冠华
(大连海洋大学 海洋科技与环境学院,辽宁 大连116023)
0 引言
随着经济的不断发展,人们对水产品的需求日益增长,在捕捞量不能满足市场需求的情况下,水产养殖业得以迅速发展,同时也带来了相应的环境问题。粗放型经营、资源依赖型水产养殖方式导致的生态失衡、环境恶化、资源萎缩的状况在国内外已十分严重。大量养殖废水的排放给周边环境造成了巨大的影响,养殖水域的水质下降,造成渔业经济损失巨大[1]。
光催化是纳米半导体颗粒材料独特的性能之一。当半导体氧化物(如SnO2)纳米颗粒受到大于禁带宽度能量的光子照射后,会产生电子/空穴对。电子具有还原性,空穴具有氧化性,在催化反应中,一般与表面吸附的H2O和O2反应生成·OH和超氧离子O-2,从而能够把许多难降解的有机物氧化为无毒副作用的CO2和H2O等无机物。光催化技术和其他污染物治理方法相比,不需通过再次处理,而且可以再生和循环利用。半导体材料的光催化技术在环境治理领域得到了广泛的研究与应用[2-3]。
SnO2是一种重要的宽带隙N型半导体金属氧化物,在光学、电学、催化、气敏、压敏、湿敏等方面均有优异性能,由于其具有大比表面积和高表面活性,以及特殊的晶体结构、表面特性和吸附特性,使其催化活性和选择性与传统催化剂相比表现出独特的性质[4-5],因而获得了很大的重视和广泛深入的研究。
本文采用化学沉淀法制备了SnO2纳米粒子,通过X光衍射仪(XRD)和扫描电子显微镜(SEM)对其进行表征,研究了SnO2纳米粒子光催化实验中,各单因素,如SnO2催化剂投加量、废水中氨氮初始质量浓度、溶液pH值和H2O2质量浓度对降解废水中氨氮效果的影响。通过五因素四水平正交实验确定了SnO2催化氧化的优化反应条件。
1 材料与方法
1.1 试剂与仪器
试剂:五水合四氯化锡(SnCl4·5H2O),氯化铵,氨水,硝酸铵,硝酸银,过氧化氢,盐酸,氢氧化钠,硫酸铵,柠檬酸钠,苯酚,次氯酸钠。
仪器:马弗炉,磁力搅拌器,恒温水浴箱,Quanta 200FEG场发射环境扫描电子显微镜,D/MAX-2500X射线衍射仪紫外灯,752型紫外分光光度计。
1.2 方法
1.2.1 SnO2催化剂的制备
以五水合四氯化锡为原料,采用共沉淀法制备纳米SnO2光催化剂。步骤如下[6-8]:
(1)称取适量的SnCl4·5H2O晶体,放入倒有一定量去离子水的烧杯中搅拌溶解,再加入适量去离子水,配成浓度为0.1mol/L的氯化锡水溶液。
(2)配制pH=8.0的 NH3·H2O/NH4Cl缓冲溶液,量取适量缓冲溶液加入反应器,将上述配制的0.1mol/L氯化锡水溶液加入反应器中,滴加氨水,不断搅拌,维持溶液pH=8.0,反应完全后继续搅拌1h。
(3)静置12h,将沉淀上层溶液用注射器吸除,用真空泵对沉淀进行抽滤,不断用含NH4NO3的去离子水对沉淀进行洗涤,直至无Cl-(用0.5mol/L的AgNO3溶液检验)。
(4)将洗净的沉淀在烘箱中110℃下,烘干12h,再将烘干的沉淀放入马弗炉中,在400℃空气氛围下焙烧3h。
(5)将制得的SnO2磨碎,过筛得到纳米SnO2颗粒。
1.2.2 模拟养殖废水的制备
海水:取自大连海洋大学附近海域。
模拟废水:将砂滤后的海水(氨氮为0.972 5mg/L,pH值为8.12)和(NH4)2SO4进行配制,(NH4)2SO4的量根据实验要求的氨氮质量浓度进行调整。
1.2.3 氨氮的测定方法
采用靛酚蓝比色法测定氨氮含量[9]。
2 结果与讨论
2.1 纳米SnO2光催化剂的表征
2.1.1 X射线衍射分析(XRD)
采用XRD分析了所制备的SnO2光催化剂的物相组成和粒子大小。晶体尺寸是决定纳米材料物理化学性质的一个重要因素,晶粒尺寸大小直接影响到材料的性能。用XRD测量纳米材料晶粒的原理是基于衍射线的宽度与材料晶粒大小有关这一现象。XRD测试结果如图1所示:
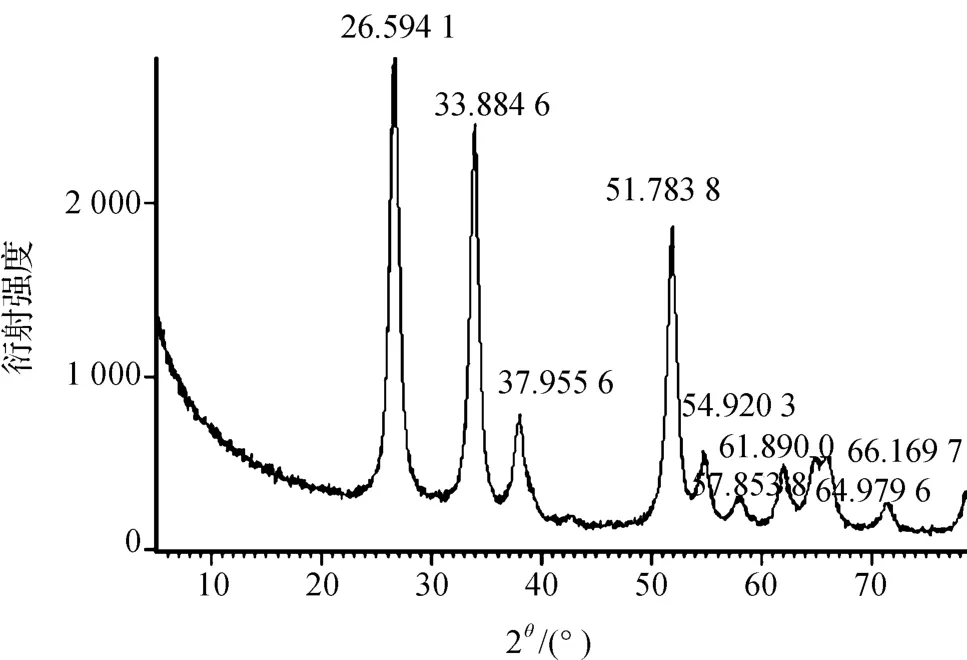
图1 纳米SnO2粒子的XRD图Fig.1 XRD pattern of nano-SnO2particle
由图1可知,在衍射角(2θ)为26.594 1°时衍射强度达到最大峰值,在33.884 6°、37.955 6°、51.783 8°和54.920 3°时都有明显的峰,峰位置和峰强度与JCPDS标准卡SnO2(JCPDS41-1445)卡片的衍射数据相一致,无杂峰,证明所制备的SnO2纳米粒子为金红石型结构。其晶格常数a、b和c分别为4.738、4.738和3.187Å。由最强衍射峰面的半高宽运用Deby-Scherrer公式[10]计算求得样品晶粒平均粒径为49.90nm,与扫描电镜得到的粒径基本一致。
2.1.2 扫描电子显微镜(SEM)结果
图2是所制备的SnO2的SEM图,从图中可以清楚看到,SnO2粒子为金红石型结构,具有良好的结晶情况,这与XRD分析结果一致。粒子尺寸大小不是很均匀,大尺寸的粒子可能是有部分晶体在高温煅烧过程中发生了凝聚。纯SnO2的粒径大约在30~50nm之间,与Scherrer公式计算所得粒径相符。
2.2 SnO2光催化降解养殖废水的单因素实验分析
2.2.1 SnO2投加量对光催化反应效果的影响
将三相逆变器等效模型通过坐标变换得到d-q轴下的等效受控源模型[14],根据逆变电路等效关系求得逆变器-电机系统归算到直流端等效的开环阻抗为:
实验在废水氨氮初始质量浓度为30mg/L,pH=8.0时,研究了SnO2光催化剂投加量对光催化反应效果的影响。催化剂投加量分别为0.4、0.8、1.2、1.6、2.0和2.4g/L,用磁力搅拌器搅拌1h,同时紫外光照2h后测定吸光度,计算出氨氮的降解率,结果如图3所示。

图2 纳米SnO2光催化剂的SEM图Fig.2 SEM image of nano-SnO2photocatalyst
随着SnO2投加量的增加,去除率逐渐增大,在投加量为0.8g/L时去除率达到最大值,此后去除率开始下降。原因可能为:当催化剂投加量较低时,随着量的增加,参与光解反应的SnO2颗粒数增加,光降解率也增加。但当其用量增加到一定程度时,随着用量的增加,溶液中SnO2对光的散射增强,光生电子和空穴的数量减少,光的利用率因此下降,影响催化效果。
2.2.2 溶液初始pH值对光催化反应效果的影响
海水养殖pH值一般控制在7.5~8.5之间。pH值过高或过低,对水产养殖生物都有直接的损害,甚至会造成死亡。实验在氨氮初始质量浓度为30mg/L,SnO2催 化 剂 投 加 量 为 0.8g/L,使 用1mol/L的HCl或NaOH调节废水的pH值分别为5.0、6.0、7.0、8.0、9.0和10.0,紫外光照2h后测定吸光度,计算出氨氮降解率,如图4所示。
由图4可知氨氮去除率随pH值的增大而增加,但pH值达到8时去除效果最好,大于8.0,催化效果明显降低。这种情况是因为pH值会影响催化剂的表面特性,当pH值较低时催化剂和含氨氮废水均带正电荷,不利于氨氮吸附到催化剂表面进行催化反应;而pH值较高时,SnO2催化剂表面会带负电荷,不利于吸附OH-,也不利于废水中氨氮催化氧化反应的进行。
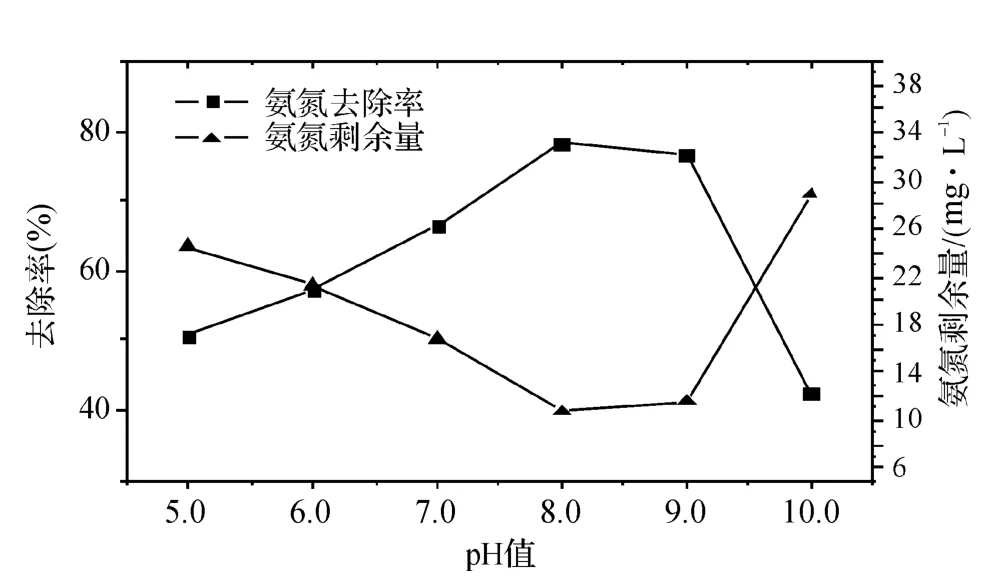
图4 pH值对光催化效果的影响Fig.4 Effects of pH value on the photocatalytic properties
2.2.3 氨氮初始质量浓度对光催化反应效果的影响
由图5可见,氨氮废水初始质量浓度对于废水的光催化降解反应有很大影响,去除率先增大后又减小,在氨氮初始质量浓度为50mg/L时,去除率达最大值。一般情况下认为反应速率与反应物质量浓度成正比,但图中显示氨氮初始质量浓度增大到一定值以后,催化氧化速率反而下降,这可能因为SnO2可吸附反应物中的活性位数有限,随着初始质量浓度的提高,吸附的氨氮分子数会随之增加,从而减少了产生羟基自由基的活性位点,说明光催化氧化更适合氨氮质量浓度不太高的废水。
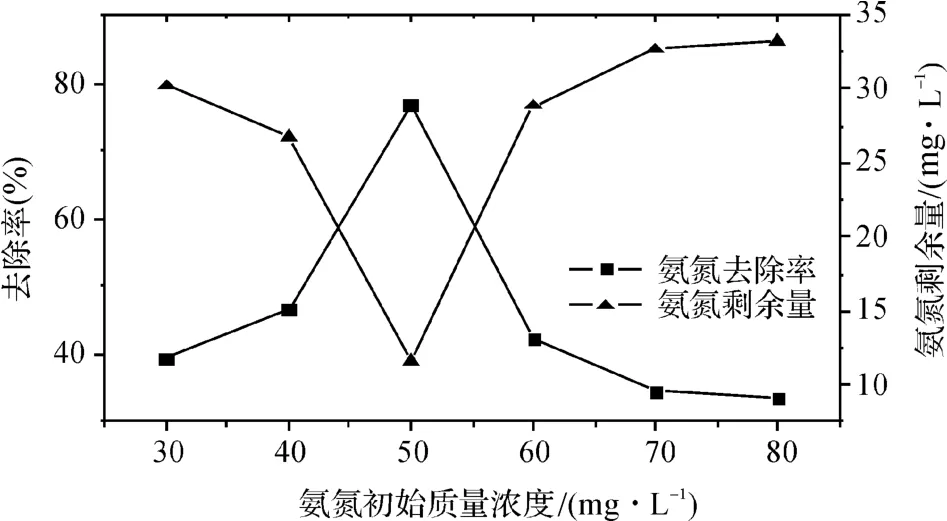
图5 氨氮初始质量浓度对光催化效果的影响Fig.5 Effects of the initial mass concentration of ammonia nitrogen in seawater on the photocatalytic properties
2.2.4 光照时长对光催化反应效果的影响
氨氮初始质量浓度为30mg/L,SnO2催化剂投加量为0.8g/L,调节废水pH=8.0的条件下,分别测定在反应时间为1、2、3、4、5和6h时氨氮的质量浓度,并计算氨氮的去除率,如图6所示。
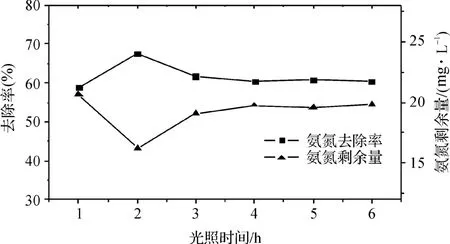
图6 光照时间对光催化效果的影响Fig.6 Effects of the illumination time on the photocatalytic properties
从去除率数值来看,随时间延长SnO2对氧化去除废水中的氨氮效果变化不是很大,去除率总体趋势先增大后减小,在2h处达到最大值。这是因为水中氧分子不断俘获电子,使羟基自由基(·OH)和高活性的超氧离子自由基(·O-2)的量也增多[11],从而达到氧化降解的目的。时间过长对氨氮的去除效果不明显。
2.2.5 H2O2质量浓度对光催化反应效果的影响
当废水pH=8.0,氨氮初始质量浓度为30mg/L,SnO2催化剂投加量为0.8g/L时,再控制H2O2最终质量浓度为0、0.2、0.4、0.6、0.8、1.0和3.0g/L,紫外光光照2h后测定吸光度,计算氨氮的降解率,如图7所示。
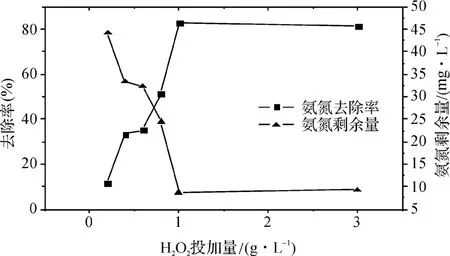
图7 投加H2O2质量浓度对光催化效果的影响Fig.7 Effects of the mass concentration of hydrogen peroxide solution on the photocatalytic properties
氧化剂是有效的带电子的捕获剂,由图7可见:加入H2O2对于光催化氧化反应有明显效果,随着H2O2质量浓度的增加,氨氮去除率增加。在1.0g/L处,达到最大值,之后基本趋于平稳。H2O2是电子的接受体,能参与催化剂表面电子争夺,阻碍了SnO2表面光生电子-空穴对的复合,从而产生更多具有很强氧化能力的·OH和O-2;其次在紫外灯的照射作用下H2O2发生光解也能产生羟基自由基,从而矿化去除废水中的氨氮及其他有机污染物,光催化氧化的速率和效率得以提高[12-13]。
2.3 正交实验对SnO2光催化降解条件的优化
为了确定SnO2光催化剂对水产养殖废水中氨氮的光催化反应优化条件,研究了光催化反应各因素的交互影响情况,正交实验数据如表1所示。
正交实验表中各水平的指标总和参数K1、K2、K3和K4可以判断对实验指标的影响大小和各因素的优化水平,以确定5个因素的最优水平组合。由表1可知SnO2光催化剂催化氧化的优化反应条件是:当SnO2催化剂投加量为1.2g/L,废水中氨氮初始质量浓度为40mg/L,pH 值为8.0,H2O2投加量为1.0g/L,反应时间为2h时,氨氮光催化氧化去除率达到72%。极差值R的大小表明各因素对相应实验效果的影响程度,即上述5个因素对纳米SnO2光催化氧化降解养殖废水的影响程度顺序依次为:氨氮初始质量浓度>H2O2质量浓度﹥pH值>反应时间≈SnO2投加量。
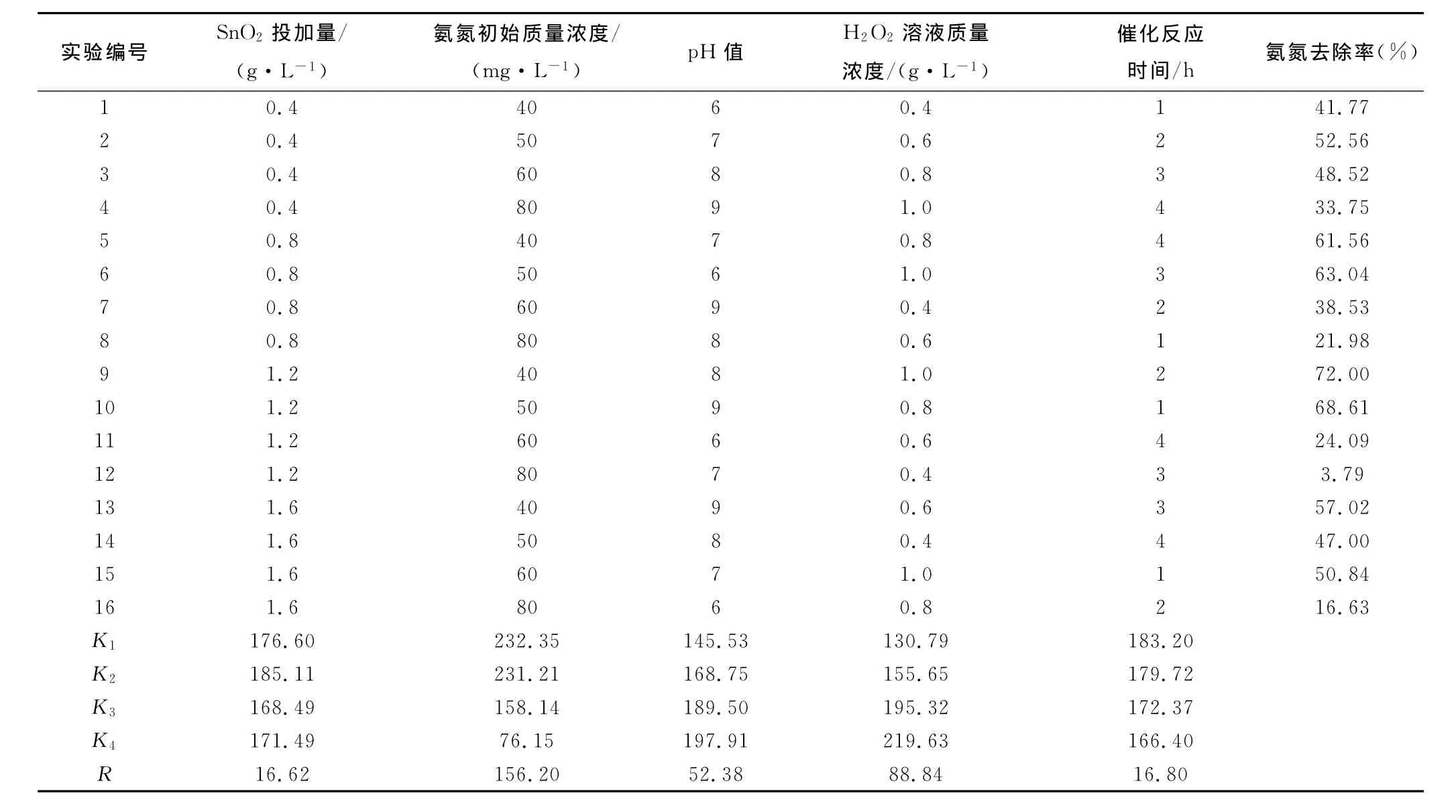
表1 正交实验表Tab.1 Results of orthogonal test
3 结论
通过上述实验的研究,可得到以下几点结论:
(1)以五水合四氯化锡为原料,可采用化学沉淀法制备纳米SnO2光催化剂。这种方法在实验过程中煅烧温度易控制,操作流程较简单,所得催化剂纯度较高。
(2)通过XRD和SEM技术手段对制得的催化剂进行晶型、粒径和形貌的表征,所得纳米SnO2为四方晶系金红石结构,结晶情况较好,平均粒径为49.90nm。
(3)以水产养殖废水中的氨氮为主要污染物,研究了紫外灯照射下SnO2光催化剂对氨氮光催化降解的情况,表明各单因素:催化剂投加量、废水中氨氮初始质量浓度、溶液PH值和H2O2质量浓度均是影响氨氮催化氧化去除率的重要因素。
(4)通过五因素四水平的正交实验,确定了SnO2光催化剂氧化的最优化反应条件为SnO2投加量为1.2g/L,氨氮初始质量浓度为40mg/L,PH 值为8.0,H2O2质量浓度为1.0g/L,催化时间为2h时,去除率可达72%。通过极差分析得到,各单因素对纳米SnO2光催化氧化降解养殖废水的影响程度顺序依次为:氨氮初始质量浓度>H2O2质量浓度>pH值>反应时间≈SnO2投加量。
(References):
[1]CUI Yi,CHEN Bi-juan,CHEN Ju-fa.Evaluation on self-pollution of marine culture in the Yellow Sea and Bohai Sea[J].Chinese Journal of Applied Ecology,2005,16(1):180-185.
崔毅,陈碧鹃,陈聚法.黄渤海海水养殖自身污染的评估[J].应用生态学报,2005,16(1):180-185.
[2]ABEYSINGHE D H,SHANABLEH A,RIGEN B.Biofilters for water reuse in aquaculture water[J].Science and Technology,1996,3(11):253-260.
[3]XU Xiao,YU Xiao-cai,GONG Xi-bin,et al.Photo-catalytic degradation of seafood processing wastewater by nano-titanium dioxide[J].Journal of Dalian Ocean University,2014,9(3):295-298.
徐晓,于晓彩,宫喜斌,等.纳米TiO2光催化降解海产品深加工废水的研究[J].大连海洋大学学报,2014,9(3):295-298.
[4]YU Xiao-cai,DU Qian,ZHU Peng-fei,et al.Photo-catalytic degradation of petroleum in seawater by nano-titanium dioxide[J].Marine Envioronmental Science,2011,30(2):264-267.
于晓彩,杜倩,朱鹏飞,等.纳米TiO2光催化降解海洋石油污染[J].海洋环境科学,2011,30(2):264-267.
[5]MARTINEZ A I,ASOSTA D R,CEDILLO G.Effect of SnO2on the photocatalytical properties of TiO2films[J].Thin Solid Films,2005,490:118-123.
[6]SHI Li-yi,GU Hong-chen,LI Chun-zhong,et al.Preparation and properties of SnO2-TiO2composite photocatalysis[J].Chinese Journal of Catalysis,1999,20(3):338-342.
施利毅,古宏晨,李春忠,等.SnO2-TiO2复合光催化剂的制备和性能[J].催化学报,1999,20(3):338-342.
[7]HAN Qiao-feng,KAN Chun,LI Dan,et al.Preparing and the study for properties of nanocrystal SnO2[J].Shanghai Chemical Industry,2002(18):18-19.
韩巧凤,阚春,李丹,等.SnO2纳米晶的制备及性能研究[J].上海化工,2002(18):18-19.
[8]YANG Hua-ming,AO Wei-qin,CAO Jian-hong,et al.Preparation Technology and applications of nanosized Tin Oxide powder[J].Materials Review,2003,17(5):36-39.
杨华明,敖伟琴,曹建红,等.纳米SnO2的制备技术及应用[J].材料导报,2003,17(5):36-39.
[9]JIANG Yue-wen.The measurement of ammoniain seawater with indophenol blue spectrophotometric[J].Marine Envioronmental Science,1990,9(1):75-80.
蒋岳文.靛酚蓝分光光度法测定海水中的氨氮[J].海洋环境科学,1990,9(1):75-80.
[10] TANG Yu-chao,HUANG Xian-huai,YU Han-qing,et al.Characterization and visible-light-activity of nitrogen-doped TiO2phtocatalyst[J].Chinese Journal of Inorganic Chemistry,2005,21(11):1 747-1 751.
唐玉朝,黄显怀,俞汉清,等.N掺杂TiO2光催化剂的制备及其可见光活性研究[J].无机化学学报2005,21(11):1 747-1 751.
[11]LIU Yun-qing,YU Xiao-cai,WU Yun-ying,et al.Application of Uv-vis conversion agent/TiO2composite photocatalyst in Marine oil pollution treatment[J].Journal of Dalian Ocean University,2014,29(4):420-424.
刘云庆,于晓彩,吴云英,等.紫外可见上转换剂/TiO2复合光催化剂在海洋石油污染处理中的应用[J].大连海洋大学学报,2014,29(4):420-424.
[12]POULIOS I,TSACHPINIS I.Photodegradation of the textile dye reactive black 5in the presence of Semiconducting Oxides[J].Chemistry and Technology of Biotechnology,1999,74(4):349-357.
[13]HACHEM C,BOCQUILLON F,ZAHRAA O,et al.Decolourization of textile industry wastewater by the photocatalytic degradation process[J].Dyes and Pigments,2001,49(2):117-125.
