1-甲基-3,4-二硝基吡唑合成与表征
2015-05-10张巧玲李雅津焦清介李永祥
张巧玲,李雅津,焦清介,任 惠,李永祥
(1.中北大学化工与环境学院,山西 太原 030051; 2.北京理工大学爆炸科学与技术国家重点实验室,北京 100081)
1 引 言
氮杂环类含能化合物[1-2]因其具有生成焓高、密度高以及环境友好等特征,近年来受到各国研究者的青睐。含氮化合物的氮、氧原子电负性高,氮杂芳环体系能形成类苯结构的大π键,具有钝感、热稳定性好的性质。国内外对硝基氮杂环含能化合物进行了大量的研究[3-6],并合成出了一系列的新型低感高能炸药,如1-甲基-3,4-二硝基吡唑(MDNP)等。MDNP的熔点为20 ℃,常温下(25 ℃)为液态,在300 ℃下的热力学状态稳定,可作为一种液体单质炸药,在熔铸炸药中可降低液相载体的熔点。含能增塑剂[7]的发展方向是高能量、低感度、液态化,因此MDNP也是一种潜在的含能增塑剂、添加剂。Grimmett等[8]以N-甲基吡唑为原料,硝硫混酸硝化,生成1-甲基-4-硝基吡唑和1-甲基-3,4-二硝基吡唑(MDNP)的混合物,二者摩尔比为4∶1,MDNP得率仅为20%,未对该物质进行相关性能研究。Pasupala Ravi[9]采用蒙脱石K-10/硝酸铋法合成出包括MDNP的一系列吡唑类衍生物,其反应条件苛刻,反应时间较长,成本较高,且后续分离困难。为此,有必要探索一种新的合成路线,以期提高得率、降低成本。
目前,国内鲜有关于MDNP的合成工艺的研究报道。因此,本研究基于文献[10]的工艺,以3-硝基吡唑为原料,硝硫混酸为硝化剂,得到3,4-二硝基吡唑(DNP),对于DNP的重结晶溶剂进行了优化,提高了产品品质。采用绿色甲基化试剂碳酸二甲酯进行甲基化反应,合成目标化合物MDNP,并优化了甲基化反应条件,探讨了甲基化反应机理,对其进行了结构表征。
2 实验部分
2.1 试剂与仪器
3-硝基吡唑、N,N-二甲基甲酰胺(DMF)、碳酸二甲酯(DMC)、碳酸钾、二氯甲烷、苯; X-4型数字显示显微熔点测试仪,北京泰克仪器有限公司; FTIR-7600S红外光谱仪(KBr压片),天津分析仪器厂; P1201高效液相色谱仪,大连依利特分析仪器厂; Elementar Vario EL CUBE型元素分析仪,德国Elementar公司。
2.2 合成路线
以3-硝基吡唑为原料,在发烟硫酸及硝酸中反应1 h得到DNP,然后以DNP为原料,DMF为溶剂,DMC为甲基化试剂反应得到目标产物,合成路线见Scheme 1。
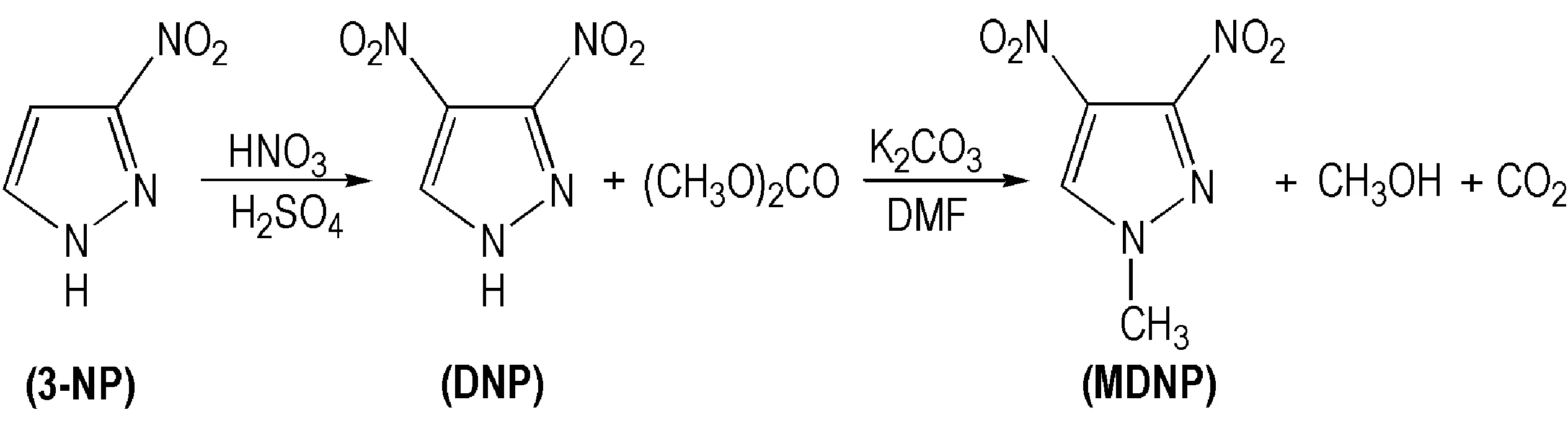
Scheme 1 Synthesis route of 1-Methyl-3,4-dinitropyrazole(MDNP)
2.3 合成实验
2.3.1 DNP的合成[14]
向装有温度计及搅拌装置的100 mL四口烧瓶中加入16 mL 20%发烟硫酸,称取3 g 3-硝基吡唑分批加入,搅拌至全溶,缓慢滴加4.9 mL 96.5%发烟硝酸,升温控制在95~110 ℃,反应0.5 h。冷却,倒入碎冰,待碎冰全溶之后,乙醚多次萃取(25 mL×4),合并有机相,蒸去溶剂,干燥,得到2.43 g粗品。利用芳烃类溶剂重结晶,采用甲苯和苯两种溶剂对目标产物进行精制,在65 ℃下,用10 mL苯将粗品重结晶,提高了产品的品质。得率57.93%,m.p.83~85 ℃(文献值[10-14]85 ℃),IR (KBr,ν/cm-1):3435(N—H),3152(N—H),2928(C—H),1555(C—NO2),1382(C—NO2),1348(C—NO2);1H NMR (CDCl3,300 MHz)δ:8.71 (t,J=8 Hz,3H)。
2.3.2 1-甲基-3,4-二硝基吡唑(MDNP)的合成
量取50 mL DMF于250 mL四口烧瓶中,将4.36 g(0.028 mol) DNP逐渐加入烧瓶中,加快搅拌速度,待DNP完全溶解后,将5.75 g(0.041 mol)碳酸钾缓慢加入其中,水浴升温到90 ℃后,开始向反应液中滴加25 mL(0.297 mol)碳酸二甲酯,控制滴加速度1 mL·min-1。滴加完毕,水浴保温反应6.5 h。停止反应,将其倒入300 mL蒸馏水中,搅拌,静置一段时间,得深红色液体,并有少量油珠。二氯甲烷多次萃取混合液(25 mL×4),合并有机相,减压旋蒸,得5 mL黄红色油状液体。用50 mL苯于15 ℃下将粗品重结晶,得到淡黄色晶体,真空低温干燥,得MDNP 4.54 g,得率95.7%,液相色谱测得纯度达96%以上,m.p.20 ℃(文献值[8]20~21 ℃),IR (KBr,ν/cm-1):3435(N—H),3152(N—H),2930(N—CH3),1555(C—NO2),1382(C—NO2),1348(C—NO2);1H NMR (CDCl3,300 MHz)δ:8.01 (t,J=8 Hz,3H),4.14(t,J=8 Hz,3H); Anal.calcd for C4H4N4O4:C 27.92,H 2.34,N 32.55; found C 28.02,H 2.52,N 32.39。
3 结果与讨论
3.1 DNP甲基化反应条件优化
3.1.1 反应温度对MDNP得率的影响
文献[14]已给出了DNP的合成优化工艺,本研究重点对DNP甲基化反应的工艺条件进行优化。
DNP 4.36 g(0.028 mol),DMC 25 mL(0.297 mol),碳酸钾5.75 g(0.041 mol),DMF 50 mL,反应6.5 h,甲基化反应温度对目标化合物MDNP得率影响的实验结果见表1。
表1 甲基化反应温度对MDNP得率的影响
Table 1 Effect of methylating temperature on the yield of MDNP
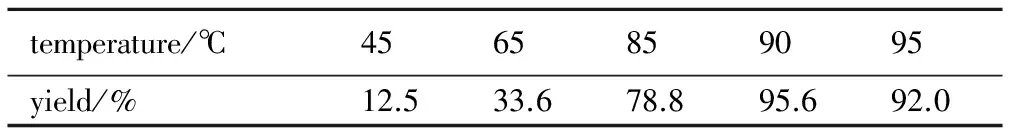
temperature/℃4565859095yield/%12.533.678.895.692.0
从表1可看出:随着反应温度的升高,产物得率呈先增大后减小的趋势,当温度达到90 ℃时得率最高(95.6%),之后随着温度的升高,得率反而下降。其原因为甲基化试剂DMC的沸点为90.2 ℃,在低于沸点的温度范围,随着温度的升高,反应速率加快,原料的转化率提高,产物得率增加。当温度高于90 ℃时,随着温度的升高,加剧DMC的蒸发,导致目标产物的得率出现下降趋势。因此,本研究的较佳反应温度为90 ℃。
3.1.2 反应时间对MDNP得率的影响
90 ℃条件下反应,反应时间对目标化合物MDNP收率影响的实验结果见表2。由表2可知,当反应时间达到6 h时,产物得率可达到95%,随着反应时间的延长,得率增长趋势变缓。而随着反应时间延长,能耗会增大。因而本研究较佳反应时间为6.5 h。
表2 甲基化反应时间对MDNP得率的影响
Table 2 Effect ofmethylating time on the yield of MDNP

time/h4566.57yield/%56.577.895.095.994.2
3.1.3 物料比对MDNP得率的影响
物料比是影响甲基化反应得率的一个非常重要的因素,尤其是对甲基化能力相对较弱的DMC。如果甲基化试剂使用量少,会降低其甲基化能力,产品得率降低; 如果甲基化试剂使用过多,除了浪费原料外,还会使目标化合物的纯度不够,给产物分离造成不便。
90 ℃,DMF 50 mL,反应6.5 h,DNP、DMC与K2CO3的物料比对目标化合物MDNP得率影响的实验结果见表3,由表3可以看出较佳摩尔比:n(DNP)∶n(DMC)∶n(K2CO3)=1∶10.5∶1.5。
综上所述:以DNP为原料、DMF为溶剂、DMC做甲基化试剂、K2CO3为催化剂合成MDNP的较佳工艺条件为:反应温度90 ℃,反应时间6.5 h,物料比n(DNP)∶n(DMC)∶n(K2CO3)=1∶10.5∶1.5。甲基化产品得率达95.7%。综合前一步DNP的得率57.93%,目标产物总得率55.6%。
表3 物料摩尔比对MDNP得率的影响
Table 3 Effect of molar ratio of raw materials on the yield of MDNP
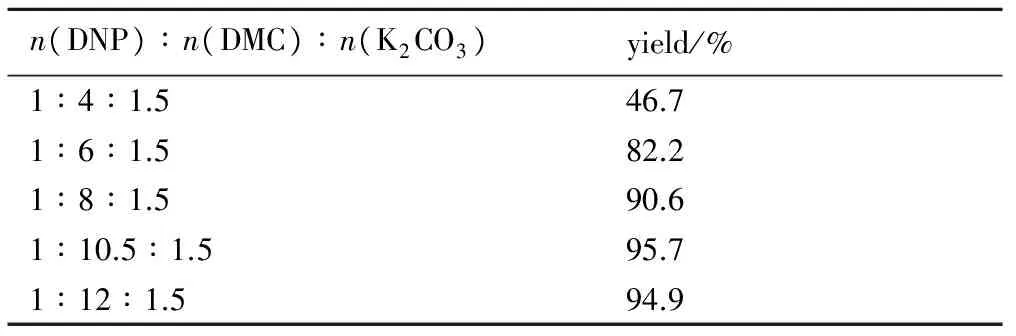
n(DNP)∶n(DMC)∶n(K2CO3)yield/%1∶4∶1.546.71∶6∶1.582.21∶8∶1.590.61∶10.5∶1.595.71∶12∶1.594.9
3.1.4 甲基化试剂的选择
甲基化反应是有机和药物合成中的常用步骤,是有机化合物分子中的氢被甲基(—CH3)取代的反应,这个过程一般都会使用亲电子的甲基源,如碘代甲烷、硫酸二甲酯、碳酸二甲酯,但是较少用亲电性更强的甲基化试剂,如三氟甲基磺酸甲酯或氟代磺酸甲酯。不同的甲基化试剂由于亲电性的不同,反应得率不同。本研究甲基化试剂采用绿色试剂碳酸二甲酯[15-16],代替了传统的甲基化试剂硫酸二甲酯、卤代甲烷等剧毒物质,符合绿色化的研究方向。DMC作为绿色化学试剂,有以下特点:可生物降解,无毒,无诱变刺激性气味,避免了操作人员吸入毒性气体的危险。在进行试验操作时,无需像CH3I,DMS,光气等采取特殊防护措施。在上述的较佳工艺条件下进行了实验验证,实验结果见表4,可以看出,采用碳酸二甲酯(毒性最低)作为甲基化试剂时,目标产物的得率比采用硫酸二甲酯提高5%。因此,本研究较优的甲基化试剂为碳酸二甲酯。
表4 甲基化试剂对反应的影响
Table 4 Effect of methylating agent on reaction
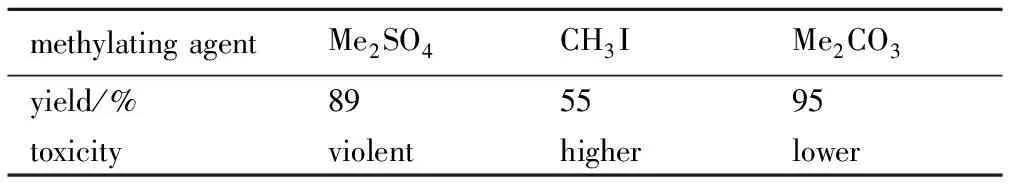
methylatingagentMe2SO4CH3IMe2CO3yield/%895595toxicityviolenthigherlower
3.2 甲基化反应机理探讨
3,4-二硝基吡唑环上含有两个硝基,具有强的吸电子能力,使吡唑环显酸性,将其溶于DMF,与K2CO3反应,得到3,4-二硝基吡唑阴离子,该阴离子为亲核试剂,在一定的条件下与亲电试剂DMC很容易进行反应得到1-甲基-3,4-二硝基吡唑。根据不同的实验条件,DMC表现出了不同的化学反应性质,它既可以发生羧甲基化反应,又可以发生甲基化反应。DMC发生的亲核取代反应,主要有BAC2(双分子亲核反应,碱性催化,酰基解离)和BAL2(双分子亲核反应,碱性催化,烷基解离)两种机理[17],可能的机理见Scheme 2。

Scheme 2 Mechanisms of methylation reaction
在反应的初始阶段,DMC作为羧甲基化试剂发生BAC2反应,亲核试剂攻击DMC的羰基碳,得到酰基转移产物,该反应是可逆反应; 当反应达到平衡时,DMC作为甲基化试剂发生BAL2反应,亲核试剂攻击DMC的甲基基团,得到甲基化后的产物。在这两种反应机理中,只有甲基化反应是不可逆的,因为CH3OCOO-阴离子形成后会立即分解成甲氧基负离子和CO2。由上述分析可知,主要反应按照BAL2反应机理进行。
3.3 MDNP的热分解
采用X-4型数字显示显微熔点测试MDNP的熔点为20 ℃。与文献[8]的20~21 ℃对应。
MDNP的热分解DSC曲线(升温速率10 ℃·min-1,样品量2.5mg)如图1所示。MDNP的热分解由一个吸热过程和一个放热过程组成,首先曲线在20~26 ℃之间有一个向上的熔融吸热峰,吸热阶段的峰顶温度为26 ℃,这一阶段主要是物质的熔化吸热; 第二阶段为放热过程,在DSC曲线上表现为急剧的放热过程,在298 ℃有一个放热峰,说明了该物质具有良好的热稳定性。

图1 MDNP的DSC曲线
Fig.1 DSC curve of MDNP
4 结 论
(1) 以3-硝基吡唑为原料,通过硝化、甲基化合成了目标产物,并对其进行了结构表征。
(2) 甲基化反应的较佳工艺条件为:反应温度90 ℃,反应时间6.5 h,n(DNP)∶n(DMC)∶n(K2CO3)=1∶10.5∶1.5。目标产物的总得率为55.6%。
(3) 甲基化试剂采用绿色试剂碳酸二甲酯,代替了传统的甲基化试剂硫酸二甲酯、碘甲烷等剧毒物质,符合绿色化工的研究方向。
参考文献:
[1] Lebedev V P,Matyushim Yu N,Inolemtcev Ya D.Thermochemical and explosive properties of nitropyrazoles[C]∥Int.ICT Conference on Energetic Materials.Russia.1998:180.
[2] 阳世清,徐松林,雷永鹏.氮杂环含能化合物的研究进展[J].含能材料,2006,14(6):475-480.
YANG Shi-qing ,XU Song-lin ,LEI Yong-peng.Development on NitogenHeterocyclic Energetic Compounds[J].ChineseJournalofEnergeticMaterials(HannengCailiao),2006,14(6):475-480.
[3] Smolin E M,Lorenee R.The chemistry of heterocyclic compounds(s-triazines and derivatives)[M].New York:Interscience Publishers Ine,1959:347-348.
[4] 杨克明,曹端林,李永祥,等.1-甲基-3,5-二硝基-1,2,4-三唑的合成及表征[J].含能材料,2011 (6):501-504.
YANG Ke-ming,CAO Duan-lin,LI Yong-xiang,et al.Synthesis and characterization of 1- methyl -3,5-dininitro-1,2,4-trazole[J].ChineseJournalofEnergeticMaterials(HannengCailiao),2011 (6):501-504.
[5] 宋磊,王建龙,李永祥,等.1-甲基-4,5-二硝基咪唑的合成及表征[J].含能材料,2009,17(5):531-533.
SONG lei,WANG Jian-long,LI Yong-xiang,et al.Synthesis and characterization of 1-methyl-4,5-dinitroimidazole[J].ChineseJournalofEnergeticMaterials(HannengCailiao),2009,17(5):531-533.
[6] Katritzky A R.Physical methods in heterocyclic chemistry [M].New York:Academic Press,1974.
[7] 姬月萍,李普瑞,汪伟,等.含能增塑剂的研究现状及发展[J].火炸药学报,2005,28(4):47-51.
JI Yue-ping,LI Pu-rui,WANG Wei,et al.A review of recent advances of energetic plasticizers[J].ChineseJournalofExplosivesandPropellants,2005,28(4):47-51.
[8] Ross Grimmett M,Richard Lim K H.Dinitration of l-methylpyrazole:l-methyl-3,4-dinitropyrazole[J].AustJChem,1978,31:68-69.
[9] Ravi P,Surya P Tewari.Facil and environmentally friendly synthesis of nitropyrazoles using montmorillonite K-10 impregnated with bismuth nitrate[J].CatalysisCommunications,2012,19(1):37-41.
[10] 杜闪.3,4-二硝基吡唑的合成及其性能研究[D].中北大学,2012.
DU Shan.Study on synthesis and properties of 3,4-dinitropyrazole[D].Taiyuan:North University of China,2012.
[11] Janssen J W A M,Koeners H J.PyrazolesXII.The preparartion of 3(5)-nitropyrazoles by thermal rearrangement of N-nitropyrazoles[J].TheJournalofOrganicChemistry,1973,38(10):1777-1782.
[12] Janssen J W A M,Habraken C L,Louw R.On the mechanism of the thermal N-nitropyrazole rearrangement evidence for a [1,5] Sigmatropic Nitro Migration[J].TheJournalofOrganicChemistry,1976,41(10):1758-1762.
[13] LI Yong-xiang,DU Shan,WANG Jian-long.3,4-dinitro-1H-pyrazole benzene 0.25-solvate[J].ActaCrystallographicaSectionE:StructureReportsOnline,2011,67(6):1369.
[14] Zaitsev A A,Kortusov I O,Dalinger I L,et al.The use of methorymethyl group as a protecting group for the synthesis ofφ-methyl-3-nitro-5-R-pyrazole[J].RussianChemicalBuldetin,2009,58(10):2118-2121.
[15] 舒婷,李光兴.碳酸二甲酯作甲基化试剂的研究进展[J].化工中间体,2008(1):20-23.
SHU Ting,LI Guang-xing.Progress in study of dimethyl carbonate as methylating reagent[J].ChemicalIntermediate,2008(1):20-23.
[16] Rivetti F.In Green Chemistry:Challening Perspectives[M].Tundo P,Anastas P,Eds,Oxford University Press,2001:201.
[17] Pietro Tundo,Alvise Perosa.Green organic syntheses:organic carbonates as methylating agents[J].TheChemicalRecord,2002,2(1):13-23.
