HPLC梯度洗脱法同时测定丹芎跌打膏中4种主要成分的含量
2015-05-05马灵珍
马灵珍
(亳州职业技术学院 药学院,安徽 亳州 236800)
HPLC梯度洗脱法同时测定丹芎跌打膏中4种主要成分的含量
马灵珍
(亳州职业技术学院 药学院,安徽 亳州 236800)
目的:建立了同时测定丹芎跌打膏中4个主要成分(京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素和姜黄素)含量的高效液相色谱检测方法。方法:采用依利特C18柱,流动相为乙腈(A)和0.4%冰醋酸溶液(B),梯度洗脱,流速为1.2 mL/min;柱温为30℃;检测波长λ1=238 nm(京尼平龙胆双糖苷和栀子苷),λ2=430 nm(去甲氧基姜黄素和姜黄素)。结果:在优化的色谱条件下,京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素和姜黄素的线性范围分别为4.10~82.00 μg/mL(r=0.999 3)、5.69~113.80 μg/mL(r=0.999 9)、7.80~156.00 μg/mL(r=0.999 5)和8.06~161.20 μg/mL(r=0.999 8);4种成分的平均加样回收率(n=6)分别为97.89%、99.24%、97.16%、96.89%,RSD分别为1.16%、0.97%、1.56%、1.23%。结论:该方法为丹芎跌打膏的质量控制提供了科学依据。
丹芎跌打膏;京尼平龙胆双糖苷;栀子苷;去甲氧基姜黄素;姜黄素
丹芎跌打膏为治疗软组织损伤类的复方制剂,现收载于国家中成药标准汇编骨伤科分册[1],由栀子、姜黄等十三味药材和植物油、硬脂酸、甘油、三乙醇胺、凡士林、羊毛脂、蒸馏水等加工而成,该制剂具有活血散瘀、消肿止痛的功效,是治疗各种急性、亚急性软组织损伤等病症的首选药物。原丹芎跌打膏标准仅对处方中单一成分进行了研究,通过对维普、万方及知网等数据库检索,未检索到对该制剂中任何药味进行定量检测的相关报道,而该制剂为十三味中药材加工而成,单一的含量检测不能有效地控制复方制剂的含量。栀子和姜黄为丹芎跌打膏中的主要药物,栀子[2]外用具有消肿止痛的功效,对外治扭挫伤痛效果显著;姜黄具有破血行气,通经止痛的功效,对风湿肩臂疼痛、跌扑肿痛等效果显著。本研究对该制剂中药材栀子、姜黄中的4个成分京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素和姜黄素进行定量测定方法学研究,对丹芎跌打膏的全面质量控制具有重要意义和应用价值。
1 仪器与试药
安捷伦1200型HPLC色谱仪;VS-100UE型恒温超声波提取机(无锡沃信仪器有限公司);XS205DU型十万分之一电子天平(梅特勒-托利多)。
栀子苷对照品(110749-201316,含量以97.5%计,常温遮光保存)、姜黄素(110823-201405,含量以98.9%计,冷冻保存)由中国食品药品检定研究院提供;京尼平龙胆双糖苷对照品(29307-60-6,含量以98.0%计,2-8℃干燥遮光密封保存)、去甲氧基姜黄素(24939-17-1,含量以98.0%计,干燥、避光、密封保存)由四川省维克奇生物科技有限公司提供;丹芎跌打膏(每支装10g;批号为20150206、20150213、20150408)购于长春普华制药股份有限公司;乙腈为色谱纯,甲醇、冰醋酸为分析纯,水为重蒸馏水。
2 试验方法
2.1 色谱条件
采用依利特C18色谱柱(200 mm×4.6 mm,5um);流动相为乙腈(A)-0.4%冰醋酸溶液(B),按表1进行梯度洗脱[3-10];检测波长(0~28min,λ1=238 nm[11-13],28~50 min,λ2=430 nm[14]);流速采用1.2 mL/min;柱温采用30℃;进样量为20 μL。
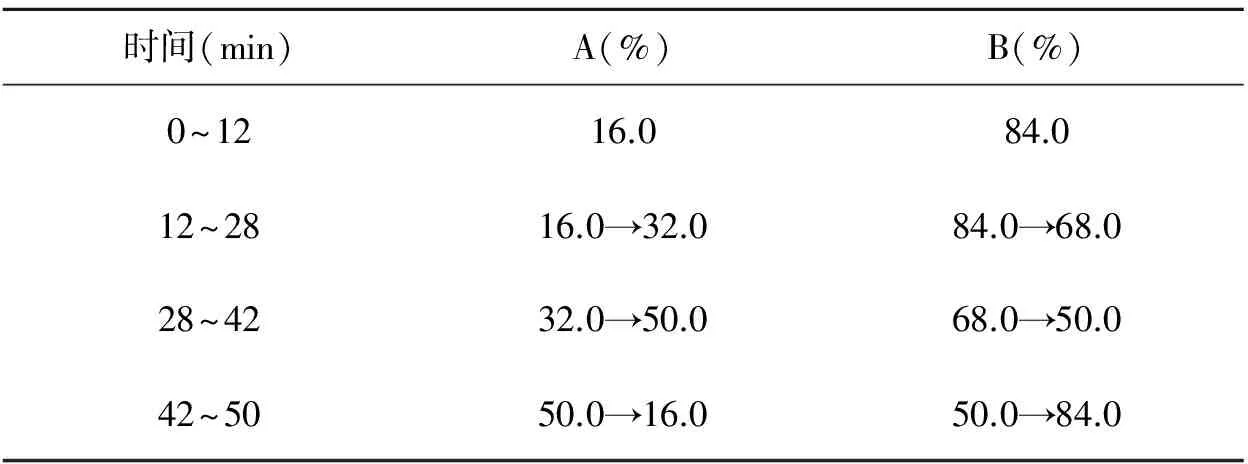
表1 流动相梯度洗脱程序
2.2 对照品溶液的配制方法
2.2.1 对照品储备液的制备 分别称取对照品京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素和姜黄素适量,分别加甲醇溶解并用甲醇稀释,制成京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素和姜黄素质量浓度分别为0.410 mg/mL、0.569 mg/mL、0.780 mg/mL、0.806 mg/mL单一成分的对照品储备液。
2.2.2 混合对照品溶液的制备 分别吸取2.2.1项下已配制的对照品储备液1.5、5.0、1.5、2.5 mL,用甲醇稀释,制成每1 mL分别含京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素、姜黄素为12.3、56.9、23.4、40.3 μg的混合对照品溶液。
2.3 样品溶液的制备方法
2.3.1 样品溶液的制备 取丹芎跌打膏4.0 g,精密称定,置于50mL具塞锥形瓶中,再精密加入甲醇50mL,称定其总重量,记录称量的数据,采用加热回流法对样品进行处理40 min,取出后自然放至室温,再次称定总重量,记录具体数据,用甲醇补足重量,振摇均匀,滤过,取续滤液,作为样品溶液。
2.3.2 阴性对照溶液的制备 按照国家中成药标准汇编骨伤科分册丹芎跌打膏质量标准中规定的处方工艺,分别制备不含栀子、姜黄的样品,按照文中2.3.1项下样品溶液的制备方法分别制备成栀子、姜黄空白溶液。
本实验选用玉米-豆粕型肉鸭饲粮,肉鸭基础饲粮配制参照中华人民共和国肉鸭营养标准(2012)和NRC(1994)标准,基础饲粮组成及营养水平见表1。
3 试验结果
3.1 专属性实验结果
分别精密吸取样品溶液、混合对照品溶液、栀子空白溶液和姜黄空白溶液,参照上述色谱条件各进样20 μL进行测定,记录色谱峰。结果在该色谱条件下,按保留时间先后的出峰顺序为:京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素、姜黄素,样品溶液和混合对照品溶液所测各组分保留时间一致;空白样品在对照品相应位置处无吸收峰。结果表明处方中其他药物对所测成份的测定无干扰。色谱图见图1~4。
3.2 线性关系考察
分别精密吸取上述制备的对照品储备液0.1、0.2、0.5、1.0、2.0mL,将其分别置于10 mL的容量瓶中并用甲醇稀释成系列浓度的混合对照品溶液,分别进样20 μL进行测定,以峰面积Y为纵坐标,以对照品质量浓度X为横坐标,绘制标准曲线并进行回归计算,实验考察结果见表2。
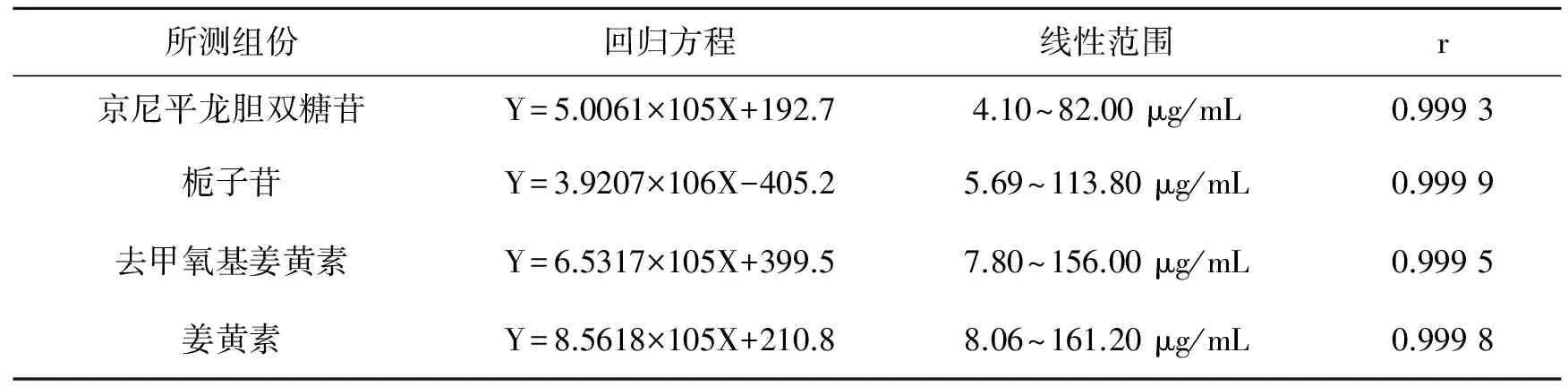
表2 线性关系实验结果(n=6)
3.3 方法的精密度
精密吸取2.2.2项下制备的混合对照品溶液20μL,参照2.1项下色谱条件进行分析测定,连续进样6次,记录京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素和姜黄素的峰面积,计算相对标准偏差,京尼平龙胆双糖苷为1.53%、栀子苷为0.74%、去甲氧基姜黄素为1.09%、姜黄素为1.31%。
3.4 方法的重复性
3.5 溶液的稳定性
取同一批次丹芎跌打膏样品(批号为20150408)的同一样品溶液,分别在0、2、4、8、12、24 h进样测定,结果京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素和姜黄素的RSD,京尼平龙胆双糖苷为1.56%、栀子苷为0.71%、去甲氧基姜黄素为1.33%、姜黄素为0.57%,表明24h内样品溶液具有良好的稳定性。
3.6 方法的加样回收率
取6份已知含量的丹芎跌打膏(批号为:20150408;京尼平龙胆双糖苷为0.142 mg/g、栀子苷为0.729 mg/g、去甲氧基姜黄素为0.304 mg/g、姜黄素为0.487 mg/g)适量,取丹芎跌打膏2.0 g,精密称定,置50mL具塞锥形瓶中,精密加入混合对照品溶液25 mL、甲醇25 mL,并称定总重量,记录具体数据,采用加热回流法对样品进行处理40 min,取出后自然放至室温,再次称定总重量,记录具体数据,用甲醇补足重量,摇匀,滤过,取续滤液,过滤,作为加样样品试液。参照2.1项下的色谱条件进行分析测定,计算各组分回收率,结果上述4个成份的平均加样回收率(n=6)分别为97.89%、99.24%、97.16%、96.89%,RSD分别为1.16%、0.97%、1.56%、1.23%。
3.7 样品测定
取3个不同批号的丹芎跌打膏样品,参照2.3.1项下制备样品溶液的处理方法,按2.1项下的色谱条件进行分析测定京尼平龙胆双糖苷、栀子苷、去甲氧基姜黄素和姜黄素含量,结果见表3。
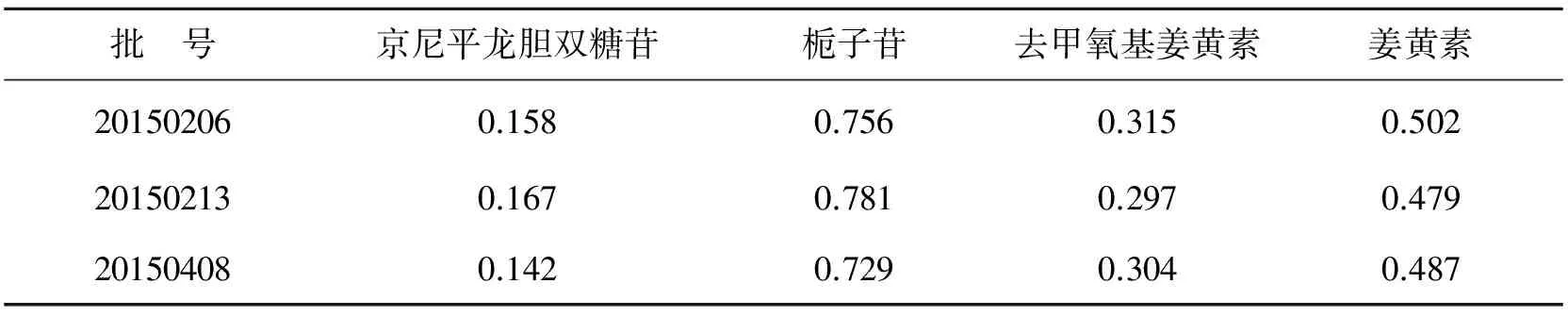
表3 样品含量测定结果(n=3,mg/g)
4 讨论
4.1 样品提取条件的优化
样品溶液制备过程中首先选取加热回流60 min和超声提取60 min分别进行试验,通过峰面积对比,结果显示加热回流60 min的提取率明显高于超声提取60 min;在此实验基础上对加热回流时间(20min、40min和60min)进行了优化,结果显示加热回流40 min和60 min峰面积相差不大,但明显大于加热回流20min时的峰面积。故选取加热回流40 min作为样品溶液制备的最佳提取条件。
4.2 流动相的选择
分别采取乙腈-水、乙腈-0.5%磷酸溶液、乙腈-0.4%冰醋酸溶液、乙腈-0.3%甲酸溶液不同比例梯度洗脱,结果表明,在乙腈-0.4%冰醋酸溶液为流动相按照文中比例洗脱时,各色谱峰的发布、峰形和分离度效果最佳,故选取乙腈-0.4%冰醋酸溶液为该制剂4个主要成分含量测定的流动相。
[1]国家药典委员会.国家药品标准中成药标准汇编骨伤科分册[S].
[2]田秀峰,李鹏跃,王宏洁 等,冰片对栀子在小鼠体内药代动力学的影响[J].中国实验方剂学,2012,18(14):135-138.
[3]徐燕,曹进,王义明,等.多波长高效液相色谱法同时测定栀子中的三类成分[J].药学学报,2003,38(7) :543-546.
[4]何兵,田吉,李春红,等.泸州纳溪GAP基地栀子中4种主要活性成分的含量测定[J].中成药,2009,31(12):1884-1887.
[5]何兵,田吉,李春红,等.不同成熟期和不同部位栀子中4种主要活性成分的含量变化[J].药物分析杂志,2010,30(5):801-805.
[6]裴彩云,蔡艳,宋剑,等.10批栀子中环烯醚萜苷类成分含量测定[J].中国现代应用药学,2011,28(13):1343-1345.
[7]刘硕谦,刘仲华,黄建安,等.反相高效液相色谱法同时测定姜黄药材中3个组分的含量[J].分析化学,2005,33(3):309-312.
[8]张颧慧,张丹,王妍,等.HPLC内标法测定姜黄中姜黄素类成分的含量[J].中国药学杂志,2009,44(18):1423-1425.
[9]史晶晶,冯素香,郝蕊,等.姜黄提取物中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的含量测定[J].中医学报,2015,30(6):853-855.
[10]赵欣,王爱里,袁园,等.姜黄中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的光稳定性分析[J].中草药,2013,44(10):1338-1341.
[11]李艳芳,范建伟,刘武占,等.一测多评法测定栀子中4 个环烯醚萜苷类成分的含量[J].中药材,2014,37(5):822-825.
[12]王晓娟,孙兆林,季宇彬,等.栀子中两种活性成分的含量测定[J].世界中医药,2013,8(2):204-206.
[13]付小梅,彭水梅,刘婧,等.HPLC法同时测定栀子类药材中10个主要有效成分的含量[J].药物分析杂志,2014,34(4):615-621.
[14]李青苗,杨文钰,唐雪梅,等.姜黄素类化合物在不同品系姜黄根茎内积累规律研究[J].中国中药杂志,2014,39(11):2000-2004.
Simultaneous Determination of Four Main Ingredients in Danxiong Dieda Gao by HPLC
MA Ling-zhen
(School of Pharmacy,Bozhou Vocational and Technical College, Bozhou,236800,China)
Objective:To establish a HPLC method for the simultaneous determination of four main components(Genipin-1-β-D-gentiobioside,geniposide,demethoxycurcumin and curcumin) in Danxiong Dieda Gao. Method:The HPLC separation was performed on a Hypersil C18 column eluted with the mobile phases of acetonitrile(A) - 0.4% acetic acid solution(B) in a gradient elution and the flow rate was 1.2 mL·min-1.The column temperature was at 30 ℃.Genipin-1-β-D-gentiobioside and geniposide were detected at 238 nm,demethoxycurcumin and curcumin were detected at 430 nm.Results:The chromatographic peaks of four main components and the corresponding spectra were ideal under the optimal conditions.Genipin-1-β-D-gentiobioside,geniposide,demethoxycurcumin and curcumin had good linearity at 4.10~82.00 μg/mL(r=0.999 3),5.69~113.80 μg/mL(r=0.999 9),7.80~156.00 μg/mL(r=0.999 5),8.06~161.20 μg/mL(r=0.999 8),respectively.The average recoveries and RSD were 97.89%(1.16%),99.24%(0.97%), 97.16%(1.56%) and 96.89%(1.23%),respectively.Conclusion:The method can provide reference for evaluating the quality of Danxiong Dieda Gao.
Danxiong Dieda Gao;Genipin-1-β-D-gentiobioside;Geniposide; Demethoxycurcumin;Curcumin
2015-05-13
安徽省高等学校教学质量与教学改革工程实训中心建设项目(20101460)。
马灵珍(1982-),男,安徽省亳州市人,硕士,讲师,主要从事中药生产与质量控制研究。
R284.1
A
1673-8772(2015)04-0033-05
