固相萃取-超高效液相色谱法检测地表水中7种氯酚类化合物
2015-04-26陈建华彭刚华乔支卫张振欣吴志强
陈建华,彭刚华,乔支卫,张振欣,吴志强
江西省环境监测中心站,江西 南昌 330039
氯酚类化合物(CPs)是一类毒性强、难分解的氯代芳香族有机污染物,对人、畜均有较大毒性,其中五氯酚被国际癌症研究机构IARC列为第2B组致癌物[1]。中国《地表水环境质量标准》(GB 3838—2002)中规定2,4-二氯酚、2,4,6-三氯酚和五氯酚的浓度限值,分别为 0.093、0.2、0.009 mg/L[2]。
水体中氯酚类化合物的检测方法主要有气相色谱 法[3-5]、液 相 色 谱 紫 外 法[6-9]、液-质 联 用法[10-14]。
目前,中国国家标准和环境行业标准规定的氯酚类检测方法均为液液萃取衍生化气相色谱法,液液萃取法虽然具有较好的回收率,但存在耗时长、萃取液易乳化和有机试剂用量较大等诸多不足;同时衍生化过程操作步骤复杂、耗时,而且会降低检测重现性和灵敏度。另外,相关检测方法都只有检测标准中规定了限值的2,4-二氯酚、2,4,6-三氯酚、五氯酚3种化合物,并未对其他有害氯酚类化合物进行分析。在此背景下,本研究建立了固相萃取-超高效液相色谱法同时分析水体中7种氯酚类化合物的检测方法,包括4-氯酚、2,4-二氯酚、2,6-二氯酚、2,4,5-三氯酚、2,4,6-三氯酚、2,3,4,6-四氯酚、五氯酚,能够满足地表水的实际检测要求。
1 实验材料与方法
1.1 样品采集与保存
地表水采样选用棕色玻璃瓶罐装,采样时水样应充满采样瓶并加盖密封,防止空气进入,样品在4℃下避光保存。
1.2 仪器与试剂
仪器:配有四元梯度泵和光电二级阵列管检测器(PDAD)的超高效液相色谱仪(Waters ACQUITY UPLC H-Class)、液相色谱柱(Waters ACQUITY UPLC BEH C181.7 μm,2.1 × 100 μm,186002350)、固相萃取小柱(Waters Oasis HLB,200 mg/6 mL)、自动固相萃取仪(Auto SPE-06c)、pH计(pHS-430)、溶剂过滤装置(T-50)、旋转蒸发仪(RE-2000E)、有机相滤头(ANPEL,SCAA-104,13 mm,0.22 μm)。
试剂和水:甲醇、二氯甲烷、丙酮均为色谱纯级,乙酸、硫酸均为优纯级,实验用水均为超纯水。
标准品:氯酚标准品(美国 Accustandart公司:Chlorinated Phenolics-Mix A,0.1 mg/mL in MeOH,210081058-01),浓度为100 mg/L。
1.3 标准曲线绘制
依次移取 10、30、50、70、100 μL 氯酚标液于棕色进样瓶中,用60%甲醇水溶液定容至1.0 mL,得到 1.0、3.0、5.0、7.0、10.0 mg/L 氯酚标准溶液,用于绘制外标标准曲线。
1.4 样品前处理
水样若为饮用水须先用硫代硫酸钠除去余氯,地表水用定量滤纸过滤,工业废水浓度过高时可以适当稀释后过滤。量取1 000 mL水样,用硫酸调节pH为1.5~3,以pH=2为最宜。
固相萃取柱先依次用5 mL二氯甲烷、5 mL甲醇、5 mL超纯水以5 mL/min流速活化平衡,1 000 mL水样以10 mL/min流速通过萃取柱,再依次用5 mL丙酮、10 mL二氯甲烷分别以5 mL/min流速洗脱,洗脱液转移到旋转蒸发瓶中,旋蒸至近干后用60%甲醇水定容至1.0 mL。
1.5 样品分析
进样体积为 5 μL,流速为 0.3 mL/min,色谱柱为 BEH C18(1.7 μm,2.1 × 100 μm),柱温为30℃,样品温度为4℃,检测波长为分段检测(表1),流动相为甲醇-水(含0.2%乙酸),梯度变化见表2。色谱图如图1所示。

表1 不同氯酚类化合物最大吸收波长及其检测波长程序设定
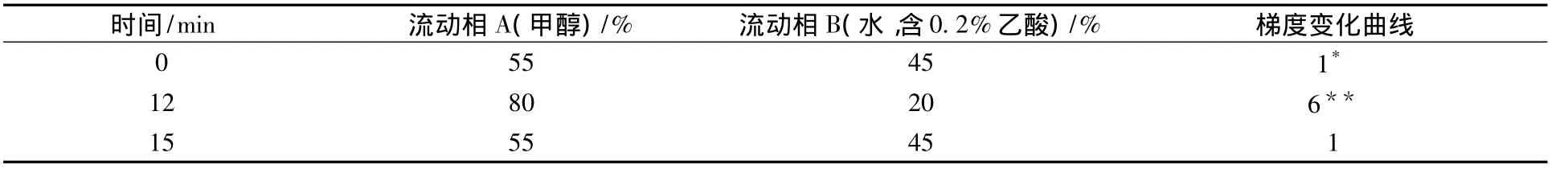
表2 超高效液相色谱法检测氯酚类化合物的流动相洗脱程序设定
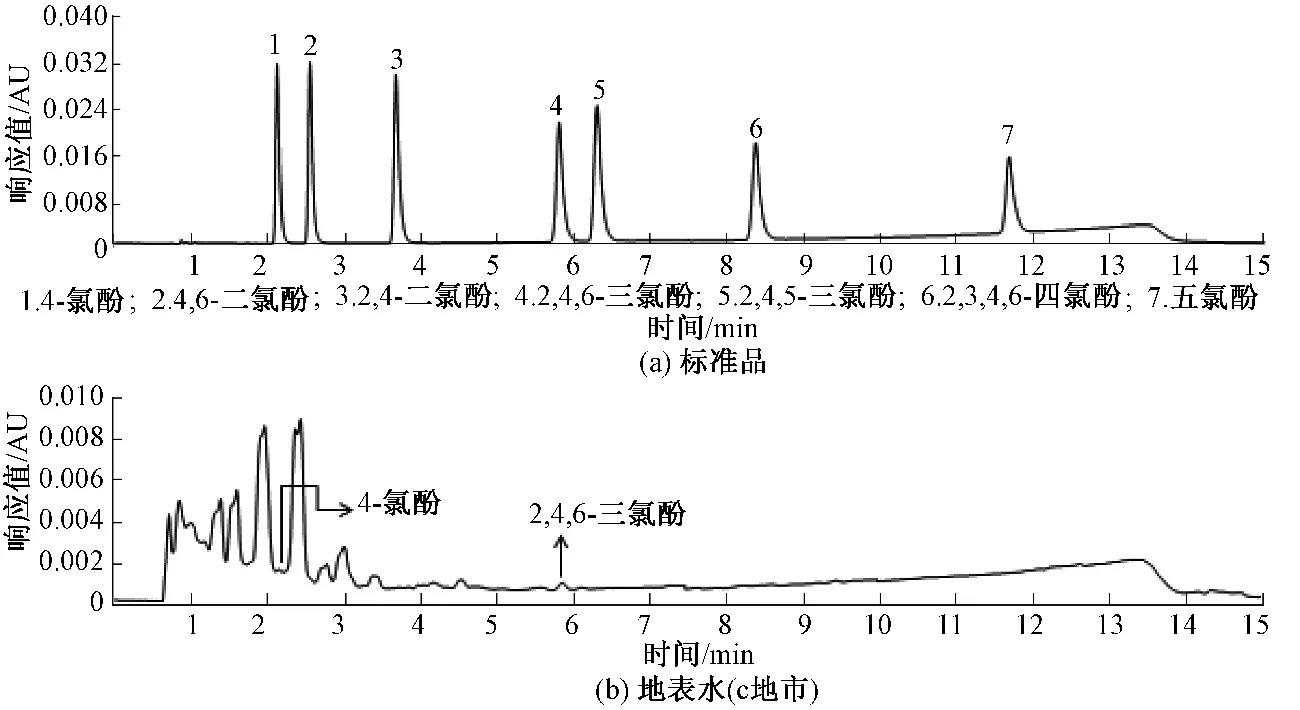
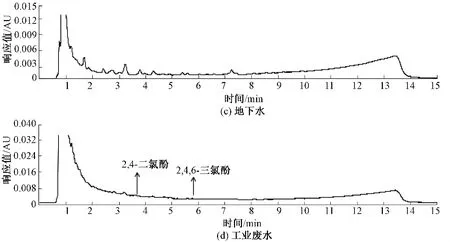
图1 超高效液相色谱法检测氯酚类化合物色谱图
2 实验结果与讨论
2.1 流动相选择
张冬梅等[8]比较了使用甲醇-水和乙腈-水作流动相时氯酚类化合物的分离效果,结果发现,使用甲醇-水作流动相峰形较好,且干扰少、分离效果更佳。苏燕、薛凤丽等[7,15]在甲醇-水流动相中加入少量乙酸后,能够抑制氯酚类的电离,进一步改善峰形,增加检测器响应信号。李晓晶、廖林川等[13,16]比较了在流动相中添加甲酸、乙酸铵、甲酸铵-甲酸对分离效果的影响,结果表明,添加乙酸铵后峰形变好,保留时间不再漂移且能够与杂质完全分离。
选择甲醇-水作为流动相,比较了向流动相中添加乙酸和乙酸铵的分离效果。实验发现,含乙酸铵的流动相虽然出峰时间较短,但是峰形较差,分离度也不够好。最终选择甲醇-水(含0.2%乙酸)为流动相,峰形尖锐、分离度良好,且样品能够与干扰物分开。
2.2 色谱柱和柱温的选择
色谱柱性能会影响目标化合物的分离效果、峰形、分析时间、稳定性等。选用第二代杂化颗粒技术的 Waters BEH C18色谱柱(2.1 ×100 μm,1.7 μm),与常规C18色谱柱相比,BEH C18柱内径和填料颗粒粒径更小,死体积小,具有柱效高、pH耐受范围宽、稳定性好、寿命长的特点,同时目标化合物分离峰形更好,分析时间也更短。
柱温直接影响氯酚类化合物在色谱柱上的吸附和解析时间,从而影响色谱峰的保留时间和分离效果。对不同柱温(25、30、35、40℃)条件下氯酚类化合物的分离效果相比较,表明不同温度对氯酚类化合物的响应和分离度影响较小,保留时间随柱温的升高略微前移。综合考虑,色谱柱温度选择为30℃。
2.3 检测波长的选择
氯酚类化合物含有苯环,具有较强的紫外吸收,可以用紫外检测器进行定量分析。通过利用二级阵列管紫外检测器对7种氯酚化合物在190~400 nm间进行全扫描,得到3D光谱图和各化合物的最大紫外吸收波长。为提高各化合物的检测灵敏度,降低检出限,采用波长分段检测模式,0 ~5 min 内检测 4-氯酚、2,4-二氯酚、2,6-二氯酚,检测波长设定为285 nm;5~7.5 min内检测 2,4,5-三氯酚、2,4,6-三氯酚,波长设定为 290 nm;7.5 ~10 min 内检测 2,3,4,6-四氯酚,波长设定为300 nm,10~15 min内检测五氯酚,波长设定为304 nm。
2.4 萃取条件的优化
样品前处理方法采用固相萃取法,既操作简单、快速,又可实现无相分离避免乳化现象,减少溶剂使用量。
2.4.1 萃取柱的选择
陈硏朦等[10]研究了 Waters HLB(6 mL,200 mg)、MCX(3 mL,60 mg)两种萃取柱的回收率,资料表明,HLB 对 2,4,6-三氯酚、五氯酚的回收率为70% ~100%,明显高于 MCX的回收率(30% ~ 60%)。杨秋红等[12]对 ODS-C18、ENVI、HLB进行的比较研究表明,3种萃取柱的回收率大小依次为HLB>ENVI>ODS-C18。
综上分析,本实验选择Waters HLB(6 mL,200 mg)萃取柱,可保证更好的回收率和重现性。
2.4.2 萃取溶剂的选择
杨秋红等[12]分别对甲醇、乙腈、二氯甲烷、丙酮、二氯甲烷-丙酮(1+1)等萃取溶剂的洗脱能力进行实验比较,结果表明,二氯甲烷/丙酮(1+1)对氯酚的洗脱能力最强,回收率最好。
选择二氯甲烷、丙酮为萃取溶剂,先用二氯甲烷洗去萃取柱中可能存在的能溶于二氯甲烷中的物质,再依次用甲醇、水活化平衡萃取柱;由于水和二氯甲烷极性相差较大,两者不互溶,水样进样后先用空气推出管路中残留水样,氮气吹干萃取柱,再用极性中等的丙酮溶剂(与水和二氯甲烷均能互溶)洗脱,最后用二氯甲烷洗脱。实验发现,依次使用丙酮、二氯甲烷相比只用二氯甲烷溶剂洗脱萃取柱,氯酚类化合物的萃取回收率明显提高,且重复性也更好。
2.4.3 水样pH的调节
氯酚类化合物略呈酸性,在水中常以氯酚钠盐的形式存在,为了提高氯酚类在萃取柱上的吸附和保留,往往需要在水样中加入酸使其转化为氯酚类化合物。由于7种氯酚类的PKa值相差较大,在水中电离程度也就不一样,实验中用硫酸将水样 pH分别调至1.5、2.0、2.5、3.0、3.5、4.0,测定不同pH的氯酚类化合物的回收率,见图2。
实验表明,2,3,4,5-四氯酚、五氯酚回收率受pH(1.5~4.0)变化的影响不大,回收率保持在78% ~87%;4-氯酚、2,6-二氯酚、2,4-二氯酚、2,4,5-三氯酚在pH≤3时回收率较稳定,但当pH>3时回收率明显降低;2,4,6-三氯酚受pH影响较大,回收率随pH增加而逐渐下降。综上所述,调节水样pH为1.5~3.0时回收率较好,其中pH=2最为适宜,各氯酚类化合物的回收率都在80%以上。
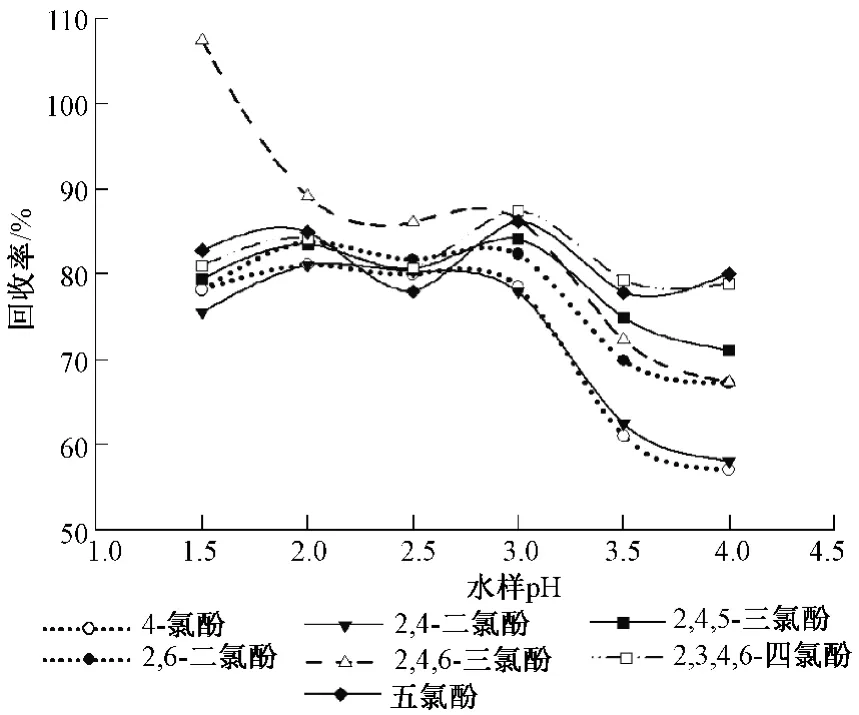
图2 各氯酚类化合物在不同pH时回收率变化情况
2.5 线性范围、相关系数和方法检出限
配制 1、3、5、7、10 mg/L 的氯酚类化合物混合标液,得到各氯酚类化合物不同浓度响应值,通过线性方程拟合,其标准曲线、相关系数、方法检出限见表3。实验表明,各氯酚化合物浓度为1~10 mg/L具有良好的线性关系,相关系数>0.999 7;当萃取体积为1 L,浓缩至1 mL,进样量为5 μL时,7种氯酚的方法检出限为12.7~32.1 ng/L,测定下限为50.8~128.4 ng/L,能够达到目前氯酚类化合物标准方法的同等水平。
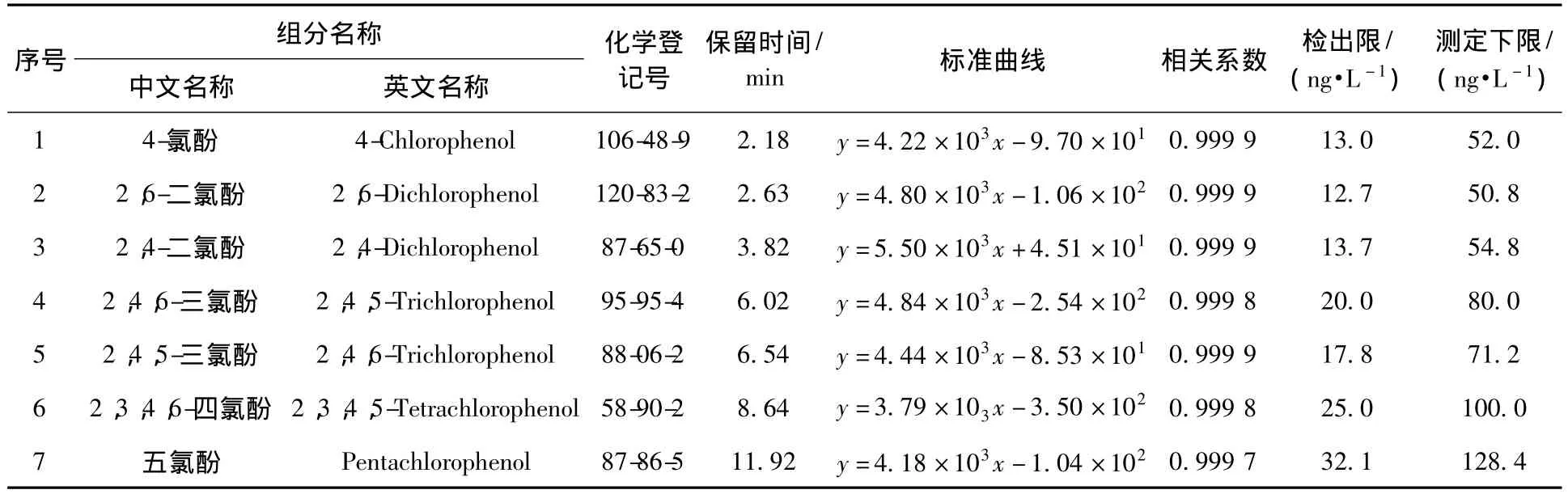
表3 各氯酚类化合物的线性方程和方法检出限
2.6 方法准确度和精密度
在空白水样中分别添加高低两组浓度水平的氯酚标准溶液,每组平行样品5份,按照上述前处理和样品分析方法,测得加标回收率和相对标准偏差,如表4所示。
低浓度组(1 μg/L)平均加标回收率为81.1% ~108.4%,相对标准偏差为 4.6% ~13.3%;高浓度组(5 μg/L)平均加标回收率为79.2%~90.0%,相对标准偏差为5.1% ~ 12.0%。
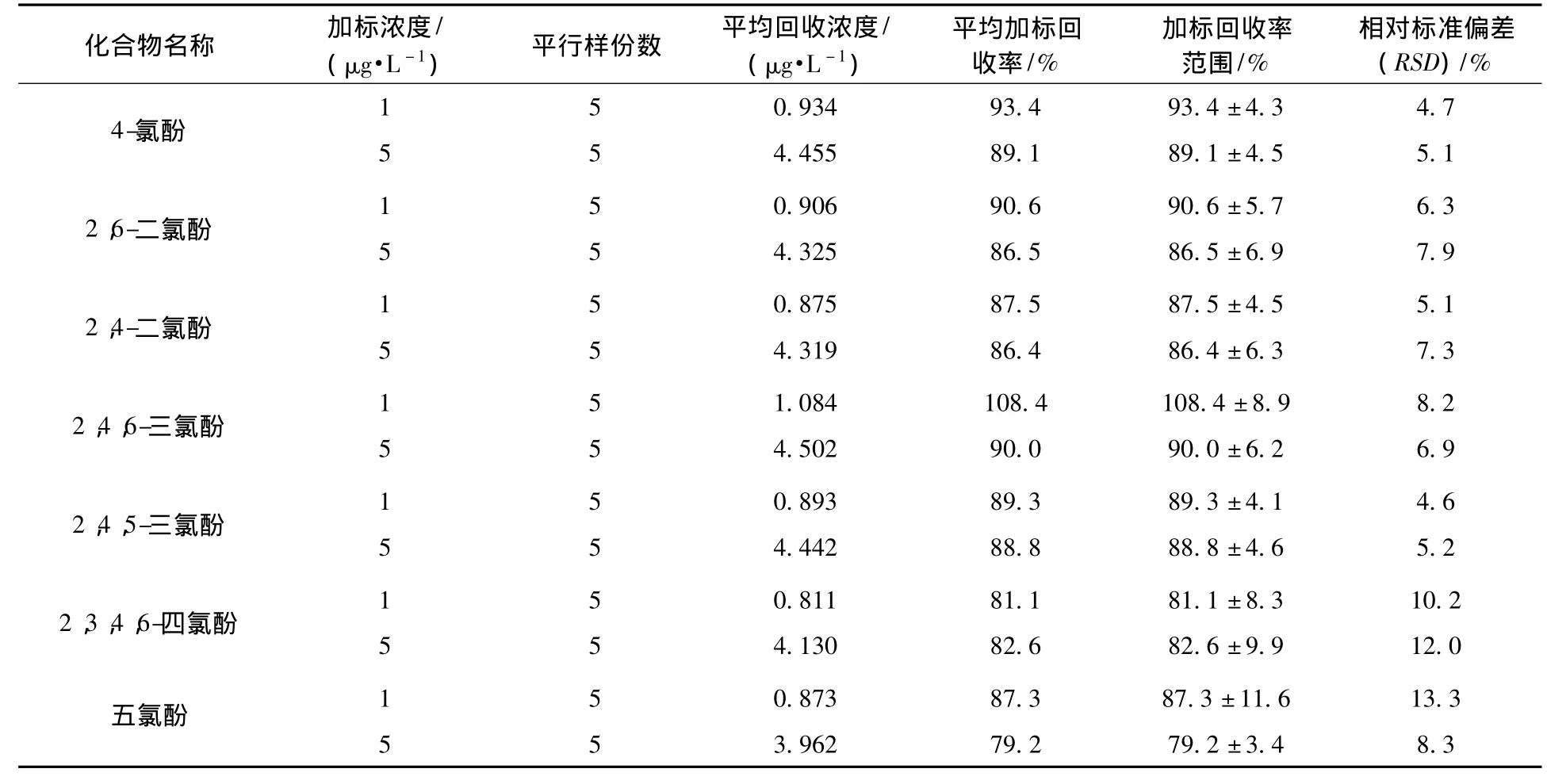
表4 各氯酚类化合物的加标回收率及其相对标准偏差
高、低浓度水平的加标样品各随机选取1个,分别重复进样6次,一周后再分别重复进样6次,各氯酚类化合物的精密度及其相对标准偏差,如表5所示。
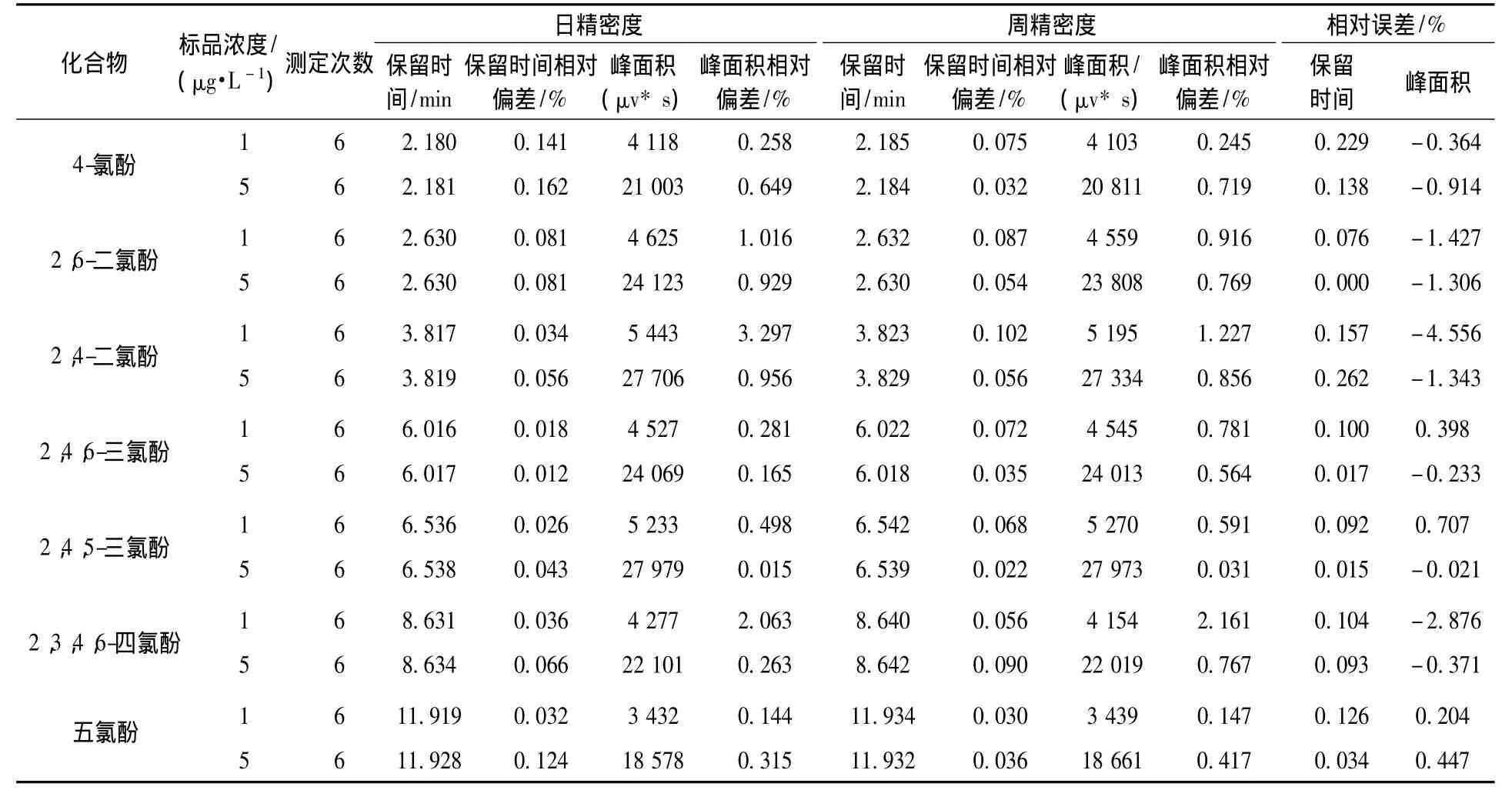
表5 各氯酚类化合物的精确度及其相对标准偏差
2.7 实际水样测定
对江西省6个地级市自来水厂取水口(A~F)水样中氯酚类化合物的检测。样品于2014年4月初采集后立即带回实验室分析,如表6所示,取水口处地表水均不同程度受到氯酚类化合物的污染,污染物为 4-氯酚、2,4,6-三氯酚、五氯酚,浓度范围分别为 ND ~0.101 μg/L、0.219~0.445 μg/L、ND ~ 0.181 μg/L。《地表水环境质量标准》(GB 3838—2002)规定,2,4,6-三氯酚、五氯酚的限值分别为0.2、0.009 mg/L,参照该标准,表明实测水样中氯酚类化合物含量较低,浓度远低于标准中规定限值。
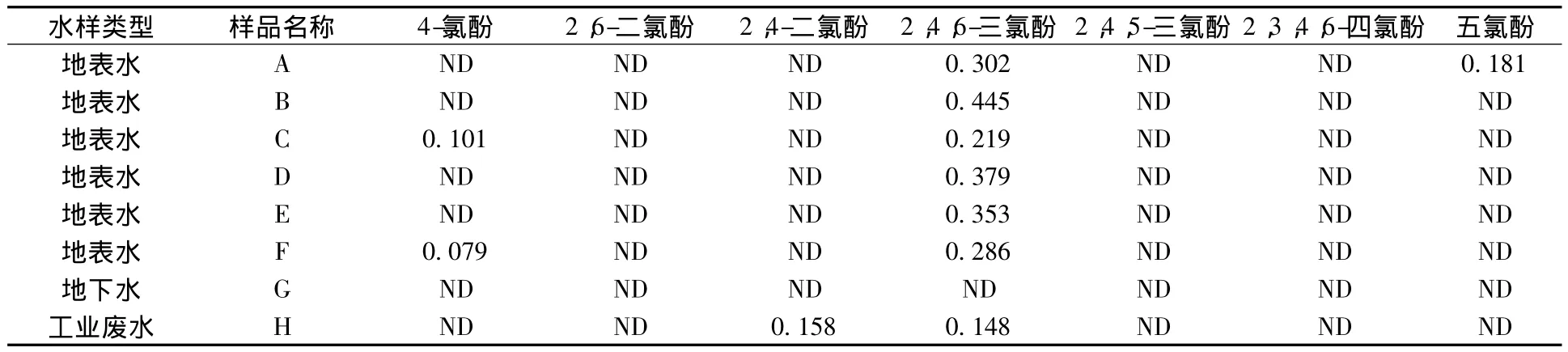
表6 集中式生活饮用水地表水源地水、地下水和工业废水中氯酚类化合物检测结果 μg/L
该方法同时应用于地下水和工业废水中氯酚类化合物的检测,结果表明,地下水中未检测到氯酚类化合物,工业废水中检出2,4二氯酚、2,4,6-三氯酚,浓度分别为 0.158、0.148 μg/L;由于样品基数少,加上工业废水成分复杂多变,能否应用于地下水和工业废水检测还有待进一步验证。
3 结论
用固相萃取法富集水样,以丙酮和二氯甲烷为洗脱液,甲醇-水溶液(含0.2%乙酸)为流动相的固相萃取-超高效液相色谱法,能够同时检测水体中7种氯酚类化合物,具有良好的线性相关性、准确度、精密度。当萃取体积为1 L,浓缩至1 mL,进样量为5 μL时,方法检出限为12.7~32.1 ng/L,测定下限为 50.8 ~128.4 ng/L,平均加标回收率为79.2% ~108.4%,相对标准偏差为4.6%~13.3%。
该方法适用于地表水中氯酚类化合物的检测,具有一定的应用和推广价值;对2014年4月江西省6个地级城市集中式生活饮用水地表水源地水样中的氯酚类化合物进行检测,结果表明,水源地地表水中有检出氯酚类化合物,但其含量很低,远低于标准中规定限值。
[1]IPCS international programme on chemical safety:Health and safety guide No.19,pentachlorophenol[EB/OL].GENEVA,World Health Organization for the International Programme on Chemical Safaty,1989[2014-05-25].http://www.inchem.org/documents/hsg/hsg/hsg019.htm.
[2]GB 3838—2002 地表水环境质量标准[S].
[3]HJ 591—2010 水质 五氯酚的测定 气相色谱法[S].
[4]GB/T 5750.10—2006 生活饮用水标准检验方法-消毒副产物指标[S].
[5]国家环境保护总局.水和废水监测分析方法[M].4版.北京:中国环境科学出版社,2002.
[6]陈明,巢猛,刘建明.SPE-HPLC法测定水中2,4,6-三氯酚和五氯酚[J].供水技术,2008,2(3):57-58.
[7]苏燕,张赟,孟烱.液相色谱法同时检测水中四种氯酚和三种除草剂[J].给水排水,2009,35:53-55.
[8]张冬梅,陈忠林,杨磊,等.反相高效液相色谱法测定水中 2,4,6-三氯酚[J].中国给水排水,2011,27(4):94-96.
[9]Penalver A,Pocurull E,Borrull F,et al.Solid-phase microextraction coupled to high-performanceliquid chromatography to determine phenolic compounds in water samples[J].Journal of Chromatography A,2002,953:79-87.
[10]陈蚬朦,钟淑婷,甘凤娟,等.超高效液相色谱串联质谱分析饮用水中2,4,6-三氯酚和五氯酚的方法研究[J].中国卫生检验杂志,2008,18(12):2 463-2 366.
[11]Alonso M C,Puig D,Silgoner I,et al.Determination of priority phenolic compounds in soil samples by various extraction methods followed by liquid chromatographyatmospheric pressure chemical ionisation mass spectrometry[J].Journal of Chromatography A,1998,823(2):231-239.
[12]杨秋红,程小艳,杨坪.固相萃取-高效液相色谱串联质谱法同时检测地表水种的 2,4-氯酚、2,4,6-三氯酚和五氯酚[J].分析化学研究报告,2011,39(8):1 208-1 212.
[13]李晓晶,黄聪,于鸿,等.液相色谱串联质谱直接进样测定饮用水中氯酚[J].中国卫生检验杂志,2013,23(3):619-621.
[14]Sarrion M N,Santos F J,Moyano E,et al.Solid-phase microextraction liquid chromatography/tandem mass spectrpmetry forthe analysisofchlorophenolsin environmental samples[J].Rapid Commun Mass Spectrom,2003,17:39-48.
[15]薛凤丽,李岩,杨瑞强,等.SPME-HPLC法测定水中的酚类化合物[J].中国给水排水,2006,22(16):81-83.
[16]廖林川,颜有仪,林岚,等.高效液相色谱法检测生物样品中五氯酚[J].四川大学学报:医学版,2004,35(3):427-428.
