腰椎退行性变的经皮椎弓根螺钉固定结合微创腰椎间融合术治疗
2015-04-25何二兴郭倞崔基浩郭志勇尹知训李创唐程何贻骞刘成伟
何二兴 郭倞 崔基浩 郭志勇 尹知训 李创 唐程 何贻骞 刘成伟
腰椎融合术广泛应用于各种腰椎退行性疾患的治疗,椎弓根螺钉固定结合椎体间融合是目前最常用的固定组合。常规的椎弓根螺钉固定术需要将脊柱两旁肌肉较大范围剥离、牵开,其造成的损伤以及椎管减压、椎体间植骨融合过程中对神经的牵拉和脊柱原有稳定性的破坏已经越来越受到重视[1-3]。近年出现的经皮置入的椎弓根螺钉固定技术对肌肉的创伤很小,其中经皮置入的长臂椎弓根螺钉造成的创伤最小,结合各种微创腰椎间融合术 ( minimally invasive lumbar interbody fusion,mini-lif ) 方法,能明显减少腰椎融合术的入路创伤[4-6]。回顾性分析2012 年 11 月至 2014 年 8 月,我院行经皮椎弓根螺钉固定结合 mini-lif 手术治疗 127 例腰椎退行性病变患者,探讨该术式治疗腰椎退行性病变的技术要点和初步疗效,报告如下。
资料与方法
一、一般资料
本组 127 例,其中男 86 例,女 41 例,年龄18~79 岁,平均 58.4 岁。所有患者均有不同程度腰、骶部酸痛,单侧 / 双侧下肢麻木感和 ( 或 ) 下肢放射性疼痛、间歇性跛行,病程 3~118 个月。所有患者均为接受过正规保守治疗后无明显疗效者。术前行腰椎正侧位、过屈过伸位 X 线和腰椎 MRI 检查,判断椎间盘突出部位、程度及椎管狭窄情况。I 度腰椎滑脱 16 例,腰椎间盘突出症 35 例,腰椎管狭窄症 76 例。L3~4间隙 6 例,L4~5间隙 54 例,L5~S1间隙 31 例,L3~4、L4~5双间隙 8 例,L4~5、L5~S1双间隙 21 例,L3~4、L4~5、L5~S1三间隙7 例。随访时间 3~21 个月,平均 6.9 个月。
二、手术器材和工具
螺钉:椎弓根螺钉是中空设计 ( 大博颖精医疗器械有限公司,厦门,中国 ),可同时作为骨水泥灌注导向管,钉头万向,U 型钉头比普通螺钉长,有 5 cm 和 7 cm 两种长度,螺钉销芯用于螺钉植入椎弓根后插入中空部,增加螺钉强度 。连接棒:有不同长度规格,分直棒和预弯棒,一端成圆锥形,另一端加工有 3 个平面,与持棒器相适应,上面有一刻度,便于弯棒时确认方向。弯棒器:弯棒部分与普通弯棒器无异,但在侧面多了一个方向控制器,后者通过连接棒的 3 个平面结构控制弧度的弯曲方向。
微创椎间撑开工具:宽 8 mm,厚度规格:3 mm、6 mm、9 mm 和 11 mm。
融合器:peek 材料,专门从厂家定制,宽度8 mm,前端呈子弹头形状,有不同规格的长度和高度。
三、手术方法
1. mini-lif:根据术前诊断和病理特点,决定椎管入路方式和减压范围。( 1 ) 椎板间开窗减压入路( minimally invasive posterior lumbar interbody fusion,mini-plif ) ( 44 例 ):适于中央型椎间盘突出、中央管狭窄症。于关节突与椎板结合部投影处插入探子,探触明确位置无误后切开皮肤,长约 3~4 cm,用扩张器逐级扩大分离肌肉纤维,用 Caspar 微拉钩牵开软组织、暴露椎板间隙;行椎板间开窗并处理椎管内病变,清理椎间盘组织及终板软骨,将减压截下来的骨组织与异体骨组织混合植入间隙内,最后植入宽度 8 mm 的椎间融合器 (图 1);( 2 ) 关节突切除减压入路 ( minimally invasive transforaminal lumbar interbody fusion,mini-tlif ) ( 49 例 ):采用Wiltse 肌肉间隙入路,切开皮肤后分离多裂肌和最长肌间隙,暴露小关节,行关节截除进入椎管,后续处理与 mini-plif 相同 (图 2);( 3 ) 椎板关节突同时截骨减压或椎板间节段性截除减压 ( 扩大减压融合术 ) ( 34 例 ):将单侧严重内聚、肥厚的关节突以及椎板黄韧带附着点以下部分一起截除减压,必要时将截骨延伸至对侧或经正中切口行两侧截骨减压(图 3)。椎间隙明显狭窄的处理:清理椎间盘组织后,用微创椎间撑开器逐级击入间隙内进行撑开,恢复至 9 mm 以上即可。椎间隙内植骨并植入单枚椎间融合器。

图1 椎板间开窗减压入路( mini-plif ) a~b:术前 MRI示 L4~5 椎间盘中央型突出、椎管中央型狭窄;c~d:行mini-plif 结合经皮长臂椎弓根螺钉固定术,术后 6 个月X 线片示内固定位置良好,椎间植骨位置良好Fig.1 Intra-laminae fenestration and decompression approach ( mini-plif ) a-b:Preoperative MRI showed L4-5 central disc herniation and vertebral canal stenosis; c-d: Mini-plif combined with percutaneous long-arm pedicle screw fixation was performed, postoperative 6-month X-ray films showed good position of internal fixation and interbody graft MRI showed L5-S1 left-side disc herniation and left intravertebral foramen stenosis; c-d: Mini-tlif combined with percutaneous long-arm pedicle screw fixation was performed, postoperative 12-month X-ray films showed good position of internal fixation and interbody graft

图3 椎板关节突同时截骨减压或椎板间节段性截除减压 ( 扩大减压融合术 ) a~b:术前 MRI 示 L3~5 椎管弥漫性狭窄、关节突严重内聚,椎板沟极小;c~d:行扩大减压融合术结合经皮长臂椎弓根螺钉固定术,术后 9 个月 X 线片示内固定位置良好,椎间植骨位置良好Fig.3 Simultaneous lamina and facet joint resection and decompression or intra-laminae segmental resection and decompression ( extended decompression and fusion ) a-b: Preoperative MRI showed L3-5 diffuse stenosis of vertebral canal, severe coherence of facet joints and extremely small laminar groove; c-d: Extended decompression and fusion combined with percutaneous long-arm pedicle screw fixation was performed,postoperative 9-month X-ray films showed good position of internal fixation and interbody graft
2. 经皮椎弓根螺钉固定术:以邻近棘突作为参考点,通过棘突上缘的水平线,结合术前 X 线片测量椎弓根旁开后正中线的距离,基本能确定椎弓根在皮肤上的投影位置;根据患者椎旁软组织厚度、目标椎弓根的头尾倾角选择好皮肤进入点。点状切开皮肤,插入直径 3 mm 的探子,按既定的方向进入直至找到骨性结构,探明小关节与横突结合部。切开皮肤,长约 18 mm,用扩张器扩大软组织通道直至能插入工作通道。改用穿刺针,循通道插入至骨性结构,找到关节突横突结合部进入点,将针在骨质内推进,多数情况可以感受到针在松质骨内。根据需要随时使用 C 型臂透视调整、监控进针过程。几个关键点有助于判断穿刺针位置是否正确:正位影像中入针点应在椎弓根投影的外侧缘或紧邻其外侧的假想第二投影的中心,此进入点即 Wiesner 进入点;侧位影像中穿刺针与椎弓根走向一致,延长线经过椎弓根中部;当进入至椎弓根全长,即侧位影像显示穿刺针经过椎弓根中部,针尖达到椎体后缘,此时,正位影像显示穿刺针尖端刚好在椎弓根内侧缘上。拔出穿刺针针芯,插入导针,导针要比穿刺针尖深 0.5~1.0 cm。拔出穿刺针,套上空心丝锥攻丝后,沿着导针置入适合的螺钉。如果出现植入椎弓根的穿刺针方向有轻度偏差,但椎弓根进入点正确,可通过下述方法调整:拔出穿刺针,沿导针插入锥形扩孔器并旋入约 1 cm,拔出导针,将扩孔器稍退出,根据需要调整锥形扩孔器,沿正确方向继续进入约 10 mm,将导针重新插入扩孔器内,超过扩孔器深约 10 mm。取出扩孔器,继续螺钉置入过程。椎弓根螺钉置入完毕后,选择适合长度连接棒,按腰椎生理弧度折弯后装棒固定,折断长臂。减压窗口内留置负压引流管,冲洗创口,逐层缝合。
四、术后处理
术后给予抗感染、脱水、镇痛等对症治疗;下床活动不限,据患者状态而定。出院前摄 X 线正侧位片。
五、观测指标
记录手术时间、X 线曝光次数、术中及术后出血量、术前及术后 3 天、2 周、3 个月视觉模拟评分 ( visual analogue scale,VAS ) 和 Oswestry 功能障碍指数 ( oswestry disability index,ODI ) 评分、住院时间、螺钉位置以及并发症发生率。术中分步透视,螺钉位置判断标准:( 1 ) 位置良好:正位像螺钉内倾角度合适、钉尖未超过椎体左右平分线;侧位像螺钉头紧贴小关节,螺钉中轴线位于椎弓根中轴线上并达椎体前 1 / 3 ( 图 4a~b );( 2 ) 位置尚可:正位像螺钉内倾、钉尖未超过椎体左右平分线,侧位像螺钉头紧贴小关节,螺钉中轴线平行于椎弓根中轴线,或与椎弓根中轴线成轻微角度,但仍在椎弓根上下缘之间并达椎体前 1 / 3 ( 图 4c~d );( 3 ) 位置不良:未达上述标准者 ( 图 4e~f )。
六、统计学分析
采用 SPSS 13.0 软件进行统计学分析,所得数据以表示,术前、术后比较采用配对t检验,三组间比较采用单因素方差分析 ( ANOVA ),P<0.05为差异有统计学意义。
结 果
手术时间 98~317 min,平均 ( 135.0±24.0 ) min;其中每颗椎弓根螺钉的置入时间为 8~44 min,平均 ( 12.6±6.3 ) min;每个减压节段的减压融合时间为 26~95 min,平均 ( 42.3±92.6 ) min;放入负压引流及关闭创口的时间为 9~35 min,平均 ( 15.8±4.3 ) min。每颗椎弓根螺钉的 X 线曝光次数为 2~14 次,平均 ( 4.2±2.3 ) 次。每个减压节段的术中出血量为 50~120 ml,平均 ( 67.9±16.7 ) ml。术后引流量为 15~105 ml,平均 ( 52.6±13.8 ) ml。三组患者术后 VAS 评分与术前相比显著降低 (P<0.05 )(表1)。此外,三组患者的术后 ODI 也均较术前有显著改善,差异有统计学意义 (P<0.05 ) (表2)。住院天数为 6~21 天,平均 ( 9.0±2.4 ) 天。共置入椎弓根钉 635枚,其中位置良好 546枚( 86.0% ),位置一般 71枚( 11.2% ),位置不良 18枚( 2.8% );10枚( 1.6% ) 螺钉内倾角过大,3枚( 0.5% ) 偏上、5枚( 0.8% ) 偏下。术中神经损伤 6 例 ( 4.7% ):mini-plif 组 2 例,mini-tlif 组 3 例,扩大减压融合组1 例。所有患者在治疗后 4 周至半年内完全恢复,未发生脑脊液漏、血肿、伤口感染等并发症。
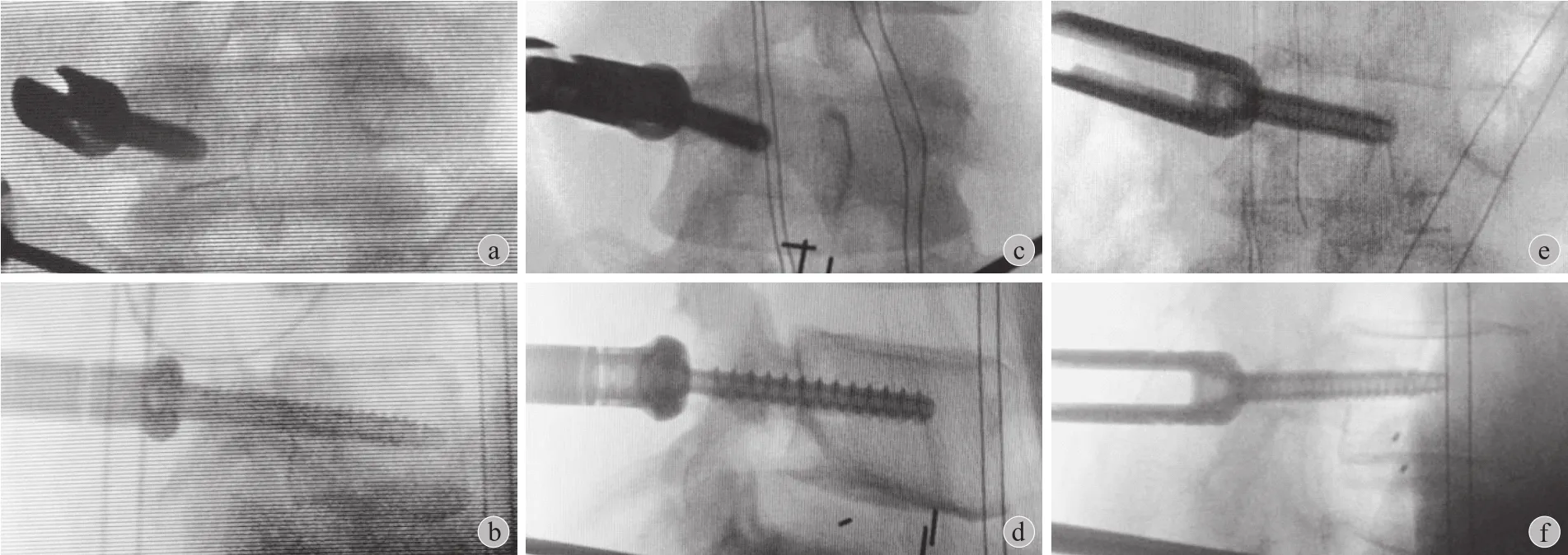
图4 术中透视判断螺钉位置 a~b:螺钉位置良好:正位像螺钉内倾角度合适、钉尖未超过椎体左右平分线;侧位像螺钉头紧贴小关节,螺钉中轴线位于椎弓根中轴线上并达椎体前 1 / 3;c~d:螺钉位置尚可:正位像螺钉内倾、钉尖未超过椎体左右平分线,侧位像螺钉头紧贴小关节,螺钉中轴线平行于椎弓根中轴线,或与椎弓根中轴线成轻微角度,但仍在椎弓根上下缘之间并达椎体前 1 / 3;e~f:螺钉位置不良:达不到上述标准者Fig.4 Intraoperative fluoroscopy for judgment of screw position a-b: Good screw position: on anteroposterior view, screw convergent angle was appropriate, screw tip did not pass across bisection line of vertebral body; on lateral view, screw head was seated on facet joint, screw axis was superpositioned with pedicle axis, screw tip reached anterior 1 / 3 of vertebral body; c-d: Acceptable screw position: on anteroposterior view, screw convergent angle was a little bit large, screw tip did not pass across bisection line of vertebral body; on lateral view, screw head was seated on facet joint, screw axis was superpositioned or slightly angled with pedicle axis, but still within the superior and inferior edges of pedicle, screw tip reached anterior 1 / 3 of vertebral body; e-f: Misplaced screw position: screws did not fit with above mentioned criteria
表1 三组患者术前、术后 VAS 评分 (±s)Tab.1 Pre- and postoperative VAS scores in three groups (±s)
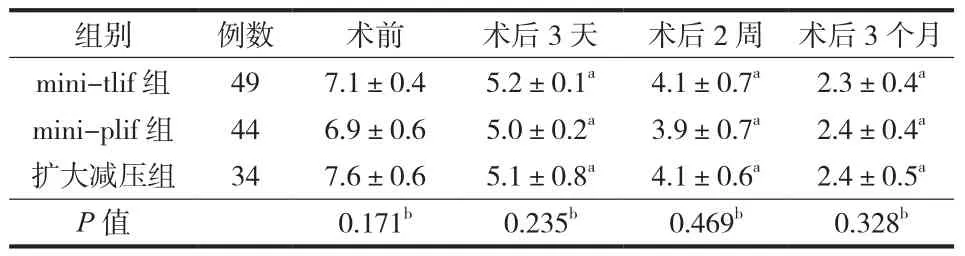
表1 三组患者术前、术后 VAS 评分 (±s)Tab.1 Pre- and postoperative VAS scores in three groups (±s)
注:a与术前比较,差异有统计学意义 (P < 0.05 );b三组间比较,差异无统计学意义 (P > 0.05 )Notice: aCompared with preoperation, differences had statistical significance(P<0.05 ); bCompared among three groups, differences had no statistical significance (P>0.05 )
组别 例数 术前 术后 3 天 术后 2 周 术后 3 个月mini-tlif 组 49 7.1±0.4 5.2±0.1a 4.1±0.7a 2.3±0.4a mini-plif 组 44 6.9±0.6 5.0±0.2a 3.9±0.7a 2.4±0.4a扩大减压组 34 7.6±0.6 5.1±0.8a 4.1±0.6a 2.4±0.5a P 值 0.171b 0.235b 0.469b 0.328b
表2 三组患者术前、术后 ODI 评分 (±s)Tab.2 Pre- and postoperative ODI scores in three groups (±s)
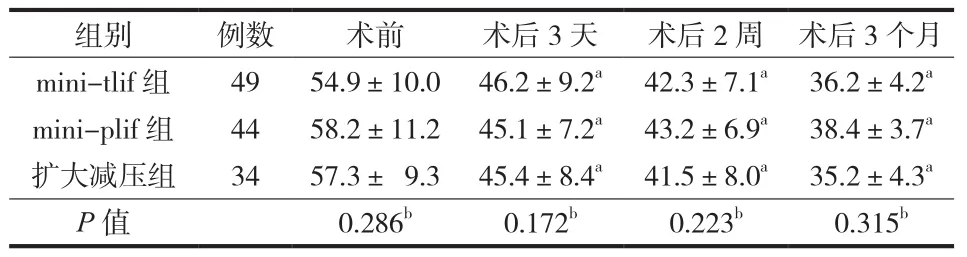
表2 三组患者术前、术后 ODI 评分 (±s)Tab.2 Pre- and postoperative ODI scores in three groups (±s)
注:a与术前比较,差异有统计学意义 (P < 0.05 );b三组间比较,差异无统计学意义 (P > 0.05 )Notice: aCompared with preoperation, differences had statistical significance(P<0.05 ); bCompared among three groups, differences had no statistical significance (P>0.05 )
组别 例数 术前 术后 3 天 术后 2 周 术后 3 个月mini-tlif 组 49 54.9±10.0 46.2±9.2a 42.3±7.1a 36.2±4.2a mini-plif 组 44 58.2±11.2 45.1±7.2a 43.2±6.9a 38.4±3.7a扩大减压组 34 57.3± 9.3 45.4±8.4a 41.5±8.0a 35.2±4.3a P 值 0.286b 0.172b 0.223b 0.315b
讨 论
腰椎间融合术是治疗腰椎退行性疾病的经典手术方式。坚强的内固定保证了脊柱稳定性,为椎间融合创造了条件,使患者术后可以早期下床活动,并且能够明显缓解腰腿疼痛等症状。然而,传统腰椎间融合手术需要广泛剥离及长时间牵拉椎旁肌肉,容易造成软组织损伤,导致术后腰部力量减弱及慢性腰痛发生[7]。近年来,随着脊柱外科微创技术的迅猛发展,用于腰椎椎间融合的微创技术应运而生。该技术避免了大范围的肌肉等软组织剥离、神经组织牵拉,具有减少术中出血、缩短住院时间等优势,得到了较普遍关注;同时患者术后疼痛轻、恢复快,有利于患者的早日康复[8-9]。目前,临床上应用最广泛的微创椎间融合技术包括 mini-plif和 mini-tlif。
mini-plif 技术在减压彻底的同时,对脊柱后柱结构的损伤较小,对脊柱的稳定性影响小。但术中须牵拉硬脊膜和神经根,易导致硬脊膜、神经根和马尾神经的损伤,增加了硬脊膜瘢痕粘连形成的可能性。Park 等[10]对比研究了 mini-plif 与开放plif 的临床疗效,发现 mini-plif 组在术中失血和术后输血、术后腰痛、康复时间、住院时间方面优于开放组,但 mini-plif 组手术时间长于开放组,差异有统计学意义;术后随访期间临床症状改善及影像学结果两组没有明显差别;两组均有 1 例术后不融合。mini-tlif 为关节突切除减压经椎间孔入路,可避免后路手术牵拉神经根及硬膜囊所致的损伤,经后方一侧入路即可完成椎间融合;保留前方韧带和后方大部分韧带,避免椎板切除和对椎管内结构的干扰。但其对椎管后方减压较受限,并且无法显露和直接减压对侧椎间孔和神经根管。Peng 等[11]对mini-tlif 和开放 tlif 患者术后随访 2 年,发现两组患者的腰痛及下肢症状均较术前明显改善,两种术式的改善程度没有显著性差异;两组患者术后椎间融合率方面差异无统计学意义;开放组并发症的发生率为 13.8%,mini-tlif 组并发症的发生率为 6.9%,差异有统计学意义。总的来说,mini-plif 和 mini-tlif的临床疗效可靠,可取得优于或不低于开放腰椎融合术的效果,值得临床应用。
腰椎间盘突出和椎管狭窄患者的疼痛绝大部分是神经受压所致,减压是解除疼痛的重要步骤[4]。mini-lif 手术可以通过以下环节达到减压目的:( 1 )直接移除压迫神经的组织,如突出的椎间盘、增生肥厚的关节突、黄韧带等;( 2 ) 扩大、恢复神经根管道容积,如撑开狭窄的椎间隙、恢复腰椎的生理曲线;( 3 ) 通过融合、固定实现局部组织萎缩、消肿[8]。前者称为直接减压,后两者可称为间接减压。手术前应认真分析每一位患者的病理特点,有针对性选择减压融合方式,尤其重要的是明确直接减压中需要截除骨性组织的部位和范围,防止手术扩大化。
使用经皮螺钉固定的椎间融合术,一般需要先行 mini-lif,因为螺钉置入后牵开肌肉暴露困难。lif手术方式应该根据病变特点来定[8]。一般认为,单侧 mini-tlif 对处理椎管外侧病变较方便,适于极外侧或外侧型椎间盘突出、单侧侧隐窝狭窄、单纯腰椎不稳、腰椎滑脱等;单侧 mini-plif 适于中央型椎间盘突出特别是与纤维环有粘连者、中央管狭窄或弥漫型椎管狭窄[8]。对于关节突严重内聚、肥厚的情况,此时椎板沟常在 3 mm 以内或完全消失,就要进行椎板及关节突同时截骨减压的扩大减压术,不要苛求区分 plif 或 tlif 术式名称。
行 mini-tlif 时,采用 Wiltse 肌肉间隙入路,mini-plif 采用经多裂肌入路。扩大减压术中的后正中入路需要剥离椎旁肌,但因狭窄内聚的椎管横径较小,对椎旁肌肉牵拉损伤不会很大,手术经验丰富的术者,仍然可以实现微切口下完成。本组患者3 种术式手术后 VAS、ODI 评分的改善没有显著差别,说明只要手术适应证掌握好,3 种方法无优劣之分。只有 4.7% 的患者出现神经牵拉伤,随访时全部患者得到临床恢复。文献报道开放椎间融合手术神经损伤发生率为 5.8%~7.9%[12-13];相比本研究mini-lif 术式略高。
微创融合术的基本原则是精准减压、有限暴露,因此操作空间较小。过大的融合器不但要求暴露范围大,置入时对神经的牵拉损伤机会也多。所以,最好使用宽度较小的融合器。至于在使用经皮椎弓根螺钉固定的情况下,要使用多大的融合器才能满足植骨成活和日常活动所需的力学稳定性,目前尚未见相关的研究报道;但人们一直探索固定器材最小而且能满足稳定要求的固定方法[14-15]。本组病例使用的宽度为 8 mm、头端呈子弹头型的融合器,在置入时较方便、安全,无须对神经过度牵拉。术中未见置入失败和神经损伤。随访期间未见椎间塌陷、螺钉断裂等,仅 1 例术后 4 周出现融合器后移 3 mm,未造成神经受压,考虑是螺钉加压不够所致。
螺钉经皮置入技术无须剥离椎旁肌,只是将肌间或肌束间分离扩张形成直径 18 mm 的小孔道,置棒也是穿过肌束间隙完成,术后孔道、间隙自然闭合,肌肉复回原位,与常规手术比较,创伤明显减少,术后疼痛轻微,恢复快[16]。常规腰椎融合术中腰背肌的损伤主要发生在开放椎弓根螺钉固定术这一环节。术中要暴露相邻两个椎弓根螺钉进入点,常常需要将椎旁肌从椎板剥离并长时间向外侧牵开4~5 cm,除了剥离伤之外,肌肉内压增高、血液循环受影响,患者术后腰背肌功能恢复欠佳[2,9,17-18]。
大部分置钉是在 C 型臂 X 线机引导下完成,如何提高置钉效率和准确性,减少射线暴露是目前亟须解决的问题。经皮椎弓根螺钉固定术最花时间、X 线透视最多的环节是寻找椎弓根进入点,其次是穿刺方向的调整[19]。常规使用的 Wiesner[20]透视穿刺技术,术前先透视,在皮肤标记好椎弓根影的位置,然后根据此标记确定皮肤切口及穿刺针进入点,但是,术中经常会出现皮肤和标记点较大幅度的移位,导致进针位置不良;另外,直接用穿刺针寻找椎弓根螺钉进入点会遇到软组织阻力大、手感不好的情况。为此,笔者对穿刺技术进行一些改进:( 1 ) 以棘突上缘和后正中线作原始参考,推测椎弓根在皮肤的投影。这两处不受术中操作对皮肤牵拉移动的影响,准确性高;( 2 ) 穿刺前先用的探子探触查找螺钉进入点,探子较穿刺针粗且硬,感觉传递清晰,正确率高;( 3 ) 穿过合适的皮肤切口和扩大的软组织通道,穿刺针是在无软组织阻力状态下操作,提高了进针点及进针方向的准确率。笔者使用两侧同时穿刺置钉,每颗螺钉置入时间平均为 ( 12.6±6.3 ) min,置入的 635枚椎弓根钉中,位置良好达 546枚( 86.0% ),这样的水平与开放置钉术相仿[21-22]。
术中使用的分步透视法,能及时发现和更正穿刺针的位置和方向。而且,这种方法比起术后摄正侧位 X 线片,对螺钉位置的判断更加准确。术者要熟悉每个患者的影像解剖特点,由于术中很难获得完全标准的图像,所以要将正位与侧位图像结合分析才能得出正确的判断。与早期使用常规技术相比,用改进后的穿刺方法,大大缩短穿刺时间、准确率明显提高[23]。
目前用于经皮置入的螺钉尾段设计有 3 种类型:延长管装置、牵开器装置和加长螺钉 U 型臂[16,22,24]。螺钉的设计不断改善。本组患者使用的长臂螺钉尾端 U 型臂长只有 5 cm 或 7 cm,置入后露出皮肤的长度绝大多数<4 cm,置入后螺钉尾段可摆动,不妨碍相邻椎弓根穿刺、置钉操作;安装连接棒时容易通过 U 型口看到棒是否正确穿过。这些特点比起使用延长管装置的经皮螺钉有明显的优势。
本组病例手术时间平均为 ( 135.0±24.0 ) min。并发症发生率低,随着手术技术的熟练,术中 X 线曝光次数明显减少。每个减压节段术中出血量平均为 ( 67.9±16.7 ) ml,明显少于开放手术。术后疼痛较轻,无 1 例使用镇痛泵,仅需口服消炎镇痛药。并且 VAS 和 ODI 评分术后 2 周时已明显降低。上述结果均表明经皮椎弓根螺钉固定术结合 mini-lif 治疗腰椎退行性疾病是安全及有效的。
[1] Styf JR, Willen J. The effects of external compression by three different retractors on pressure in the erector spine muscles during and after posterior lumbar spine surgery in humans.Spine, 1998, 23(3):354-358.
[2] Kawaguchi Y, Yabuki S, Styf J, et al. Back muscle injury after posterior lumbar spine surgery. Topographic evaluation of intramuscular pressure and blood flow in the porcine back muscle during surgery. Spine, 1996, 21(22):2683-2688.
[3] Kim KT, Lee SH, Suk KS, et al. The quantitative analysis of tissue injury markers after mini-open lumbar fusion. Spine,2006, 31(6):712-716.
[4] Isaacs RE, Podichetty VK, Santiago P, et al. Minimally invasive microendoscopy-assisted transforaminal lumbar interbody fusion with instrumentation. J Neurosurg Spine, 2005, 3(2):98-105.
[5] Jang JS, Lee SH. Minimally invasive transforaminal lumbar interbody fusion with ipsilateral pedicle screw and contralateral facet screw fixation. J Neurosurg Spine, 2005, 3(3):218-223.
[6] Ringel F, Stoffel M, Stuer C, et al. Minimally invasive transmuscular pedicle screw fixation of the thoracic and lumbar spine. Neurosurgery, 2006, 59(4 Suppl 2):ONS361-367.
[7] Gejo R, Matsui H, Kawaguchi Y, et al. Serial changes in trunk muscle performance after posterior lumbar surgery. Spine,1999, 24(10):1023-1028.
[8] Foley KT, Holly LT, Schwender JD. Minimally invasive lumbar fusion. Spine, 2003, 28(Suppl 15):S26-35.
[9] Stevens KJ, Spenciner DB, Griffiths KL, et al. Comparison of minimally invasive and conventional open posterolateral lumbar fusion using magnetic resonance imaging and retraction pressure studies. J Spinal Disord Tech, 2006, 19(2):77-86.
[10] Park Y, Ha JW. Comparison of one-level posterior lumbar interbody fusion performed with a minimally invasive approach or a traditional open approach. Spine, 2007, 32(5):537-543.
[11] Peng CW, Yue WM, Poh SY, et al. Clinical and radiological outcomes of minimally invasive versus open transforaminal lumbar interbody fusion. Spine, 2009, 34(13):1385-1389.
[12] Mehta VA, McGirt MJ, Garcés Ambrossi GL, et al. Transforaminal versus posterior lumbar interbody fusion: comparison of surgical morbidity. Neurol Res, 2011, 33(1):38-42.
[13] Sakeb N, Ahsan K. Comparison of the early results of transforaminal lumbar interbody fusion and posterior lumbar interbody fusion in symptomatic lumbar instability. Indian J Orthop, 2013, 47(3):255-263.
[14] Kim DH, Jeong ST, Lee SS. Posterior lumbar interbody fusion using a unilateral single cage and a local morselized bone graft in the degenerative lumbar spine. Clin Orthop Surg, 2009,1(4):214-221.
[15] Moreland DB, Asch HL, Czajka GA, et al. Posterior lumbar interbody fusion: comparison of single intervertebral cage and single side pedicle screw fixation versus bilateral cages and screw fixation. Minim Invasive Neurosurg, 2009, 52(3):132-136.
[16] Foley KT, Gupta SK. Percutaneous pedicle screw fixation of the lumbar spine: preliminary clinical results. J Neurosurg,2002, 97(Suppl 1):S7-12.
[17] Bammer R. Basic principles of diffusion-weighted imaging.Eur J Radiol, 2003, 45(3):169-184.
[18] Kim DY, Lee SH, Chung SK, et al. Comparison of multifidus muscle atrophy and trunk extension muscle strength:percutaneous versus open pedicle screw fixation. Spine, 2005,30(1):123-129.
[19] Magerl FP. Stabilization of the lower thoracic and lumbar spine with external skeletal fixation. Clin Orthop Relat Res, 1984,(189):125-141.
[20] Wiesner L, Kothe R, Ruther W. Anatomic evaluation of two different techniques for the percutaneous insertion of pedicle screws in the lumbar spine. Spine, 1999, 24(15):1599-1603.
[21] Raley DA, Mobbs RJ. Retrospective computed tomography scan analysis of percutaneously inserted pedicle screws for posterior transpedicular stabilization of the thoracic and lumbar spine: accuracy and complication rates. Spine, 2012,37(12):1092-1100.
[22] Oh HS, Kim JS, Lee SH, et al. Comparison between the accuracy of percutaneous and open pedicle screw fixations in lumbosacral fusion. Spine J, 2013, 13(12):1751-1757.
[23] Weinstein JN, Rydevik BL, Rauschning W. Anatomic and technical considerations of pedicle screw fixation. Clin Orthop Relat Res, 1992, (284):34-46.
[24] Lieberman IH, Togawa D, Kayanja MM, et al. Bone-mounted miniature robotic guidance for pedicle screw and translaminar facet screw placement: Part I--Technical development and a test case result. Neurosurgery, 2006, 59(3):641-650.
