不同温度对甜瓜的蔗糖和乳酸通量的影响
2015-04-24王会松庞广昌刘婷婷
王会松,庞广昌,刘婷婷
(天津商业大学生物技术与食品科学学院,天津300134)
不同温度对甜瓜的蔗糖和乳酸通量的影响
王会松,庞广昌*,刘婷婷
(天津商业大学生物技术与食品科学学院,天津300134)
从代谢的角度讲,果蔬保鲜实际上是保证其存活的情况下降低它的分解代谢来达到延长货架期,代谢通量规律的深入研究会更好的实现这一目的。本实验以甜瓜为材料研究果蔬在贮藏过程中代谢网络通量规律。将甜瓜放置在10个不同温度(0、5、8、10、20、30、40、45、50、55℃),得到在不同温度下甜瓜不同部位糖酵解途径、TCA循环、蔗糖合成途径、戊糖磷酸途径的代谢通量。结果显示:8℃和50℃时蔗糖有较高的合成通量,乳酸也在8℃时有较高的代谢通量,所以8℃是较好的贮藏温度。这为从代谢的角度深入研究果实的贮藏,延长果蔬的贮藏寿命提供参考。
甜瓜,蔗糖,乳酸,代谢通量
关于果蔬贮藏保鲜,本质上就是在保证活体的情况下最大限度地降低分解代谢,延长生存期或寿命。目前最普遍有效的方法大致分为两种,即传统方法(冷藏保鲜和气调保鲜)和现代贮藏保鲜方法(减压贮藏[1]、热处理[2]和保鲜剂等)。其中温度的调节应用最广泛,并且越来越多的研究证明经热处理后的果实贮藏效果更佳[3-5]。温度对果蔬贮藏品质影响的研究越来越成熟,但是对于贮藏过程中温度对呼吸代谢的研究比较少。
糖分构成是影响果实品质的一个重要因子[6],尤其是蔗糖[7-9]。有研究表明,蔗糖等代谢物在甜瓜不同组织间的代谢分布有明显差异[10-11],并且这种差异对甜瓜的营养和感官品质有重大影响[12]。哈密瓜中蔗糖的含量会随贮藏时间和温度的升高而不断减少[11],在甜瓜的贮藏过程中控制蔗糖分解,降低糖类代谢消耗显得尤为重要。
在果蔬贮藏过程中,分解代谢产生的NADH+H+的氢质子和电子经递氢体和呼吸链传递给氧生成水,并通过氧化磷酸化提供能量。储藏过程中应减少呼吸消耗,将呼吸代谢控制在既能保证其生存,又能维持在最低水平。呼吸作用发生在线粒体中,当超过其呼吸能力或供氧不足时,NADH+H+只能在乳酸脱氢酶催化下,将氢质子交回丙酮酸生成乳酸。正是因为乳酸和NADH+H+这一偶联关系,以及乳酸的穿梭作用[13]使它在调节有机体细胞呼吸、氧化磷酸化、氧化还原状态以及合成与分解代谢中发挥关键作用[14-16]。已经有研究表明,乳酸在果蔬的贮藏保鲜中发挥重要作用[17]。关于乳酸和蔗糖的代谢通量分析已经应用到了哈密瓜的贮藏与保鲜中[18]。
本实验对不同温度下甜瓜不同部位的蔗糖和乳酸通量的变化情况进行研究,旨在寻找甜瓜在贮藏过程中代谢通量的变化规律,为进一步通过代谢分析,从甜瓜生命活动的本质方面延长货架期提供参考。
1 材料与方法
1.1 材料与仪器
甜瓜 天津甜瓜种植基地采摘后,选取无机械损伤、无病虫害、大小均匀、成熟度一致的优质甜瓜。
3K15高速冷冻离心机 美国Sigma公司;J2-21高速冷冻离心机 美国Beckman公司;HVE-50哈雅玛高压灭菌器 日本Hirayama Manufacturing公司;SBA-40C生物传感器分析仪 山东省科学院生物研究所;Fluoroskan Ascent FL荧光-化学发光检测仪 美国Thermo公司。
1.2 实验方法
1.2.1 样品制备 将甜瓜放于气调箱(25 cm×43 cm× 19.5 cm)中,气调比例[19]为5%O2+2%CO2。所有的样本气调条件是一致的。采用微型实验冷库控制温度,根据近些年国内外所研究的典型温度以及本实验室所做成果[18]作参照,将温度设置为0、5、8、10、20、30、40、45、50、55℃,气调贮藏24 h,仅仅贮藏24 h的目的是甜瓜在处理24 h之后达到了在该温度下的一种稳定的代谢状态。较高温度设置的目的是为了了解热处理时甜瓜的代谢情况,以期为后期的热处理提供参考。每个温度设3个平行,取出后按甜瓜中间部位2 cm厚沿赤道平面切开,从瓜皮向瓜心取样,将甜瓜分为外果皮、内果皮、外果肉、中果肉、内果肉5个部分,分别对应于图1[6]的1、2、3、4、5,用液氮迅速冷冻,在冰浴条件下研磨,匀浆后将匀浆液全部转移入离心管,以10000×g、4℃离心10 min,收集上清液,并于-80℃条件贮藏。

图1 甜瓜部位分割图Fig.1 The segmentation map of Cucumis melon
1.2.2 甜瓜乳酸和蔗糖代谢网络图的构建 根据代谢网络的研究方法及代谢网络的构建原则[20],本实验以甜瓜为研究对象,选择糖酵解、蔗糖合成途径、戊糖磷酸途径和TCA循环为主要代谢途径来构建代谢网络,将直线反应合并为一个反应,忽略不在研究范围内的代谢途径,减少代谢网络的反应数目,得到以下代谢网络图。
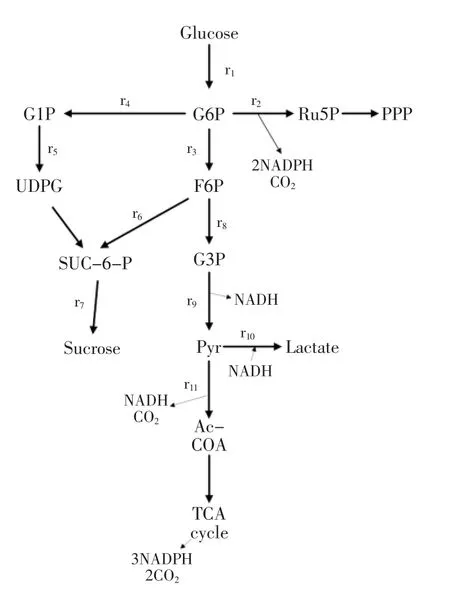
图2 蔗糖乳酸代谢网络图Fig.2 Sucrose and lactate metabolic network diagram

表1 代谢反应方程Table 1 Metabolic reaction
1.2.3 葡萄糖、蔗糖、乳酸和NADH浓度的测定 根据所建立的甜瓜代谢通量模型,测定的代谢速率有12个(表1),而由胞内中间代谢产物可以确定的质量平衡方程有8个(表2)。假设胞内中间途径代谢物处于拟稳态,即这8个途径代谢物没有积累,它们的质量平衡方程均为0,这样就可以得到8个约束向量。此时该系统的自由度F=4。而代谢产物系统中的NADH可通过实验测得,那么总约束向量变为9。通过实验测定葡萄糖的变化速率r1、蔗糖变化速率r7、乳酸的变化速率r10,已知速率为4个,此方程可以得到唯一解,进而通过计算方程得到蔗糖和乳酸的通量。
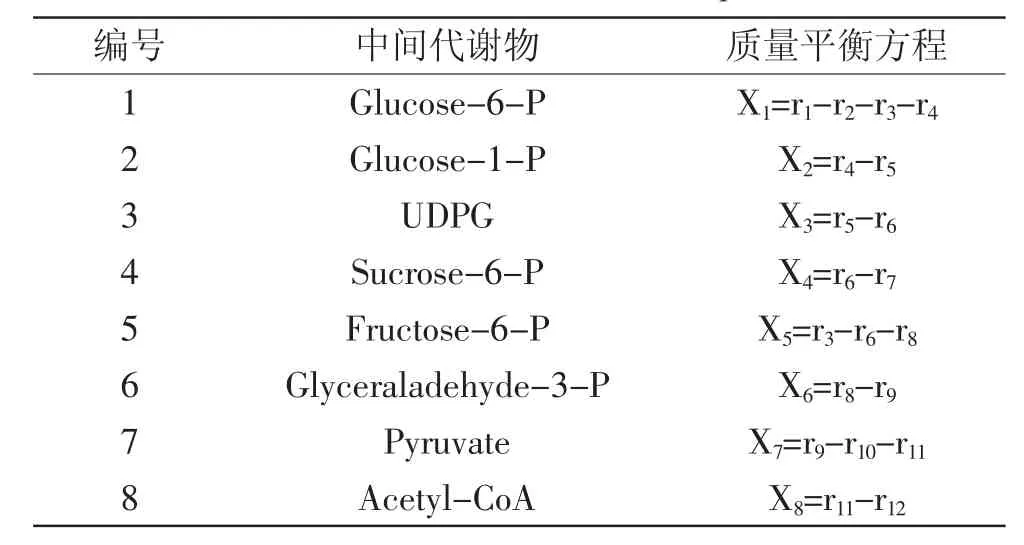
表2 甜瓜的质量平衡方程式Table 2 Metabolic flux model equation
运用SBA-40C型生物传感器分析仪测定出不同温度贮藏的哈密瓜不同部位中葡萄糖、蔗糖和乳酸的含量。之后分别对其进行时间微分,以测定出变化速率(单位:mg·mL-1·h-1),用于通量的计算。NADH的测定采用Fluoroskan Ascent FL荧光-化学发光检测仪,其原理采用酶法进行测定,参考Schaefer等[21-23]的研究,并进行了改进,其反应体系为(0.25 mmol/L HEPES/EDTA缓冲液,100 mmol/L KCl,10 mmol/L MgSO4,3 mmol/L 1,3-BPG,0.5 mmol/L DHAP,0.4 U/mL GAPDH)。

1.3 数据分析
使用Matlab 7.0软件以及SPSS 17.0 for windows软件计算。
2 结果与分析
2.1 代谢通量图
测得不同贮藏温度(0、5、8、10、20、30、40、45、50、55℃)甜瓜蔗糖、葡萄糖、乳酸变化速率,通过平衡方程,利用Matlab 7.0数据处理软件得到归一化后的甜瓜蔗糖和乳酸代谢通量图见图3~图7(图中数据对应的顺序为0、5、8、10、20、30、40、45、50、55℃)。从通量分布图可以看出相同样本在不同贮藏温度下的蔗糖和乳酸代谢通量明显不同,并且在同一温度下不同组织的蔗糖和乳酸代谢通量也有较大不同。
在内果肉中,0、8℃和40℃的条件下进入磷酸戊糖合成途径的通量较少,更多的流向糖酵解和蔗糖合成途径;其他温度进入磷酸戊糖途径的通量相对较多。从丙酮酸节点来看,较低温度(0℃和5℃)以及较高温度(55℃)进入TCA循环途径的通量较多,有氧呼吸较强,环境胁迫导致机体作出响应以适应周围恶劣的环境。

图3 甜瓜内果肉蔗糖、乳酸通量图Fig.3 Sucrose,lactic acid flux in Melon pulp 3
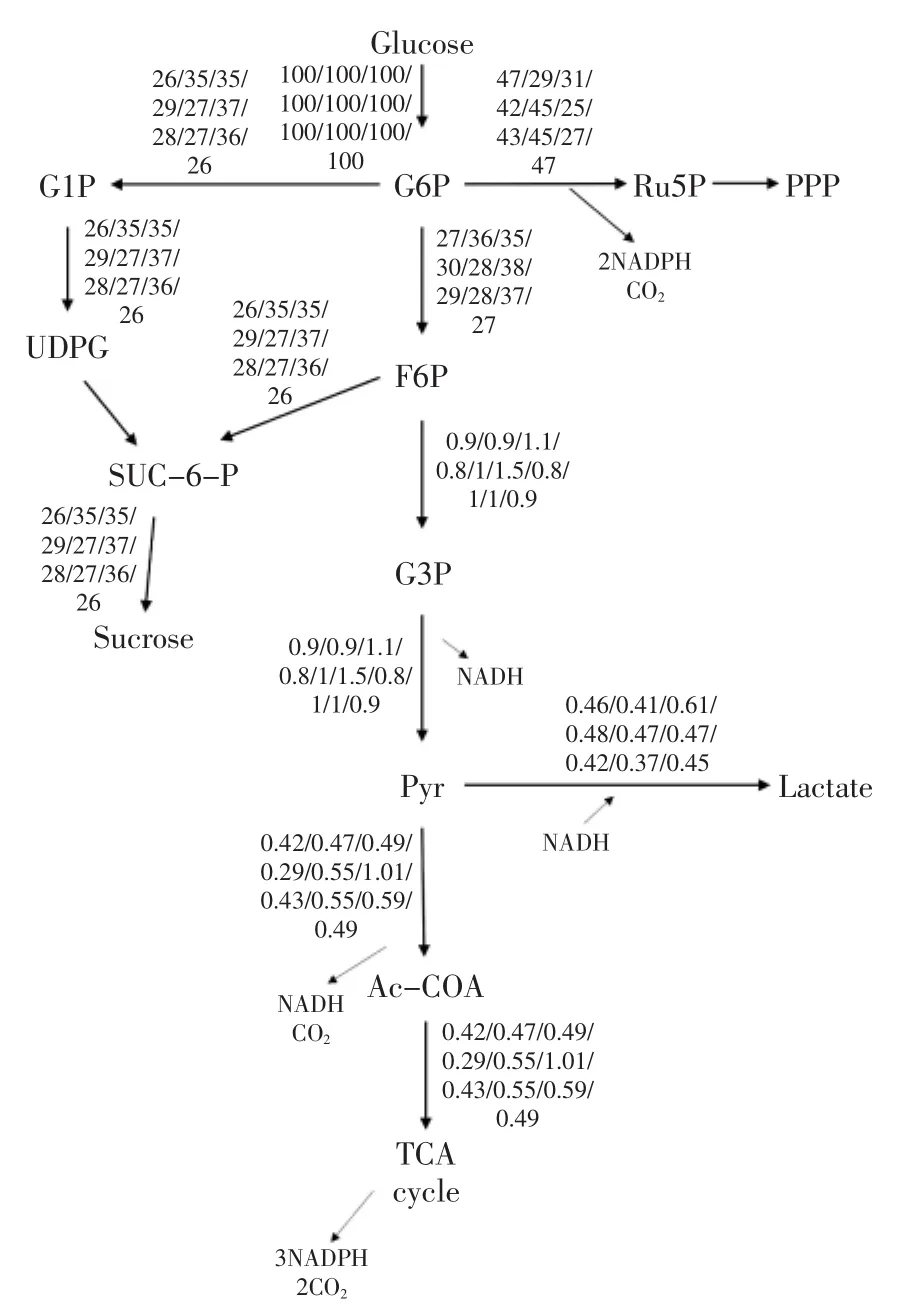
图4 甜瓜中果肉蔗糖、乳酸通量图Fig.4 Sucrose,lactic acid flux in Melon pulp 2
在中果肉中,5、8、30℃和50℃进入磷酸戊糖途径的通量较少,其他温度进入磷酸戊糖途径的通量接近葡萄糖通量的一半。就丙酮酸节点而言,10℃情况下进入TCA循环途径通量较少,这时候无氧呼吸大于有氧呼吸,而在45℃和50℃状态下有氧呼吸较强,高温使机体分解代谢增强。
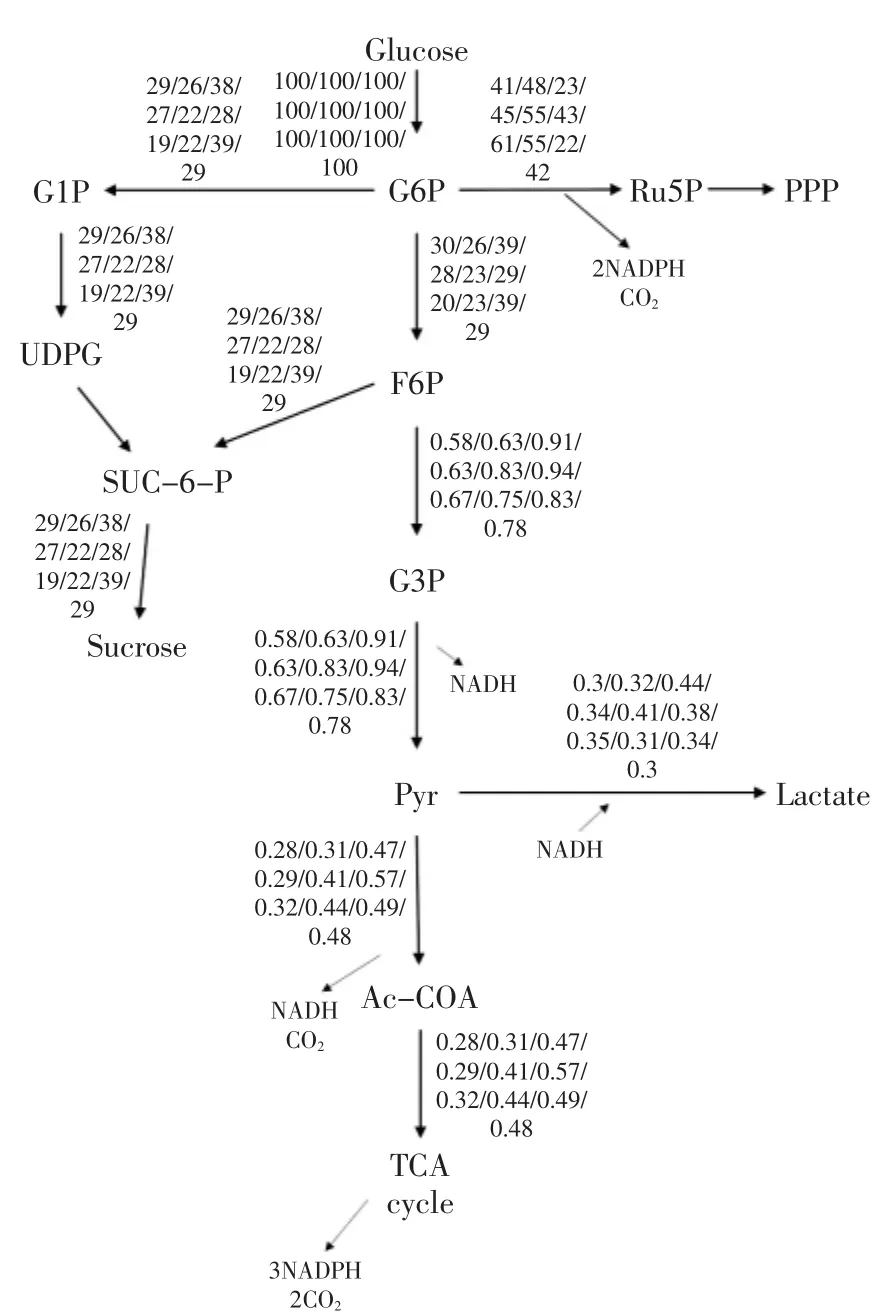
图5 甜瓜外果肉蔗糖、乳酸通量图Fig.5 Sucrose,lactic acid flux in Melon pulp 1
在外果肉中,8℃和50℃进入磷酸戊糖途径的通量较少,进入蔗糖途径的通量较多;其他的实验组磷酸戊糖途径通量随温度呈现波动的趋势。丙酮酸节点,低于45℃的实验组进入TCA循环的通量与进入乳酸的相差不大,而45~55℃之间进入TCA循环的通量较多,有氧呼吸较强,可能是随温度的升高机体的分解代谢随之增强。
在内果皮中,8、10℃和50℃三个温度下进入磷酸戊糖途径的较少,合成其他物质的通量降低,甚至在8℃时进入磷酸戊糖途经的通量是负的;而进入蔗糖合成的通量较多。而丙酮酸节点,0℃下进入TCA循环的通量非常大,有氧呼吸强度很大,在寒冷的环境下,机体通过提高分解代谢以应对环境对自身造成的损伤。
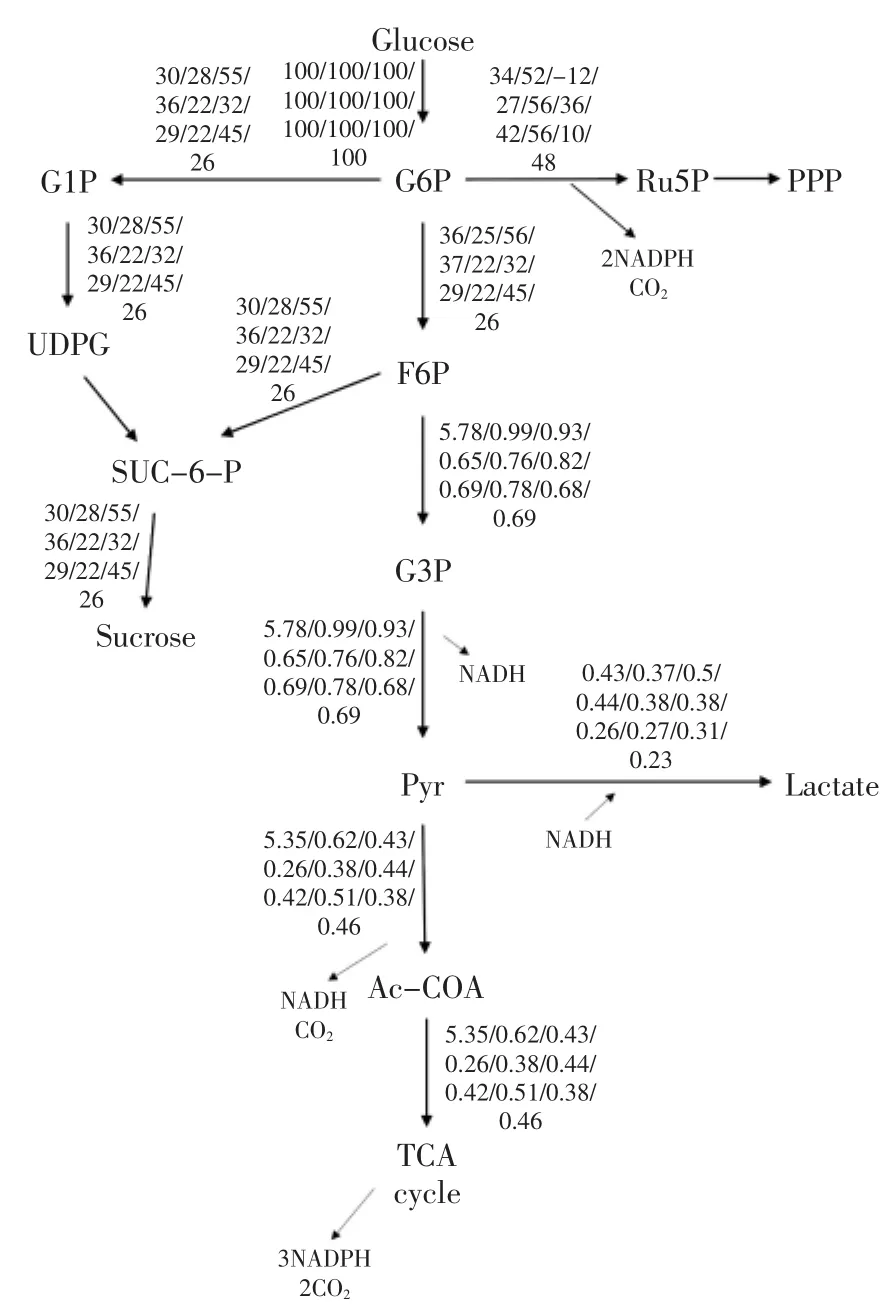
图6 甜瓜内果皮蔗糖、乳酸通量图Fig.6 Sucrose,lactic acid flux in Melon endocarp
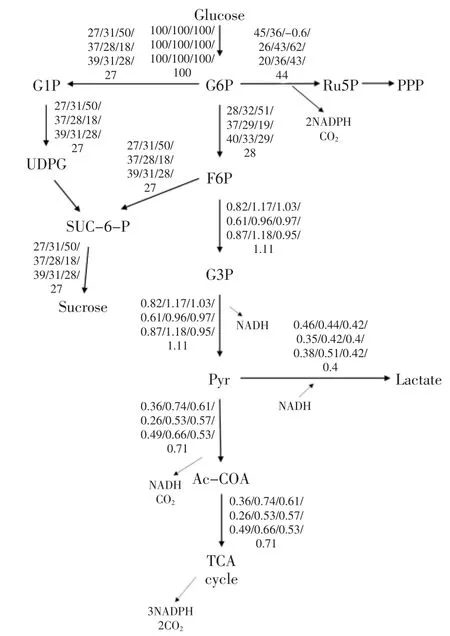
图7 甜瓜外果皮蔗糖、乳酸通量图Fig.7 Sucrose,lactic acid flux in Melon epicarp
在外果皮的通量分布中,进入磷酸戊糖途径的通量随温度呈现波动的趋势,在0、20、30、50℃和55℃情况下进入磷酸戊糖途经的通量较多;而在8℃时进入磷酸戊糖途经的通量仍为负的,但是相对于内果皮而言较小。就丙酮酸节点来看,大部分丙酮酸生成乙酰辅酶A进入TCA循环,进行有氧呼吸,维持机体正常的能量和物质代谢,生成乳酸的通量相对较少。相对于内果皮,外果皮的有氧呼吸增强;在甜瓜外果皮中有氧呼吸占主要优势。

图8 不同温度下甜瓜五部位蔗糖和乳酸的通量Fig.8 The metabolic flux of sucrose and lactate in five parts of melon fruit under different storage temperatures
2.2 蔗糖的代谢通量
糖分构成是影响果实品质的一个重要因素[24],尤其是蔗糖。蔗糖是光合作用的主要产物,是韧皮部运送的主要形式,也是果实贮存的主要物质。蔗糖含量是甜瓜果实糖分高低的主要决定因素[25]。此外,它还是细胞代谢的调节因子,可能通过影响基因表达发挥作用[26]。在贮藏中降低糖代谢尤为重要。如图8显示,就总体而言甜瓜在8℃和50℃有较高的蔗糖通量,但是以8℃最高,尤其是在果皮部位;在内果皮中,8℃是20℃和45℃的蔗糖通量的2.5倍,在外果皮中,8℃是30℃蔗糖通量的2.7倍;在50℃情况下也出现了较高的蔗糖通量,蔗糖是甜瓜果实含量最多且最为稳定的糖分,在一定的温度范围内,根据稀溶液依数性原理,蔗糖含量增加有利于机体抵抗高温的胁迫;这个温度可以为果蔬的热处理温度值域提供参考。而在不同的部位之间通量来看,甜瓜的蔗糖通量由内到外有先降低后升高的趋势,而甜瓜中组织的发育和组织代谢物的交流与协调对果实营养品质和感官品质都具有重要的影响。从贮藏温度来看,显然8℃大部分的葡萄糖通量流入蔗糖合成途径,更有利于甜瓜的保藏。
2.3 乳酸代谢通量
乳酸在果蔬的贮藏保鲜中发挥重要作用[27]。乳酸的通量有很重要的意义,它既可以反映呼吸代谢的受限情况,也可以反映合成代谢的增强情况[19]。由图8可以看出,在温度为8℃时乳酸通量较高;在内果肉中,50℃时也有较高的乳酸通量;在中果肉和外果肉中温度高于20℃时乳酸通量有下降的趋势。在内果皮中温度从8℃开始出现乳酸通量先下降然后再上升的趋势,在55℃时出现较低的乳酸通量;在外果皮中乳酸通量随温度呈现波动的趋势。结果显示,处于8℃时乳酸通量较高,更有利于限制呼吸代谢并促进蔗糖的合成。
3 结论与讨论
本实验进行了不同温度下甜瓜的蔗糖和乳酸代谢网络通量分析,结果表明:蔗糖的代谢通量在不同温度贮藏时有较大的不同,在8℃时蔗糖合成通量较高,甜瓜的糖分解代谢处于较低状态;并且在40~50℃的范围内也出现了较高的蔗糖通量,尤其是在中果肉、外果肉和内果皮三个部位,这说明一定的高温处理可能会起到更好的保鲜效果。这样的原因可能是果实经过短时间高温处理之后产生的应激反应[28]。而在55℃时蔗糖通量开始下降,其中的原因可能是温度过高而导致其相关的酶的合成量降低以适应高温度对自身造成的损伤。果实经过适当的热处理之后置于较低温度的环境下会起到更好的贮藏效果,且一般认为处理温度在30~52℃是最佳的热处理温度[29],结合本实验中蔗糖在高温区域的通量变化,很有可能50℃就是甜瓜热处理的最适温度,这也与张辉等研究的结果相一致[30]。乳酸在果蔬的贮藏保鲜中发挥重要作用[16],它的通量反映了呼吸代谢的受限状态和合成代谢的增强情况,如结果所示,8℃条件下乳酸通量较高,此温度下贮藏更有利于降低呼吸代谢,增加蔗糖的合成代谢,而蔗糖的通量在8℃也是最高的,因此从代谢的角度讲8℃是甜瓜的最适贮藏温度。在内果肉和外果皮部位,较高温度时也有较高的乳酸通量,适当的高温也有利于降低呼吸代谢,延长贮藏时间。根据所得到的结果,从代谢的角度优化贮藏保鲜的条件和方法为果蔬贮藏保鲜提供新的研究思路。
[1]常燕平.减压贮藏新技术的研究与发展前景[J].粮食加工与食品机械,2002(2):8-9.
[2]栾金水.果蔬保鲜新技术[J].农产品加工,2005(5):25-27.
[3]毛晓英,吴庆智,李宝坤,等.热处理对新疆哈密瓜采后贮藏特性的研究[J].食品科学,2007,28(12):491-493.
[4]袁莉,毕阳,葛永红,等.采后热处理对厚皮甜瓜贮藏品质的影响[J].食品科学,2010,31(20):421-424.
[5]李健,张萌,李丽萍,等.热处理对草莓品质与活性氧代谢影响的多变量解析[J].食品科学,2013,34(16):306-310.
[6]张明方,李志凌,陈昆松,等.网纹甜瓜发育果实糖分积累与蔗糖代谢参与酶的关系[J].植物生理与分子生物学学报,2003,29(5):455-462.
[7]Lester G E,Areas L S,Gomez L M.Muskmelon fruit soluble acid invertase and sucrose phosphate synthase activity and polypeptide profiles during growth and maturation[J].Journal of the American Society for Horticultural Science,2001,126:33-36.
[8]Yamaguchi M,Hughes Dm,Yabumoto K.Quality of cantaloupe muskmelons:Quality and attributes[J].Sci Hortic,1977,6:59-70.
[9]lester G e,Dunlap J R.Physiological changes during development and ripening of(Perlita) muskmelon fruits[J]. Hortic Sci,1985,26:311-323.
[10]Biais B T,Beauvoit B,Allwood J W,et al.Metabolic acclimation to hypoxia revealed by metabolite gradients in melon fruit[J].Journal of Plant Physiology,2010,167:242-245.
[11]Hong K Q,Xu H B,Wang J N.Quality changes and internal browning developments of summer pineapple fruit during storage at different temperatures[J].Scientia Horticulturae,2013,151:68-74.
[12]Moing A,Aharoni A,Biais B,et al.Extensive metabolic crosstalk in melon fruit revealed by spatial and developmental combinatorial metabolomics[J].New Phytologist,2011,190(3):683-696.
[13]Brooks G A,Dubouchaud H,Brown M,et al.Role of mitochondrial lactic dehydrogenase and lactate oxidation in the intra-cellular lactate shuttle Proc Natl Acad[J].Sci USA,1999,96:1129-1134.
[14]Coppari R.Metabolic actions of hypothalamic SIRT1[J]. Trends in Endocrinology and Metabolism,2012,23:179-185.
[15]Chowdhury S K,Dobrowsky R T.Nutrient excess and altered mitochondrialproteome and function contribute to neurodegeneration in diabetes[J].Mitochondrion,2011,11:845-854.
[16]Imai S,Guarente L.Ten years of NAD-dependent SIR2 family deacetylases:implicationsformetabolic diseases[J].Trends Pharmacol Sci,2010,31:212-220.
[17]Castellanos G M,Zaldívar C P,Flores L J P,et al. Postharvest litchi(Litchi chinensis Sonn.)quality preservation by Lactobacillus Plantarum[J].Postharvest Biology and Technology,2011,59:172-178.
[18]Cai X Z,Wang H S,Pang G C.Flux control analysis of a lactate and sucrose metabolic network atdifferentstorage temperatures for Hami melon(Cucumis melo var.saccharinus)[J]. Scientia Horticulturae,2015,181:4-12.
[19]李萍,李凤斌,胡柏文,等.气调贮藏不同气体比例对哈密瓜86-1贮期品质及生理活性的影响[J].新疆农业科学,2010,47(1):104-109.
[20]赵学明,白冬梅.代谢工程—原理与方法[M].化学工业出版社,2003.
[21]Schaefer U,Boos W,Takors R,et al.Automated Sampling Device for Monitoring Intracellular Metabolite Dynamics[J].Analy Biochem,1999,270:88-96.
[22]Theobald U,Milinger,Baltes M,et al.In vivo Analysis of Metabolic Dynamics in Saccharomyces Cerevisiae Experimental Observations[J].Biotechnol Bioeng,1997,55(2):305-316.
[23]Hoquea M A,Ushiyama H,Tomita M,et al.Dynamic responses of the intracellular metabolite concentrations of the wild type and pykA mutant Escherichia coli against pulse addition of glucose or NH3 under those limiting continuous cultures[J].Biochem Eng J,2005,26:38-49.
[24]Lester G E,Areas L S,Gomez L M.Muskmelon fruit soluble acid invertase and sucrose phosphate synthase activity and polypeptide profiles during growth and maturation[J].Journal of the American Society for Horticultural Science,2001,126:33-36.[25]Polenta G,Lucangeli C,Budde C,et al.Heat and anaerobic treatments affected physiological and biochemical parameters in tomato fruits[J].LWT,2006,39:27-34.
[26]Jang J C,Sheen J.Sugar sensing in higher plants[J].Plant Cell,1994,6:1665-1679.
[27]Imai S,Guarente L.Ten years of NAD-dependent SIR2 family deacetylases:implications for metabolic diseases[J].Trends Pharmacol Sci,2010,31:212-220.
[28]Yun Z,Li W,Pan Z,et al.Comparative proteomics analysis of differentially accumulated proteins in juice sacs of ponkan(Citrus reticulata) fruit during postharvest cold storage[J]. Postharvest Biology and Technology,2010,56:189-201.
[29]Lurie S.Postharvest Heat Treatments[J].Postharvest Biology and Techonlogy,1998,14(3):257-269.
[30]张辉,耿守东,王静.热处理对采后甜瓜品质的影响[J].北方园艺,2008(2):20-22.
Effects of different temperature on sugar and lactic acid flux in melon
WANG Hui-song,PANG Guang-chang*,LIU Ting-ting
(College of Biotechnology and Food Science,Tianjin University of Commerce,Tianjin 300134,China)
From the perspective of metabolism,fresh-keeping actually was to reduce catabolism of fruits and vegetables in their living condition so that their shelf life were prolonged,in-depth research of the law of metabolic flux will achieve the purpose better.This study used melon as a test subject discussed the law of metabolic flux of fruits and vegetables during their storage.In order to obtain the metabolic flux of the following pathways:embden meyerhof pathway(EMP),pentose phosphate pathway(PPP),sucrose synthesis pathway(SSP)and TCA cycle(TCA),melon was stored at different temperatures(0,5,8,10,20,30,40,45,50,55℃). The results showed that sucrose had a higher synthesis flux at the temperatures of 8℃and 50℃,and lactate had a higher metabolic flux at the temperature of 8℃.Thus,8℃was the optimal storage temperature.These findings would be enable to provide the reference for the in-depth study fruits and vegetables storage from the perspective of metabolic,improve the quality of the fruit store.
melon;sugar;lactate;metabolic flux
TS255.1
A
1002-0306(2015)22-0344-07
10.13386/j.issn1002-0306.2015.22.062
2015-03-09
王会松(1990-),男,硕士研究生,研究方向:代谢工程,E-mail:master.whs@hotmail.com。
*通讯作者:庞广昌(1956-),男,博士,教授,研究方向:食品生物技术,E-mail:pgc@tjcu.edu.cn。
国家自然科学基金面上项目(31371773)。
