仿酶型磁性Fe0-Fe3O4复合催化剂的制备及其催化性能
2015-04-24卢露露王光华李文兵吕立君魏晓币
卢露露,王光华,李文兵,万 栋,吕立君,魏晓币
(武汉科技大学 化学工程与技术学院,湖北 武汉 430081)
仿酶型磁性Fe0-Fe3O4复合催化剂的制备及其催化性能
卢露露,王光华,李文兵,万 栋,吕立君,魏晓币
(武汉科技大学 化学工程与技术学院,湖北 武汉 430081)
采用原位氧化沉淀法制备出仿酶型磁性Fe0-Fe3O4复合催化剂,并将其作为非均相类Fenton催化剂用于溶液中对硝基苯酚的降解;采用SEM和XRD等技术对催化剂进行了表征。表征结果显示,Fe3O4与Fe0结合牢固,有利于Fe0的分散。实验结果表明:Fe0-Fe3O4对对硝基苯酚的降解为拟一级反应;在Fe0与Fe3O4的质量比为0.75、Fe0-Fe3O4投加量为1.2 g/L、初始H2O2浓度为10 mmol/L、初始溶液pH为3、反应温度为30 ℃的条件下反应90 min,反应速率常数为0.067 min-1,COD去除率为77.28%,Fe溶出量为2.12 mg/L;在对硝基苯酚的降解过程中,pH先增大后减小,Fe溶出量先降低后升高;Fe0-Fe3O4是一种稳定的催化剂,可再生使用。
仿酶复合催化剂;四氧化三铁;零价铁;非均相催化剂;对硝基苯酚;降解
Fenton技术以其易操作、催化效率高等优点而被广泛应用于废水中有机污染物的去除[1-3]。但传统的Fenton技术存在不可忽视的缺点:催化剂(铁盐)无法回收及循环使用,会产生大量含铁污泥,存在二次污染。近年来,非均相类Fenton催化剂成为国内外环境工作者的研究热点[4-6]。其中,具有廉价易得、催化效率高、超顺磁性等特点的纳米Fe3O4备受青睐。
Fe3O4属于反尖晶石晶体结构,Fe2+起着提供电子引发类Fenton反应的重要作用。在Fe3O4晶格中,存在两种不同价态的等效阳离子(Fe2+和Fe3+),有些晶格点的占位由这两种离子共同组成,电子能够在Fe2+和Fe3+之间自由转移,使得Fe3O4具有独特的性能。研究表明,在H2O2存在的条件下,辣根过氧化物酶能催化降解苯酚、对二苯酚和苯胺[7]。而Fe3O4磁性纳米颗粒在H2O2存在的条件下能催化降解3,3,5,5-四甲基联苯胺和邻苯二胺[8]。这表明,Fe3O4磁性纳米颗粒具有类似过氧化物酶的功能。由于过氧化物酶对有机基质的氧化反应具有催化性,故Fe3O4磁性纳米颗粒作为一种类似过氧化物酶的物质具有应用于污水治理的潜能。
由于在Fe3O4晶格中,Fe2+与Fe3+之间的电子转移缓慢,因而导致类Fenton氧化过程中获得羟基自由基的过程减慢。而Fe0属于3电子供体,Fe0的加入可使Fe3O4更加活跃,并能补充Fe2+,进而促进类Fenton反应的进行。
本工作采用原位氧化沉淀法制备出仿酶型磁性Fe0-Fe3O4复合催化剂,并将其作为非均相类Fenton催化剂用于溶液中对硝基苯酚的降解。
1 实验部分
1.1 试剂
30%(w)H2O2溶液、NaBH4、FeSO4·7H2O、NaNO3、NaOH、无水乙醇、对硝基苯酚:分析纯。
1.2 Fe0-Fe3O4复合催化剂的制备
以NaBH4和FeSO4·7H2O为原料,采用湿法还原法[9]制备Fe0纳米颗粒。
采用原位氧化沉淀法[10]制备磁性Fe0-Fe3O4复合催化剂。将一定量制得的Fe0纳米颗粒加入到盛有200 mL蒸馏水(驱氧30 min)的烧瓶中,搅拌均匀,并升温至95 ℃;将7.2g FeSO4·7H2O溶于100 mL蒸馏水中,一次性加入烧瓶;将2.2 g NaOH和2.0 g NaNO3溶于100 mL蒸馏水中,逐滴滴入烧瓶,使Fe3O4的理论质量为2.0 g,持续搅拌3 h;磁分离出产物,以蒸馏水和无水乙醇交替洗涤至中性,最后于85 ℃下真空干燥12 h,冷却后研磨,即得不同Fe0与Fe3O4质量比的Fe0-Fe3O4复合催化剂。
1.3 对硝基苯酚的催化降解
取100 mg/L对硝基苯酚溶液100 mL于250 mL锥形瓶中,用0.1 mol/L H2SO4调节对硝基苯酚溶液的初始pH至3;加入1.2 g/L Fe0-Fe3O4复合催化剂,于30 ℃下恒温磁力搅拌30 min,以达到吸附平衡。加30%(w)H2O2溶液,使H2O2的初始浓度为10 mmol/L,并开始计时;每隔一段时间取样,磁分离,取滤液待测。反应结束后,磁分离出催化剂,洗涤,于85 ℃下干燥12 h,备用。
1.4 分析方法
Fe0-Fe3O4表征试样中,Fe0与Fe3O4的质量比均为0.75。采用德国FEI公司的Nava 400 Nano型扫描电子显微镜观察试样的微观形貌。采用英国牛津仪器公司的INCA Energy 350型能谱仪分析试样的元素组成。采用日本理学公司的Rigaku D/MAXRB型X射线衍射仪考察试样的结晶性质:CuKα射线,λ=0.154 056 nm,管电压40 kV,管电流40 mA。采用美国Thermo Fisher Scientific公司的DXR型智能拉曼光谱仪表征试样的化学结构:激光功率2 mW、波长780 nm,曝光时间5 s,曝光次数10,扫描范围70~3 000 cm-1。
采用Amersham Biosciences公司的Ultrospec 3300 pro型紫外-可见分光光度计测定滤液于波长400 nm处的吸光度,由标准吸光度曲线求得滤液中对硝基苯酚的浓度[11-12]。采用重铬酸盐法(GB 11914—1989)[13]测定COD,为了消除残余H2O2对COD的影响,测量之前将溶液pH调至碱性,然后加入适量MnO2静置过夜。采用1,10-菲啰啉分光光度法(GB/T 3049—2006)[14]测定Fe离子的浓度,得到Fe的溶出量,计算得到Fe的溶出率。采用美国Thermo Fisher Scientif c公司的ORION 5-STAR型pH计测定溶液pH。
2 结果与讨论
2.1 表征结果
2.1.1 SEM照片和EDS数据
Fe0,Fe3O4,Fe0-Fe3O4试样的SEM照片见图1。由图1可见:纯Fe0呈球形,平均粒径为60 nm左右,同时球形的Fe0颗粒相互连接成链状结构,且团聚严重;纯Fe3O4颗粒大致呈球状,部分为八面体结构,平均粒径为110 nm左右,团聚严重;Fe0与Fe3O4结合之后,团聚的现象依然存在,这是因为Fe0与Fe3O4均有较强的磁性,负载之后Fe0的链状结构被破坏,且颗粒的大小不均一(60~180 nm)。由此可见,Fe0与Fe3O4结合牢固,有利于Fe0的分散。
EDS分析结果表明,Fe0-Fe3O4主要由O和Fe组成,其摩尔分数分别为40.88%和59.12%。经计算可知Fe主要以Fe3O4和Fe0的形式存在。
2.1.2 XRD谱图
Fe0,Fe3O4,Fe0-Fe3O4试样的XRD谱图见图2。由图2可见:纯Fe3O4在2θ=18.1°,30.2°,35.6°,43.2°,53.6°,57.1°,62.7°处与JCPDS的Fe3O4标准谱峰吻合,说明所制备的纳米Fe3O4颗粒具有良好的结晶形态;Fe0-Fe3O4的XRD谱图由Fe0和Fe3O4的谱图叠加而成,Fe0和Fe3O4的特征衍射峰均出现在谱图中,且Fe3O4衍射峰较强,负载之后的Fe3O4与纯Fe3O4的衍射峰一致,说明Fe0与Fe3O4结合牢固,且结晶保持完好。根据Scherrer公式计算出纯Fe3O4晶体平均粒径约为30 nm,Fe0晶体为9 nm,与负载后的粒径(35 nm和10 nm)相差不大。
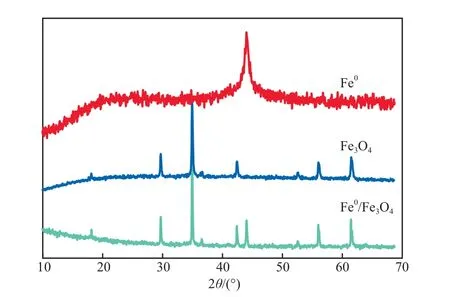
图2 Fe0,Fe3O4,Fe0-Fe3O4试样的XRD谱图
2.1.3 拉曼光谱
Fe0,Fe3O4,Fe0-Fe3O4试样的拉曼光谱见图3。
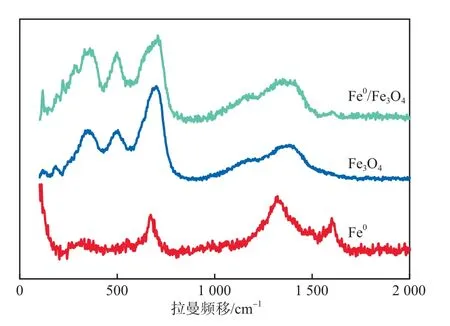
图3 Fe0,Fe3O4,Fe0-Fe3O4试样的拉曼光谱
由图3可见:在纯Fe0的拉曼光谱中,Fe0的吸收峰出现在670,1 320,1 600 cm-1处;Fe0-Fe3O4的拉曼光谱中出现了Fe3O4和Fe0的吸收峰,其中,350,500,670 cm-1处为Fe3O4的特征峰,500 cm-1和670 cm-1处的特征峰分别归属于Fe3O4的T2g和A1g振动模[15];另外,与纯Fe3O4相比,Fe0-Fe3O4中Fe3O4的特征峰整体向高波数位移,表明Fe0与Fe3O4是通过化学键而不是简单的物理吸附作用结合在一起的[16]。
2.2 Fe0与Fe3O4的质量比对Fe0-Fe3O4催化性能的影响
Fe0与Fe3O4的质量比对硝基苯酚降解效果的影响见图4,其中,ρ0和ρt分别为反应初始和t时刻的对硝基苯酚质量浓度,mg/L。由图4可见,Fe0-Fe3O4复合催化剂对对硝基苯酚的降解属于拟一级反应,拟合直线的相关系数均大于0.994。拟合直线的斜率为拟一级反应速率常数(k,min-1),k值越大,说明催化剂的催化性能越好。由图4还可见:随Fe0与Fe3O4质量比的增大,k值先增大后减小,在Fe0与Fe3O4的质量比为0.75时,k值达到最大(0.067 min-1),即0.75为Fe0与Fe3O4的最佳质量比;最佳质量比催化剂的k值明显高于其他催化剂,这说明Fe0与Fe3O4之间存在协同作用,促进了对硝基苯酚的降解。
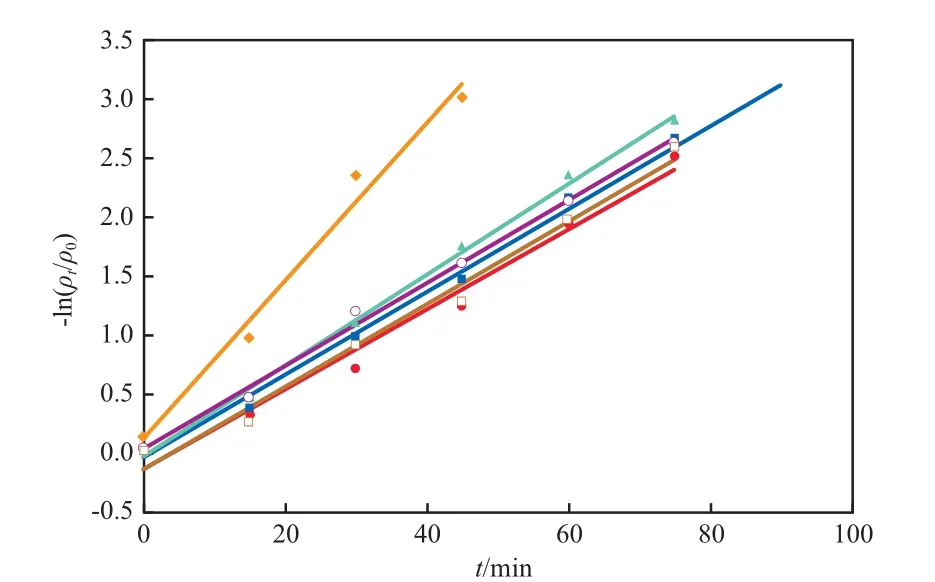
图4 Fe0与Fe3O4的质量比对硝基苯酚降解效果的影响
反应90 min,Fe0与Fe3O4的质量比对Fe溶出量和COD去除率的影响见图5。由图5可见,随Fe0与Fe3O4质量比的增大,COD去除率先增大后减小,Fe溶出量先减小后增大,均在质量比为0.75时达到极值,对应的COD去除率为77.28%、Fe溶出量为2.12 mg/L。这与上文最佳质量比为0.75的结论相一致。
以下实验均在Fe0与Fe3O4的质量比为0.75的条件下进行。
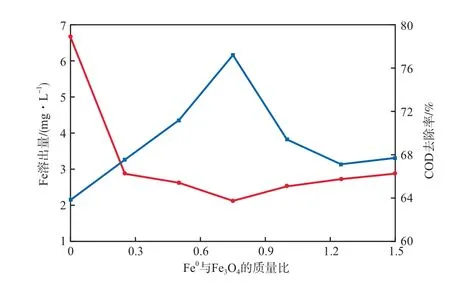
图5 Fe0与Fe3O4的质量比对Fe溶出量和COD去除率的影响
2.3 催化降解过程
对硝基苯酚在降解过程中会产生中间产物,有些中间产物可能比对硝基苯酚的毒性更大。对于废水处理,COD是一项重要指标,对于COD的去除远比对硝基苯酚的降解更重要。反应时间对对硝基苯酚降解率及COD去除率的影响见图6。由图6可见:COD的去除速率慢于对硝基苯酚的降解速率;对硝基苯酚的降解速率很快,反应30 min时对硝基苯酚降解率就达到97%以上,而此时COD去除率只有63%左右。因此,在对硝基苯酚降解的过程中可能产生了一些中间产物,并较难降解。

图6 反应时间对对硝基苯酚降解率及COD去除率的影响
反应时间对溶液pH和Fe溶出量的影响见图7所示。由图7可见,随反应的进行,溶液pH先增大后减小。这可能是因为:在对硝基苯酚降解的过程中先产生了对苯二醌等中间体,使溶液pH增大;随后,中间体逐渐被降解成酸性物质,使得溶液pH逐渐降低[17];最终,对硝基苯酚降解为CO2,H2O,HNO3[18]。由图7还可见,随反应的进行,Fe溶出量先降低再逐渐升高,最终升至5.81 mg/L,溶出率为7%。Fe的溶出量变化可能与一些反应中间体有关。研究结果表明,Fe离子能与对硝基苯酚降解的中间产物之一草酸形成Fe配合物[19],从而进入到溶液中。
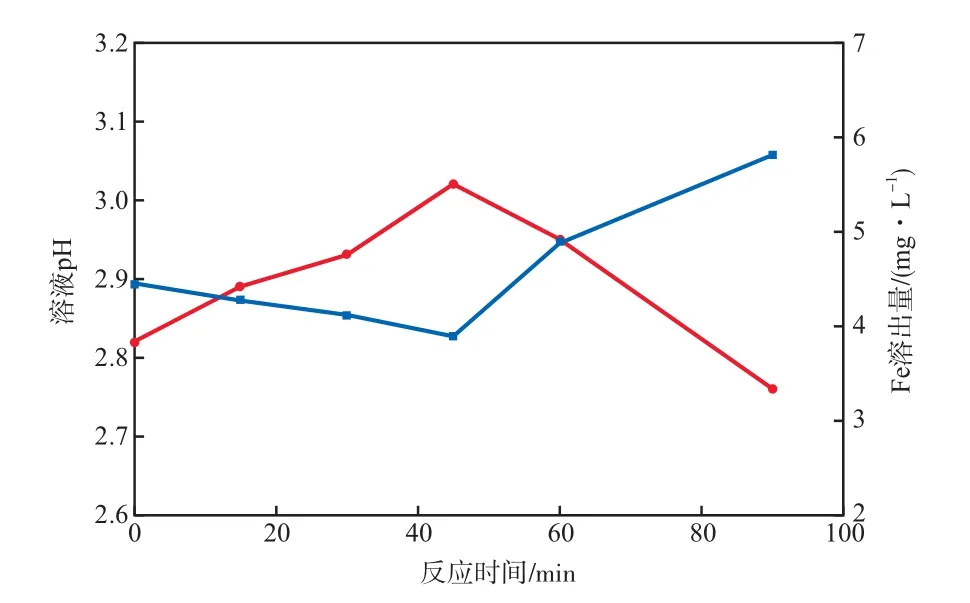
图7 反应时间对溶液pH和Fe溶出量的影响
2.4 Fe0-Fe3O4复合催化剂的稳定性
催化剂的稳定性是表征催化剂性能的一项重要指标。在反应90 min的条件下,Fe0-Fe3O4复合催化剂的重复使用性能见图8。
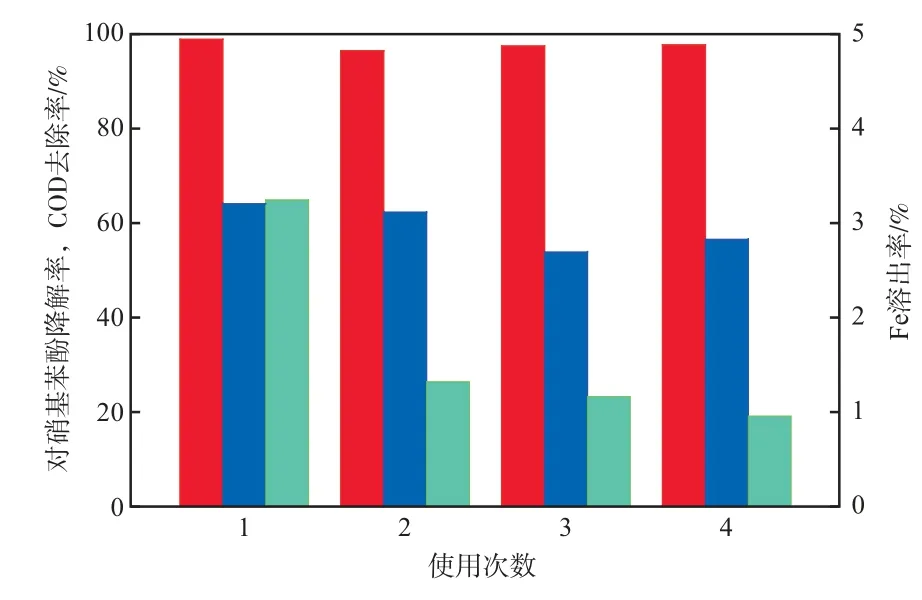
图8 Fe0-Fe3O4复合催化剂的重复使用性能
由图8可见:催化剂使用4次,对硝基苯酚降解率分别为98.79%,96.33%,97.35%,97.59%,COD去除率分别为64.13%,62.33%,53.87%,56.6%;催化剂使用4次后,对硝基苯酚降解率和COD去除率均有所降低,但降幅较小,说明催化剂的重复使用性较好。去除率降低可能是由于催化剂中的Fe流失导致的。由图8还可见,随使用次数的增加,Fe的溶出率降低,由3.25%降至0.95%。说明Fe3O4中的Fe离子主要在催化剂表面循环转化,只有少量扩散到溶液中。综上所述,Fe0-Fe3O4是一种稳定的催化剂,可再生使用。
3 结论
a)采用原位氧化沉淀法制备出Fe0-Fe3O4复合催化剂。Fe0与Fe3O4结合牢固,颗粒大小不均一(粒径60~180 nm)。
b)Fe0-Fe3O4复合催化剂对对硝基苯酚的降解为拟一级反应。
c)Fe0与Fe3O4的最佳质量比为0.75。在Fe0与Fe3O4的质量比为0.75、Fe0-Fe3O4复合催化剂投加量为1.2 g/L、初始H2O2浓度为10 mmol/L、初始溶液pH为3、反应温度为30 ℃的条件下反应90 min,反应速率常数为0.067 min-1,COD去除率为77.28%,Fe溶出量为2.12 mg/L。
d)在对硝基苯酚的降解过程中,随反应的进行,pH先增大后减小,Fe溶出量先降低后升高。
e)Fe0-Fe3O4是一种稳定的催化剂,可再生使用。
[1] 王昶,张丽萍,李伶,等. Fenton试剂氧化降解紫丁香醇的研究[J]. 环境工程,2011,29(1):62 - 66.
[2] 王光华,胡琴,李文兵,等. 磁性膨润土的制备及类Fenton氧化法处理焦化废水[J]. 化工环保,2014,34(6):575 - 580.
[3] Zhang Shengxiao,Zhao Xiaoli,Niu Hongyun,et al. Superparamagnetic Fe3O4Nanoparticles as Catalysts for the Catalytic Oxidation of Phenolic and Aniline Compounds[J]. J Hazard Mater,2009,167(1/2/3):560 - 566.
[4] Khaloo S S,Zolfaghari H,Gholamnia R. Response Surface Methodology for Optimization of 4-Nitrophenol Degradation by a Heterogeneous Fenton-Like Reaction on Nano-Zero-Valent Iron[J]. Desal Water Treat,2014(959061):1 - 8.
[5] Bonetti E,Del Bianco L,Signoretti S,et al. Synthesis by Ball-Milling and Characterization of Nanocrystalline Fe3O4and Fe/Fe3O4Composite System[J]. J Appl Phys,2001,89(3):1806 - 1815.
[6] Hirota Ken,Obatal Motoki,Kato Masaki,et al. Fabrication of Full-Density Mg-Ferrite/Fe-Ni Permalloy Nanocomposites with a High-Saturation Magnetization Density of 1 T[J]. Int J Appl Ceram Technol,2012,29(6):1085 - 1097.
[7] Durán N,Esposito E. Potential Applications of Oxidative Enzymes and Phenoloxidase-Like Compounds in Wastewater and Soil Treatment:A Review[J]. Appl Catal,B,2000,28 (2):83 - 99.
[8] Gao Lizeng,Zhuang Jie,Nie Leng,et al. Intrinsic Peroxidase-Like Activity of Ferromagnetic Nanoparticles[J]. Nat Nanotechnol,2007,2:577 - 583.
[9] Zhang Yun,Li Yimin,Li Jianfa,et al. Enhanced Removal of Nitrate by a Novel Composite:Nanoscale Zero Valent Iron Supported on Pillared Clay[J]. Chem Eng J,2011,171(2):526 - 531.
[10] Yang Shijian,He Hongping,Wu Daqing,et al. Decolorization of Methylene Blue by Heterogeneous Fenton Reaction Using Fe3-xTixO4(0 ≤x≤0.78) at Neutral pH Values[J]. Appl Catal,B,2009,89(3/4):527 - 535.
[11] 蒋建华. 声化学降解水体中对硝基苯酚的研究[D].天津:天津大学,2000.
[12] Feng Jiyun,Hu Xijun,Yue P L. Discoloration and Mineralization of Orange Ⅱ by Using a Bentonite Clay-Based Fe Nanocomposite Film as a Heterogeneous Photo-Fenton Catalyst[J]. Water Res,2005,39(1):89 - 96.
[13] 北京市化工研究院. GB 11914—1989 水质 化学需氧量的测定 重铬酸钾法[S]. 北京:中国环境科学出版社,1990.
[14] 天津化工研究设计院,上海出入境检验检疫局,天津出入境检验检疫局. GB/T 3049—2006 工业用化工产品 铁含量测定的通用方法 1,10-菲啰啉分光光度法度法[S]. 北京:中国标准出版社,2007.
[15] Li Honghong,Qin Li,Feng Ying,et al. Preparation and Characterization of Highly Water-Soluble Magnetic Fe3O4Nanoparticles via Surface Double-Layered Self-Assembly Method of Sodium Alpha-Olef n Sulfonate[J]. J Magn Magn Mater,2015,384:213 - 218.
[16] Mishra A K,Ramaprabhu S. Magnetite Decorated Multiwalled Carbon Nanotube Based Supercapacitor for Arsenic Removal and Desalination of Seawater[J]. J Phys Chem C,2010,114(6):2583 - 2590.
[17] Sun Shengpeng,Lemley A T.p-Nitrophenol Deg-radation by a Heterogeneous Fenton-Like Reaction on Nano-Magnetite:Process Optimization,Kinetics,and Degradation Pathways[J]. J Mol Catal A:Chem,2011,349(1/2) 71 - 79.
[18] Wang Nannan,Zheng Tong,Jiang Jiping,et al. Pilot-Scale Treatment ofp-Nitrophenol Wastewater by Microwave-Enhanced Fenton Oxidation Process: Effects of System Parameters and Kinetics Study[J]. Chem Eng J,2014,239:351 - 359.
[19] Chen Jianxin,Zhu Lizhong. UV-Fenton Discolouration and Mineralization of Orange Ⅱ over Hydroxyl-Fe-Pillared Bentonite[J]. J Photochem Photobiol,A,2007,188(1):56 - 64.
(编辑 魏京华)
Preparation of Biomimetic Magnetic Fe0-Fe3O4Composite Catalyst and Its Catalytic Capability
Lu Lulu,Wang Guanghua,Li Wenbing,Wan Dong,LüLijun,Wei Xiaobi
(College of Chemical Engineering and Technology,Wuhan University of Science and Technology,Wuhan Hubei 430081,China)
The biomimetic magnetic Fe0-Fe3O4composite catalyst was prepared by in-situ oxidation-precipitation method,and used as a heterogeneous Fenton-like catalyst in degradation ofp-nitrophenol in solution. The catalyst was characterized by SEM and XRD. The characterization results indicate that Fe3O4combines steadily with Fe0,which is good for the desperation of Fe0. The experimental results show that:The degradation ofp-nitrophenol on Fe0-Fe3O4follows the pseudo-f rst-order kinetic law;Under the conditions of mass ratio of Fe0to Fe3O40.75,Fe0-Fe3O4dosage 1.2 g/L,initial H2O2concentration 10 mmol/L,initial solution pH 3,reaction temperature 30 ℃ and reaction time 90 min,the apparent reaction rate constant is 0.067 min–1,the COD removal rate is 77.28%,and the dissolved quantity of Fe is 2.12 mg/L;During thep-nitrophenol degradation process,the solution pH decreases f rst and then increases,while the dissolved quantity of Fe reduces f rst and then rises;Fe0-Fe3O4is a catalyst showing good stability and reusability.
biomimetic composite catalyst;ferroferric oxide;zero-valent iron;heterogeneous catalyst;p-nitrophenol;degradation
TQ426.8
A
1006-1878(2015)06-0634-06
2015 - 07 - 10;
2015 - 08 - 31。
卢露露(1989—),女,湖北省枣阳市人,硕士生,电话 18164050228,电邮 490638856@qq.com。
高等学校博士学科点专项科研基金项目(201142191 10002);湖北省教育厅重点项目(D20131107);湖北省自然科学基金(2014CFB810)。
