急性感染致老年糖尿病患者多器官功能不全综合征1例
2015-04-21黄金华崔光淑
黄金华,崔光淑,张 凌
急性感染致老年糖尿病患者多器官功能不全综合征1例
黄金华*,崔光淑,张 凌
(北京市中关村医院内分泌科,北京 100190)
感染;糖尿病;老年人;多器官功能衰竭
1 病历摘要
老年多器官功能不全综合征(multiple organ dysfunction syndrome in the elderly,MODSE)是一种病因繁多、病死率极高的临床综合征,2014年9月我们成功抢救了1例2型糖尿病合并MODSE患者,报告如下。
患者,男性,69岁,因呕吐伴腹泻1d入院。既往有糖尿病病史7年,无心肌梗死及肾脏疾病病史。入院前1d患者与家人在家食用“涮羊肉”火锅、进食凉牛奶1盒及有部分溃烂凉桃后,患者出现阵发性腹痛,伴有恶心、呕吐、腹泻,持续约20h不缓解而入院。查体:血压150/90mmHg(1mmHg=0.133kPa),脉搏68次/min,体温36.5℃,呼吸19次/min,神清,精神弱,双肺呼吸音清,未闻及啰音。心律齐,心率68次/min,腹部膨隆,腹软,上腹部轻压痛、无反跳痛及肌紧张,肠鸣音正常。辅助检查:入院后急查D−二聚体13.51mg/L,乳酸脱氢酶17 614U/L,α−羟丁酸脱氢酶4 846U/L,乳酸脱氢酶同工酶1204U/L,肌酸激酶同工酶56U/L,尿素氮13.83mmol/L,肌酐204μmol/L,葡萄糖27.23mmol/L。心电图未见明显ST段改变。入院当日给予静脉滴注小剂量胰岛素[0.1U/(kg·h)]降糖、止吐、补液等对症治疗,但患者入院后24h入量2300ml、尿量不足200ml。入院诊断考虑:(1)急性胃肠炎;(2)2型糖尿病;(3)急性肾功能不全。入院后第2天继续给予补液、降糖等治疗,24h入量3000ml,但患者仍旧无尿,患者化验白细胞总数及中性粒细胞比例升高,考虑胃肠道感染,给予抗生素治疗,患者全血细胞分析变化见表1。化验结果提示肝肾功能损伤加重,见表2。凝血相变化见表3。心脏超声提示节段性运动异常(左室前间隔、心尖部)。血气分析提示轻度代谢性酸中毒、低钠血症,入院后随机末梢血糖在19.0~28.6mmol/L之间。我们组织了相关专科会诊、讨论,考虑为急性感染导致MDDSE(心、肝、肾、凝血障碍),立即给予重症监护,加强补液、水化、利尿、抗心力衰竭、抗感染治疗,并于入院后第2天给予规律床旁血液净化治疗,输注新鲜血浆及纤维蛋白原改善凝血功能,肌注维生素K避免血栓进展,谷胱甘肽及硫普罗宁保肝、质子泵制酸止血、保护胃黏膜、维持水电解质平衡、静脉滴注胰岛素降糖、营养支持等治疗,共输注新鲜冰冻血浆1000ml。第3天患者化验肝酶、肌酶、血肌酐水平仍在进展,最高丙氨酸氨基转移酶3 219U/L,天门冬氨酸氨基转移酶568U/L,尿素氮18.67mmol/L,肌酐534μmol/L,每日给予规律透析,保肝、降纤等综合治疗,患者化验指标开始好转,逐渐减少透析次数,入院后第15天停止血液透析,复查肝酶、肌酶、凝血功能已恢复正常,复查尿素氮6.2mmol/L,肌酐131μmol/L,随机静脉血糖8.93mmol/L。现患者病情控制平稳,已经出院。
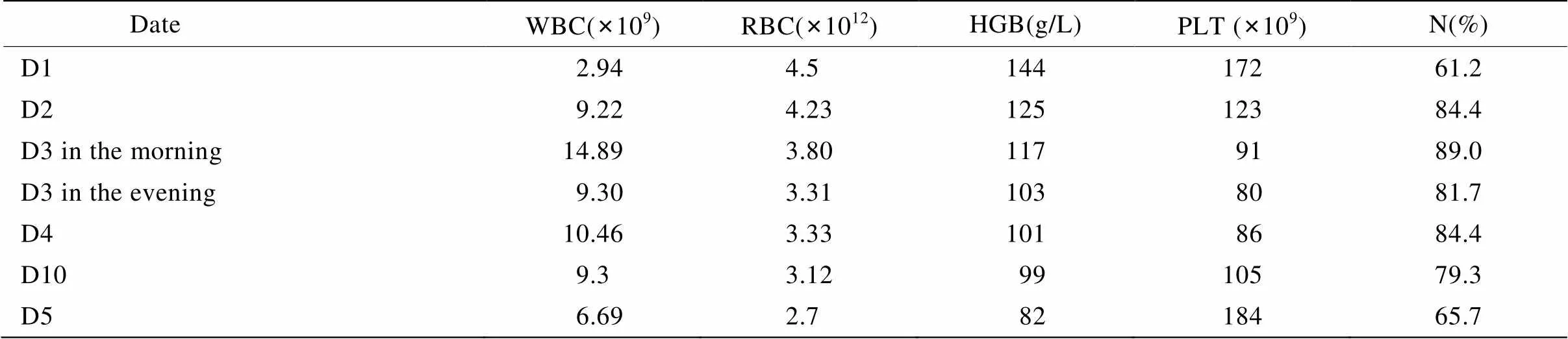
表1 患者入院后全血细胞分析变化
WBC: white blood cell; RBC: red blood cell; HGB: hemoglobin; PLT: blood platelet; N: neutrophil; D: day

表2 患者入院后生化指标变化
ALT: alanine transaminase; AST: aspertate trans aminase; LDH: lactate dehydrogenase; HBDH: hydroxybutyrate dehydrogenase; TBIL: total bilirubin; DBIL: direct bilirubin; IBIL: indirect bilirubin; BUN: blood urea nitrogen; SCr: serum creatinine; D: day
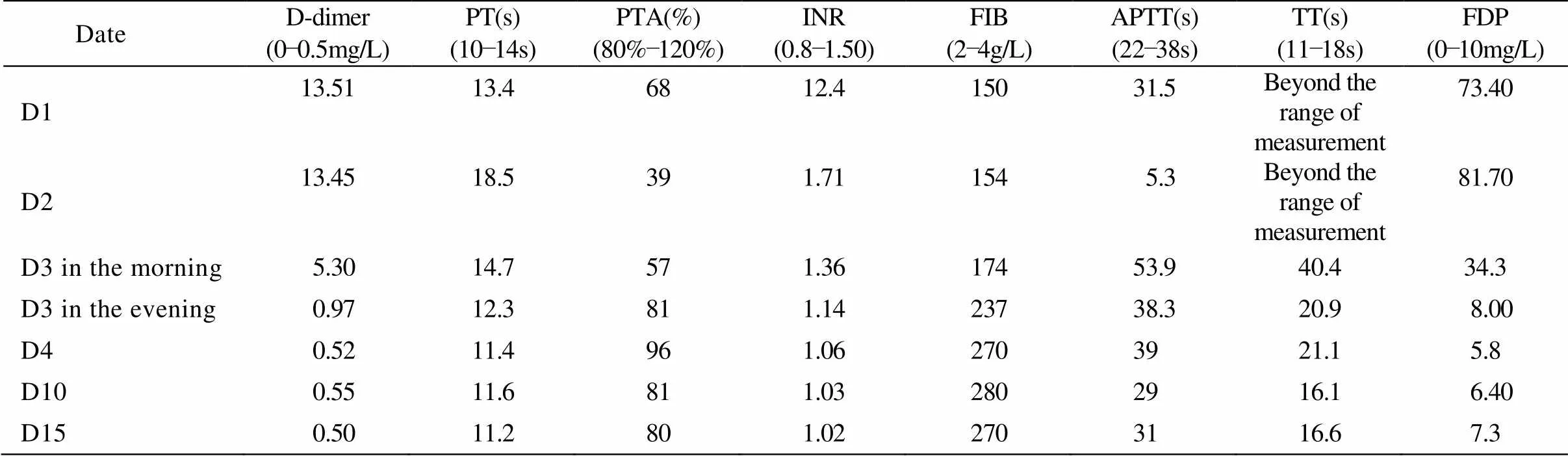
表3 凝血指标变化
PT: prothrombin time; PTA: plasma thromboplastin antecedent; INR: international normalized ratio; FIB: plasma fibrinogen; APTT: activated partial thromboplastin time; TT: thrombin time; FDP: fibrinogen degradation product; D: day
2 讨 论
MODSE是指老年人(>65岁)在器官老化和患有多种慢性疾病的基础上,由于某种诱因激发,在短时间内出现≥2个器官序贯或同时出现功能不全或衰竭的临床综合征[1]。本患者为老年糖尿病患者,此次进食不洁饮食后出现肠道感染,继之出现心、肝、肾功能衰竭及凝血机制障碍,应积极控制原发病因,对各重要脏器功能进行正确评估,采用必要的监测手段,严密地动态观察各重要器官的功能变化,并及时予以积极有效的支持。总结如下。
2.1 糖尿病致患者感染因素增多
高血糖时,机体血液黏度升高,细胞调节免疫反应差,而且高血糖破坏胰岛素依赖性黏膜和皮肤屏障的营养作用,导致细菌易位利感染。同时,高血糖可引起免疫球蛋白与补体发生糖基化,使其功能降低。因此,应在发病时及时给予抗感染治疗,避免感染加重病情。
2.2 肝损害
感染引起微血栓形成,补体减少以及毒性因子释放,网状内皮细胞吞噬能力降低,微血栓栓塞毛细血管,毒性因子和免疫复合物直接损害脏器细胞。本例患者入院时转氨酶为正常水平,短期内增高至数百倍,肝损害进展迅速,应动态观察肝功能,及时给予保肝、营养支持治疗,阻断有害介质和毒物对各器官的作用以及组织肠道细菌的易位,维持机体的正氮平衡。
2.3 感染与心肾损害
感染导致患者出现低灌流状态(乳酸性酸中毒、少尿或精神状态的改变),从而导致急性肾功能衰竭[2](acute renal failure,ARF),ARF时血液中含氮代谢产物增多、毒素堆积,并且由于水电解质平衡紊乱而产生高钾血症,导致心肌功能障碍。应密切监测患者的尿量、尿比重、肾功能、电解质等,尽快恢复有效循环血量以增加肾脏血流量,避免使用对肾功能有损害的药物。血液净化在急性肾衰的救治中起到关键的作用,使死亡率大大下降[3]。可根据肾功能恢复情况逐渐减少透析次数直至停止透析。
2.4 凝血功能障碍
过度炎症反应、缺血再灌注等均可引起血管内皮细胞损伤,参与免疫的各种蛋白产生减少,活性明显下降,导致止凝血功能紊乱,容易发生微血栓和弥散性血管内凝血(disseminated intravascular coagulation,DIC)[4],加重其他重要器官损伤。本例患者根据DIC诊断标准(1999年全国第六届血栓与止血会议修订),符合DIC诊断,经给予新鲜冰冻血浆、纤维蛋白原、维生素K等治疗后,凝血功能明显改善。
MODS患者病死率为30%~100%,主要取决于器官衰竭的数目和持续时间[5],除非到终末期,MODS可以逆转。因此,早期诊断至关重要,一旦出现某单一脏器功能衰竭,即应采取综合措施积极治疗,加强监测重要脏器的功能变化,如抗感染、清除毒素、合理利用血管活性药物,防治肝肾功能衰竭和肠道菌群失调所致的胃肠衰竭,尽力控制病情的发展,降低死亡率。
[1] Osterbur K, Mann FA, Kuroki K,. Multiple organ dysfunction syndrome in humans and animals[J]. J Vet Intern Med, 2014, 28(4): 1141−1151.
[2] Haller H,Strauer BE.End-organ damages in diabetes[J]. Internist (Berl), 2011, 52(5): 493−494.
[3] Bani HS, Showkat A. Renal function recovery in dialysis dependent patients[J]. Tenn Med 2013, 106(8): 36−40.
[4] Callum JL, Rizoli S. Plasma transfusion for patients with severe hemorrhage: what is the evidence[J]? Transfusion, 2012, 52(Suppl 1): 30S−37S.
[5] Kuz’min V. Treatment and diagnostic tactics of the injured persons with multisystem and multiorgan damages[J]. Klin Khir, 2008, (11−12): 107−109.
(编辑: 周宇红)
2014−11−26;
2015−01−19
黄金华, E-mail: huangjinhua@yeah.net
R587.1; R592
B
10.11915/j.issn.1671-5403.2015.03.052
