固相萃取-高效液相色谱法测定极性注射液中抗氧剂BHT 含量
2015-04-13曲亚南徐苏华陈浩瀚谢新艺颜林广东省医疗器械质量监督检验所包装材料容器检验中心广州510663
曲亚南 徐苏华 陈浩瀚 谢新艺 颜林 广东省医疗器械质量监督检验所包装材料容器检验中心 (广州 510663)
随着包装技术的快速发展以及人们对包装材料的深入研究,药品包装材料与药物相容性研究越来越受到关注。《化学药品注射剂与塑料包装材料相容性研究技术指导原则(试行)》和《化学药品注射剂与药用玻璃包装容器相容性研究技术指导原则(网站征求意见稿)》有力地推动了我国药品包装材料与药物相容性的研究工作。橡胶材料是最为常用的包装材料之一,且与药品直接接触。由于丁基橡胶塞在加工过程中需要加入硫化剂等多种助剂,因而在胶塞中不可避免地会残存一些未被化学键合或者分解硫化的物质。这些物质渗透在药物中或者是吸附药物,从而与药物发生反应,影响药物的活性物质含量,进而威胁药物的安全性[1]。国内学者对胶塞进行过一些研究[2~5],研究表明当胶塞与注射剂直接接触时,胶塞可能会吸附注射剂中的活性成份,而胶塞本身的有毒有害成份也可能迁移至注射剂中。
2,6-二叔丁基-4-甲基苯酚(BHT)是橡胶常用的一种抗氧剂,具有抑制或延缓橡胶氧化降解而延长使用寿命的功能。研究表明 BHT 对肺、肝等组织有直接损害作用,并有可能促进肿瘤发生[6]。目前在日本、欧洲、美国已禁止在婴儿和儿童食品中使用。在注射剂与溴化丁基橡胶塞长期直接接触的过程中,抗氧剂BHT 也具有迁移至注射剂中的危险,对于这方面的研究还未见报道。本文首次采用固相萃取技术进行前处理、高效液相色谱法测定对乙酰氨基酚注射液和复方氨基酸(15)双肽(2)注射液中抗氧剂BHT 的含量。
1.实验部分
1.1 试剂、材料与仪器
高效液相色谱仪(日本岛津公司LC-2010A);万分之一电子天平(北京赛多利斯天平有限公司,BSA224S-CW);超声波清洗器(中国昆山超声仪器有限公司,KQ-150DY型);移液枪(北京青云卓立精密设备有限公司,20~200μl);
固相萃取柱(WondaSep C18,500mg/6mL);固相萃取仪(天津奥特赛恩斯仪器有限公司,AES-12);
2,6-二叔丁基-4-甲基苯酚(BHT)对照品(Dr. Ehrenstorfer GmbH,批号:20627);
对乙酰氨基酚注射液(钠钙玻璃输液瓶及溴化丁基橡胶塞包装,加速试验6 个月样品);
复方氨基酸(15)双肽(2)注射液(钠钙玻璃输液瓶及溴化丁基橡胶塞包装,加速试验6 个月样品及长期试验6 个月样品);
甲醇(LiChrosolv,色谱纯);二氯甲烷(天津市科密欧化学试剂有限公司,色谱纯);乙醚(广州化学试剂厂,分析纯);实验用水为二级纯化水。
1.2 溶液的配制
1.2.1 标准储备溶液将抗氧剂BHT 标准品109.1mg 溶于100mL甲醇中,作为标准储备溶液。
1.2.2 标准溶液的配制
用甲醇将抗氧剂BHT 储备液逐级稀释至0.2182、5455、1.091、2.182、5.455、10.91µg/mL系列标准溶液。
1.3 液相色谱条件
色谱柱:Inertsil®ODS-SP,5µm,4.6mm×250 mm;流动相:水:甲醇=20:80;流速:1.0mL/min;检测波长:280nm;柱温:40˚C;进样量:20µl。
1.4 试样的前处理
固相萃取柱使用前分别用5mL 甲醇和5mL水活化。量取100mL 对乙酰氨基酚注射液,以约2~3mL/min 的流速通过固相萃取柱,随后用15mL 二级纯化水淋洗,负压抽15min 后分别用2mL 甲醇,7mL 二氯甲烷依次洗脱,收集洗脱液,用甲醇稀释至10mL,用0.45µm 滤膜过滤后待测。
2.结果与讨论
2.1 固相萃取柱的选择
以2mL 甲醇和7mL 二氯甲烷为洗脱液,分别研究了HLB 柱(Chromclean,200mg/6mL)、PEP 柱(Cleanert,500mg/6mL)、C18 柱 对 抗氧剂BHT 的吸附情况(表1)。C18 柱对抗氧剂BHT 的吸附大于其他2 种萃取柱,其在此柱的洗脱回收率最大,达到91.95%,且C18 萃取柱的价格最便宜,故选择C18 柱作为固相萃取柱。
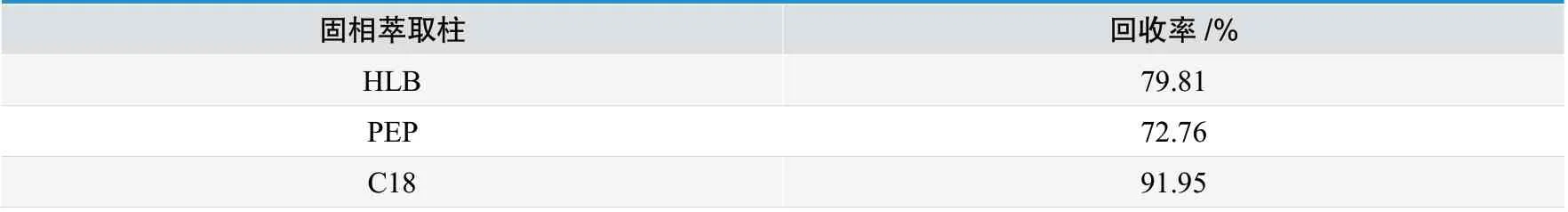
表1. 固相萃取柱的选择
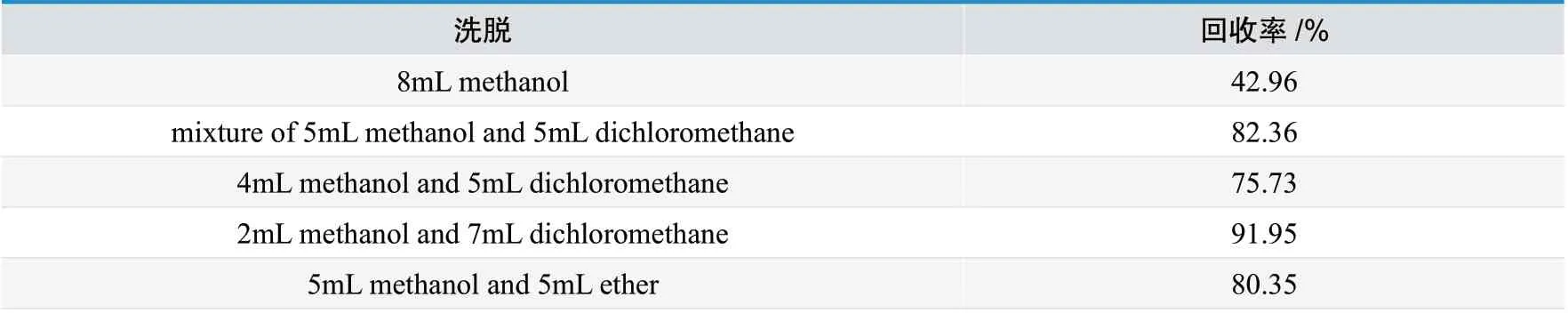
表2. 洗脱液及用量的选择
2.2 洗脱液及用量的选择
以C18 柱为固相萃取柱,考察了5 组溶剂(8mL 甲醇,5mL 甲醇5mL 二氯甲烷混合溶液,4mL 甲醇5mL 二氯甲烷依次洗脱,2mL 甲醇7mL 二氯甲烷依次洗脱,2mL 甲醇7mL 乙醚依次洗脱)的洗脱效果。实验表明(见表2),8mL甲醇、2mL 甲醇7mL 二氯甲烷、2mL 甲醇7mL乙醚中2mL 甲醇7mL 二氯甲烷依次洗脱的结果最好,这是由于二氯甲烷的极性最小,与吸附在C18 填料上的BHT 作用最强。5mL 甲醇5mL 二氯甲烷混合溶液、4mL 甲醇5mL 二氯甲烷、2mL甲醇7mL 二氯甲烷中2mL 甲醇7mL 二氯甲烷依次洗脱的结果最好,这是由于极性较小的二氯甲烷所占比例最大,可以洗脱出较多的抗氧剂BHT。所以选择2mL 甲醇7mL 二氯甲烷依次洗脱作为洗脱步骤。
2.3 HPLC 条件优化
将添加抗氧剂BHT 标准溶液的对乙酰氨基酚注射液按1.4 进行前处理后注入HPLC,比较了抗氧剂BHT 在甲醇-水比例分别为90:10、85:15、80:20 流动相色谱条件下的分离情况。结果表明,用甲醇:水=80:20 流动相进行洗脱,抗氧剂BHT 出峰较晚,保留时间约为13.4min,与对乙酰氨基酚以及未知杂质具有较好分离度,且色谱峰尖锐、对称。加标对乙酰氨基酚注射液的色谱图,见图1。
2.4 方法有效性的评价
2.4.1 检出限
称取抗氧剂BHT 对照品适量,用甲醇溶解稀释,定容,将标准溶液不断稀释至信噪比为3计算检出限,信噪比为10 计算定量限。抗氧剂BHT 的检出限和定量限见表3。结果显示抗氧剂BHT 的样品检出限为0.0039µg/mL,定量限为0.0121µg/mL。对乙酰氨基酚注射液的每日建议用量为200mL/day,人每日允许最大暴露量(PDE)为1.5mg/day,灵敏度满足检测需求。
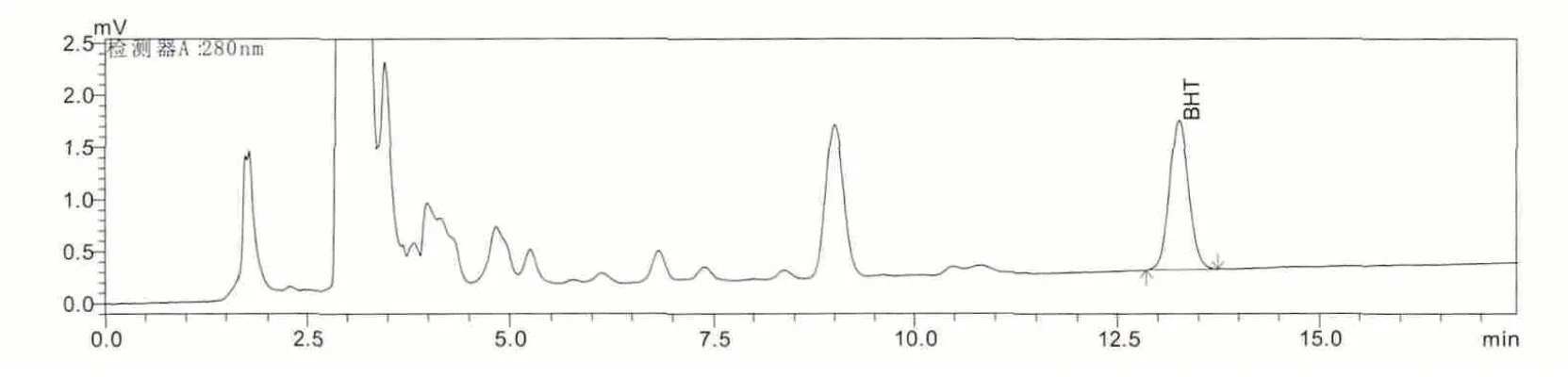
图1. 加标对乙酰氨基酚注射液的色谱图

表3. 测定抗氧剂BHT 的线性范围、线性方程、相关系数、检出限、定量限

表4. 测定对乙酰氨基酚注射液抗氧剂BHT 的加标回收率与相对标准偏差

表5. 测定复方氨基酸(15)双肽(2)注射液抗氧剂BHT 的加标回收率与相对标准偏差
抗氧剂BHT 作为食品添加剂每日最大服用量(ADI)为0.3mg/kg bw/day,数据获取来源为UNEP PUBLICATIONS 发布的2,6-di-tert-butyl-pcresol(BHT)。由于未查询到BHT 静脉给药的相关毒理数据,本次计算过程中使用了相关假设,所以计算出来的PDE 仅为参考值。体重取50kg,则抗氧剂BHT 的PDE=15mg/day。
由于口服、静脉、吸入给药会显示出不同的毒性,也会有不同的PDE 限度。本次试验假设静脉给药PDE 是口服给药PDE 的10%。(此处的10%参考European Medicines Agency2008 年2 月21 号在伦敦发布的Guideline of the specification limits for residues of metal catalyst of metal reagents。即BHT 静脉给药的PDE=1.5mg/day)
2.4.2 回归方程及相关系数
以定量限1.5 倍左右作为线性最低浓度,在最佳的测定条件下,以抗氧剂BHT 色谱峰面积(A)对浓度(C,μg/mL)建立标准曲线。抗氧剂BHT 在表3 列出的浓度范围内,相关系数为0.9999。
2.4.3 回收率
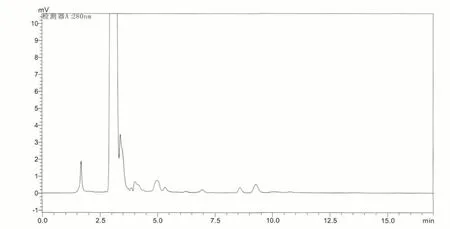
图2. 对乙酰氨基酚注射液样品色谱图

图3. 复方氨基酸(15)双肽(2)注射液样品色谱图
移取100mL 对乙酰氨基酚注射液,分别加 入30µl、60µl、120µl 的BHT 标 准 储 备 溶液,使对乙酰氨基酚注射液中抗氧剂BHT 含量为0.03273μg/mL、0.06546μg/mL、0.1225μg/mL,每个水平平行测3 个样,其回收率和相对标准偏差见表4。结果表明,抗氧剂BHT 平均回收率在76.75%~91.95%,RSD 在1.06%~6.00%范围内。方法显示了良好的准确度和精密度。
此外本试验还用此方法对复方氨基酸(15)双肽(2)注射液进行了回收率的测定,回收率和相对标准偏差详见表5。结果表明,抗氧剂BHT 平均回收率在106.37%~110.03%,RSD 在1.20%~6.53%范围内。复方氨基酸(15)双肽(2)注射液的每日建议用量为1000mL/day,人每日允许最大暴露量(PDE)为7.5mg/day,灵敏度满足检测需求。说明该方法也适用于复方氨基酸(15)双肽(2)注射液中的抗氧剂BHT 的检测。
2.5 实际样品的检测
利用本方法对某企业生产的对乙酰氨基酚注射液(加速试验6 个月样品)及复方氨基酸(15)双肽(2)注射液(加速试验6 个月样品及长期试验6 个月样品)进行测定。样品中均未检出抗氧剂BHT,色谱图见图2、3。应用本方法测定对乙酰氨基酚注射液中的抗氧剂BHT,可有效监控极性注射剂中的抗氧剂BHT 含量是否超过人每日允许最大暴露量(PDE),且方法灵敏度高,稳定性好,为溴化丁基橡胶塞与极性注射液提供了技术支持。
[1] 赵霞,胡昌勤,金少鸿. 药用丁基胶塞中易挥发性成分的成分分析[J].药物分析杂志, 2006, 26( 3): 315-318.
[2] 李婷婷,朱碧君,胡红刚.药用卤化丁基胶塞溶血试验[J].科技广场, 2010, 10: 120-121.
[3] 姚蕾,王立新,王红梅,高志峰,胡昌勤. 229 批国产注射用头孢噻肟钠的质量评价[J].评价与指南, 2012, 9( 11): 22-27.
[4] 殷果,秦斌,王铁杰, 邓颖, 李军, 周劼.药用丁基胶塞与注射用阿莫西林钠的相容性研究[J].中国抗生素杂志, 2012, 37( 9): 699-701.
[5] 赵霞,胡昌勤,金少鸿. 对考察药用丁基胶塞与药物相容性的思考与建议[J].中国药事, 2007, 21(10): 810-812.
[6] 周劼,殷果,刘洪伟,刘尧,王晓炜. 药用丁基胶塞中BHT 的GC.MS/MS 法测定[J].中国医药工业杂志, 2013, 44(8): 801-803.
