3-(2,4-二羧基苯基)-2,6-二羧基吡啶原位脱羧构筑两个配位聚合物的结构及磁性
2015-04-01由立新王淑菊熊刚丁茯孙亚光
由立新 王淑菊 熊刚 丁茯 孙亚光
3-(2,4-二羧基苯基)-2,6-二羧基吡啶原位脱羧构筑两个配位聚合物的结构及磁性
由立新 王淑菊 熊刚 丁茯 孙亚光*
(沈阳化工大学应用化学学院,沈阳110142)
通过水热法合成了2个配位聚合物:[Cu(H2dpcp)2]n(1)和[Mn2(Hdpcp)2(H2O)2·2H2O]n(2)[H3dpcp=5-(2,4-二羧基苯基)-2-羧基吡啶],H3dpcp由3-(2,4-二羧基苯基)-2,6-二羧基吡啶(H4dpdp)原位脱羧生成。X-射线单晶衍射测得2个化合物都属于单斜晶系,化合物1结晶在P21/c空间群,a=0.639(13)nm,b=1.835(4)nm,c=1.115(2)nm,β=102.29(3)°,Z=2;化合物2结晶在C2/c空间群,a=3.126(6)nm,b=1.004(2)nm,c=1.080(2)nm,β=93.73(3)°,Z=4。化合物1以配体H2dpcp-桥连Cu(Ⅱ)形成一维链状结构。化合物2通过Hdpcp2-桥连Mn(Ⅱ)形成二维层状结构,并进一步通过氢键作用形成三维超分子结构。负的Weiss常数θ表明化合物2存在反铁磁耦合作用。
配位聚合物;原位脱羧;3-(2,4-二羧基苯基)-2,6-二羧基吡啶;磁性
0 引言
配位聚合物因其结构多样及兼备无机材料和有机材料的优点,在分子磁体、荧光材料、非均相催化、气体吸附等领域显示出诱人的应用前景[1]。在构筑配位聚合物的过程中,配体的选择对其结构具有重要影响,其中氮杂芳香多酸因为多变的配位方式和良好的配位能力,已成为合成金属配位聚合物研究的热点之一[2-3]。
2,6-吡啶二羧酸及其衍生物作为配体构筑的系列配位聚合物先后被报道,其中一些化合物具有铁磁作用和荧光性质[4-10]。3-(2,4-二羧基苯基)-2,6-二羧基吡啶(H4dpdp)是2,6-吡啶二羧酸的衍生物,其含有的苯环和吡啶环具有刚性骨架结构,而且两个芳环之间的C-C键可以旋转,又表现出一定的柔性,具备多种配位模式和构筑新颖结构的基础。另外,芳环上的羧基能够参与形成氢键,易于构筑高维配位聚合物。近来,通过原位脱羧反应合成配位聚合物逐渐发展起来,并涌现出许多新型结构的化合物[11-13],而这是通过配体和金属离子直接反应难以实现的。
本文以H4dpdp为配体,在水热条件下通过原位脱羧形成5-(2,4-二羧基苯基)-2-羧基吡啶(H3dpcp)与Cu(Ⅱ)自组装得到一维链状化合物[Cu(H2dpcp)2]n(1),与Mn(Ⅱ)自组装得到二维层状化合物[Mn2(Hdpcp)2(H2O)2·2H2O]n(2)。磁性测定表明化合物2存在反铁磁耦合作用。
1 实验部分
1.1 试剂与仪器
所用试剂均为分析纯试剂,未经进一步纯化处理。元素分析使用Perkin-Elemer 470型元素分析仪;红外光谱使用Nicolet IR-6700型红外光谱仪,波长4 000~400 cm-1,KBr压片;粉末X射线衍射采用BRUKER D8 ADVANCE(Cu Kα辐射)测定;金属配合物的变温磁化率采用Quantum Design MPMS-7 SQUID型磁量计进行,所有数据均经Pascal′s常数进行反磁校正;单晶测定是采用Bruker SMART 1000 CCD面探衍射仪。
1.2 化合物1~2的合成
[Cu(H2dpcp)2]n(1)的合成及元素分析:取H4dpdp 0.066 2 g(0.2 mmol),Cu(NO3)2·3H2O 0.036 3 g(0.15 mmol),9 mL蒸馏水和1 mL NaOH(0.1 mol·L-1),搅拌10 min后置于密封25 mL聚四氟乙烯反应釜中,在160℃下反应72 h,然后在24 h内程序冷却至室温,得到蓝色透明长条状晶体。晶体不溶于水和一般的有机溶剂。基于Cu(NO3)2·3H2O的计算产率为:50.5%。元素分析(C28H16CuN2O12)实验值(%):C 52.39;H 2.26;N 4.33。理论值(%):C 52.88;H 2.53;N 4.40。
[Mn2(Hdpcp)2(H2O)2·2H2O]n(2)的合成及元素分析:除了将Cu(NO3)2·3H2O换为MnCl2·4H2O 0.029 7 g(0.15 mmol),其余步骤与1类似,得到黄色透明长条状晶体。晶体不溶于水和一般的有机溶剂。基于MnCl2·4H2O的计算产率为:62.3%。元素分析(C28H26Mn2N2O16)实验值(%):C 44.29;H 3.38;N 3.73。理论值(%):C 44.46;H 3.46;N 3.70。
1.3 晶体结构测定
化合物1和2的晶体结构测定在293 K下采用Bruker SMART 1000型X-射线衍射仪进行,石墨单色器单色化Mo Kα射线(λ=0.071 073 nm)作入射光,以φ-ω扫描方式收集衍射点。晶体结构使用SHELXS-97程序由直接法解出[14];用SHELXL-97程序对非氢原子坐标及其各向异性热参数基于F2进行全矩阵最小二乘法精修[15];氢原子为理论加氢。化合物1和2的晶体学数据在表1列出。部分键长和键角列于表2。
CCDC:1021238,1;1021239,2。

表1 化合物1和2的晶体学数据表Table 1Crystal data and structure refinement of 1 and 2
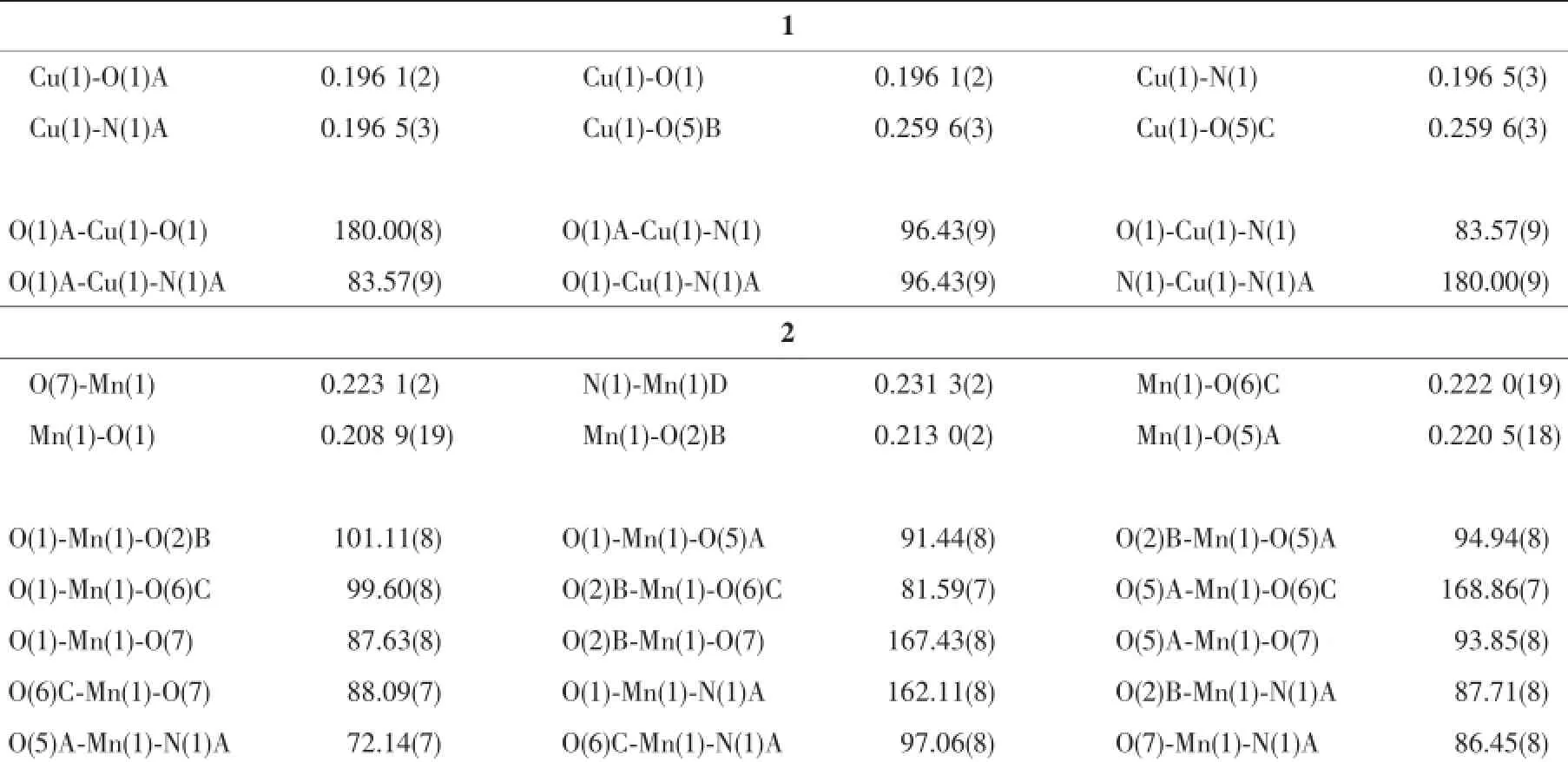
表2 化合物1和2结构中部分键长键角Table 2Selected bond lengths(nm)and angkes(°)for 1 and 2
2 结果与讨论
2.1 配位聚合物的表征
红外光谱分析表明,化合物1在3 438 cm-1的吸收峰为羧基O-H伸缩振动吸收峰,1 692 cm-1和1 597 cm-1为羧基中C=O伸缩振动吸收峰,1 502 cm-1和1 482 cm-1为芳环碳骨架伸缩振动吸收峰。化合物2在3 415 cm-1处的强宽峰为水的O-H伸缩振动吸收峰,1 698 cm-1和1 623 cm-1为羧基中的C=O伸缩振动吸收峰。另外,室温下化合物1和2的粉末X射线衍射图谱与单晶结构模拟图谱基本吻合,表明2个化合物样品均为纯相。
2.2 配位聚合物晶体结构
单晶X-射线衍射分析表明,配体H4dpdp以 H2dpcp-和Hdpcp2-形式分别与Cu(Ⅱ)和Mn(Ⅱ)配位形成化合物[Cu(H2dpcp)2]n(1)和[Mn2(Hdpcp)2(H2O)2· 2H2O]n(2)。这可能是由于在高温气相条件下,与Cu(Ⅱ)或Mn(Ⅱ)共存时,含氮芳香多酸配体H4dpdp原位脱羧生成H3dpcp,并分别与Cu(Ⅱ)、Mn(Ⅱ)反应得到化合物1和2(见图1)[13]。
2.2.1 [Cu(H2dpcp)2]n(1)晶体结构描述
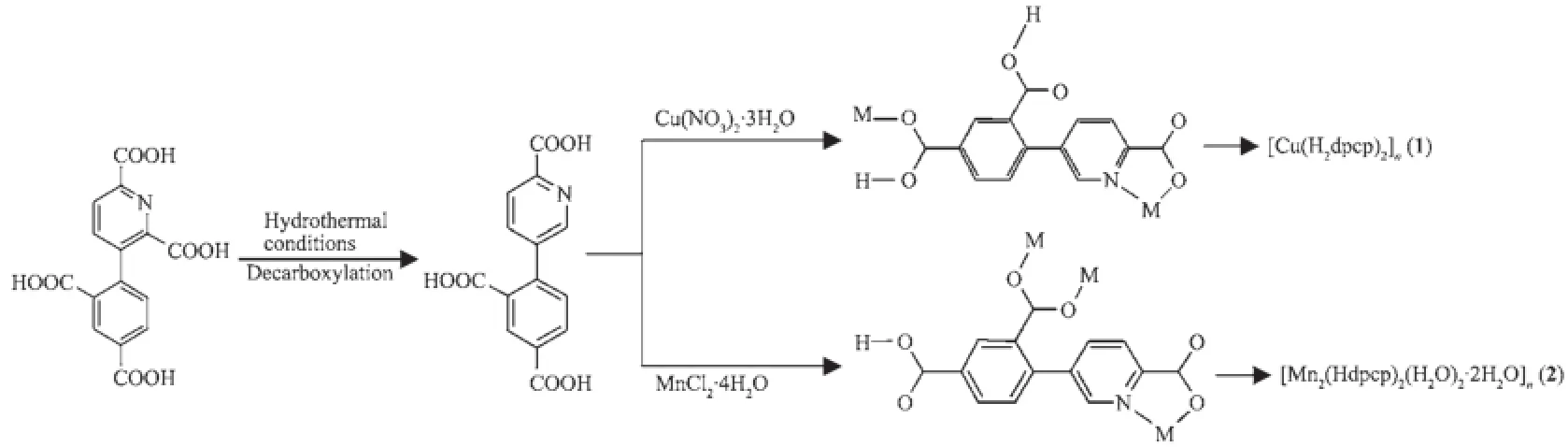
图1 化合物1和2合成路线Fig.1Synthetic route of 1 and 2
如图2所示,在化合物[Cu(H2dpcp)2]n中,配体H4dpdp在水热条件下发生原位脱羧生成H3dpcp,与金属Cu(Ⅱ)结晶在P21/c空间群中,H2dpcp-的配位方式见图1。4个赤道平面配位点分别被H2dpcp-配体中O1、O1A、N1和N1A占据,O5B和O5C位于轴向位置。由于姜-泰勒效应(Jahn-Teller effect)造成轴向配位键Cu1-O5B和Cu1-O5C键长稍长,为0.259 6(3)nm[16-17],Cu1-N1键长为0.196 5(3)nm,Cu1-O1键长为0.196 1(2)nm,O5B-Cu1-N1A键角为89.84°,O5B-Cu1-O1键角为76.93°,形成六配位轻微变形的八面体配位构型(键长和键角见表2)。如图3所示,化合物1中,由于H2dpcp-中连接苯环和吡啶环的C-C键旋转,2个芳环平面间的二面角是80.51°。配体桥连2个Cu(Ⅱ)离子形成相距1.115 nm的双核铜环,而且2个配体分子中的吡啶环间和苯环间的二面角都是0°,分别平行。以金属离子Cu(Ⅱ)为节点,进一步沿a轴方向形成串珠形一维链状结构。
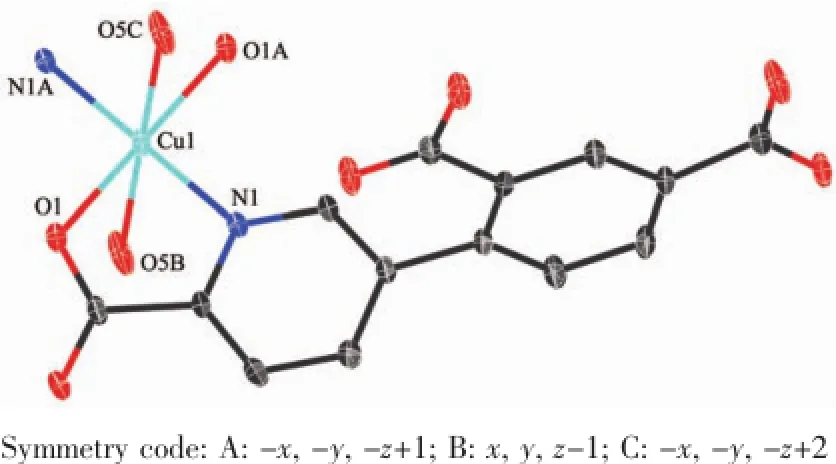
图2 化合物1中金属Cu(Ⅱ)配位环境图Fig.2Coordination environment of Cu(Ⅱ)in complex 1 with ellipsoids of 30%level
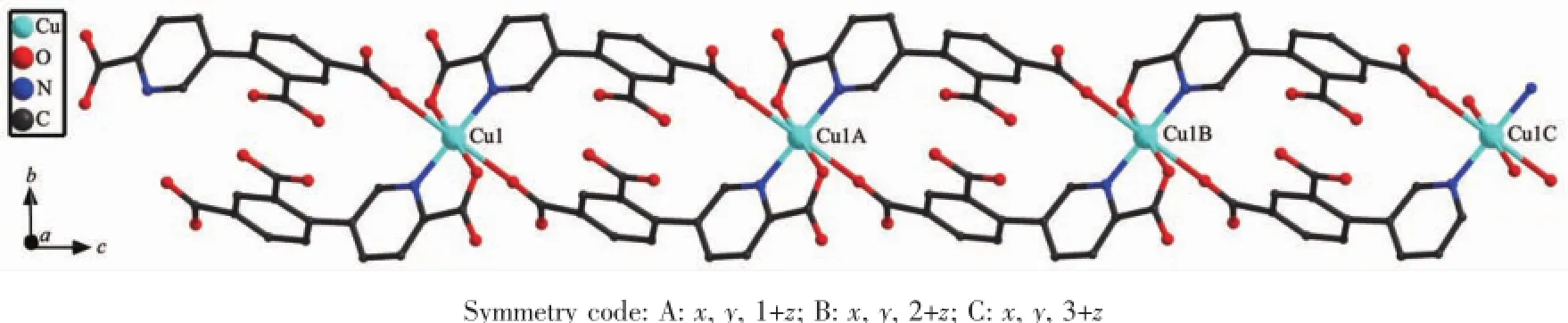
图3 化合物1的一维链状结构Fig.31D chain structure of the complex 1
2.2.2 [Mn2(Hdpcp)2(H2O)2·2H2O]n(2)晶体结构描述
在化合物[Mn2(Hdpcp)2(H2O)2·2H2O]n生成过程中,配体H4dpcp在水热条件下也原位脱羧生成H3dpcp,与金属Mn(Ⅱ)结晶在C2/c空间群中。如图4所示,1个Mn(Ⅱ)离子与4个Hdpcp2-配体和1分子水配位。4个赤道平面的配位点分别被Hdpcp2-配体中O5A,O2C和O6B以及配位水分子O7占据,N1A和O1占据轴向位置。Mn1-O7键长为0.223 1(2) nm,Mn1-O5键长为0.220 49(18)nm,Mn1-O2键长为0.213 0(2)nm,Mn1-O6键长为0.222 03(19)nm,N1A-Mn1-O1键角为162.11°,形成了畸变的六配位八面体配位构型(键长和键角见表2)。其中Hdpcp2-配体分子吡啶环上羧基的O5和O6以双齿反-反(anti-anti)桥连配位方式链接2个Mn(Ⅱ)离子,形成沿c轴方向以金属为中心,配体为桨轮状的一维链状结构(图5a)。配体苯环上羧基的O1和O2以双齿顺-顺(syn-syn)桥连配位方式链接相邻两条一维链的Mn(Ⅱ),形成二维层状结构(图5b)。二维层间通过羧基的氢键作用(O(4)-H(4)…O(3))形成三维超分子结构(图5c)。
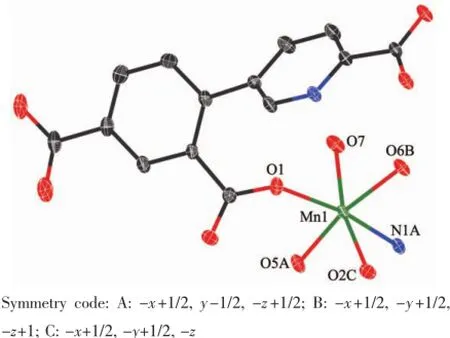
图4 化合物2中金属Mn(Ⅱ)配位环境图Fig.4Coordination environment of Mn(Ⅱ)in complex 2 with ellipsoids of 30%level
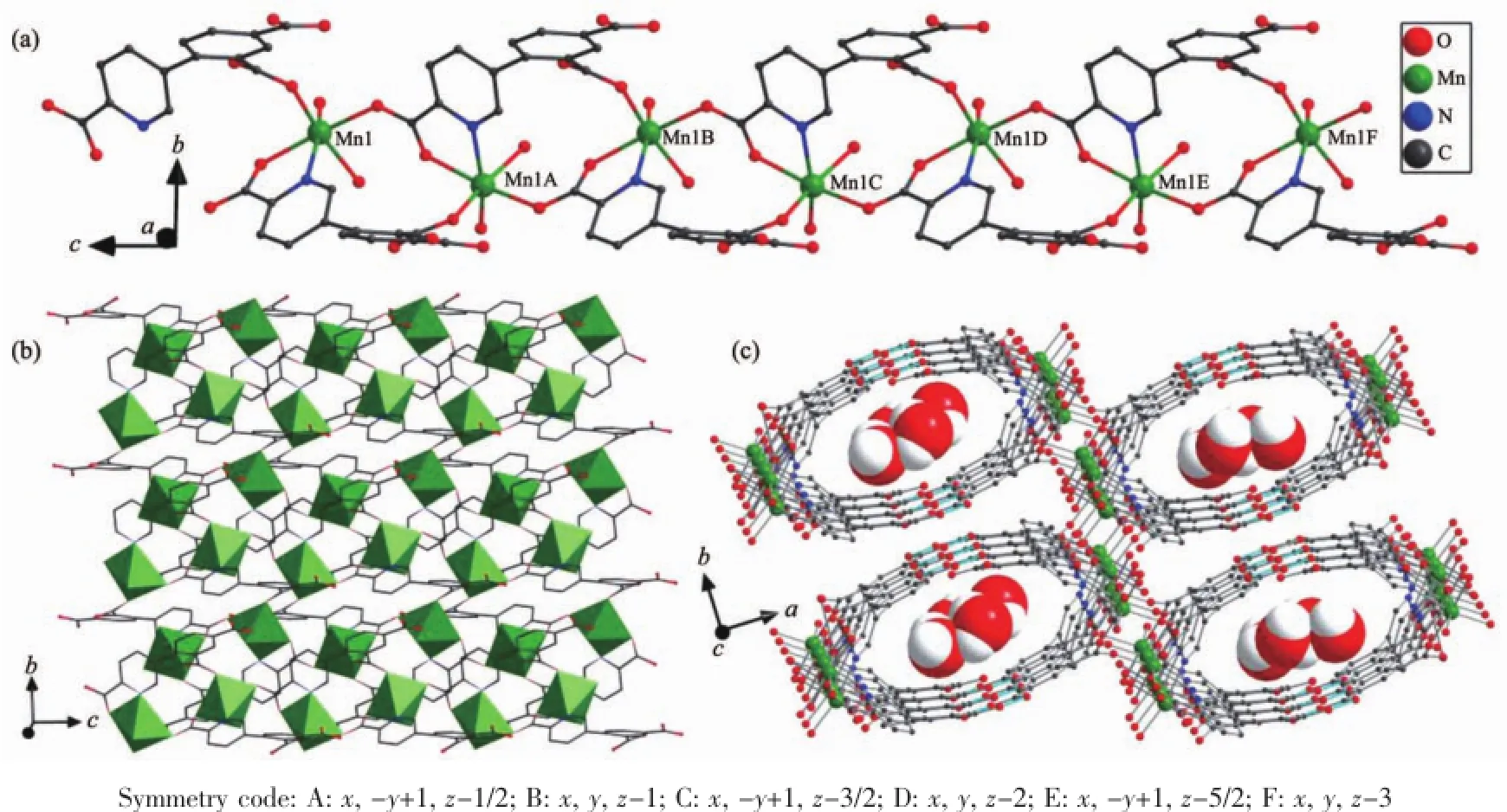
图5 化合物2的一维(a)、二维(b)和三维(c)结构Fig.5Views of 1D(a),2D(b)and 3D(c)structure of the complex 2
2.3 化合物2的磁性
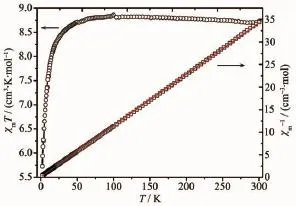
图6 化合物2的χmT对T和χm-1对T曲线Fig.6Plots of χmT vs T and χm-1vs T for 2
化合物2的变温磁化率是采用粉晶样品在1 000 Oe场强下,2~300 K温度范围内测定的,其χmT对T曲线见图6。当T=300 K时,化合物2的χmT值为8.72 cm3·K·mol-1,与没有耦合作用的2个Mn(Ⅱ)离子(6S5/2,g=2)所对应的仅自旋值之和(8.75 cm3·K·mol-1)十分相近。温度在约100~300 K之间,配合物2的χmT值几乎保持不变,然后随着温度继续下降,χmT迅速下降到最低温度2 K时的5.72 cm3·K·mol-1。化合物2的χm-1对T曲线如图6所示,该曲线是一条直线,符合Curie-Weiss定律χm-1=(T-θ)/C。利用χm-1=(T-θ)/C对实验数据进行最小平方拟合得出的直线如图6中的实线所示。最佳拟合参数Weiss常数θ=-0.80 K,Curie常数C=8.78 cm3·K· mol-1。负的Weiss常数θ表明化合物2存在反铁磁耦合作用。
[1]LIU Zhi-Liang(刘志亮).Functional Coordination Polymers (功能配位聚合物).Beijing:Science Press,2013.
[2]Liu T,Wang S N,Lu J,et al.CrystEngComm,2013,15:5476 -5489
[3]Chang X H,Qin J H,Ma L F,et al.Cryst.Growth Des., 2012,12:4649-4657
[4]ZENG Xiao-Zhe(曾晓哲),ZHANG Ai-Yun(张爱云),HE Chong(贺冲),et al.Chinese J.Inorg.Chem.(无机化学学报), 2013,29:1557-1562
[5]Zhao X Q,Zhao B,Shi W,et al.Dalton Trans.,2009:2281-2283
[6]Cui S X,Zhao Y L,Zhang J P,et al.Cryst.Growth Des., 2008,8:3803-3809
[7]Liu M S,Yu Q Y,Cai Y P,et al.Cryst.Growth Des.,2008, 8:4083-4091
[8]Zhao B,Cheng P,Dai Y,et al.Angew.Chem.,Int.Ed., 2003,42:934-936
[9]MIAO Fang-Ming(缪方明),WANG Jin-Ling(王瑾玲),JIN Tian-Zhu(金天柱),et al.Chinese J.Inorg.Chem.(无机化学学报),1992,8:180-183
[10]Goodgame D M L,Muller T E,Williams D J.Polyhedron., 1992,11:1513-1516
[11]You L X,Li Z G,Ding F,et al.Inorg.Chem.Commum., 2014,46:340-343
[12]Zhong D C,Lu W G,Jiang L,et al.Cryst.Growth Des., 2010,10:739-746
[13]Deng B,Qiu Y C,Li Y H,et al.Chem.Commun.,2008,19: 2239-2241
[14]Sheldrick G M.SHELXS-97,Program for X-ray Crystal Structure Solution,University of Göttingen,Germany,1997.
[15]Sheldrick G M.SHELXS-97,Program for X-ray Crystal Structure Refinement,University of Göttingen,Germany, 1997.
[16]CHEN Xiao-Ming(陈晓明),CAI Ji-Wen(蔡继文).Theory and Practice of Single Crystal Structure Analyses.2nd Ed. (单晶结构分析的原理与实践.2版).Beijing:Science Press, 2007.
[17]D E Billing,B J Hathaway,P Nivholls,J.Chem.Soc.A, 1970:1877
Two Coordination Polymers Generated via in situ Decarboxylation of 3-(2,4-Dicarboxylphenyl)-2,6-dicarboxylpyridine:Structure and Magnetism
YOU Li-XinWANG Shu-JuXIONG GangDING FuSUN Ya-Guang*
(Laboratory of Coordination Chemistry,Shenyang University of Chemical Technology,Shenyang 110142,China)
Two coordination polymers,[Cu(H2dpcp)2]n(1)and[Mn2(Hdpcp)2(H2O)2·2H2O]n(2)[H3dpcp=5-(2,4-dicarboxylphenyl)-2-carboxylpyridine]have been synthesized under hydrothermal conditions,and the H3dpcp ligand was formed in situ via decarboxylation of the initial 3-(2,4-dicarboxylphenyl)-2,6-dicarboxylpyridine (H4dpdp).Crystal structural analyses indicate that two complexes crystallize in the same monoclinic system,and space group P21/c for complex 1 with a=0.639(13)nm,b=1.835(4)nm,c=1.115(2)nm,β=102.29(3)°,Z=2,and space group C2/c for complex 2 with a=3.126(6)nm,b=1.004(2)nm,c=1.080(2)nm,β=93.73(3)°,Z=4.For 1,Cu(Ⅱ)were bridged by H2dpcp-ligands to form a 1D chain structure.For 2,Mn(Ⅱ)were linked by Hdpcp2-ligands to form 2D layers and further extend to a 3D structure through the hydrogen bonding interaction.The negative value of θ shows the existence of antiferromagnetic coupling in 2.CCDC:1021238,1;1021239,2.
coordination polymers;in situ decarboxylation;3-(2,4-dicarboxylphenyl)-2,6-dicarboxylpyridine;magnetism
O614.121;O614.7+11
A
1001-4861(2015)02-0323-06
10.11862/CJIC.2015.049
2014-10-13。收修改稿日期:2014-11-09。
国家自然科学基金(No.21071100)和辽宁特聘教授资助项目(No.2013204)资助项目。*
。E-mail:yaguangsun@aliyun.com
