离子色谱法测定美司钠注射中2-巯基磺酸钠的含量
2015-03-27杨柳明彭园珍林燕语
杨柳明, 彭园珍, 孙 杰, 林燕语
(1. 福建师范大学 湿润亚热带生态-地理过程省部共建教育部重点实验室, 福建 福州 350007;2. 福建师范大学 地理科学学院, 福建 福州 350007)
离子色谱法测定美司钠注射中2-巯基磺酸钠的含量
杨柳明1,2, 彭园珍1,2, 孙 杰1,2, 林燕语1,2
(1. 福建师范大学 湿润亚热带生态-地理过程省部共建教育部重点实验室, 福建 福州 350007;2. 福建师范大学 地理科学学院, 福建 福州 350007)
基于2-巯基磺酸钠的离子性,首次建立了离子色谱法测定美司钠注射液中2-巯基磺酸钠含量的新方法。采用阴离子色谱柱IonPac AS19(4 mm×250 mm)以60 mmol/L的KOH为淋洗液,进样量为25 μL、流速为1.0 mL/min的条件下,测定美司钠注射液中2-巯基磺酸钠的含量,结果在0.5~20.0 mg/L 范围内线性关系良好,相关系数为0.999 6,检出限为0.065 3 mg/L,加标回收率在95.4%~101.0%之间,方法准确可靠。
美司钠注射液; 2-巯基磺酸钠; 离子色谱
2-巯基磺酸钠(HS—CH2—CH2—SO3-Na+)也称美司钠,是一类重要的巯基化合物。在医学上美司钠作为泌尿系统的保护剂,常与抗肿瘤药物(磷酰胺或异环磷酰胺)联合使用预防肿瘤化疗时引起的出血性膀胱炎等泌尿系统上皮毒性[1-3],但过量注射亦可能带来一定副作用[4]。因此,建立高效、灵敏的美司钠分析方法对于相关药物的纯度检验及药物代谢动力学研究有重要的意义。
文献报道的测定美司钠含量的方法有容量法、比色法、高效液相色谱法、荧光光谱法、电化学方法以及拉曼光谱法[5-13]。这些测定方法,在检测限及灵敏度方面都取得较好的结果。然而,也存在操作繁琐、耗时长、环境不友好等缺点。离子色谱以其较高的准确性、高灵敏度及环境友好等特点被广泛用于阴离子、阳离子、有机酸的测定[14-16]。2-巯基磺酸钠具有磺酸基团在碱性条件下以磺酸根的形式存在,通过离子交换机制在阴离子色谱柱上具有保留能力。基于此机制,本文首次建立了一种快速、简单、环境友好的2-巯基磺酸钠测定方法,并将其用于美司钠注射液中2-巯基磺酸钠含量的测定。
1 实验
1.1 仪器与试剂
Dionex ICS-2100型离子色谱仪:配备KOH自动淋洗液发生装置,ASRS 300 4 mm抑制器,电导检测器;2-巯基磺酸钠购于Sigma (M1511; CAS:19767-45-4),美司钠注射液国内一家制药公司生产;实验用水为Milipore制备超纯水(电阻率≥18.2 MΩ.cm)。
1.2 样品处理
移取一定量的美司钠注射液并用超纯水稀释至10 000~100 000倍,过0.22 μm滤膜待测。
1.3 色谱条件
AS19阴离子分析柱(4×250 mm),AG19(4×50 mm)保护柱,柱箱温度30 ℃,60 mmol/L的溶液等浓度淋洗,流速1 mL/min,进样量25 μL。
2 结果与讨论
2.1 色谱条件选择
实验考察了不同浓度的KOH溶液(淋洗液)对2-巯基磺酸钠分离的影响,结果见图1。由图1可知,随着淋洗液浓度增加,2-巯基磺酸钠出峰时间不断变小,柱效也不断提高,当淋洗液浓度从60 mmol/L变为70 mmol/L时,出峰时间变化相对较小。因此,本方法最终选择淋洗液浓度60 mmol/L、流速为1.0 mL/min的离子色谱测定2-巯基磺酸钠的分离条件。
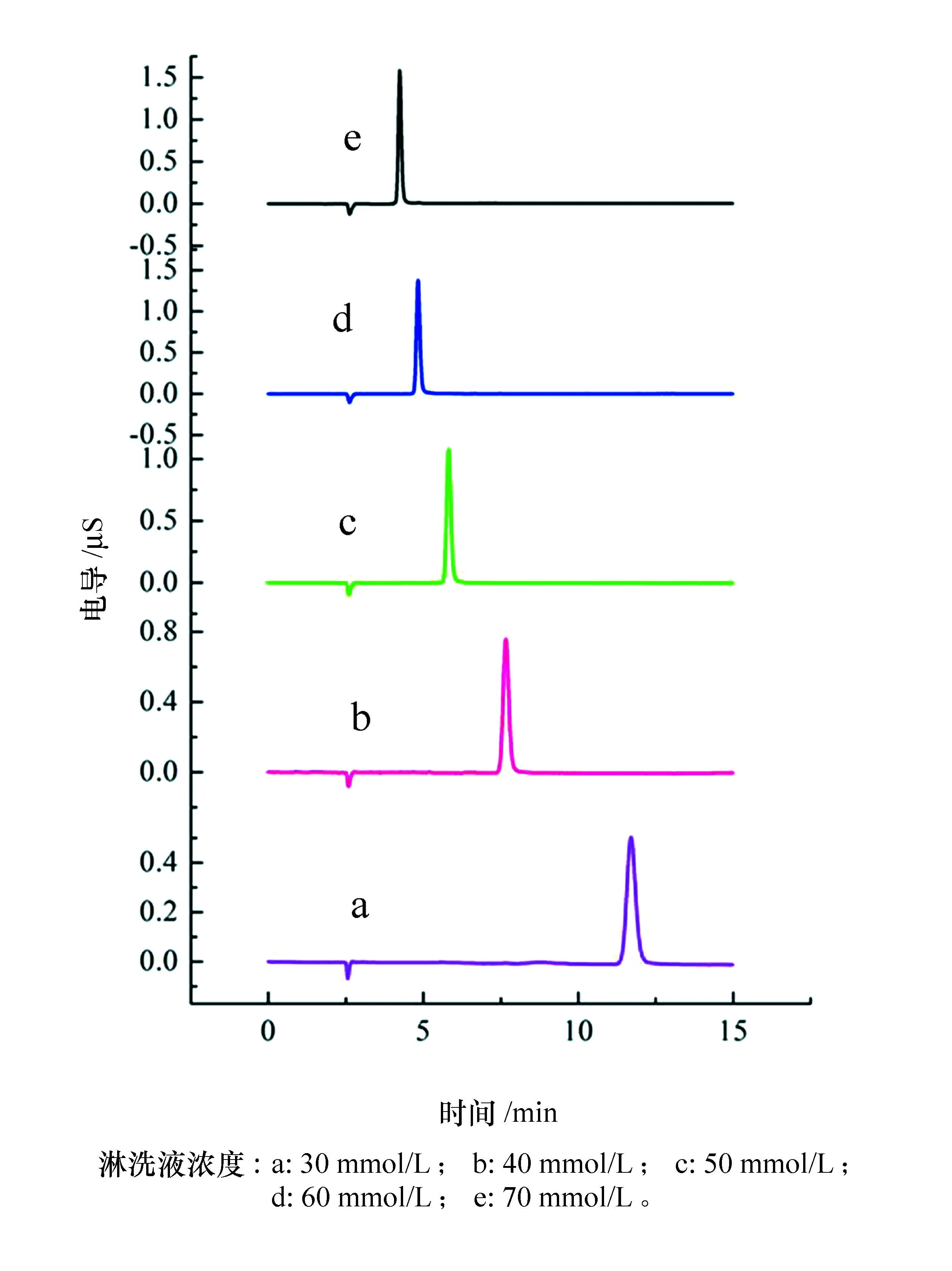
图1 不同淋洗液浓度分离2-巯基磺酸钠色谱图
2.2 线性范围和检出限
在优化的色谱条件下,得到不同浓度(浓度分别为0、0.5、1、2、5、10、20 mg/L)的2-巯基磺酸钠标准溶液的色谱图,如图2所示,2-巯基磺酸钠浓度在0.5~20.0 mg/L范围内线性良好(r=0.999 6),其线性回归方程为y=0.0455x-0.0109,以3信噪比求得检出限为0.0653 mg/L。

图2 不同浓度的2-巯基磺酸钠标准溶液的色谱图
2.3 实际样品分析及加标回收率
采用本方法对购置同一个产家的2个样品进行重复测定6次,测得2-巯基磺酸钠含量分别为98.6 g/L和98.2 g/L,相对标准偏差分别为2.47%和1.68%,将稀释不同倍数的样品溶液进行加标回收率实验,结果如表1所示(表1中样品量是指样品中2-巯基磺酸钠的含量),加标回收率在95.4%~101.0%之间,表明该方法测定的数据是准确可靠的。
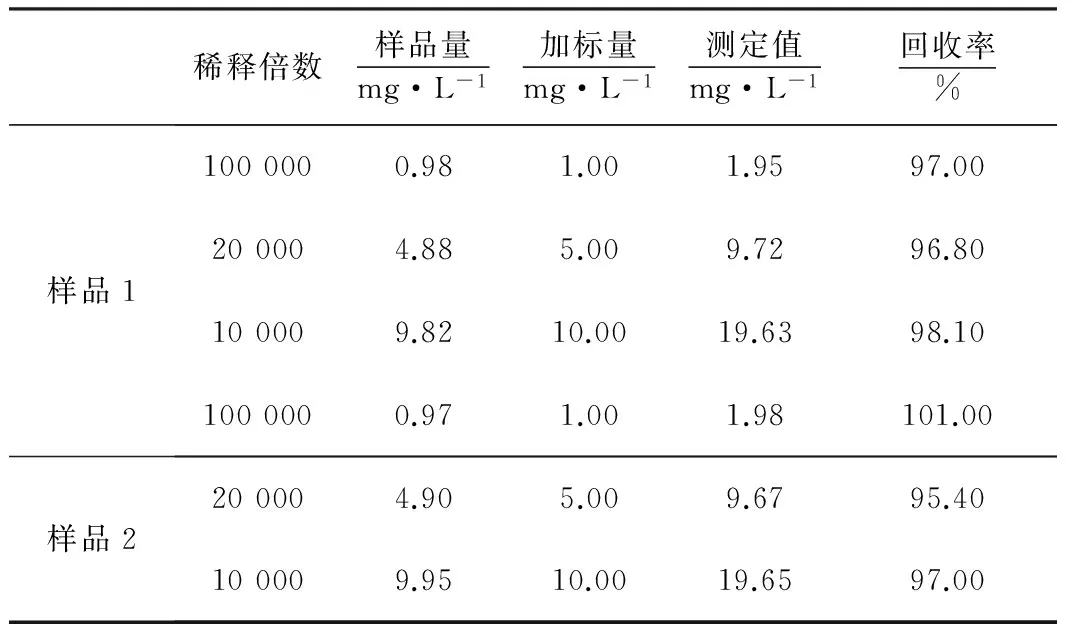
表1 2-巯基磺酸钠回收率测定(n=6)
3 结论
针对当前美司钠注射液中2-巯基磺酸钠含量的测定方法相对繁琐、耗时长等不足,本文基于2-巯基磺酸钠的离子性,建立了操作简便、环境友好的离子色谱法,并用于2-巯基磺酸钠的测定,另将其用于美司纳注射液的分析,加标回收率在95.4%~101.0%之间,表明此方法准确可靠。
)
[1]CoxPJ.Cyclophosphamidecystitis:identificationofacroleinasthecausativeagent[J].Biochemicalpharmacology,1979,28(13):2045-2049.
[2]CoxPJ.Cyclophosphamidecystitisandbladdercancer.Ahypothesis[J].EuropeanJournalofCancer,1979,15(8):1071-1072.
[3]BrockN,PohlJ,StekarJ.Detoxificationofurotoxicoxazaphosphorinesbysulfhydrylcompounds[J].Journalofcancerresearchandclinicaloncology,1981,100(3):311-320.
[4]ThackeryE.TheGaleencyclopediaofcancer[M].ThomsonDelmarLearning,2002.
[5] 中国药典委员会.中国药典[J].北京:中国医药科技出版社,2010.
[6]El-YazigiA,YusufA.Al-RawithiS.Liquidchromatographicanalysisofmesnaanddimesnainplasmaandurineofpatientstreatedwithmesna[J].Therapeutic.DrugMonitoring,1995,17(2):153-158.
[7]ApostolidesZ,VermeulenNMJ,PotgieterDJJ.High-performanceliquidchromatographyofsomecoenzymeM(2-mercaptoethanesulphonicacid)derivativesbyionpairingonreversed-phasecolumns[J].Journalofchromatography,1982,246(2):304-307.
[8]GlowackiR,WojcikK,BaldE.Facileandsensitivemethodforthedeterminationofmesnainplasmabyhigh-performanceliquidchromatographywithultravioletdetection[J].JournalofChromatographyA,2001,914(1):914,29-35.
[9]VerschraagenM,ZwiersTHU,KoningPD,etal.QuantificationofBNP7787 (dimesna)anditsmetabolitemesnainhumanplasmaandurinebyhighperformanceliquidchromatographywithelectrochemicaldetection[J].JournalofChromatographyB,2001,753(2):293-302.
[10]SidauB,ShawIC.Determinationofsodium2-mercaptoethanesulphonatebyhigh-performanceliquidchromatographyusingpost-columnreactioncolorimetryorelectrochemicaldetection[J].JournalofChromatographyB,1984,311:234-238.
[11]JamesCA,RogersHJ.Estimationofmesnaanddimesnainplasmaandurinebyhigh-performanceliquidchromatographywithelectrochemicaldetection[J].JournalofChromatographyB,1986,382:394-398.
[12]VerschraagenM,BosmaM,ZwiersTHU,etal.Quantificationofmesnaandtotalmesnainkidneytissuebyhigh-performanceliquidchromatographywithelectrochemicaldetection[J].JournalofChromatographyB,2003,783(1):33-42.
[13]ZhengX,ChenY,BiN,etal.Determinationofthesodium2-mercaptoethanesulfonatebasedonsurface-enhancedRamanscattering[J].SpectrochimicaActaPartA:MolecularandBiomolecularSpectroscopy,2011,81(1):578-582.
[14] 胡静,赵瑞峰,施文庄,等.烟草中 9 种有机酸的梯度离子色谱法测定研究[J].分析测试学报,2011,30(10):1171-1174.
[15] 刘静,李静,聂黎行,等.离子色谱法同时测定注射用丹参 (冻干)中有机酸和无机阴离子[J].药物分析杂志,2012,32(10):1774-1777.
[16] 曹家兴,杭义萍,陆建平,等.固相萃取-离子色谱法测定甘蔗糖蜜及糖蜜酒精废液中的非氮有机酸和无机阴离子[J].色谱,2010,28(9):893-897.
Determination of sodium 2-mercaptoethanesulfonate in mesna injection by using ion chromatography
Yang Liuming1,2, Peng Yuanzhen1,2, Sun Jie1,2, Lin Yan yu1,2
(1. Key Laboratory of Humid Subtroical Eco-geographical Processes,School of Geographical Science,Fujian Normal University,Fuzhou 350007, China; 2. School of Geographical Sciences,Fujian Normal University, Fuzhou 350007, China)
A new ion chromatography method is established for determination of sodium 2-mercaptoethanesulfonate base on its ionic.The ion chromatography separation is performed on an IonPac CS19 ( 4 mm×250 mm)column with 60 mmol/LKOH as the elution at the flow rate of 1.0 mL/min.The linear range of 2-mercaptoethanesulfonate is 0.5-20.0 mg/L (r=0.999 6).The detection limit is 0.065 3 mg/L. The average recovery rate is 95.4-101.0%.The method is accurate and reliable.
mesna injection; sodium 2-mercaptoethanesulfonate; ion chromatography
2014- 10- 27
国家自然科学基金项目(31300523)
杨柳明(1984—),男,福建福州,硕士,实验师,主要从事实验室仪器管理和生态环境方面的研究.
E-mail:yanglm2007@aliyun.com
R927.2
B
1002-4956(2015)6- 0059- 02
