基于聚苯胺/氧化钴的磷酸根修饰电极研究*
2015-03-27李琳娜姜涛钦杨慧中
李琳娜,姜涛钦,杨慧中
(江南大学 轻工过程先进控制教育部重点实验室,江苏 无锡214122)
0 引 言
磷是生物不可缺少的重要元素,但是随着经济的发展和人口的增长,大量含磷污水的排放,使藻类过度繁殖,导致水体富营养化,对生态平衡和人类生活产生破坏性影响,因此,水体中磷的含量是水质好坏的一项重要指标。目前,我国的水体中总磷的监测基本上采用GB 11893—1989 规定的方法[1],但是该方法检测水体总磷含量,操作复杂,检测周期长,需要消耗化学试剂,易造成二次污染。离子选择性电极测定物质浓度,简易快速,便于实现在线分析和生产自动控制,在化学化工、环保、生命科学领域的实际应用中具有重要意义[2]。在磷酸根离子选择电极的研究中,钴一直是研究重点之一。肖丹等人[3]研究了基于金属钴的磷酸根离子选择电极,同时对钴合金电极[4]对磷酸根的响应也做了研究;Lee Jin-Hwan 等人[5]研究了镀钴针形微电极阵磷酸根传感器,在磷酸二氢根的含量为1×10-5.1~1×10-3mol/L的时候响应斜率达到-96 mV。Meruva R K 和Meyerhoff M E[6]进一步研究了溶液的pH 值,离子强度,缓冲液和搅拌率对钴电极的影响。Chen Z 等人[7]用流动注射法测试了钴电极对磷酸根的响应。Engblom S O[8]用钴电极检测土壤浸出液中的磷酸根,考察磷酸根浓度范围为10-3~10-4mol/L 时斜率为-30 mV。综上可见钴电极对磷酸根有很好的斜率和电位响应,钴可以作为检测磷酸根的敏感物质。
聚苯胺是一种高分子合成材料,俗称导电塑料,是一类特种功能材料,具有塑料的密度,又具有金属的导电性和塑料的可加工性,还具备金属和塑料所欠缺的化学和电化学性能。聚苯胺作为一种敏感材料,如今已被广泛应用到分析传感探测领域。Karami H 等人[9]在铂金属电极上电聚合沉积十二烷基苯磺酸掺杂聚苯胺膜修饰电极传感器,用于探测十二烷基苯磺酸阴离子,电极在浓度范围为5.0×10-6~4.1×10-3mol/L 表现出极好的能斯特斜率(59.1±0.3)mV,检测下限低至1.0×10-6mol/L。Mousavi M F 等人[10]用类似方法在铂电极上形成的十二烷基磺酸掺杂聚苯胺膜修饰电极传感器可用于探测超微量的十二烷基磺酸阴离子,探测浓度范围为1.0×10-9~3.0×10-6mol/L,检测下限更是低至1.0×10-9mol/L。可见掺杂聚苯胺修饰电极有很大的发展前景。本文将硫酸钴作为掺杂剂,利用恒电流法,将钴掺杂入聚苯胺薄膜中,以玻碳电极为基底电极,制作了掺杂钴—氧化钴的聚苯胺修饰玻碳电极,并研究其对磷酸根的响应。
1 电极的制备
1)将玻碳电极先后在800#,1200#,1500#,2000#的金相砂纸上分别进行打磨,直到电极表面平整,再将打磨好的玻碳电极放在氧化铝粉末中打磨成光滑镜面,最后将打磨好的玻碳电极放入盛有无水乙醇的超声波清洗仪中,用功率50 W 的超声波清洗5 min,之后将无水乙醇换成去离子水,再用功率50 W 的超声波清洗10 min,如此反复2 次,保证玻碳电极表面没有其他物质残留。
2)掺杂氧化钴的聚苯胺合成:采用三电极体系,工作电极为玻碳电极,对电极为铂电极,参比电极为饱和甘汞电极。用恒电流法,聚合时间300 s。电解质溶液为0.5 mol/L的苯胺,1 mol/L 的硫酸,不同质量的硫酸钴。
3)聚合完成后,用去离子水冲洗,之后将电极放在通风处自然晾干,再将电极放在10-1mol/L 的磷酸二氢钠溶液中活化24 h。
2 实验结果与讨论
2.1 电极的响应电势
在室温,不搅拌的条件下,电位测量系统为三电极体系,即工作电极为聚苯胺/氧化钴修饰的玻碳电极,对电极为铂电极,参比电极为饱和甘汞电极。配制磷酸二氢根离子浓度为10-7,10-6,10-5,10-4,10-3,10-2,10-1mol/L 的溶液作为测试溶液,电极在每个数量级的溶液中停留测试的时间为300 s。电极的测量均在室温下进行。
不同含量硫酸钴制成的电极的线性范围均在10-1~10-4mol/L,电极的斜率和在10-2mol/L 浓度溶液中的响应时间如表1 所示。
由表1 数据可以看出:当硫酸钴的含量增多时,响应时间减少,但是电极斜率的绝对值并没有随之增加,甚至在硫酸钴含量大于50 g/L时有所减少。当硫酸钴含量为50 g/L时,电极斜率的绝对值最大,斜率为-27.1 mV/dec,根据IUPAC 建议对离子选择电极检测下限的定义,此时的电极的检测下限为9.3×10-5mol/L,因此,以下都是研究以此为条件制成的电极的特性。图1 为硫酸钴含量为50 g/L 时制成的电极对磷酸二氢根的响应曲线。
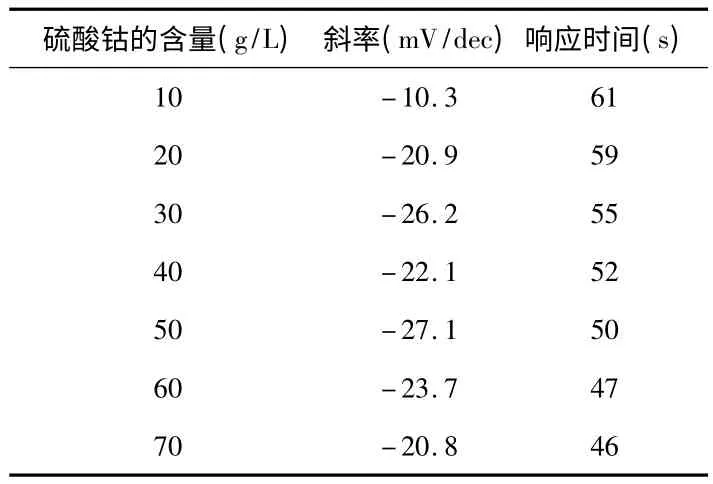
表1 不同含量硫酸钴制成电极的响应斜率以及在10-2mol/L 的磷酸二氢钠溶液中响应时间Tab 1 Response slope of electrode with different CoSO4 and the response time in 10-2mol/L NaH2PO4
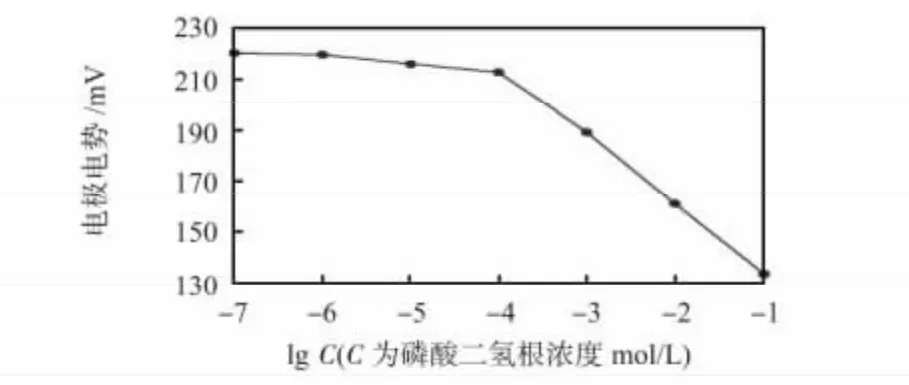
图1 电极对磷酸二氢根的响应电势曲线Fig 1 Potentiometric response curve of electrode to dihydrogen phosphate ion
在室温未搅拌的条件下,每隔一天对电极在10-1~10-7mol/L的磷酸二氢钠溶液中进行测试,记录每次的电极响应时间如表2 所示。
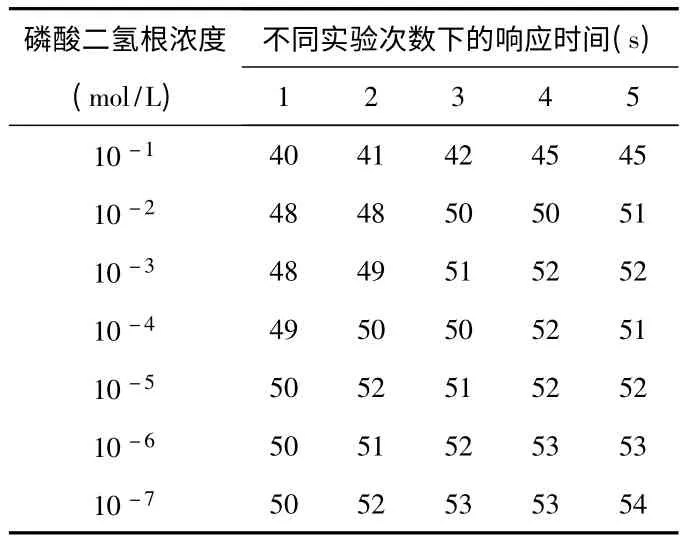
表2 电极在不同浓度磷酸二氢根溶液中的响应时间Tab 2 Response time of electrode in different concentration of phosphate ion
由表2 可以看出:电极响应时间均小于1 min,可以满足快速检测磷酸根的要求,同时随着电极的使用时间增长以及使用次数增多,电极的响应时间会有所延长。
2.2 电极的稳定性和重复性
将电极在10-2mol/L 的磷酸根离子溶液中连续测量30 min,所得结果如图2 所示,电极的电位变化浮动在±1.4 mV之间,可见电极具有较好的稳定性。
电极的重现性测试是在磷酸二氢根浓度为10-4,10-3,10-2,10-1mol/L 的溶液中,每种溶液检测10 次,每次检测时间为180 s,检测结果如图3 所示。

图2 电极在10-2mol/L 的磷酸根离子溶液中连续测量30 min 的电位曲线Fig 2 Potential curve of the electrode in 10-2mol/L phosphate anion
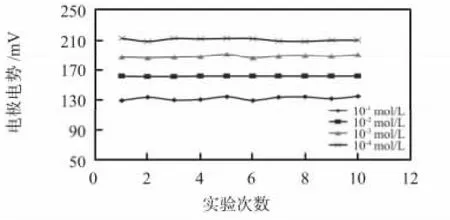
图3 不同浓度的磷酸二氢根溶液中电极的重复性测试Fig 3 Repeatability test of electrode potential in different concentration of dihydrogen phosphate solution
由图3 可以看出:该电极在同一种数量级的溶液中所产生的电势变化不大,其标准差和相对标准差如表3 所示,电极的标准差均在3 mV 之内,在每一种浓度中的相对标准偏差均小于2%,表明该电极具有良好的重复性。
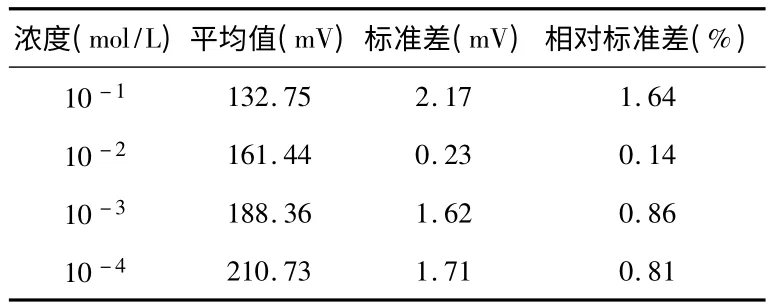
表3 电极重复性测试的标准差与相对标准差Tab 3 Standard deviation and relative standard deviation of repeatability test of electrode
2.3 电极的选择性
由于膜电极的响应没有专属性,只有相对选择性,因此,在被测溶液中,电极除对被测离子产生能斯特响应外,对被测溶液中共存的其他离子也有不同程度的响应,电极的选择性就是用来反映这种响应程度差别的。本文采用固定干扰法进行选择性测试,该方法操作过程较为复杂,但是比分别溶液法得到的结果更接近实际情况下干扰离子的影响。根据水体中常见的阴离子,本文选择,几种阴离子为固定干扰离子进行电极选择性系数的测定。在室温下,配置固定干扰离子的浓度为1.0×10-3mol/L 的一系列的磷酸二氢钠溶液,搅拌均匀后进行测试。测试结果显示水中常见阴离子对磷酸二氢根无严重干扰影响,具体结果如表4 所示。
3 结 论
本文利用电化学法中的恒电流法,成功将掺杂氧化钴的聚苯胺均匀地聚合在玻碳电极上,制作了掺杂钴—氧化钴的聚苯胺修饰玻碳电极。研究不同浓度的钴离子掺杂聚苯胺修饰电极对磷酸二氢根的响应特性,经实验比较,发现当硫酸钴的浓度为50 g/L 时,电极斜率的绝对值最大,在磷酸二氢根浓度为10-1~10-4mol/L 的范围有较好的线性,响应时间小于1 min,且具有较好的选择性,稳定性和良好的重复性。同时,此方法制作电极工艺流程比较简单,为水质中磷酸根的检测提供了一种比较有效的方法。
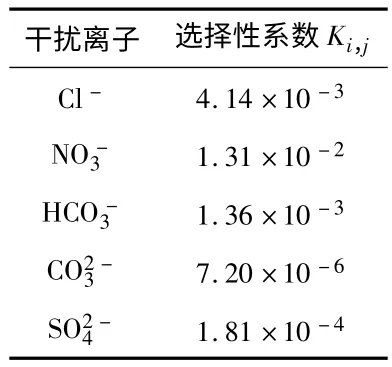
表4 磷酸根离子选择电极的选择性系数Tab 4 Selectivity coefficients of phosphate anion selective electrodes
[1] GB—11893—89.水质总磷的测定——钼酸铵分光光度法[S].北京:中国标准出版社,2002.
[2] 张军军,杨慧中.磷酸根离子选择电极的研究现状[J].传感器与微系统,2010,29(8):1-4.
[3] 肖 丹,俞汝勤,李 军,等.一种新的磷酸根离子敏感电极研究[J].高等学校化学学报,1994,15(2):193-194.
[4] 肖 丹,夏绍喜,唐志文,等.钻镍合金镀层磷酸根离子敏感电极研究[J].化学传感器,1998,18(1):63-66.
[5] Lee Jin Hwan,Lee Woo Hyoung,Bishop Paul L,et al.A cobaltcoated needle-type microelectrode array sensor for in situ monitoring of phosphate[J].Journal of Micromechanics and Microengineering,2009,19(2):025022.
[6] Meruva R K,Meyerhoff M E.Mixed potential response mechanism of cobalt electrodes toward inorganic phosphate[J].Analytical Chemistry,1996,68(13):2022-2026.
[7] Chen Z,De Marco R,Alexander P W.Flow-injection potentiometric detection of phosphates using a metallic cobalt wire ion-selective electrode[J].Analytical Communications,1997,34(3):93-95.
[8] Engblom S O.Determination of inorganic phosphate in a soil extract using a cobalt electrode[J].Plant and Soil,1999,206(2):173-179.
[9] Karami H,Mousavi M F.Dodecyl benzene sulfonate anion-selective electrode based on polyaniline-coated electrode[J].Talanta,2004,63(3):743-749.
[10]Mousavi M F,Shamsipur M,Riahi S.Design of a new dodecyl sulfate-selective electrode based on conductive polyaniline[J].Analytical Sciences,2002,18:137-140.
