钙钛矿化合物SrFe1−xCuxO3−δ(0≤x≤0.3)的制备及磁性
2015-03-25董存军彭国令聂耀庄郭光华
董存军,彭国令,聂耀庄,郭光华
(中南大学 物理与电子学院,长沙 410083)
钙钛矿化合物具有许多优良的物理、化学性质,例如量子输运、氧输运等,使它在自旋电子器件、氧燃料电池等应用上有较广阔的发展前景[1−5],引起了人们的广泛关注。立方结构的钙钛矿化合物SrFeO3在液氦温度有着螺旋自旋结构,这种螺旋自旋结构可以理解为双交换和超交换相互作用的相互竞争,其中双交换相互作用倾向于表现铁磁性(FM),超交换相互作用倾向于表现反铁磁性(AFM)[1]。大量研究表明,通过调节高压、成分和空位等条件可以实现电子结构的调控,如SrFeO3在7 GPa下也已经实现从螺旋自旋态向铁磁态的转变[6],调节氧空位可以实现(SrTiO3)n(SrFeO3−δ)1超点阵发生磁结构相变[7]等。通过Fe位或Sr位掺杂可以调节SrFeO3的自旋结构和费米能级,例如MAIGNAN 等[8]发现SrFe1−xCoxO3−δ在0≤x≤0.7的范围内可表现出金属性和铁磁性。SrFeO3-δ的晶体结构与氧含量也有很大关系,不仅如此,氧含量和Fe4+/Fe3+离子比例也在很大程度上影响着SrFeO3−δ的磁结构和性质[9−10]。
SrFeO3−δ是目前研究较多的钙钛矿化合物之一,对它的磁性做了大量的研究。但是对Fe位掺较低价态元素的研究却很少,在钙钛矿结构的化合物中Fe通常是+3和+4的混合价态[11],将Fe离子替代成+2和+3价态[12]的Cu离子会产生更多的氧空位,从而影响铁磁Fe4+-O-Fe3+相互作用和反铁磁Fe4+-O-Fe4+交换相互作用,这会导致磁性的巨大变化。本文采用溶胶凝胶法通过Fe位掺Cu研究其对晶体结构和磁性的影响。
1 实验
1.1 SrFe1−xCuxO3−δ(0≤x≤0.3) 的制备
采用溶胶−凝胶法制备SrFe1−xCuxO3−δ多晶样品[13]。原料为Sr(NO3)2(99.99%)、Fe(NO3)3·9H2O(99.99%)和Cu(NO3)2·6H2O(99.99%)。按SrFe1−xCuxO3−δ中金属阳离子的比例计算出所需要的各种硝酸盐的质量,用电子分析天平(99.99%)称取后溶于适量的去离子水中,加入适量柠檬酸和乙二醇作络合剂,再缓慢滴加浓氨水调节pH=3,然后在353 K的水浴环境下搅拌使形成凝胶,将凝胶转入393 K的干燥箱中保温12 h,再将干凝胶在空气中加热使其自燃以分解其中的有机物,研磨成粉后放入马弗炉中在673 K空气环境下保温4h,研磨后得到SrFe1−xCuxO3−δ的前驱物。再将前驱物在34 MPa下保压20 min成直径12 mm、厚2 mm的圆片,最后在1 273 K下烧结8 h,随炉冷却,得到最终样品。
1.2 测试分析
采用日本理光Rigaku D/Max 2500转靶X射线衍射仪(XRD)检测样品的单相性(CuKα射线源,入射波长0.154 1 nm),测量角度2θ范围为20°~80°,步进0.02°。采用Rietveld方法进行晶体结构精修[14],精修程序是Fullprof refinement program[15]。采用美国Quantum Design物性综合测量系统(PPMS)来测试样品的磁性,温度变化范围为3~300 K,磁场变化范围为−5~5 T。
2 结果与讨论
2.1 晶体结构
制备Fe位掺Cu的SrFe1−xCuxO3−δ(x= 0~0.3)的同时,通过原子吸收光谱ICP进一步验证样品的Cu含量。在室温条件下检测所有样品的XRD,结果如图1所示,图1表明x=0和x=0.1的样品中没有任何杂相存在,x=0.2,0.3的样品中存在少量Sr3Cu5O8的杂相,而当x≥0.4时,Sr3Cu5O8杂相非常明显,结晶性较差。如图1插图所示,在衍射峰2θ~47°处,x=0的样品在(200)峰处有一个劈裂,这与Hemery等人的研究结果类似。他们认为立方结构的SrFeO3没有劈裂,而随氧缺位δ增加,对称性降低,就会出现一些劈裂峰,如正方结构的Sr8Fe8O23的(200)峰[16−17]。而掺Cu之后的SrFe1−xCuxO3−δ在晶面(200)处没有劈裂,通过Rietveld结构精修进一步研究SrFe1−xCuxO3−δ(x=0~0.3)的结构变化。
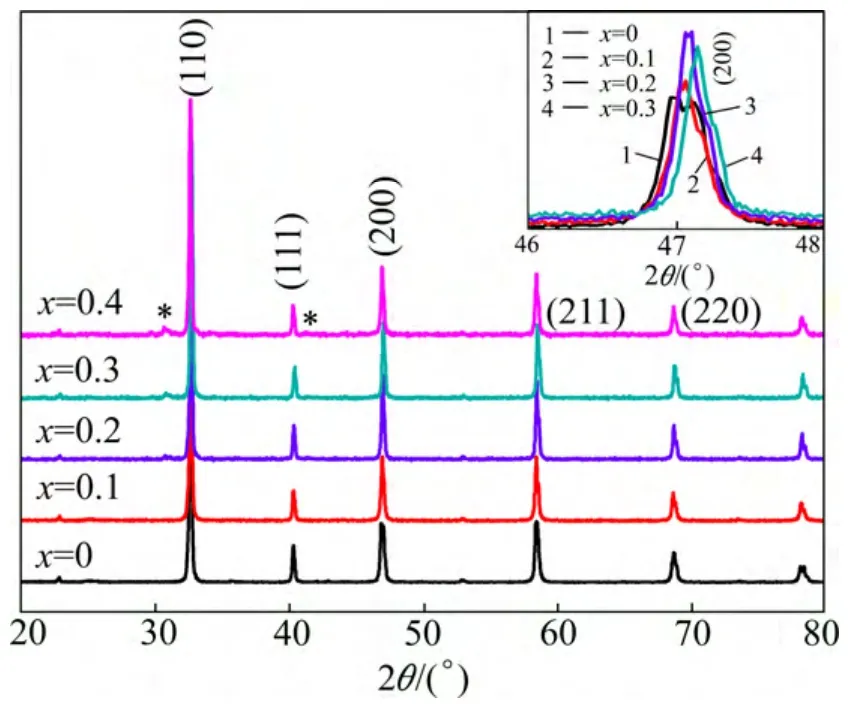
图1 SrFe1−xCuxO3−δ(x=0~0.4)的XRD图谱,其中插图是样品在(200)晶面处放大的图谱Fig.1 XRD patterns of SrFe1−xCuxO3−δ(x=0~0.4), and the inset shows an enlarged view of the (200) plane from the samples with x=0, 0.1, 0.2 and 0.3
采用正方结构(I4/mmm点群)、斜方结构(Cmmm点群)和立方结构(Pm点群)3种空间点群对所有样品的XRD图谱进行指标化,结果表明正方结构(I4/mmm点群)和立方结构(Pm点群)空间点群分别能很好地拟合SrFeO3-δ和SrFe1−xCuxO3−δ(x=0.1~0.3)的XRD实验数据。如表1所列,表1中,用<Sr-O>/<B-O>比值表示容忍因子t,其中<Sr-O>表示Sr2+和O2−的离子间距,<B-O>表示B离子和O2−的离子间距。对于x=0的样品,<Sr-O>和<B-O>表示平均键长,为样品的部分结构参数,采用正方结构(I4/mmm点群)指标化得到样品x=0的衍射谱峰型因子Rp、权重因子Rwp和拟合的平方误差χ2分别为11.3、18.2和1.58,而采用斜方结构(Cmmm点群)指标化得到的Rp、Rwp和χ2分别为29.5、36.4和6.29,明显高于正方结构(I4/mmm点群)的结果,误差很大,而采用立方结构则完全不能指标化。所以,x=0的样品可能是正方结构,空间点群为I4/mmm(a=b=10.922 2Å,c=7.694 7Å),与KAGEYAMA等[18]的研究结果一致;而同样采用正方结构模型对SrFe1−xCuxO3−δ(x=0.1~0.3)进行指标化得到的误差较大,采用Pm 3 m点群进行指标化,得到点阵参数依次为3.860 7,3.858 2和3.857 3Å,这一结果与ER-RAKHO L等的研究结果也基本一致。他们认为SrFe1−xCuxO3−δ(x=0.1~0.3)为有一定氧空位的立方结构[19−23]。由图2可以看出晶格常数随Cu含量增加而减小,这是由于将钙钛矿结构的Fe离子替代成Cu2+或Cu3+,会导致形成更多的氧空位[12],也符合Goldschmidt定律[24],而且x=0和x=0.1的样品的晶格常数变化很大,这也说明样品可能发生了结构相变。不仅如此,根据容忍因子
表1 SrFe1−xCuxO3−δ(x=0, 0.1, 0.2, 0.3)样品的部分结构参数Table 1 Some structure parameters of the SrFe1−xCuxO3−δ(x=0, 0.1, 0.2, 0.3), and the Rietveld structural refinement of sample x=0 and x=0.1, 0.2, 0.3 performed using the space group I4/mmm and Pmas a starting model
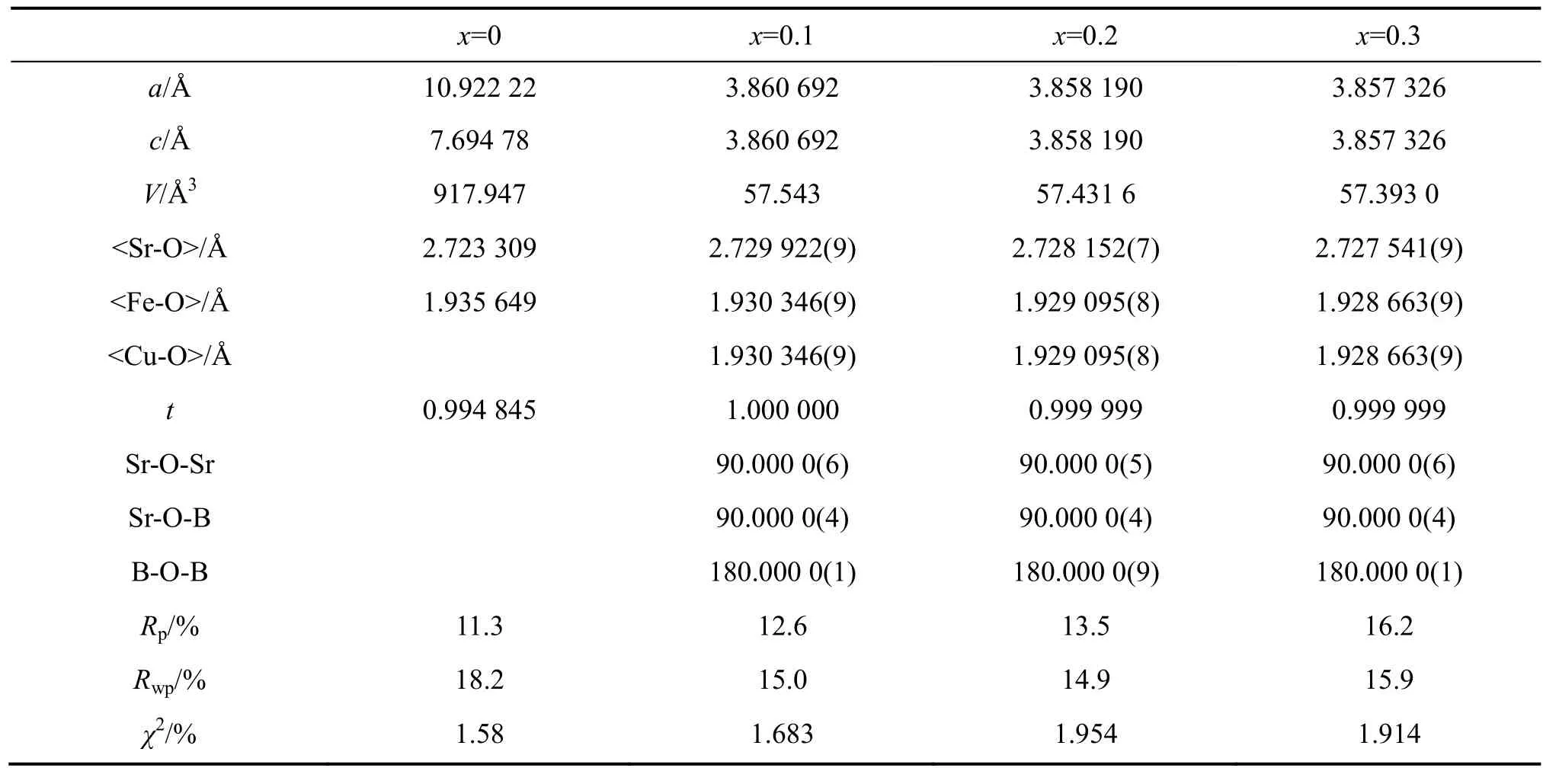
表1 SrFe1−xCuxO3−δ(x=0, 0.1, 0.2, 0.3)样品的部分结构参数Table 1 Some structure parameters of the SrFe1−xCuxO3−δ(x=0, 0.1, 0.2, 0.3), and the Rietveld structural refinement of sample x=0 and x=0.1, 0.2, 0.3 performed using the space group I4/mmm and Pmas a starting model
?

式中:rL、rO分别为Sr离子和氧离子半径;rB为金属阳离子FeCu的平均离子半径。由式(1)得到x=0样品的容忍因子t=0.994 845,随Cu含量增加键长逐渐减小,尽管如此容忍因子仍保持0.999 999值基本不变,而理想的立方结构的钙钛矿结构化合物的容忍因子t=1[25],说明实验结果与理想的立方结构符合得很好。图3所示为x=0.1样品的结构精修拟合曲线,拟合曲线与实验曲线符合很好,说明立方结构(Pm 3 m点群)能更合理的描述SrFe1−xCuxO3−δ(x= 0.1~0.3)的晶体结构。
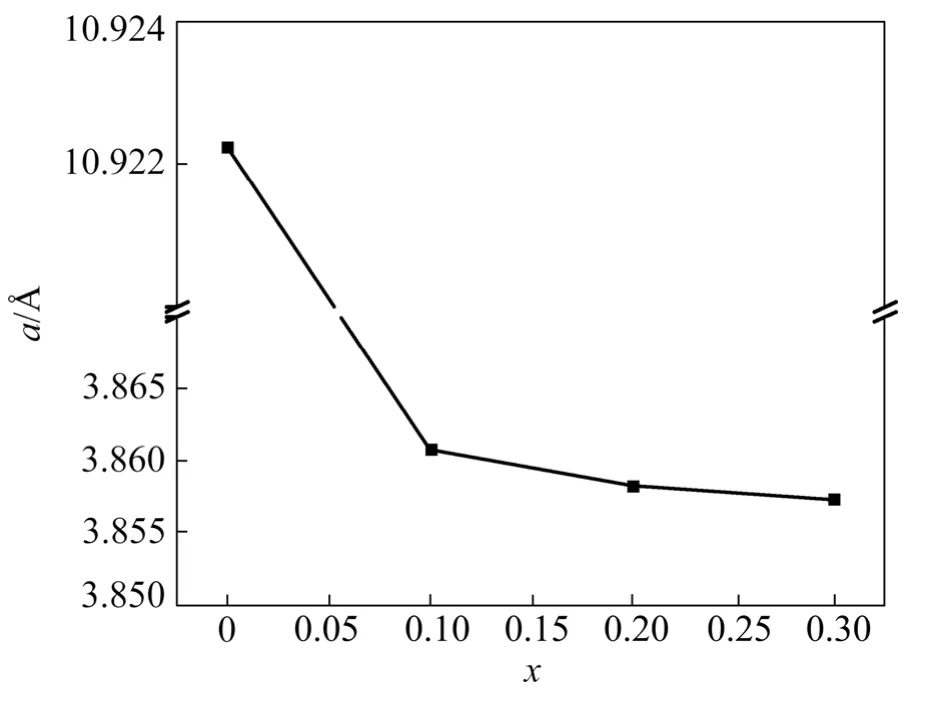
图2 晶格参数随掺Cu程度的变化Fig.2 Unit cell parameters versus Cu dopping of SrFe1−xCuxO3−δ
2.2 磁性能研究
大量研究表明SrFeO3在低温下有螺旋自旋结构[26−28],这也引起了SrFeO3−δ的零场冷(ZFC)和场冷(FC)曲线不可逆[29]。本研究也得出了类似的结果,如图4所示,给出了SrFe1−xCuxO3−δ(0≤x≤0.3)系列在外场0.1 T下测得的零场冷(ZFC)−场冷(FC)曲线。x=0样品在低温32 K附近有一个明显的转变点,这可能是样品在低温下有螺旋自旋结构引起的。对比0≤x≤0.3样品的零场冷(ZFC)−场冷(FC)曲线不难看出,在转变温度以下随着温度的降低,这两个过程是不可逆的,且Cu含量越高,ZFC和FC曲线表现出的差异越大,这说明样品在转变温度以下可能处于自旋玻璃态。其原因可能是随Cu含量增加,氧空位浓度会逐渐升高,由于Sr保持一个相对稳定的+2价态不变,会使部分Fe4+转变成Fe3+以维持价态平衡,使得Fe3+/Fe4+离子比例增加,铁磁交换相互作用和反铁磁交换相互作用的竞争也可能越来越激烈,从而形成自旋玻璃态。
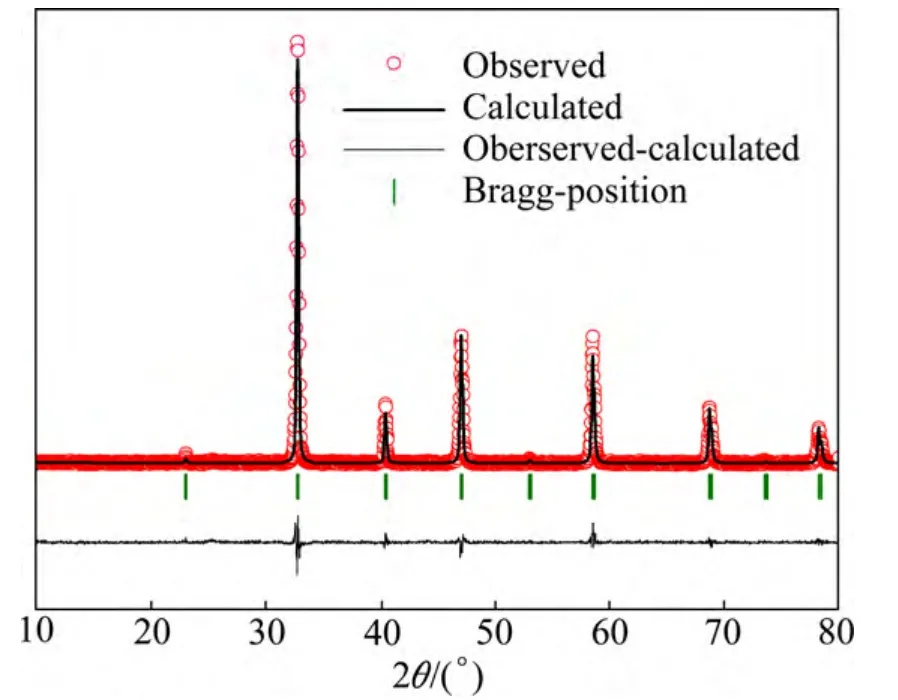
图3 SrFe0.9Cu0.1O3-δ样品的结构精修图Fig.3 Observed (circle), calculated (lines), and different plots from the structural refinement of the XRD data for SrFe0.9Cu0.1O3−δ.The ticks represent the positions of the calculated Bragg reflection
从x=0的样品的零场冷(ZFC)曲线可以看出,随温度升高,磁化强度显著增加,在83 K处达到最大,随温度继续升高,磁化强度显著减小,这说明样品的奈尔温度为TN=83 K,这与Sr8Fe8O23的奈尔温度70 K很接近。其它不同氧空位的SrFeO3−δ都有不同的奈尔温度,如Sr4Fe4O11的奈尔温度为240 K[17]。而且从精修结果来看,x=0的样品与Sr8Fe8O23有相同的点群结构[18],所以x=0的样品可能是Sr8Fe8O23。不仅是83 K附近的转变,在120 K附近也能看到一个类似台阶的变化,这一结果正好和SRINATH等的研究结果相吻合。他们认为这是残余立方相SrFeO3造成的[29],而样品SrFe1−xCuxO3−δ(0.1≤x≤0.3)中则没有这个现象。从其它样品的零场冷曲线可以看出,掺Cu引起样品x=0.1,0.2和0.3的转变温度低于x=0的样品,但随掺杂程度增加,样品x=0.1,0.2和0.3的转变温度又逐渐上升。假设这里的转变温度是奈尔温度,由于影响奈尔温度的因素很多,例如Fe3+/Fe4+比例的变化、点阵空间以及点阵对称性等都会影响奈尔温度[30],所以也很难简单地解释SrFe1−xCuxO3−δ(0≤x≤0.3)样品中奈尔温度的变化。但是要确定样品的转变温度是奈尔温度还是自旋玻璃态转变温度,还需要进一步研究。
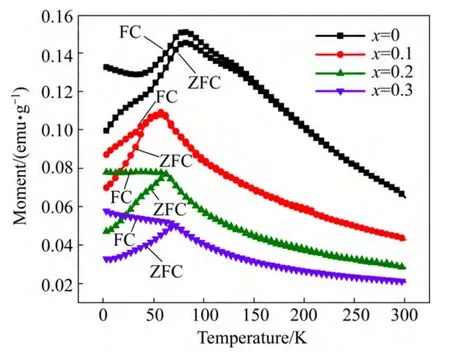
图4 SrFe1−xCuxO3−δ(0≤x≤0.3)系列在外场0.1 T下测得的ZFC-FC曲线Fig.4 Zero field cooled (ZFC) and field cooled (FC)measurement for SrFe1.xCuxO3−δ(0≤x≤0.3) at 0.1T
从图4中还可以看出,单位样品的磁化强度随Cu含量增加而减小。这可能是掺Cu使得Fe离子浓度降低,造成Fe/Cu位总有效磁矩减小,从而引起磁化强度的降低。根据反铁磁物质的分子场理论简单估算样品的有效磁矩。对简立方晶体而言,居里常数C和有效磁矩µeff分别为
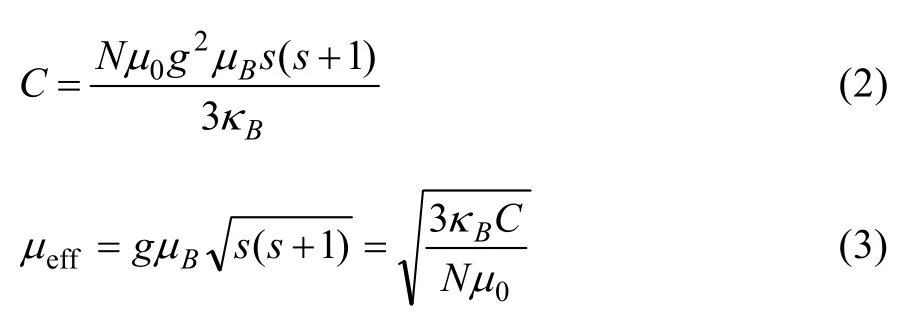
式中:N为单位体积内的磁性离子数;g为朗德因子;S为磁性离子白旋;µ0为真空磁导率,µB为波尔磁子。根据以上两式得到样品有效磁矩µeff的方程式为

再通过拟合磁化率的可逆部分,得到C值,根据方程(4)计算Fe/Cu位的有效磁矩。图5所示为转变温度和有效磁矩随掺杂程度的变化。其中x=0的样品有效磁矩为5.77μB,正好介于Fe4+(S=2)和Fe3+(S=5/2)的理论值4.9μB与5.9μB之间。随Cu含量(0.1≤x≤0.3)增加,Fe/Cu位的有效磁矩逐渐减小,分别为5.24μB,4.16μB和3.90μB,所以单位样品的磁化强度随Cu含量增加而减小。
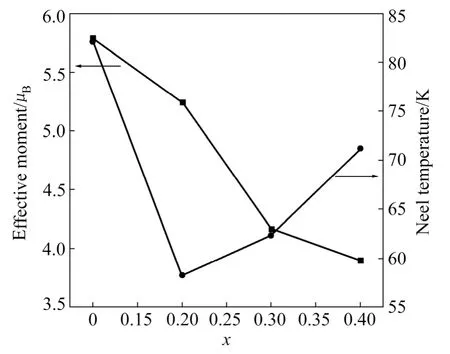
图5 有效磁矩与转变温度随Cu含量的变化Fig.5 The effective magnetic moment and transition temperature versus content of Cu in SrFe1−xCuxO3−σ
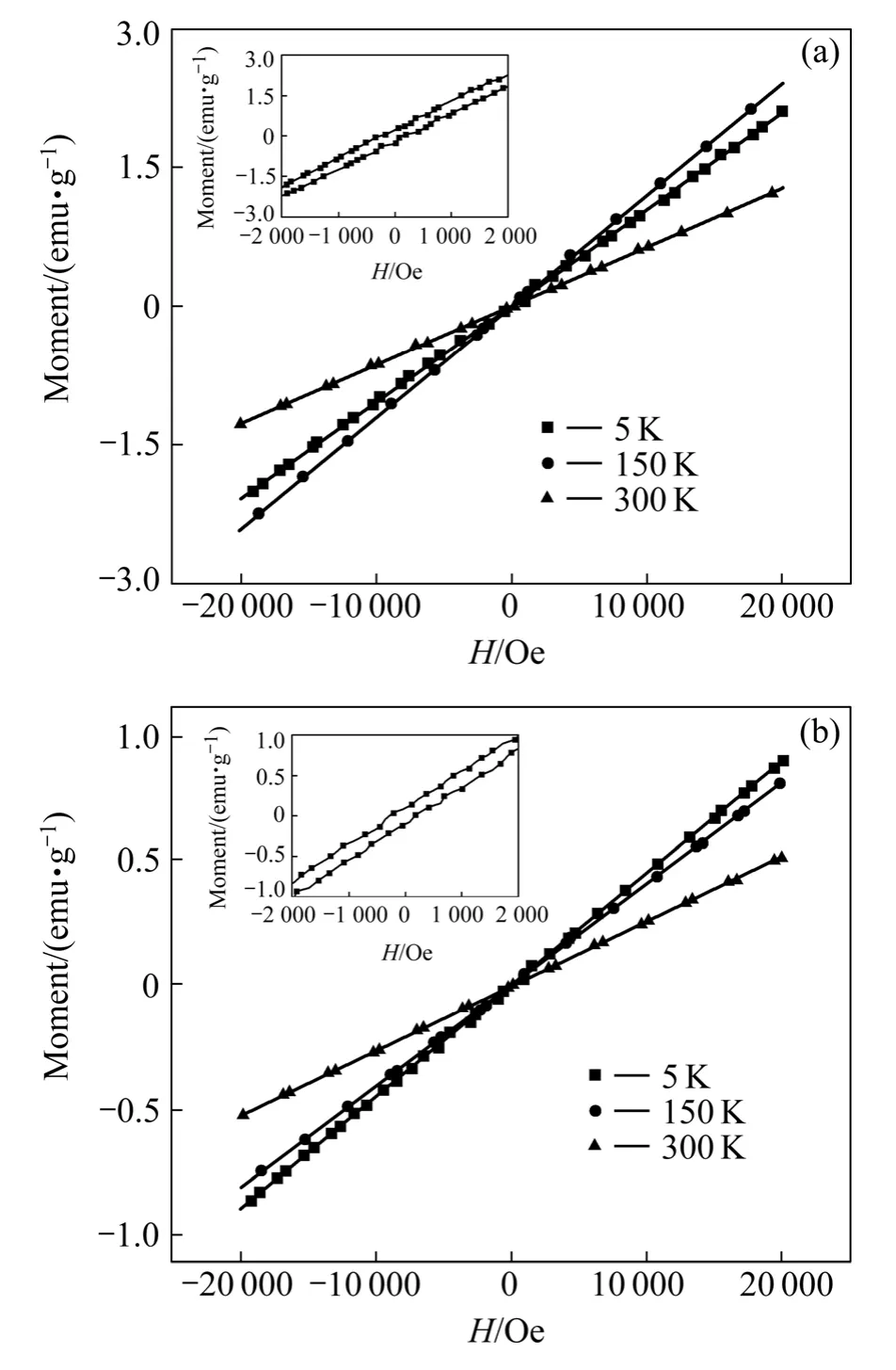
图6 x=0(a)和x=0.2(b)的样品在5、150和300 K时的磁化曲线Fig.6 Magnetization curves of samples x=0 (a)and x=0.2 (b) at 5, 150 and 300 K
进一步测量所有样品的磁化曲线,结果如图6所示。由图可知,x=0(a)和x=0.2(b)样品的磁化曲线在5、150和300 K时都呈现很好的线性关系,这也进一步说明样品在转变温度以下呈自旋玻璃态,在转变温度以上则是顺磁性。但是,在低温(5 K)时,样品都表现出非常微弱的磁滞现象,如图6的插图所示。这可能是样品中存在铁磁相互作用的结果,即铁磁相互作用和反铁磁相互作用共存的结果。在螺旋磁结构的材料中是很典型的,例如在MnSi的磁化曲线中也能看到这种现象[31]。
3 结论
1) 掺Cu诱发结构相变,x=0的样品为正方结构(I4/mmm点群),容忍因子t=0.994 845,而x=0.1,0.2和0.3的样品均为立方结构(Pm点群),容忍因子保持t=0.999 999基本不变。随Cu含量增加,样品的晶格常数减小,遵循Goldschmidt定律。
2) 随Cu含量增加,钙钛矿氧化物SrFe1−xCuxO3−δ零场冷(ZFC)曲线和场冷(FC)曲线的差异越来越明显,形成自旋玻璃态;样品x=0.1,0.2和0.3的转变温度低于x=0样品的转变温度,但随Cu含量增加,样品x=0.1,0.2和0.3的转变温度逐渐升高;
3) 随Cu含量增加,钙钛矿化合物SrFe1−xCuxO3−δ的Fe离子浓度降低,造成Fe/Cu位总的有效磁矩减小,从而引起磁化强度降低。
[1]LI Z, IITAKA T, TOHYAMA T.Pressure-induced ferromagnetism in cubic perovskite SrFeO3and BaFeO3[J].Physical Review B, 2012, 86(9): 094422.
[2]ISHIWATA S, TOKUNAGA M, KANEKO Y, et al.Versatile helimagnetic phases under magnetic fields in cubic perovskite SrFeO3[J].Physical Review B, 2011, 84(5): 054427.
[3]KAWASAKI S, TAKANO M, TAKEDA Y.Ferromagnetic properties of SrFe1−xCoxO3synthesized under high pressure [J].Journal of Solid State Chemistry, 1996, 121(1): 174−180.
[4]SCHMIDT M, CAMPBELL S J.Crystal and magnetic structures of Sr2Fe2O5at elevated temperature [J].Journal of Solid State Chemistry, 2001, 156(2): 292−304.
[5]祝宝军, 贡 涛, 唐元洪, 等.固体氧化物燃料电池阴极材料La1−xSrxMnO3的制备方法[J].粉末冶金材料科学与工程,2005(5): 264−267.ZHU Bao-jun, GONG Tao, TANG Yuan-hong, et al.Preparation method of La1−xSrxMnO3as cathode materials of solid oxide fuel cell [J].Materials Science and Engineering of Powder Metallurgy, 2005(5): 264−267.
[6]KAWAKAMI T, NASU S.High-pressure Mössbauer spectroscopy of perovskite high valence iron oxides under external magnetic field [J].Journal of Physics: Condensed Matter, 2005, 17(11): S789−S793.
[7]BERGER R F, BROBERG D P, NEATON J B.Tuning the electronic structure of SrTiO3/SrFeO3−xsuperlattices via composition and vacancy control [J].APL Materials, 2014, 2(4):46101.
[8]MAIGNAN A, MARTIN C, NGUYEN N, et al.Magnetoresistance in the ferromagnetic metallic perovskite SrFe1−xCoxO3[J].Solid state sciences, 2001, 3(1): 57−63.
[9]ADLER P, LEBON A, DAMLJANOVIĆ V, et al.Magnetoresistance effects in SrFeO3−δ: dependence on phase composition and relation to magnetic and charge order [J].Physical Review B, 2006, 73(9): 094451.
[10]LEBON A, ADLER P, BERNHARD C, et al.Magnetism,charge order, and giant magnetoresistance in SrFeO3−δsingle crystals [J].Physical Review Letters, 2004, 92(3): 037202.
[11]MARTYNCZUK J, LIANG F, ARNOLD M, et al.Aluminum-Doped perovskites as high-performance oxygen permeation materials [J].Chemistry of Materials, 2009,21(8):1586−1594.
[12]BRINGLEY J F, SCOTT B A, LA PLACA S J, et al.Synthesis of the defect perovskite series LaCu03−δwith copper valence varying from 2+ to 3+ [J].Nature, 1990, 347: 263−265.
[13]彭建兵, 宋慧娟, 喻宁亚, 等.磁性SrFeO3−x/SrFe12O19光催化材料的制备及可见光催化性能测试[J].化工新型材料,2010(003): 71−73.PENG Jian-bing, SONG Hui-juan, YU Ning-ya, et al.Preparation and photocatalytic performance of magnetic SrFeO3−x/SrFe12O19composite [J].New Chemical Materials,2010(003): 71−73.
[14]RIETVELD H.A profile refinement method for nuclear and magnetic structures [J].Journal of Applied Crystallography,1969, 2(2): 65−71.
[15]RODR GUEZ-CARVAJAL J.Recent advances in magnetic structure determination by neutron powder diffraction [J].Physica B: Condensed Matter, 1993, 192(1): 55−69.
[16]MANIMUTHU P, VENKATESWARAN C.Evidence of ferroelectricity in SrFeO3−δ[J].Journal of Physics D: Applied Physics, 2012, 45(1): 15303.
[17]HEMERY E, WILLIAMS G, TRODAHL H.Anomalous thermoelectric power in SrFeO3−δfrom charge ordering and phase separation [J].Physical Review B, 2007, 75(9): 092403.
[18]HODGES J P, SHORT S, JORGENSEN J D, et al.Evolution of oxygen-vacancy ordered crystal structures in the perovskite series SrnFenO3n−1(n=2, 4, 8, and ∞), and the relationship to electronic and magnetic properties [J].Journal of Solid State Chemistry, 2000, 151(2): 190−209.
[19]KAUS I, ANDERSON H U.Electrical and thermal properties of La0.2Sr0.8Cu0.1Fe0.9O3−δand La0.2Sr0.8Cu0.2Fe0.8O3−δ[J].Solid State Ionics, 2000, 129(1): 189−200.
[20]TAO S, YAN J, LU T, et al.Model of microdomain structure in crystalline SrFe0.7Cu0.3O3−δ[J].Solid State Ionics, 2005,176(13/14): 1225−1228.
[21]ZHANG H, WANG T, DONG X, et al.Preparation and oxygen permeation properties of SrFe(Cu)O3−δdense ceramic membranes [J].Journal of Natural Gas Chemistry, 2009, 18(1):45−49.
[22]ER-RAKHO L, MICHEL C, STUDER F, et al.The oxygen deficient perovskites AFe1−xCuxO2.5−x/2+δ(A=Sr, Ba) exhibiting mixed valence of iron and copper ions [J].Journal of Physics and Chemistry of Solids, 1988, 49(9): 1101−1106.
[23]张 恒, 董新法, 林维明.Cu, Ti掺杂的SrFeO3−δ基混合导体透氧材料的制备与性能研究[J].无机材料学报, 2007, 22(1):97−100.ZHANG Heng,DONG Xin-fa,LING Wei-ming.Preparation and properties of SrFeO3−δbased mixed conducting membrane material doped with Cu and Ti [J].Journal of Inorganic Materials, 2007, 22(1): 97−100.
[24]GOLDSCHMIDT V M.Die gesetze der krystallochemie [J].Die Naturwissenschaften, 1926, 14(21): 477−485.
[25]SVARCOVA S.Structural instability of cubic perovskite BaxSr1−xCo1−yFeyO3−δ[J].Solid State Ionics, 2008, 178(35/36):1787−1791.
[26]ODA H, YAMAGUCHI Y, TAKEI H, et al.Screw spin structure in SrFeO3[J].Le Journal de Physique Colloques, 1977, 38(C1):C1−C121.
[27]TAKEDA T, YAMAGUCHI Y, WATANABE H.Magnetic structure of SrFeO3[J].Journal of the Physical Society of Japan,1972, 33(4): 967−969.
[28]CHAKRAVERTY S, MATSUDA T, WADATI H, et al.Multiple helimagnetic phases and topological Hall effect in epitaxial thin films of pristine and Co-doped SrFeO3[J].Physical Review B, 2013, 88(22): 220405.
[29]SRINATH S, KUMAR M, POST M, et al.Magnetization and magnetoresistance in insulating phases of SrFeO3−δ[J].Physical Review B, 2005, 72(5): 054425.
[30]MACCHESNEY J B, SHERWOOD R C, POTTER J F.Electric and magnetic properties of the strontium ferrates [J].The Journal of Chemical Physics, 1965, 43(6): 1907−1913.
[31]LAMAGO D, GEORGII R, B NI P.Magnetic susceptibility and specific heat of the itinerant ferromagnet MnSi [J].Physica B:Physics of Condensed Matter, 2005, 359: 1171−1173.
