氢化钛氧化处理及其热分解行为
2015-03-03王耀奇任学平侯红亮张艳苓张建国
王耀奇,任学平,侯红亮,张艳苓,张建国
氢化钛氧化处理及其热分解行为
王耀奇1, 2,任学平1,侯红亮2,张艳苓2,张建国1
(1. 北京科技大学材料科学与工程学院,北京100083;2. 北京航空制造工程研究所,北京100024)
在大气条件下进行氢化钛的氧化处理试验, 利用扫描电镜和X射线衍射仪研究氧化处理后氢化钛的形貌与相组成,通过TG/DSC热分析,研究氧化处理对氢化钛热分解行为的影响规律。结果表明,氧化处理后氢化钛颗粒形貌无明显变化,随温度升高和时间延长,其颜色经历了灰黑色—蓝色—浅灰色的转变,且颗粒表面形成了Ti3O和TiO2的氧化物薄膜。与此同时,随氧化处理温度升高和时间延长,氢化钛热分解的质量损失率降低,但氢化钛的热分解温度显著提高,以AlSi12合金为基体,应用粉末冶金法制备泡沫铝,其氢化钛的氧化处理工艺为480 ℃/1 h。
泡沫铝;氢化钛;氧化处理;分解行为
泡沫铝作为一种新型的轻质结构功能材料,具有优异的能量吸收、阻尼、阻燃和吸声性能,可广泛用于航空、航天、汽车和舰船等诸多领域,近些年来受到人们的广泛关注[1−2]。氢化钛作为泡沫铝制备过程中最常用的发泡剂,其分解温度低、速度快,分解行为难与泡沫铝基体材料的性能相匹配,这对泡沫铝的孔隙结构产生极其不利的影响,因此研究氢化钛的缓释处理技术对制备孔隙尺寸分布均匀,微观缺陷可控的泡沫铝具有重要的意义。
目前氢化钛的缓释处理技术主要有物理包覆,化学包覆和氧化改性等。物理包覆是通过研磨法将氢化钛与包覆介质混合研磨,以实现氢化钛的包覆,该方法制备的包覆层致密性较差,包覆厚度不均匀,且机械包覆过程中氢化钛易发生分解造成发泡剂浪费。化学包覆是将氢化钛与相应的无机盐溶液混合,通过化学反应在氢化钛表面形成一层包覆层,常见的化学包覆介质有SiO2、AL2O3、TiO2和Ni等[3−5]。该方法工艺过程复杂,成本高,不利于大规模生产。氧化改性是在空气中加热氧化处理氢化钛,使其生成一层致密的氧化膜,从而减缓氢的释放,这种方法操作简便,是一种有较好应用前景的缓释处理方法。国内外的一些研究学者对此展开了研究,证明了该方法的有效 性[6−8],同时探讨了氧化处理的缓释机理,但由于不同的研究者所采用的分析手段不同,试验条件也有所差异,因此还没有获得一致性的研究结论。
本研究在深入研究氢化钛动态分解行为的基础上[9],进一步开展氢化钛的氧化处理工艺研究,并在Ar气氛下利用TG/DSC联合热分析模拟氧化处理后氢化钛在泡沫铝基体内部的热分解行为,揭示氧化处理氢化钛的缓释机理,对泡沫铝的制备提供技术指导。
1 实验
试验材料为西北有色研究院制备的氢化钛粉末,粒度为44 µm,颗粒形貌如图1所示。氢化钛呈灰黑色,颗粒为多边形不规则形状。
利用SX3-10-13箱式电阻炉在460~520 ℃/1~7 h条件下开展氢化钛的氧化处理试验,温度间隔为 20 ℃,时间间隔为2 h。SX3-10-13箱式电阻炉的温度均匀性为±3 ℃,试验过程中,取10 g氢化钛粉末均匀平铺于陶瓷坩埚内,然后将陶瓷坩埚置于电阻炉的均温区内进行氧化处理,升温速率为10 ℃/min,在本试验中的氧化处理时间是指在试验温度下的保温 时间。
采用LEO-1450型扫描电镜对氧化处理后氢化钛的颗粒形貌进行观察,研究氧化处理对其形貌的影响。利用DMAX-RB12KW旋转阳极X射线衍射仪对氧化处理后的氢化钛进行物相分析。衍射仪使用Cu靶,扫描范围为10°~100°,扫描速度0.02°,电压40 KV,电流30 mA。采用NETZSCH STA 409C/CD差示扫描量热仪对氧化处理后的氢化钛进行TG+DSC联合热分析,在Ar气中以30 ℃/min的速度从室温连续加热到900 ℃,获得氢化钛的热分解曲线,试验过程中Ar气的流量为20 ml/min.

图1 氢化钛颗粒形貌
2 结果与分析
2.1 氧化处理对氢化钛颗粒特征的影响
氢化钛氧化处理后的颗粒形貌如图2所示,研究显示,在不同的氧化处理条件下,氢化钛颗粒的外观、尺寸并无明显变化,依旧为多边形颗粒,但不同氧化处理条件下,氢化钛表面的颜色不同,460 ℃/3 h、 480 ℃/1 h条件下,氢化钛的颜色为蓝色,随氧化处理温度升高和氧化时间延长,氢化钛的颜色逐渐过渡为浅灰色。
在氧化处理的过程中,氢化钛的表面会形成一层氧化物薄膜,其颜色的转变与表面氧化产物的相组成与相比例密切相关。不同的氧化产物其颜色不同,相关的研究显示[10],TiHO的为金绿色,TiO为金黄色,Ti2O3为紫色,TiO2为白色。然而,氢化钛在氧化处理过程中生成的氧化产物往往并不是单一的物相,是由多种氧化物例如Ti2O3+TiO2和Ti3O+TiO2组成的混合物,虽然它们的成分不同,但是均呈蓝色,这说明,并不能通过氢化钛表面的颜色判断其氧化产物的相组成。
氢化钛氧化处理后,其XRD图谱如图3所示,其中未标注的为TiH2或亚TiH的化合物,研究显示,氢化钛原始粉末成分为TiH1.97,460 ℃/3 h或480 ℃/1 h氧化处理后,衍射峰变宽,说明在此过程中有不同成分的亚TiH化合物产生,如TiH1.92等,且分解产生了氢气。随温度升高、时间延长,TiH的衍射峰变窄,且向高散射角方向移动,表明在此过程中氢持续释放,TiH的晶格常数持续降低。与此同时,460 ℃/3 h或480 ℃/1 h氧化处理后,在XRD图谱中出现了Ti3O和TiO2衍射峰,说明有Ti3O和TiO2氧化产物形成,与Malachevsky和Kadoi的研究结果一致[11−12],且随温度升高、时间延长,衍射峰增强。此外,在XRD图谱中并未观察到氢氧化物TiHO(TIH1.99O0.1和TiH1.82O0.3)的衍射峰[13]。氢化钛在氧化处理过程中,其物相的转变过程可以用下式来表示:
TiH1.97+O→TiH+Ti3O+TiO2(1)
可见氧化处理后,氢化钛表面形成了Ti3O和TiO2氧化物薄膜,这将对其在高温下的热分解行为产生重要的影响。

图2 氧化处理后氢化钛颗粒形貌与颜色

图3 氧化处理后氢化钛的相成分
2.2 氧化处理对氢化钛热分解行为的影响
氢化钛氧化处理后,其热质量损失(TG)曲线如图4所示。观察发现,热分析过程中随温度升高,氢化钛发生热分解反应,在520~640 ℃氢化钛开始出现质量损失现象,热分解反应开始,反应过程中,释放出氢气,在660~750 ℃质量损失现象结束,热分解反应完成。根据公式(2)的计算[14],可以看出,随氧化处理温度升高和时间延长,氢化钛的质量损失率呈现明显的下降趋势。其中,520 ℃/3 h热处理后,氢化钛的质量损失率仅为0.59%,与未经热处理氢化钛的质量损失(2.54%)相比降低了77%,说明氢化钛在氧化处理过程中发生了热分解反应。可见氢化钛的氧化处理温度不宜过高,时间不宜过长,否则氧化处理过程中的热分解反应将造成氢化钛的浪费。

式中:—氢化钛质量损失率,%;H—热分解过程中氢化钛的质量变化值,g;TiH2—热分解前氢化钛的质量,g。
图4 氧化处理后氢化钛的TG曲线(a)不同温度(b)不同时间
Fig.4 TG curves of titanium hydride after oxidation treatment for different temperatures (a) and different times (b)
氧化处理后氢化钛的DSC曲线如图5所示,由图可知,氢化钛的热分解反应由2个放热峰组成,已有的研究显示,不同的放热峰与不同的热分解反应相对应,如公式(3)和(4)所示。氧化处理后氢化钛的热分解反应仅有一个放热峰,说明氧化处理过程中热分解反应(3)已经完成,分解过程中仅发生了式(4)所示热分解反应,与XRD图谱分析一致。氢化钛的热分解温度为527 ℃,氧化处理后,随氧化温度升高,氧化时间延长,氢化钛的热分解温度向高温方向移动,520 ℃/3 h氧化处理后,其热分解温度为624 ℃,升高了97 ℃。对于以AlSi12(熔点577~600 ℃)为基体来制备泡沫铝,氢化钛的氧化处理工艺为480 ℃/1 h,在此条件下,氢化钛的热分解行为与AlSi12热熔化行为较为匹配。
TiH1.97→TiH+(1.97−)H (3)
TiH→Ti+H (4)
氢化钛的热氧化过程与热分解过程如图6所示。根据Matijasevic-Lux的研究显示[7],氧化处理后,氢化钛由内向外的相成份依次为TiH-Ti3O-TiO2-H2。氢化钛的热分解过程符合收缩核模型[15],与未氧化的氢化钛相比,热分解产生的氢需通过扩散穿过氧化膜Ti3O/ TiO2,才能溢出材料表面,因此氧化处理后,氢化钛的热分解开始温度向高温方向移动。

图5 氧化处理后氢化钛的DSC曲线
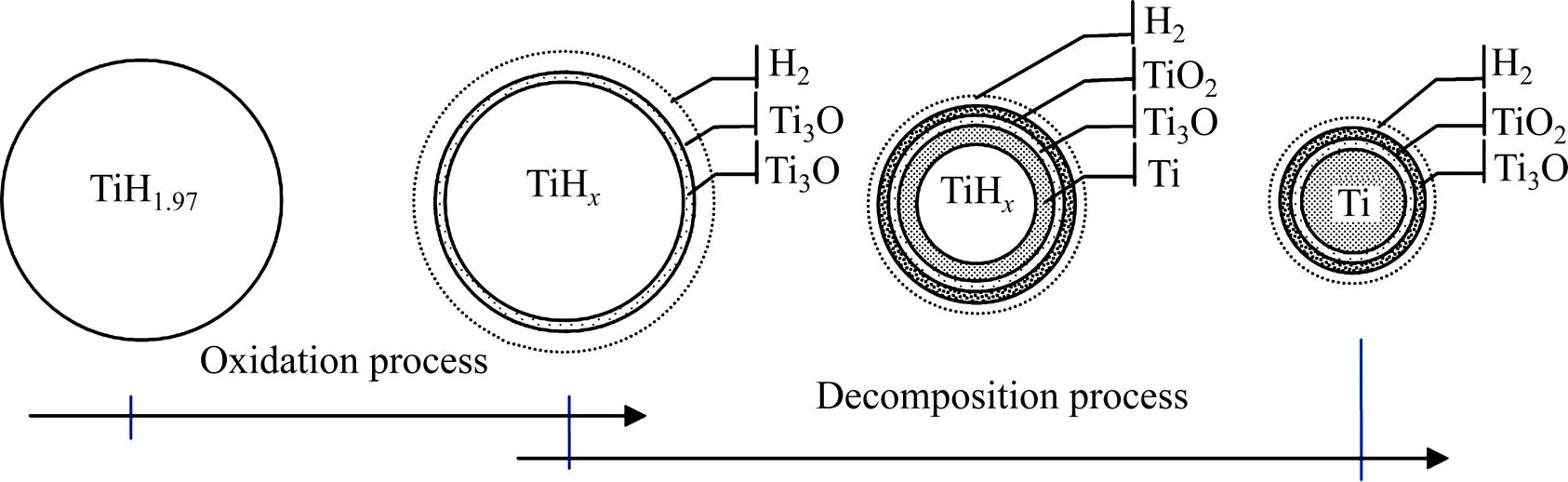
图6 氢化钛转变模型
3 结论
1) 氧化处理后, 氢化钛颗粒形貌无明显变化,氢化钛由内至外依次形成了Ti3O和TiO2的氧化物薄膜,Ti3O/TiO2的不同比例,氢化钛将呈现不同的颜色。
2) 随氧化处理温度升高和时间延长,氢化钛热分解的质量损失率降低,热分解开始温度显著提高,依据泡沫铝基体的性能选择适合的氧化处理工艺,将有助于改善泡沫铝的孔隙结构。
REFERENCES
[1] DAVIES G J, ZHEN S. Review Metallic foams: their production, properties and applications [J]. Journal of Materials Science, 1983, 18: 1899−1911.
[2] BANHART J. Manufacture characterizations and application of cellular metals and metal foams [J]. Progress in Materials Science, 2000, 46(3): 559−632.
[3] 方吉祥, 赵康, 谷臣清. 化学法制备Al2O3包覆TiH2颗粒发泡剂[J]. 中国有色金属学报, 2002, 12(6): 1205−1209. FANG Ji-xiang, ZHAO Kang, GU Chen-qing. Preparation of Al2O3-coated TiH2foaming reagent by chemical method [J]. The Chinese Journal of Nonferrous Metals, 2002, 12(6): 1205−1209.
[4] 陈永楠, 梁 戈, 张从容, 等. SiO2/Al2O3复合包覆TiH2颗粒发泡剂的制备[J]. 材料工程, 2006, 2: 23−25. CHEN Yong-nan, LIANG Ge, ZHANG Cong-rong, et al. Study on preparation of TiH2particles compound coated with SiO2/Al2O3[J]. Journal of Materials Engineering, 2006, 2: 23−25.
[5] 朱学卫, 王日初, 何 娟, 等. 泡沫铝用 Ni/TiH2包覆型发泡剂的制备工艺及性能[J]. 粉末冶金材料科学与工程, 2009, 14(4): 270−274. ZHU Xue-wei, WANG Ri-chu, HE Juan, et al. Preparation and properties of Ni-coated TiH2foaming agent used in foamed aluminum production [J]. Materials Science and Engineering of Powder Metallurgy, 2009, 14(4): 270−274.
[6] KENNEDY A R, LOPEZ V H. The decomposition behavior of as-received and oxidized TiH2foaming-agent powder [J]. Materials Science and Engineering, 2003, A357: 258−263.
[7] MATIJASEVIC-LUX B, BANHART J, FIECHTER S, et al. Modification of titanium hydride for improved aluminium foam manufacture [J]. Acta Materialia, 2006, 54: 1887−1900.
[8] 左孝青, 潘晓亮, 寥明顺, 等. 氧化处理对TiH2分解特性及组织结构的影响[J]. 材料科学与工艺, 2008, 16(2): 211−215. ZUO Xiao-qing, PAN Xiao-liang, LIAO Ming-shun, et al. Effects of heat treatment on TiH2decomposition behavior and microstructure [J]. Materials Science & Technology, 2008, 16(2): 211−215.
[9] 王耀奇, 张 宁, 任学平, 等. 氢化钛的动态分解行为与规律[J]. 粉末冶金材料科学与工程, 2011, 16(6): 795−798. WANG Yao-qi, ZHANG Ning, REN Xue-ping, et al. Behavior and rule of titanium hydride dynamic decomposition [J]. Materials Science and Engineering of Powder Metallurgy, 2011, 16(6): 795−798.
[10] GROMOV A R, KOUZNETSOVA N N, YUDINA S L, et al. The investigation of titanium hydride oxidation process [J]. Journal of Alloys and Compounds, 1997, 261: 269−272.
[11] MALACHEVSKY M T, D’OVIDIO. Thermal evolution of titanium hydride optimized for aluminium foam fabrication [J]. Scripta Materialia, 2009, 61: 1−4.
[12] KADOI K, BABCSA´N N, NAKAE H. Heat treatment of TiH2powder to control decomposition phenomenon for aluminum foam fabrication by melt route [J]. Materials Transactions, 2009, 50(4): 727−733.
[13] FOKIN V N, MALOV Y I, FOKINA E E, et al. Investigation of interactions in the TiH2-O2system [J]. Int J Hydrogen Energy, 1995, 20(5): 387−389.
[14] 张月红, 苏彦庆, 郭景杰, 等. 升温速率对TiH2热分解过程的影响[J]. 稀有金属材料与工程, 2010, 39(6): 1107−1110. ZHANG Yue-hong, SU Yan-qing, GUO Jing-jie, et al. Influence of heating rate on heat decomposition of TiH2[J]. Rare Metal Materials and Engineering, 2010, 39(6): 1107−1110.
[15] SHUNJI H, SHINJI O, JIRO K, et al. Gas-Solid reaction model for a shrinking spherical particle with unreacted shrinking core [J]. Chemical Engineering Science, 2005, 60: 4971−4980.
(编辑 高海燕)
Oxidation treatment and hot decomposition behavior of titanium hydride
WANG Yao-qi1, 2, REN Xue-ping1, HOU Hong-liang2, ZHANG Yan-ling2, ZHANG Jian-guo1
(1. School of Materials Science and Engineering, University of Science and Technology of Beijing,Beijing 100083, China; 2. Beijing Aeronautical Manufacturing Technology Research Institute, Beijing 100024, China)
The oxidation treatment of titanium hydride was processed in air. The morphology and the phase composition of titanium hydride after oxidation treatment were investigated by scanning electron microscope and X-ray diffraction. The effect of oxidation treatment on the decomposition behavior of titanium hydride was studied by TG/DSC. The results show that the surface feature of titanium hydride changes a little after oxidation treatment. With increasing the temperature and time, the colour of titanium hydride changes from dark grey to blue and then to light grey, on which the Ti3O and TiO2film have come into being. At the same time, the mass loss rate decreases with increasing the oxidation treatment temperature and time, but the initial temperature of decomposition increases obviously. During the preparation process of aluminum foam based on AlSi12matrix by powder metallurgic method, the oxidizing paramter of the titanium hydride is 480 ℃/1 h。
aluminium foam; titanium hydride; oxidation treatment; decomposition behavior
TF123.12
A
1673-0224(2015)1-1-06
国家自然科学基金资助项目(50875294); 航空基金资助项目(20081125)
2014-04-04;
2014-07-12
侯红亮, 研究员,博士。电话:13381281964;E-mail: hou_hl@163.com
