普瑞巴林化学拆分过程研究
2015-03-25刘春霞于玉振陈水库张方杰
李 雯,刘春霞,于玉振,张 华,陈水库,张方杰
(1.郑州大学 化工与能源学院,河南 郑州450001;2.河南辅仁医药科技开发有限公司,河南 郑州450003)
0 引言
神经病理性疼痛的治疗是当前临床医学难题,普瑞巴林为解决该医学难题提供了可供选择的有效药物,其镇痛作用强、用药剂量低且副作用小.目前已在全球80 多个国家和地区上市[1]. 工业生产普瑞巴林的主要方法为化学拆分法,已有文献报道中,采用多种拆分剂进行普瑞巴林或其中间体的拆分,如文献[2]采用手性有机碱作对普瑞巴林中间体进行拆分,再经Hoffmann 降解得到普瑞巴林;文献[3]采用N -对甲苯磺酰化、苯磺酰化、对甲苯甲酰化作为拆分剂;文献[4 -5]采用L-酒石酸、二对甲基苯基-L-酒石酸或樟脑磺酸拆分普瑞巴林消旋体. 但以上方法中存在部分产物消旋化,拆分剂制备繁琐,析晶困难且拆分剂易分解等问题使得生产效率低、成本高.近年来,文献[6 -12]均采用S -(+)-扁桃酸做拆分剂,经过在异丙醇-水中成盐、四氢呋喃-水中盐分解、异丙醇-水中重结晶这3 个步骤进行拆分得到普瑞巴林(图1),这些文献对拆分所采用的3 个步骤中各组分的含量变化情况却语焉不详,在实际实验过程中,发现目标产品的含量随实验条件的稍加变化即发生较大变化,获得合格品的实验条件苛刻. 因而探索拆分过程中每一步的组分含量及影响因素,对获得一种高效、品质稳定的拆分条件具有显著的价值. 笔者以S -(+)-扁桃酸为拆分剂,采用HPLC 测定拆分过程中各组分含量,考察了不同拆分条件下各组分含量变化的规律,得出普瑞巴林较佳拆分条件.
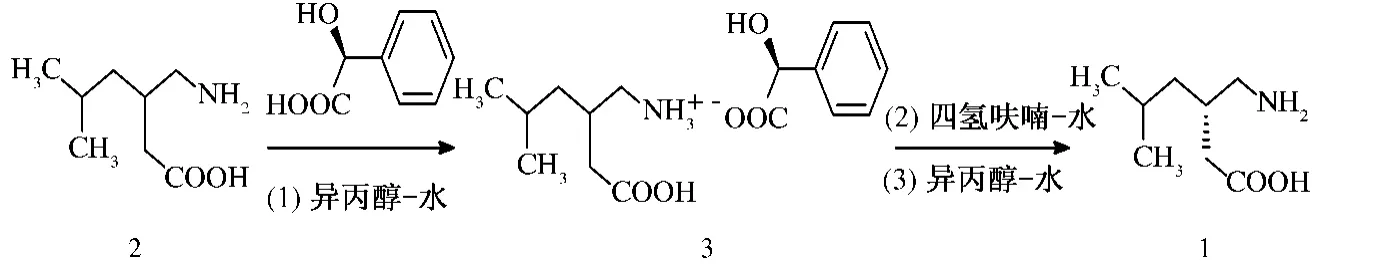
图1 普瑞巴林的化学拆分路线Fig.1 Resolution route of Pregablin
1 实验部分
1.1 分析仪器及试剂
BrukerAvance Digital 400 核磁共振分析仪;WRS-1B 型数字熔点仪;岛津LC -10ATvp 高效液相色谱仪(SPD-10ATvp 检测器);普瑞巴林对照品,购于中国药品生物制品检定所;普瑞巴林消旋体,自制;S-(+)-扁桃酸(≥98%),购于上海海曲化工有限公司;四氢呋喃、异丙醇均为分析纯.
1.2 HPLC 检测依据及标准
HPLC 检测按照国家食品药品监督管理局化药试行标准YBH02442013 规定进行:(S)-3 -(氨甲基)- 5 - 甲基己酸,按干燥品计算,含C8H17NO2不得少于98.5%[13].
1.3 普瑞巴林化学拆分操作过程
取普瑞巴林消旋体2(7.8 g,0.049 mol)与S-(+)-扁桃酸(9.3 g,0.061 mol)加入到三口烧瓶中,经过3 个步骤:(1)加入异丙醇66 mL 和水2 mL,微热至固体全溶,冷却析晶,抽滤得到S,S-盐(表示(S)-3 -氨甲基-5 -甲基己酸与S-(+)-扁桃酸所生成的盐,下同);(2)将所获得的S,S-盐加入到四氢呋喃160 mL 和水8 mL中,回流0.75 h,冷却析晶,抽滤得到白色固体,经检验,该白色固体为含有普瑞巴林和S,S -盐混合物;(3)将所获得的白色固体加入到异丙醇35 mL 和水7 mL 中,加热溶解,热抽滤,冷却析晶,得到2.5 g 白色固体普瑞巴林(含量99.5%以上,HPLC 测定),收率64.10%. mp185.0 -187.0 ℃[文献值184.0-185.0 ℃],(c1.0,H2O)[文献值+10. 5°(c1. 0,H2O)]. 1H-NMR(DMSO):δ 0.81-0. 84(d,6H,CH3),1. 03-1. 06[m,2H,CH2],1.55[m,1H,CH],2.11 ~2.21(m,2H,CH2COOH),2.74 ~2.78(m,2H,CH2N).
2 实验研究
2.1 S,S-盐在异丙醇-水中生成条件的选择和优化
拆分过程的第一步,普瑞巴林消旋体与S -(+)-扁桃酸成盐反应,为有机弱酸弱碱成盐的过程,由于弱酸弱碱在中性条件下不稳定,因而,成盐反应需在适当过量酸存在下进行,这就需要考察适宜的普瑞巴林消旋体与S-(+)-扁桃酸的投料比例.经研究在异丙醇和水以33∶1(体积比)条件下,普瑞巴林消旋体与S-(+)-扁桃酸的摩尔比按1∶1.25 ~1.55 投料时,其实验结果见表1 所示.
由表1 可知,S,S -盐的含量和纯度随普瑞巴林消旋体与S-(+)-扁桃酸比例变化而发生明显的变化,S-(+)-扁桃酸投料量的增加,收率增大,但含量下降,当两者以摩尔比为1∶1.4 成盐时,可获得最佳的S,S - 盐含量,其收率为92.4%,综合考虑含量和收率的因素,选择该条件为较佳条件,并进一步考察不同异丙醇-水体积比对S,S -盐形成的影响,选取异丙醇与水的体积比从9 ∶1 至∞进行实验,其实验结果见表2所示.
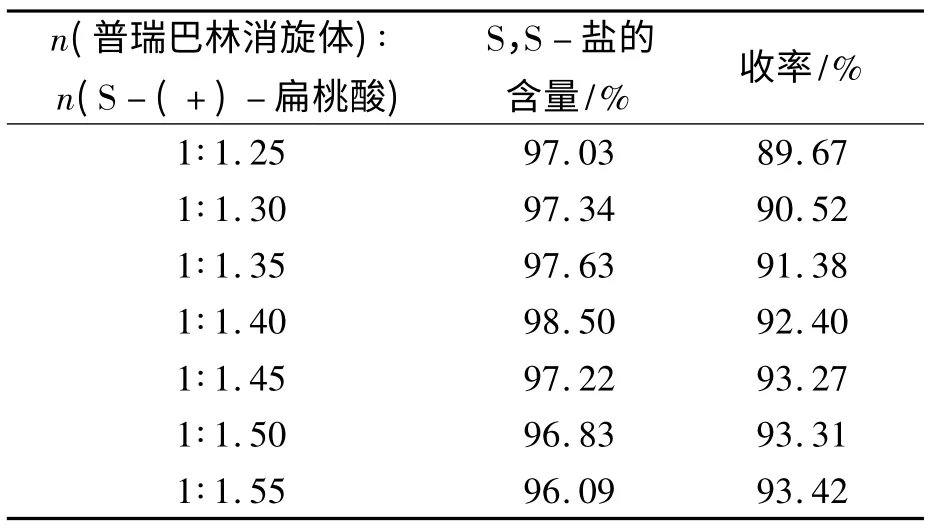
表1 不同的普瑞巴林消旋体与S-(+)-扁桃酸投料比例对含量和收率的影响Tab.1 The effect of different molar ratio of Racemic Pregabalin and (S)-(+)-Mandelic acid on Purity and yield
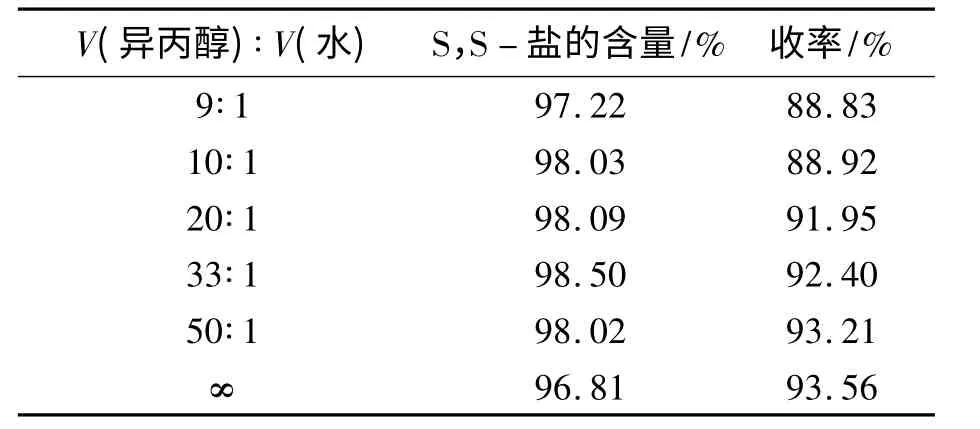
表2 不同异丙醇和水的体积比对照试验Tab.2 The comparative experiments of different volume ratio of isopropyl alcohol(IPA)to H2O
由表2 可知,不同异丙醇-水体积比对所生成的S,S -盐的纯度影响较小但收率影响较大,其中体积比为33 ∶1 时,盐含量达到最高即98.50%,随着水含量的增加,S,S-盐收率显著下降,因此综合考虑含量和收率因素,选择异丙醇-水体积比为33∶1.
总之,化学拆分第一步,较佳的实验条件为普瑞巴林消旋体与S - (+)- 扁桃酸的摩尔比为1∶1.4的比例投料,异丙醇-水体积比为33∶1,可获得含量为98. 50% 的目标物,收率可达到92.40%(HPLC 检测结果如图2).
2.2 S,S-盐在四氢呋喃-水中初步解离条件的选择和优化
拆分过程的第2 步,S,S -盐在四氢呋喃中进行初步解离. 以往的文献中,均假定该步骤为S,S-盐全部盐解离,后续的第3 步即异丙醇-水加热析晶为普瑞巴林重结晶过程. 经对盐解离溶剂含水量、盐解离时间进行实验研究后,发现在四氢呋喃-水体系中,S,S -盐只能发生部分解离.以普瑞巴林峰面积与S,S -盐峰面积的比来表示S,S-盐解离程度,经测定S,S-盐的校正因子为0.41,对应的S,S-盐解离程度可达67.8%.可见,后续的异丙醇-水加热析晶过程为进一步解离的过程.水量对普瑞巴林含量和收率的影响. 选取以上最佳条件下制得的S,S -盐混合物为原料,异丙醇与水的体积比从2∶1 至7∶1 进行实验,其实验结果见表4 所示.
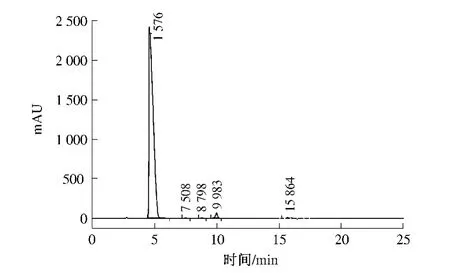
图2 S,S-盐的HPLC 含量分析Fig.2 Purity analysis of racemic pregabalin and (S)-(+)-mandelic acid by HPLC
首先讨论盐分解溶剂含水量对盐解离程度的影响,取四氢呋喃和水体积比从10∶1 至35∶1 进行实验,其实验结果见表3 所示.
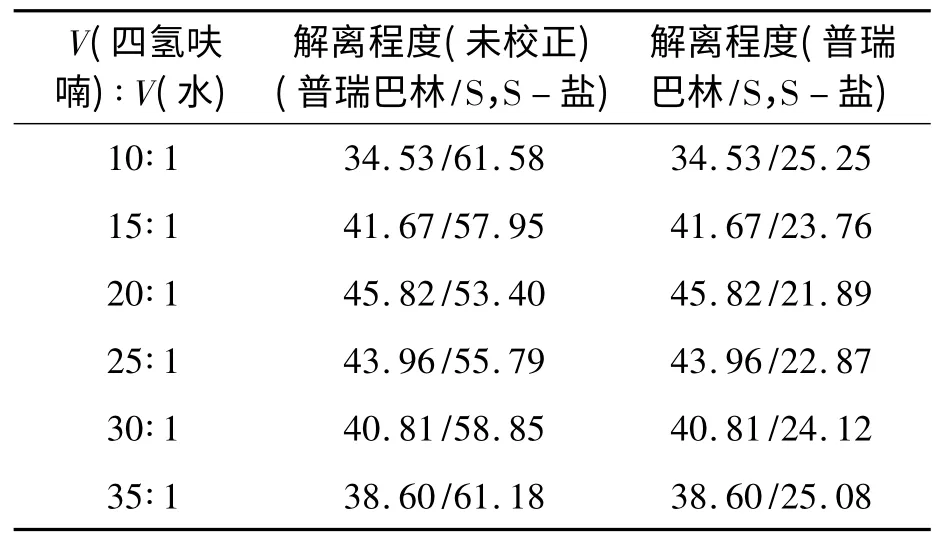
表3 不同四氢呋喃和水的体积比的对照试验Tab.3 The comparative experiments of different volume ratio of THF to H2O %
由表3 可知,不同四氢呋喃和水的体积比对S,S-盐解离效果影响较大,当体积比变化时,盐解离的程度先逐渐增加后又下降,其中当体积比为20∶1 时,解离程度最高,因而,选择四氢呋喃与水体积比为20∶1 为较佳工艺条件.
总之,化学拆分第二步,S,S -盐初步解离的较佳实验条件为:四氢呋喃和水的体积比为20∶1,代表性的HPLC 检测结果如图3 所示.
2.3 S,S -盐在异丙醇-水中进一步盐解离条件的选择和优化
拆分过程的第3 步,异丙醇-水中S,S -盐进一步盐解离.在以上研究的基础上,考察溶剂含
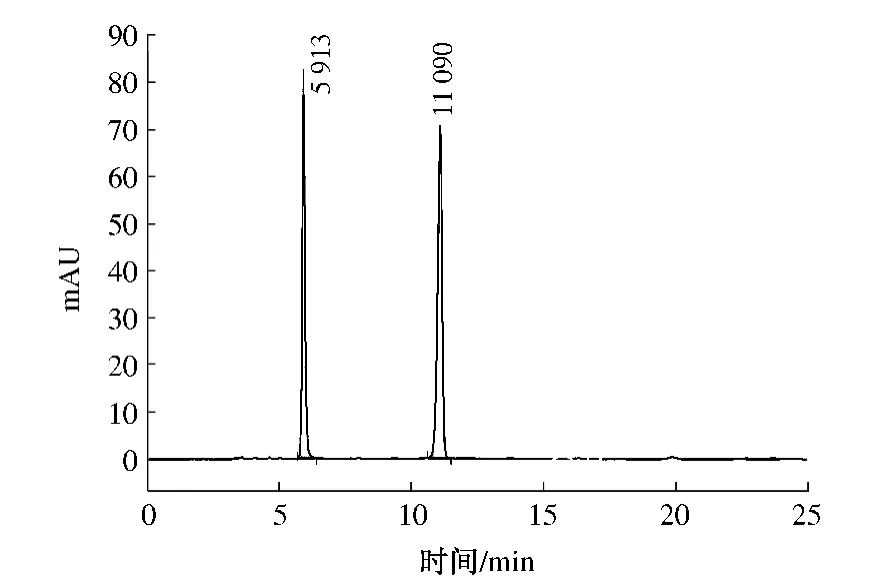
图3 S,S-盐四氢呋喃中盐分解HPLC 含量分析Fig.3 Purity analysis of degrees of salt decomposition in tetrahydrofuran by HPLC
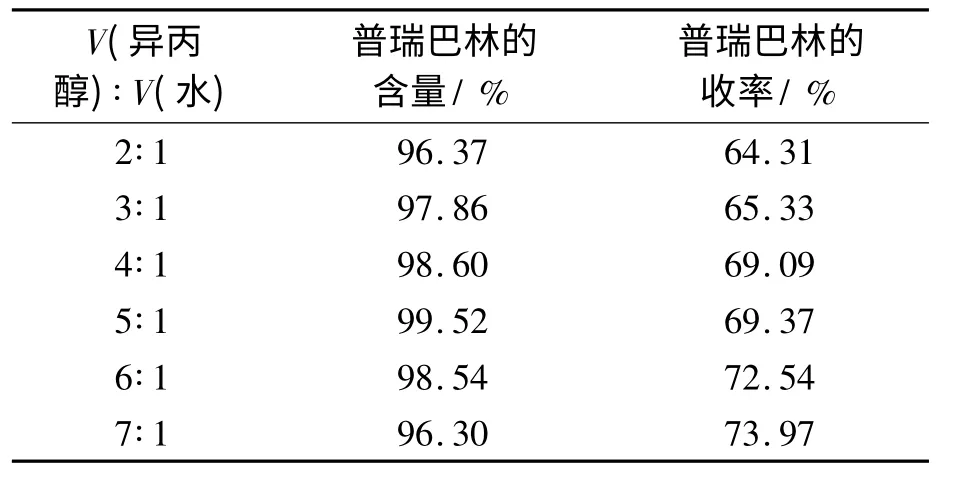
表4 不同异丙醇和水的体积比的对照试验Tab.4 The comparative experiments of different volume ratio of IPA to H2O
由表4 可知,不同异丙醇和水的体积比对S,S-盐的盐解离程度影响较大,当体积比为3∶1 至5∶1 时,盐解离所得普瑞巴林的含量>97%;较佳的溶剂为异丙醇和水体积比为5∶1,可得含量为99.52% 的 目 标 物. 以S,S - 盐 计 收 率 达 到69.37%,HPLC 检测结果如图4 所示.
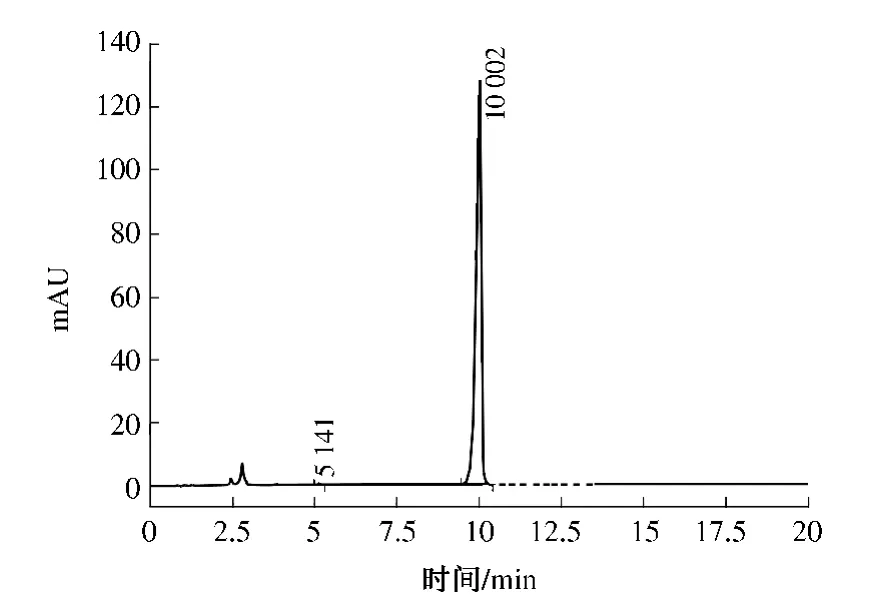
图4 S,S-盐异丙醇中盐分解HPLC 含量分析Fig.4 Purity analysis of degrees of salt decomposition in isopropanol by HPLC
3 结论
通过进行反复实验,最终确定较佳工艺条件为普瑞巴林消旋体与S-(+)-扁桃酸摩尔比为1∶1.4投料,异丙醇-水体积比为33∶1 体系中成盐,经四氢呋喃-水体积比为20∶1 的溶剂回流,再经异丙醇-水体积比为5∶1 的体系进一步盐解离,最终得到含量不低于99.52%的目标产物.
(1)探明了普瑞巴林消旋体拆分过程中,在异丙醇-水、四氢呋喃-水、异丙醇-水中分别进行的3 个步骤,并非先前文献认为的成盐、盐解离和重结晶的拆分过程,而是成盐、初步盐解离、进一步盐解离的过程.
(2)该研究考查影响每步反应的关键因素,取得了较佳工艺条件,与现有文献相比,所获得的化学拆分较佳的投料、溶剂含水比例等条件,为规模化制备普瑞巴林提供了详实的实验依据;
(3)基于该研究所获得的较佳拆分条件重复性良好,经后续试验验证,所获得的普瑞巴林含量完全符合药典要求.
[1] LEE C H,LIOH H H. Pregabalin activates ROMK1 channels via cAMP-dependent protein kinase and protein kinase C[J]. Eur J Pharmacol,2014,740(5):35 -44.
[2] PRADHAN B S. Process for the synthesis of (R)-(-)-3-(carbamoylmethyl)-5-methylhexanoic acid and the intermediates,its intermediates and its use in the preparation of Pregabalin:WO,2012093411A2[P].2012 -07 -12.
[3] 付德才,张伟,王博.一种S-构型普瑞巴林的化学拆分制备方法:中国,103626668A[P].2014 -03-12.
[4] GORE V,DATTA D,GADAKAR M,et al. Resolution of pregabalin:WO,2009122215 A1[P]. 2009-10 -08.
[5] KONAKANCHI D P,PILLI R,PULA S R,et al. Novel resolution process for pregabalin: WO,2009044409 A2[P]. 2009 -04 -09.
[6] 陈敖,张建军. 普瑞巴林的合成[J]. 中国医药工业杂志,2004,35(4):195 -196.
[7] 杨健,黄燕. 普瑞巴林的合成[J]. 高校化学工程学报,2009,23(5):825 -829.
[8] PRADHAN B S. Processes for preparing pregabalin:WO,2011016052 A2[P]. 2011 -02 -10.
[9] RAZZETTI G,ALLEGRINI P,PASTORELO D.Process for the synthesis of pregabalin:CA,2701656 A1[P]. 2010 -11 -07.
[10]李璟,田铁牛,李秀峰. 抗惊厥药物普瑞巴林的合成工艺改进[J]. 中国药物化学杂志,2007,17(1):44 -46.
[11]张桂森,杨相平,刘笔锋. 普瑞巴林的合成[J].中国医药工业杂志,2007,38(9):617 -618.
[12]陈国华,姚秀梅,柴雨柱,等. 普瑞巴林的合成工艺改进及还原副产物的分离鉴定[J]. 中国药物化学杂志,2008,18(6):439 -441.
[13]国家食品药品监督管理局. YBH02442013 普瑞巴林[S].
