晚期非小细胞肺癌的治疗进展
2015-03-22刘维,罗以
刘 维,罗 以
(1.南华大学,湖南衡阳421001;2.湖南省肿瘤医院老干头颈内科,湖南长沙410005)
晚期非小细胞肺癌的治疗进展
刘 维1,2,罗 以2
(1.南华大学,湖南衡阳421001;2.湖南省肿瘤医院老干头颈内科,湖南长沙410005)
癌,非小细胞肺; 受体,表皮生长因子; 突变; 药用制剂; 综述
对大多数晚期非小细胞肺癌(NSCLC)患者的治疗标准仍然是采取含铂双药化疗4~6个周期。所有铂类联合吉西他滨、紫杉醇、多西紫杉醇、长春瑞滨及培美曲塞双药化疗的研究,均显示患者有效率及生存期无明显差异,有关长期含铂双药化疗疗效的实验显示无疾病进展期无显著延长[1]。
到目前为止,如何选择治疗方案并非基于NSCLC组织学亚型,但亚型的分析对比试验显示,培美曲塞对鳞癌患者治疗效果比较差,这使得其在一线和二线鳞癌患者上的使用受到限制[2]。
老年患者或那些身体状态较差的患者可使用单药化疗,尽管最近的研究表明,这些亚组能很好地耐受以卡铂为基础的治疗方案,该方案可明显改善治疗有效率和提高患者生存率[3]。
在许多恶性肿瘤的控制上,抑制血管生成扮演了一个重要角色,包括肺癌。一项全球性关于贝伐单抗(7.5或15.0mg/kg)加吉西他滨或顺铂的研究评估发现该疗法可以提高有效率和无复发生存率,但与总生存率无关,而且除此之外,7.5~15.0mg/kg的剂量没有产生明显的疗效[4]。虽然许多小分子酪氨酸激酶抑制剂(TKIs)结合标准化疗在Ⅲ期临床试验中已经进行研究,但还没有研究出比较理想的结果,而事实上一些研究显示TKIs药物的疗效相当差[5]。一线化疗试验都是在未进行分子选择的情况下进行的,令人吃惊的是这也恰恰是表皮生长因子受体(EGFR)TKIs早期试验的问题所在。一线治疗时,化疗联合EGFR TKIs不会增加反应率或总生存期,甚至可能对化疗有负面影响[6]。
厄洛替尼和吉非替尼被认为是一些指定人群的一线单药,其中包括老年患者和那些体力状态不佳以至于无法化疗的患者。对于除此之外的其他患者,鲜有研究表明EGFR TKIs的疗效优于标准化疗[7]。
到目前为止,没有一种可以预测疗效和生存期的基因能帮助选择化疗方式[8]。培美曲塞在鳞癌和非鳞癌患者的不同疗效,被认为是由于更高目标酶的表达,尤其是胸苷酸合成酶,但这并没有被临床试验所验证。在辅助治疗上,切除修复交叉互补基因1(ERCC1)在DNA修复途径上是很重要的,对疗效和预后有预测的作用,但是,ERCC1抗体不稳定,所以不能用其来验证这些结果。同时,乳腺癌1号基因(BRCA1)在DNA修复过程中也发挥了一定的作用。Kristen鼠肉瘤基因(KRAS)突变对化疗和EGFR治疗的患者产生的作用仍存在争议,它是预后不良的标志,但KRAS的出现也不是建议患者放弃治疗的指标。其他经检测的标记,包括p35区域的βtubulin、RRM1和p27[5],这些标记都没有足够的证据证明有必要用于患者的治疗。
1 NSCLC的分子靶向治疗
1.1 EGFR 有研究表明EGFR高表达于癌前阶段,伴随着不断增加的高表现率,高达80%浸润性肺癌显示EGFR的结构异常程度及表达呈上升趋势[9],这些研究使EGFR成为极具吸引力的药物作用靶点,同时,单克隆抗体和小分子TKIs被研究出来。这些药物的早期试验在随机抽取化疗耐受晚期NSCLC患者身上显示不到10%的有效率,但是有些药物反应稳定持久[10]。加拿大国家癌症研究所将厄洛替尼作为二线或三线最佳支持治疗(BSC)的研究显示有效率、无进展生存期(PFS)及总生存时间(OS)均得到显著改善,厄洛替尼这一研究使其作用得到肯定[11]。随机试验BSC选择吉非替尼虽显示较厄洛替尼有更好的疗效,但差异并不明显[12]。
在一线治疗的基础上,相关的4个随机预测试验厄洛替尼和吉非替尼联合含铂双药化疗对NSCLC晚期患者进行研究[13-14],所有这些试验均未得出理想的结果,反而有证据表明在化疗阶段使用TKIs药物会出现不好的效果。关于细胞株的研究显示对预测生物标记识别能明确哪一株得到了最好的效果[15]。2004年有2个波士顿团队报道EGFR基因突变的激活与EGFR TKIs的反应有联系[16]。这个试验结论随后在很多研究中被证实[17-24],见表1。在这些试验中,对于有EGFR突变激活的患者,与化疗相比,EGFR TKIs能带来更好的疗效和更长的PFS。与此相反,在没有EGFR突变的试验中,化疗带来的是更好的有效率和PFS[17-18,25],见表2。尽管毒性的差异,病检报告支持EGFR突变患者使用TKI而野生型EGFR的患者更适合化疗。基于这些结果,美国临床肿瘤学会(ASCO)、欧洲肿瘤内科学会(ESMO)、美国国立综合癌症网络(NCCN)、国际肺癌研究协会(IASLC)、美国病理学家协会(CAP)、美国分子病理学分(AMP)都发布了指南,建议所有晚期NSCLC患者及任何腺癌患者在进行一线化疗之前先对EGFR突变进行分子分析。这些尝试使那些有EGFR突变的患者得到EGFR TKIs治疗的可能,而化疗仍会被选为没有突变的患者的一线疗法。
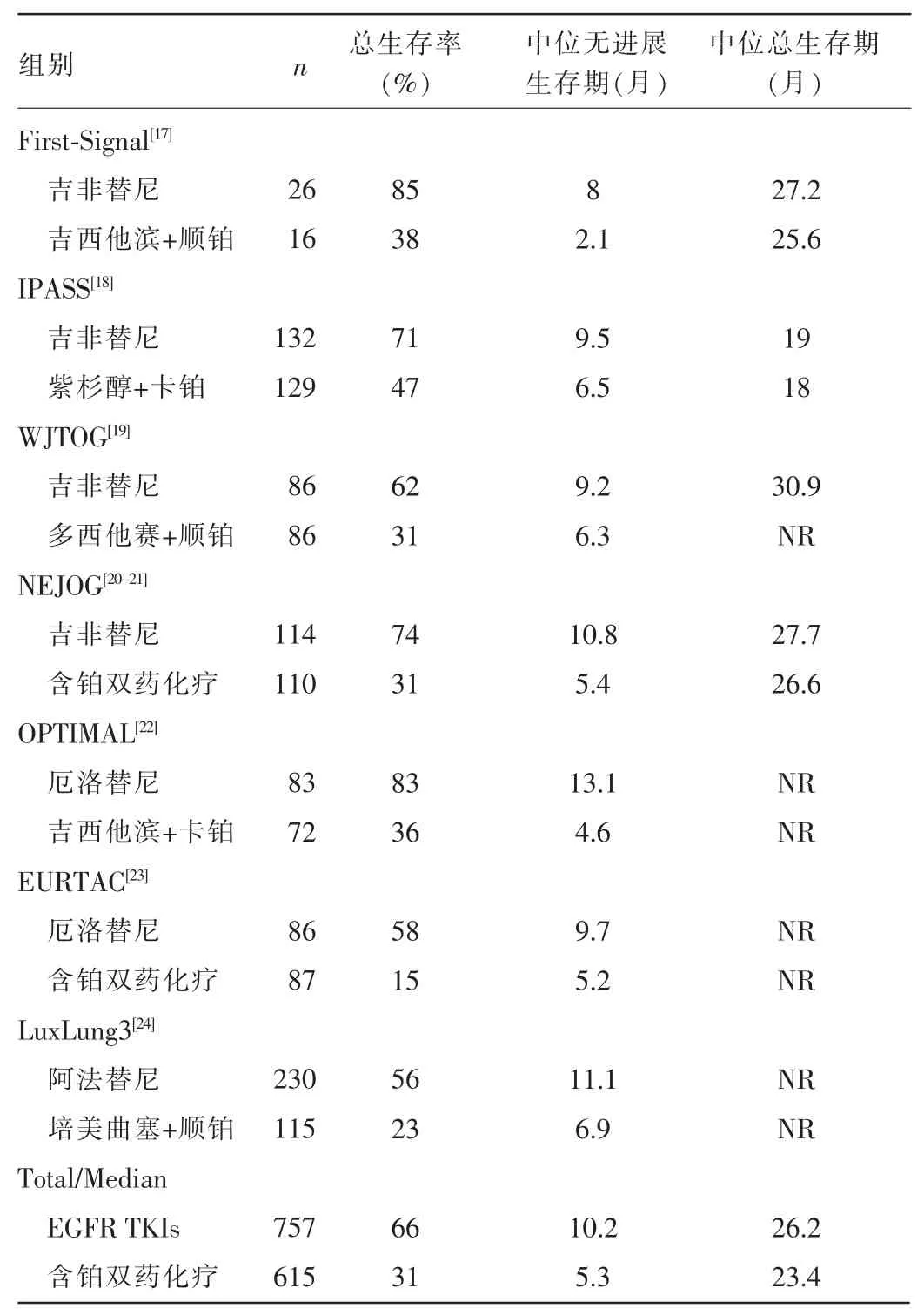
表1 关于EGFR基因突变且未经治疗的晚期肺腺癌患者比较TKI和含铂化疗的随机试验
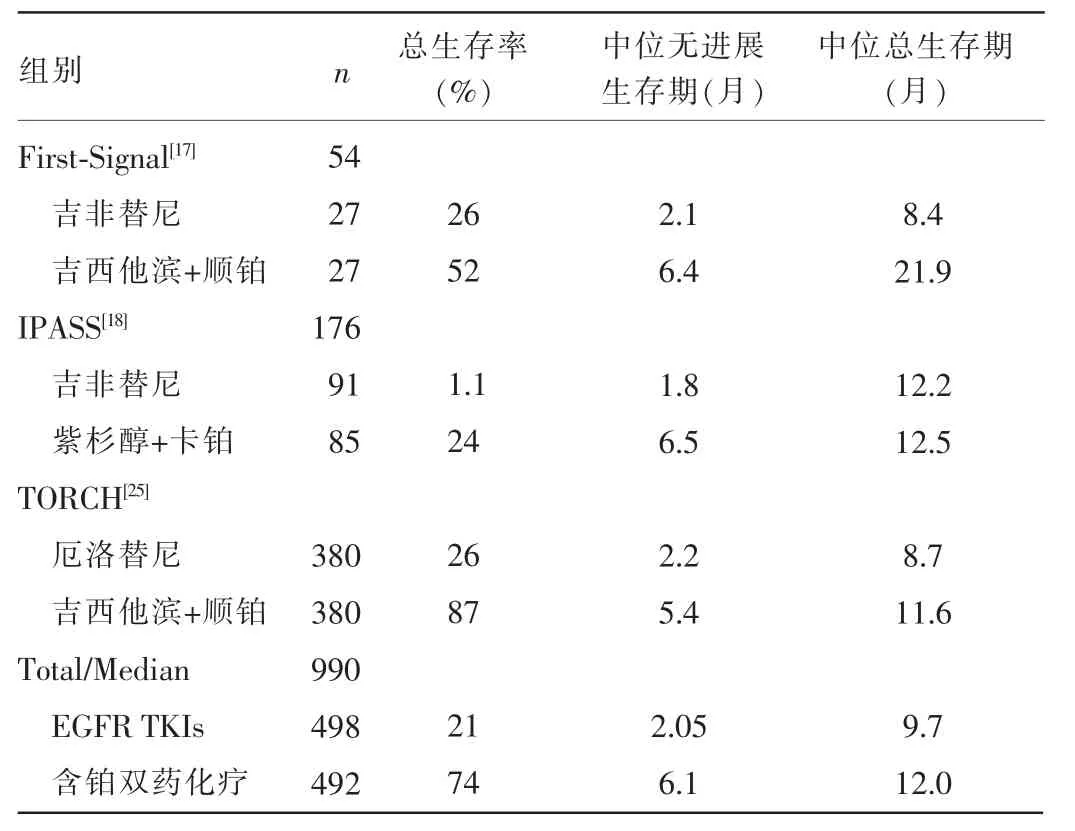
表2 关于EGFR野生型且未经治疗的晚期肺腺癌患者比较TK I和含铂化疗的随机试验
1.2 间变性淋巴瘤激酶(ALK) 2007年,Soda等[26]报道ALK基因因2号染色体上的EML4基因融合而被激活,这种融合基因在肺癌细胞株中是最致癌的。克唑替尼是一种口服ALK TKIs药物,Ⅰ期临床试验显示肿瘤可以阻止EML4/ALK基因融合,这项试验研究显示有效率为57%~61%,平均PFS是9.7个月[27],这与吉非替尼和厄洛替尼对EGFR突变的肿瘤效果类似[11-12]。Ⅱ期单药实验研究显示出类似的结果,Ⅲ期随机试验显示,克唑替尼比多西紫杉醇或培美曲塞单药治疗效果好。在一次回顾性分析中发现,有ALK基因重组的患者使用克唑替尼相比其他治疗可以获得更长的寿命。美国食品与药物管理局已经批准克唑替尼用于荧光原位杂交技术(FISH)试验阳性的患者,ALK测试对于所有含有腺癌成分的NSCLC患者及使用克唑替尼显示阳性反应的患者是必需的。
近年来,有关其他NSCLC致癌驱动基因被报道,早期发表的针对TKIs的报道中都是有关人类表皮生长因子受体2、鼠类肉瘤滤过性毒菌致癌同源体B1、磷脂酰肌醇-3激酶催化亚基α基因的突变和酪氨酸激酶受体跨膜蛋白与原癌基因蛋白酪氨酸激酶(ROS)的重组以及肝细胞生长因子受体和成纤维生长因子受体1的增强表达。ROSTKI克唑替尼治疗ROS融合时,反应率和PFS的原始结果可能与EGFR TKIs治疗有EGFR突变的患者及克唑替尼治疗有ALK融合时类似。
2 维持治疗
4~6个周期的系统性含铂类化疗是标准一线治疗,延长治疗周期联合诱导方案可以延长PFS,但对存活率没有显著影响,同时以产生相关毒性为代价,特别像紫杉醇类药物[28]。诱导治疗后,患者无疾病进展到“观察和等待期”中,周期性疾病复发直到有新的进展,二线治疗便开始了。但约有1/2的患者第1次随访时出现了未控制疾病,相当比例健康状况恶化,无法进行下一步的治疗。
2.1 继续维持疗法 继续维持疗法是只实施低于一级护理的治疗,通常联合使用药物,直到疾病出现进展或相关的毒性。一个欧洲实验通过吉西他滨和顺铂诱导治疗4个周期来评估比较诱导维持治疗和BSC治疗的优劣,病程进展时间是主要观察点,很明显维持治疗的患者需要更长的时间(3.6 vs.2mo,P<0.001),同时吉西他滨维持治疗组显示更长的OS[29]。
PARAMOUNT实验是为了确定4个疗程的顺铂/培美曲塞治疗后培美曲塞维持治疗是否能提高疗效,本研究的主要目的是比较培美曲塞维持治疗与使用安慰剂(4.1 vs.2.8mo,HR0.62)后PFS改善的程度。试验显示OS也明显提高(13.9 vs.11mo,HR 0.78)[30]。关键的试验(ECOG 4899、AVAiL及FLEX)不是用来确定在感应阶段(使用双重铂药物)和维持阶段(单独用药)的不同效果[31-32],第2阶段的试验分析了培美曲塞加贝伐单抗以及顺铂3联体的维持治疗在感应阶段的结果,使用培美曲塞联合贝伐单抗后,在感应阶段(10.2 vs.6.6mo,HR 0.50)及随机分配(7.4 vs.3.7mo,HR 0.48)检测PFS显示其显著延长[33]。
2.2 早期的二线或间断支持治疗 间断支持治疗是诱导化疗阶段完成后立即对晚期NSCLC实施治疗。Fidias等[34]首创了这种疗法,随机分配使用立即或延迟二线多西紫杉醇6个周期治疗(在疾病进展期),相比延迟多西紫杉醇疗法的PFS中位数,直接多西紫杉醇疗法明显延长(5.7 vs.2.7mo,P=0.0001)。
最近2项类似的安慰剂对照试验设计评估了厄洛替尼和培美曲塞作为支持治疗的作用,试验中NSCLC患者在4个周期的含铂治疗后(不包括培美曲塞或厄洛替尼)[35-36],疾病得到控制。培美曲塞支持疗法明显提高了PFS(4.0 vs.2.0mo,HR 0.60)和OS(13.4 vs.10.6mo,HR 0.79)。同样,SATURN试验显示与安慰剂比较,使用厄洛替尼治疗的患者显著延长了PFS(12.3 vs.11.1weeks,HR 0.71)和OS(HR 0.81)[34]。最近一项法国试验(IFCTGFPC 0502)已经证实了支持疗法中EGFR TKIs对PFS的作用[37]。
3 小 结
目前有关晚期NSCLC靶向治疗的研究是热点,也能延长生存期、缓解症状、提高患者生活质量,已成为临床治疗决策中不可或缺的重要组成部分。近代药理遗传学和基因组学研究表明,细胞基因的多样性导致肿瘤细胞的异质性,因此,未来肿瘤个体化治疗将是主要方向及趋势,最终服务于肿瘤患者。
[1]Coate LE,Shepherd FA.Maintenance therapy in advanced non-small cell lung cancer[J].JThorac Oncol,2010,5(5):723-734.
[2]ScagliottiG,Brodowicz T,Shepherd FA,etal.Treatment-by-histology interaction analyses in three phaseⅢtrials show superiority of pemetrexed in nonsquamous non-small cell lung cancer[J].JThorac Oncol,2011,6(1):64-70.
[3]Quoix E,Zalcman G,Oster JP,et al.Carboplatin and weekly paclitaxel doublet chemotherapy compared with monotherapy in elderly patients with advanced non-small cell lung cancer:IFCT 0501 randomized,phase 3 trial[J].Lancet,2011,378(9796):1079-1088.
[4]Soria JC,Mauguen A,Reck M,etal.Systematic review andmeta-analysis of randomised,phaseⅡ/Ⅲtrials adding bevacizumab to platinum-based chemotherapy as first-line treatment in patientswith advanced non-smallcell lung cancer[J].Ann Oncol,2013,24(1):20-30.
[5]Aggarwal C,Somaiah N,Simon G.Antiangiogenic agents in themanagementofnon-small cell lung cancer:where dowe stand now and where are weheaded?[J].Cancer Biol Ther,2012,13(5):247-263.
[6]Leung L,Mok TS,LoongH.Combiningchemotherapywithepidermalgrowth factor receptor inhibition in advanced non-small cell lung cancer[J].Ther AdvMed Oncol,2012,4(4):173-181.
[7]Xu C,Zhou Q,Wu YL.Can EGFR-TKIs be used in f?rst line treatment for advanced non-small cell lung cancer based on selection according to clinical factors?-A literature-based meta-analysis[J].JHematol Oncol,2012,5:62.
[8]Coate LE,John T,Tsao MS,et al.Molecular predictive and prognostic markers in non-small-cell lung cancer[J].Lancet Oncol,2009,10(10):1001-1010.
[9]FranklinWA,Veve R,Hirsch FR,etal.Epidermalgrowth factor receptor family in lung cancer and premalignancy[J].Semin Oncol,2002,29(1Suppl4):3-14.
[10]HerbstRS,Bunn PA Jr.Targeting theepidermalgrowth factor receptor in non-small cell lung cancer[J].Clin Cancer Res,2003,9(16 Pt 1):5813-5824.
[11]Shepherd FA,Rodrigues Pereira J,Ciuleanu T,et al.Erlotinib in previously treated non-small-cell lung cancer[J].NEngl JMed,2005,353(2):123-132.
[12]Thatcher N,Chang A,Parikh P,etal.Gefitinib plus best supportive care in previously treated patients with refractory advanced non-small-cell lung cancer:results from a randomised,placebo-controlled,multicentre study(Iressa Survival Evaluation in Lung Cancer)[J].Lancet,2005,366(9496):1527-1537.
[13]Gatzemeier U,Pluzanska A,Szczesna A,etal.Phase IIIstudy oferlotinib in combinationwith cisplatin and gemcitabine in advanced non-small-cell lung cancer:the Tarceva Lung Cancer Investigation Trial[J].JClin Oncol,2007,25(12):1545-1552.
[14]Giaccone G,Herbst RS,Manegold C,etal.Gefitinib in combination with gemcitabine and cisplatin in advanced non-small-cell lung cancer:a phaseⅢtrial—INTACT 1[J].JClin Oncol,2004,22(5):777-784.
[15]Helfrich BA,Raben D,Varella-Garcia M,et al.Antitumor activity of the epidermal growth factor receptor(EGFR)tyrosine kinase inhibitor gefitinib(ZD1839,Iressa)in non-small cell lung cancer cell lines correlates with gene copy numberand EGFRmutationsbutnotEGFR protein levels [J].Clin CancerRes,2006,12(23):7117-1725.
[16]Lynch TJ,Bell DW,Sordella R,etal.Activatingmutations in the epidermal growth factor receptor underlying responsiveness of non-small-cell lung cancer togefitinib[J].NEngl JMed,2004,350(21):2129-2139.
[17]Han JY,Park K,Kim SW,etal.First-SIGNAL:first-line single-agent iressa versus gemcitabine and cisplatin trial in never-smokerswith adenocarcinomaof the lung[J].JClin Oncol,2012,30(10):1122-1128.
[18]Mok TS,Wu YL,ThongprasertS,etal.Gefitinib or carboplatin-paclitaxel in pulmonary adenocarcinoma[J].N Engl JMed,2009,361(10):947-957. [19]Mitsudomi T,Morita S,Yatabe Y,etal.Gefitinib or chemotherapy for nonsmall-cell lung cancer with mutated EGFR[J].Lancet Oncol,2010,11(2):121-128.
[20]Maemondo M,Inoue A,KobayashiK,etal.Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR[J].N Engl Med,2010,362(25):2380-2388.
[21]Inoue A,Kobayashi K,Maemondo M,et al.Updated overall survival results from a randomized phaseⅢ trial comparing gefitinib with carboplatin-paclitaxel for chemo-na?ve non-small cell lung cancer with sensitive EGFR genemutations(NEJ002)[J].Ann Oncol,2013,24(1):54-59.
[22]Zhou C,Wu YL,Chen G,etal.Erlotinib versus chemotherapyas first-line treatment for patientswith advanced EGFRmutation-positive non-smallcell lung cancer(OPTIMAL,CTONG-0802):a multicentre,open-label,randomised,phase3 study[J].LancetOncol,2011,12(8):735-742.
[23]Rosell R,Carcereny E,Gervais R,et al.Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFRmutation-positive non-small-cell lung cancer(EURTAC):amulticentre,open-label,randomised phase 3 trial[J].Lancet Oncol,2012,13(3):239-246.
[24]Karachaliou N,Costa C,Gimenez-Capitan A,etal.BRCA1,LMO4,and CtIP mRNA expression in erlotinib-treated non-small-cell lung cancer patientswith EGFRmutations[J].JThorac Oncol,2013,8(3):295-300.
[25]GridelliC,Ciardiello F,Gallo C,etal.First-line erlotinib followed by second-line cisplatin-gemcitabine chemotherapy in advanced non-small-cell lung cancer:the TORCH randomized trial[J].JClin Oncol,2012,30(24):3002-3011.
[26]Soda M,Choi YL,Enomoto M,et al.Identification of the transforming EML4-ALK fusion gene in non-small-cell lung cancer[J].Nature,2007,448(7153):561-566.
[27]Kwak EL,Bang YL,Camidge DR,et al.Anaplastic lymphoma kinase inhibition in non-small-cell lung cancer[J].NEngl JMed,2010,363(18):1693-1703.
[28]Lima JP,dos Santos LV,Sasse EC,et al.Optimal duration of first-line chemotherapy for advanced non-small cell lung cancer:a systematic review withmeta-analysis[J].Eur JCancer,2009,45(4):601-607.
[29]Brodowicz T,KrzakowskiM,Zwitter M,et al.Cisplatin and gemcitabine first-line chemotherapy followed bymaintenance gemcitabine or bestsupportive care in advanced non-small cell lung cancer:a phaseⅢtrial[J]. LungCancer,2006,52(2):155-163.
[30]Pujol JL,Paz-Ares L,de Marinis F,etal.Long-term and low-grade safety results of a phaseⅢ study(PARAMOUNT):maintenance pemetrexed plusbest supportive care versus placebo plus best supportive care immediately after induction treatmentwith pemetrexed plus cisplatin for advanced nonsquamous non-small-cell lung cancer[J].Clin Lung Cancer,2014,15(6):418-425.
[31]Sandler A,Gray R,Perry MC,et al.Paclitaxel-carboplatin alone or with bevacizumab for non-small-cell lung cancer[J].N Engl JMed,2006,355(24):2542-2550.
[32]Pirker R,Pereira JR,Szczesna A,et al.Cetuximab plus chemotherapy in patientswith advanced non-small-cell lung cancer(FLEX):an open-label randomised phaseⅢtrial[J].Lancet,2009,373(9674):1525-1531.
[33]BarlesiF,Scherpereel A,Rittmeyer A,etal.Randomized phaseⅢtrialof maintenance bevacizumab with orwithout pemetrexed after first-line induction with bevacizumab,cisplatin,and pemetrexed in advanced nonsquamous non-small-cell lung cancer:AVAPERL(MO22089)[J].JClin Oncol,2013,31(24):3004-3011.
[34]Fidias PM,Dakhil SR,Lyss AP,et al.PhaseⅢstudy of immediate compared with delayed docetaxel after front-line therapy with gemcitabine plus carboplatin in advanced non-small-cell lung cancer[J].JClin Oncol,2009,27(4):591-598.
[35]Ciuleanu T,Brodowicz T,ZielinskiC,etal.Maintenance pemetrexed plus bestsupportive care versusplacebo plusbestsupportive care fornon-smallcell lung cancer:a randomised,double-blind,phase 3 study[J].Lancet,2009,374(9699):1432-1440.
[36]Cappuzzo F,Ciuleanu L,Stelmakh L,etal.Erlotinib asmaintenance treatment in advanced non-small-cell lung cancer:amulticentre,randomised,placebo-controlled phase 3 study[J].Lancet Oncol,2010,11(6):521-529.
[37]PérolM,Chouaid C,PérolD,etal.Randomized,phaseⅢstudy ofgemcitabine or erlotinibmaintenance therapy versusobservation,with predefined second-line treatment,after cisplatin-gemcitabine induction chemotherapy in advanced non-small-cell lung cancer[J].JClin Oncol,2012,30(28):3516-3524.
10.3969/j.issn.1009-5519.2015.07.027
:A
:1009-5519(2015)07-1033-04
2015-01-21)
刘维(1986-),男,湖南益阳人,硕士研究生,主要从事肿瘤内科化学治疗研究;E-mail:46108432@qq.com。
罗以(E-mail:luoyi702@163.com)。
