电-生物耦合法对酸性红18染料废水处理效能的试验
2015-03-16郎佳丽赵玉华刘天明李奇聪
郎佳丽,赵玉华,刘天明,李奇聪
(沈阳建筑大学市政与环境工程学院,辽宁沈阳 110168)
染料种类繁多,按化学结构分类可分为偶氮染料、靛蓝染料、蒽醌染料、硫化染料、酞菁染料等[1]。其中偶氮染料是全世界使用最多的一种染料,约占80%以上[2],被广泛用于纺织品、皮革制品等染色及印花工艺[3]。偶氮染料分子结构中含有一个或多个偶氮基(—N==N—),其发色基团是偶氮基与一个或多个芳香环相连构成的一个共扼体。根据偶氮基数目可以分为单偶氮染料、双偶氮染料和多偶氮染料[4]。偶氮染料废水具有成分复杂、有机物浓度高、分布面广、水质变化大、有机毒物含量高、色度深、难生物降解,并含有大量的无机盐、硫化物等。此外其染料分子不易分解,可以在水环境以及光照的条件下稳定存在。其代谢产物为有毒难降解有机物,化学稳定性强,具有致癌、致畸、致突变的“三致”作用[5]。偶氮染料废水是较难处理的工业废水,处理方法有很多,其中电-生物耦合法综合了生物法和电化学法的优势,具有处理难降解有毒污染物效果好、成本低、方便控制、设备简单等特点[6]。本试验采用电-生物耦合法处理酸性红18(单偶氮基偶氮染料)配制的模拟染料废水,研究其处理效能和电流密度的影响。
1 试验方法
1.1 试验用水
实际工程中的偶氮染料废水组分复杂,其中包括有机中间体、胺类、苯胺、无机酸类(盐酸或硫酸)、碳酸钠、无机盐(亚硝酸钠、氯化钠、氯化钙、硫酸铝等)、偶氮组合物及其他杂质;其水质也变化较大,各组分的浓度波动大,各方面条件都不利于试验研究的良好进行,所以本试验采用人工模拟染料废水进行试验。
试验选用的染料为酸性红18(单偶氮基偶氮染料),分 子 式 为 C20H11N2Na3O10S3,分 子 量 为604.47 Da,在508 nm处有最大吸收峰。取地下水原水,投加一定量的酸性红18染料、淀粉、硫酸铵、氯化钙、磷酸二氢钾、硫酸镁及硫酸锰。配置成分如表1所示,试验用水水质各项指标情况如表2所示。

表1 试验用水配置成分Tab.1 Components of Experimental Water
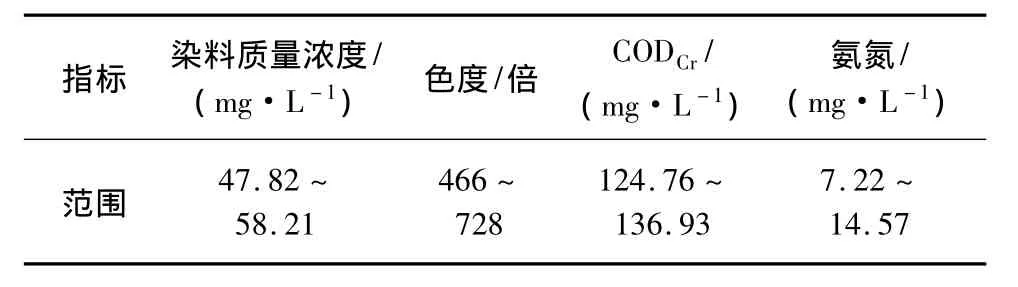
表2 试验用水水质Tab.2 Water Quality of Experimental Water
1.2 试验装置
试验装置如图1所示。
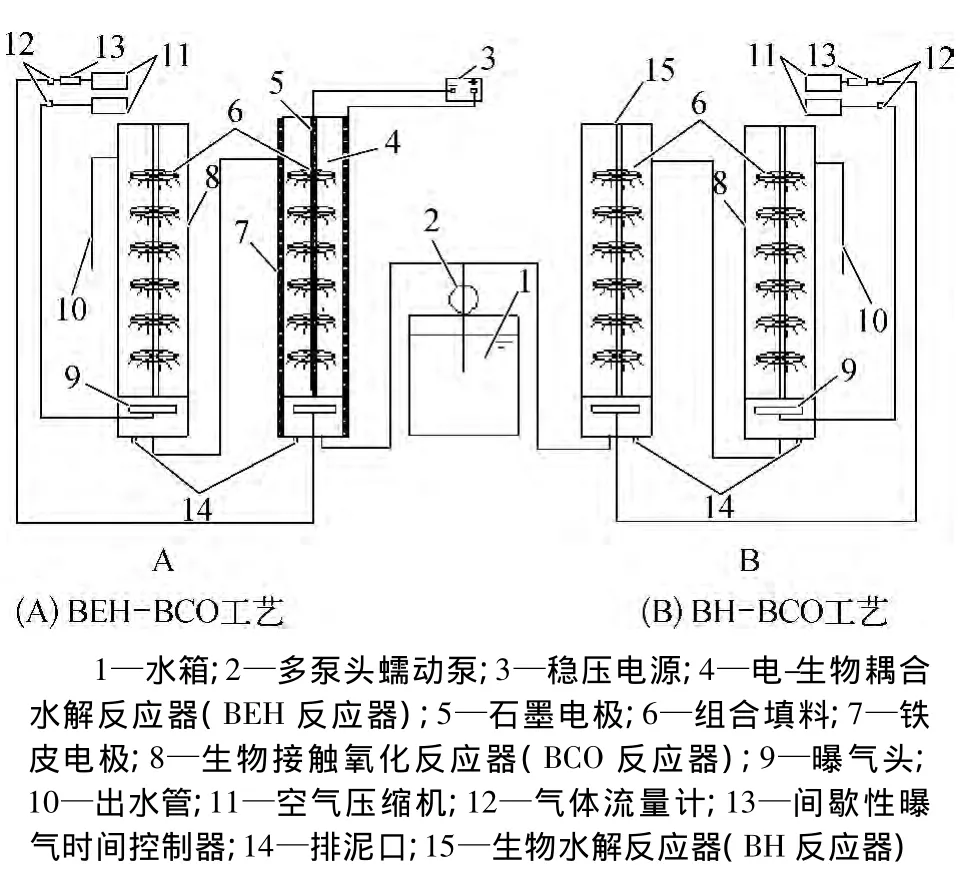
图1 试验装置示意图Fig.1 Schematic Diagram of Experimental Apparatus
由图1可知试验装置分为A、B两部分,A部分由电-生物耦合水解反应器和好氧生物接触氧化反应器串联而成,B部分为传统的水解-接触氧化工艺,反应器中心均放置填料。
A中的水解反应器内壁装有铁皮作阳极,中间装有石墨柱作阴极,通电后铁皮和石墨柱构成一对电极。铁皮高为1 m,宽为0.5 m;石墨柱直径为4 cm,高为1.2 m,超高0.2 m。直流稳压电源提供试验所需直流电。A和B两工艺的试验设计参数基本相同。水解反应器内径为18.5 cm,高为1.07 m,水深为1 m,有效容积为24 L,HRT为12 h;接触氧化反应器内径为15 cm,高为1 m,水深为0.9 m,有效容积为 15.9 L,HRT 为7.95 h,流量为2 L/h。
电-生物水解反应器用空气压缩机、气体流量计和时间控制器提供间歇性曝气,以保证反应器处于兼氧水解状态,同时搅拌空气可以使微生物保持悬浮流动状态,使其更容易挂膜,且与染料充分接触。接触氧化反应器采用连续曝气,保证了反应器内充足的溶解氧,并促使污水与微生物充分接触。
1.3 检测指标与方法
检测指标包括染料质量浓度、色度、CODCr、氨氮,具体如表3所示。
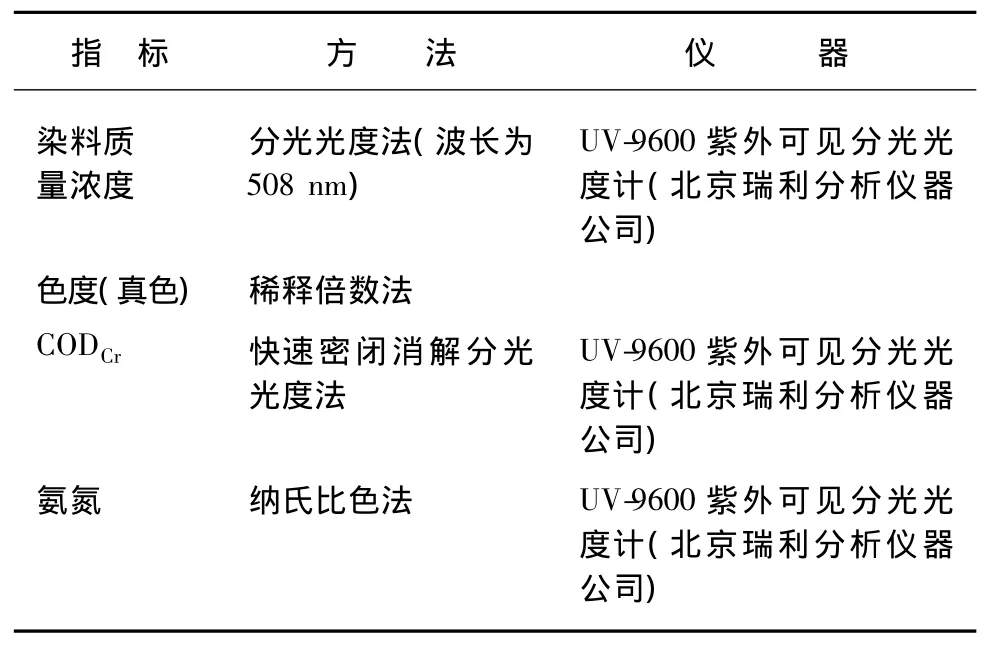
表3 水质检测指标、方法及仪器Tab.3 Analysis Items,Methods and Instrumentations
2 结果与讨论
水解与接触氧化反应器分别投加活性污泥进行接种启动,接种污泥是经过电-生物耦合水解与生物接触氧化法处理活性艳红X-3B染料废水驯化过的。
装置启动前3 d,电流密度为0.012 mA/cm2,加入营养物质(不加染料),正常曝气,每天更换一次反应器内的水。经过3 d培养后可观察到填料上出现生物膜且厚度逐渐增加,第4 d开始采用连续流方式运行,电流密度不变,添加染料并逐渐增加进水染料浓度。经过近两周的培养驯化,反应器内生物系统基本达到稳定状态,镜检生物膜发现有大量微生物出现,且出水CODCr、氨氮、染料浓度和色度的去除效果均趋于平稳,系统挂膜成功。从第16 d开始,试验正式运行,其间电流密度有变化,如表4所示。
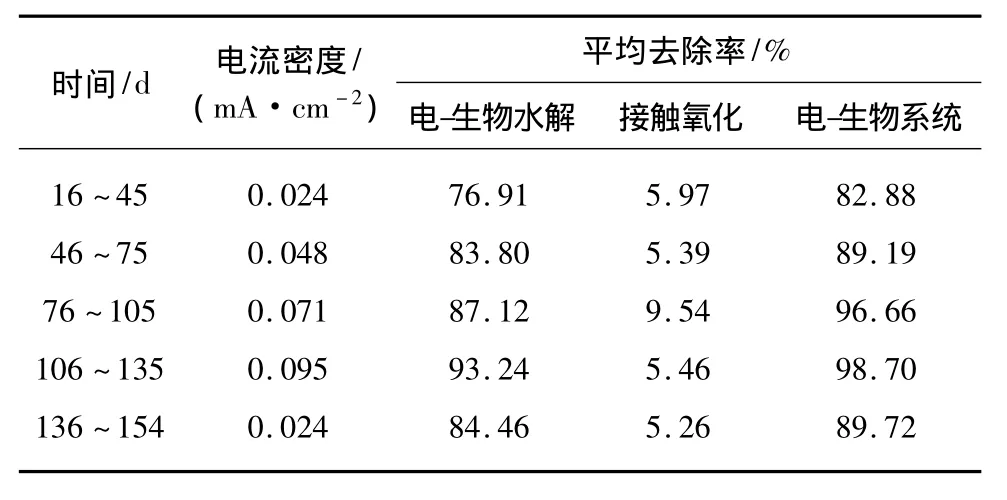
表4 酸性红18染料质量浓度去除率变化Tab.4 Variation of Mass Concentration's Removal Rates of Acid Red 18 Wastewater
2.1 酸性红18废水染料质量浓度的去除效果
酸性红18染料废水染料质量浓度变化情况及各阶段出水染料质量浓度去除率变化情况,如图2和表4所示。
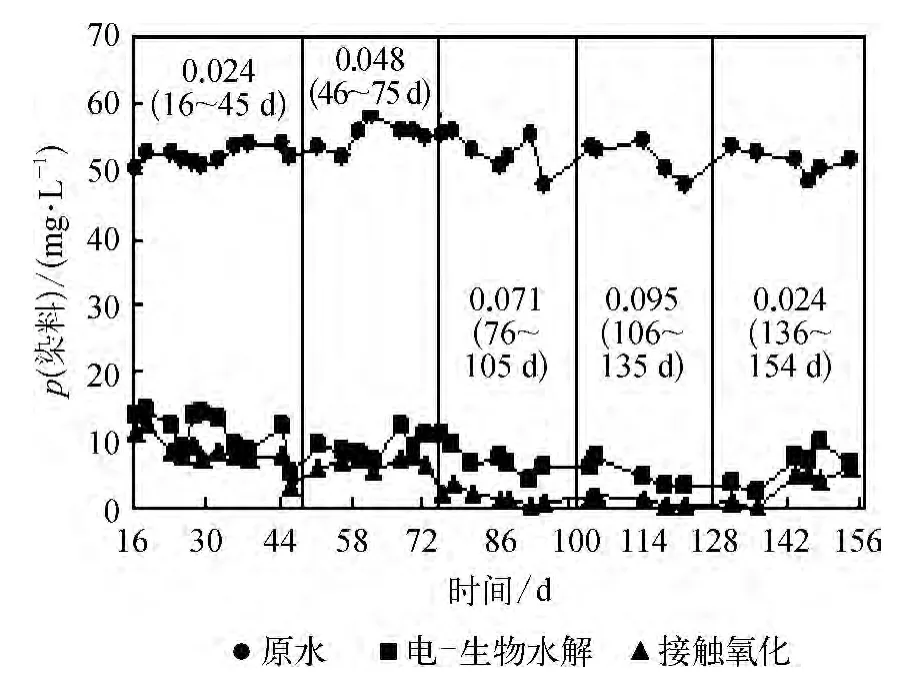
图2 酸性红18染料质量浓度变化情况Fig.2 Variation of Mass Concentration of Acid Red 18 Wastewater
由图2和表4可知电-生物系统对酸性红18染料质量浓度的去除效果较好。酸性红18原水染料质量浓度平均值分别为 52.22、54.85、52.71 和51.81 mg/L,电-生物耦合水解出水染料质量浓度平均值分别为12.20、8.89、6.78 和3.51 mg/L,系统出水染料质量浓度平均值分别为 8.93、5.93、1.78 和0.68 mg/L。由此可见,其染料质量浓度去除效果随电流密度的增加而提高。
在电-生物耦合水解反应器中,出水染料质量浓度去除率随电流密度的增加也不断升高,从76.91%升高到93.24%。其较高去除率的原因有以下三方面。(1)微生物的作用。水解微生物由于受到微电场刺激,生长能力和偶氮还原酶的活性都有所增强[7],进而增强对染料废水的降解能力。(2)电化学作用。电极的直接和间接氧化作用,使得染料分子被氧化。(3)物理作用。阳极铁皮电解时,产生的Fe(OH)3和Fe(OH)2具有絮凝沉淀作用[8],可吸附染料废水中的染料胶体微粒,并随着阴阳极产生的氢气和氧气上浮到反应器表面。
在生物好氧接触氧化阶段(16~135 d),染料质量浓度的去除率逐渐增加,从5.78%提高到5.57%。随着生物系统逐渐成熟,生物量有所增加;其次,随着电流密度的增加,电-生物耦合水解阶段对染料的去除效果逐渐变好,使染料和有毒中间产物得到充分降解,这为接触氧化阶段的生物毒性减弱,提供了一个适合微生物生长的环境。电-生物系统对染料质量浓度的平均去除率分别为82.28%、89.19%、96.66%和98.70%,都超过了80%。在136~154 d电流密度下降至0.024 mA/cm2,此时原水染料质量浓度平均值为50.44 mg/L,电-生物水解出水染料质量浓度平均值为 7.83 mg/L,平均去除率降到84.46%。去除效果下降主要有两方面原因:首先,电流密度突降,生物受到影响,需要慢慢适应;其次,电场作用减弱,影响去除效果。与初期同电流密度比效果较好,是由于试验运行的室温由初始阶段10℃左右上升到25℃左右,微生物的种类和数量随着温度的升高而增多,微生物体内的酶活性也逐渐增强,对染料分子的降解能力增强;除此之外,系统运行时间较长,生物系统较成熟,对染料分子水解能力得到提高。
2.2 酸性红18废水色度的去除效果
出水色度变化及去除率变化情况,如图3、表5所示。
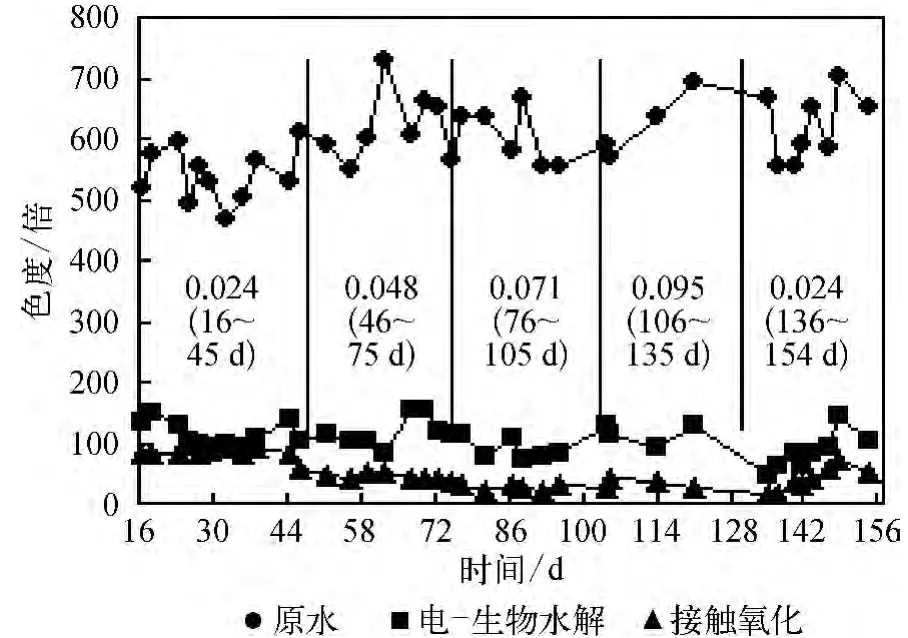
图3 酸性红18染料废水色度变化情况图Fig.3 Variation of Color of Acid Red 18 Wastewater
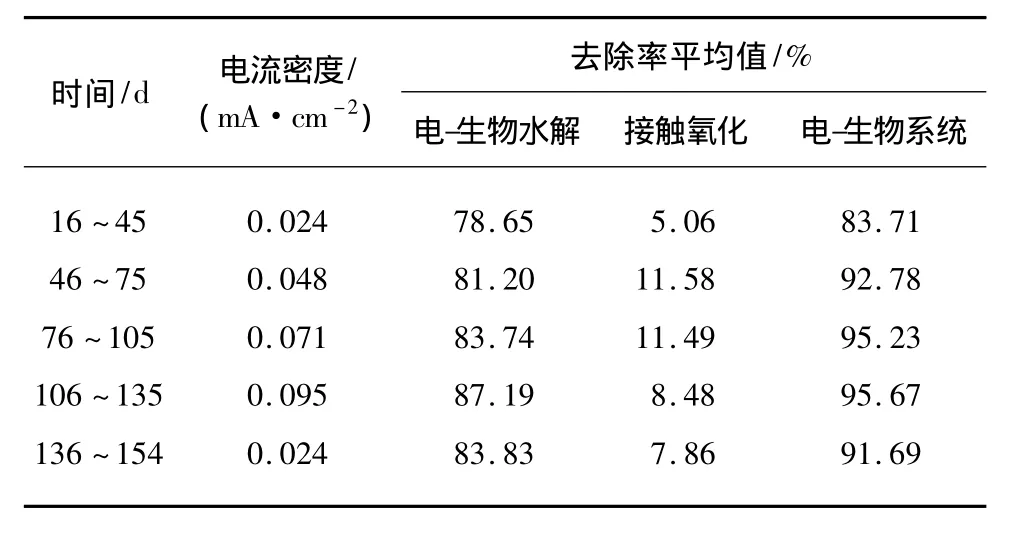
表5 酸性红18染料废水色度去除率变化Tab.5 Variation of Color's Removal Rate of Acid Red 18 Wastewater
由图3和表5可知电-生物系统对酸性红18染料废水的色度有较好的去除效果。表5中前四个时间段所对应的系统进水色度平均值分别为532、618、598和615倍,系统出水色度平均值分别为82、44、28和26倍,去除率平均值分别为 83.71%、92.78%、95.23%和 95.67%,出水色度随电流密度的增加而降低。
在电-生物耦合水解阶段(16~135 d),染料废水的色度随电流密度的增加而逐渐降低。在16~45 d,反应器内电流密度为 0.024 mA/cm2,酸性红97原水色度平均值为532倍,电-生物水解出水色度为114倍。此阶段脱色效果相对较差,原因是电流密度小,系统运行时间较短,电化学作用和电-生物的耦合水解作用都较弱;另外,微生物对废水水质还不适应,导致脱色率低。当电流密度分别为0.048、0.071 和0.095 mA/cm2时,原水色度平均值分别为618、598和615倍,电-生物水解出水色度分别为115、97和79倍。与染料质量浓度相似,都是由于电流密度的增大、温度的升高及微生物数量和种类随运行时间增加而逐渐增加逐步增强对染料分子的水解作用。
在生物好氧接触氧化阶段(136~154 d),电流密度降低至0.024 mA/cm2,脱色率降到 7.86%,但与试验初期同电流密度染料色度去除率相比提高了2.80%。
2.3 酸性红18废水COD的去除效果
出水CODCr变化情况及各阶段对COD去除效果,如图4、表6所示。

图4 酸性红18染料废水CODCr变化情况图Fig.4 Variation of CODCrof Acid Red 18 Wastewater
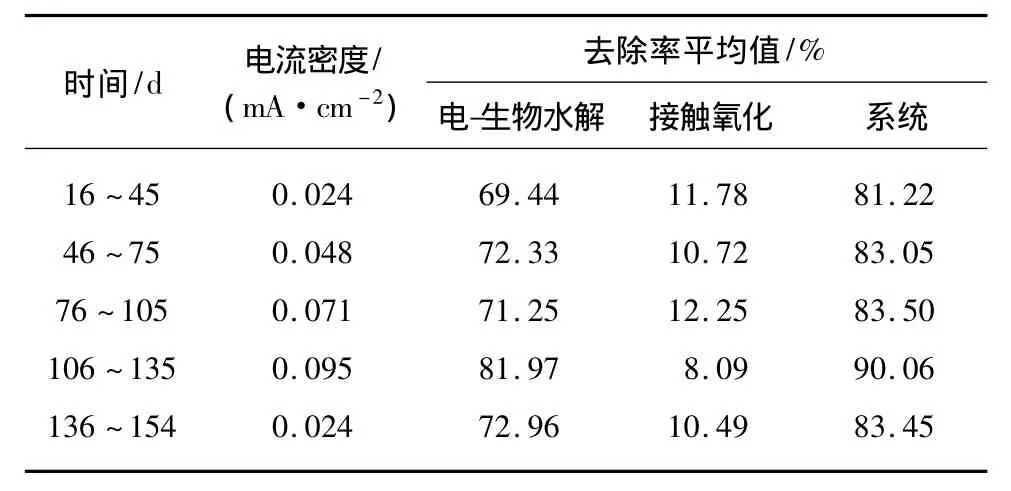
表6 酸性红18染料废水CODCr去除率变化Tab.6 Variation of COD Removal Rate of Acid Red 18 Wastewater
由图4和表6可知电-生物耦合系统对酸性红18染料废水COD的去除效果较好,其去除率随着电流密度的增加而升高。COD去除率平均值分别为81.22%、83.05%、83.50% 和 90.06%。在四个不同时间和电流密度的情况下,进水CODCr平均值分别为124.15、126.50、123.74 和 116.93 mg/L,系统出水 CODCr平均值分别为 23.10、21.27、20.25 和11.70 mg/L。当电-生物系统电流密度从 0.024升高到0.095 mA/cm2时,COD 去除率从69.44%上升到 81.97%。
在电-生物耦合水解阶段(16~135 d),染料废水的CODCr随着电流密度的增加呈下降趋势。在16 ~ 45 d,电流密度为 0.024 mA/cm2,电-生物水解出水平均CODCr为37.71 mg/L,此阶段COD去除效果较差且波动较大,原因可能是电流密度小,染料没完全降解,产生有毒的中间产物对微生物有害。大体来看COD去除率随着电流密度的增加而提高。随电流密度的增大,电极的直接氧化和间接氧化作用增强,大分子更快被降解为小分子,同时其降解产物也容易被微生物利用去除。
2.4 酸性红18废水氨氮的去除效果
出水氨氮值变化情况及各阶段对氨氮的去除效果,如图5、表7所示。

图5 酸性红18染料废水氨氮变化情况Fig.5 Variation of Ammonia Nitrogen of Acid Red 18 Wastewater
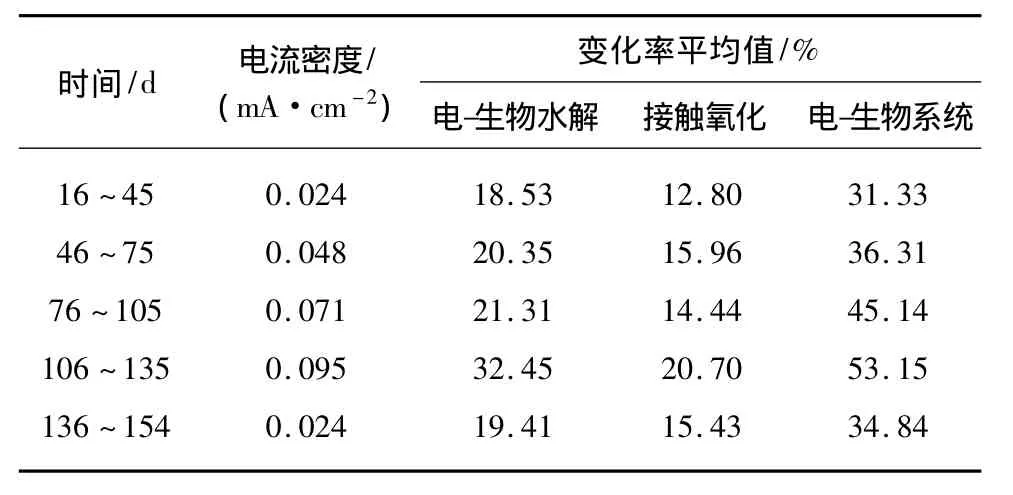
表7 酸性红18染料废水氨氮变化率Tab.7 Variation of Ammonia Nitrogen's Removal Rate of Acid Red 18 Wastewater
由图5和表7可知电-生物耦合系统对酸性红18染料废水氨氮有一定的去除效果,但与质量浓度、色度和CODCr相比,去除效果较差,去除率平均值分别为 31.33%、36.31%、45.14% 和 53.15%。系统氨氮去除率相对较低,可能跟好氧阶段的溶解氧不足有关,在反应器的顶部测得的溶解氧为3~5 mg/L,反应器内部的溶解氧应较低,不能满足好氧菌的硝化细菌对溶解氧的需求。电流密度从0.048 mA/cm2升高到 0.095 mA/cm2,去除率由20.35%升高到32.45%。在四个不同时间和电流密度阶段,系统进水氨氮平均值分别为11.95、12.47、12.25 和 11.17 mg/L,系统出水氨氮平均值分别为 7.95、7.69、6.87 和 5.15 mg/L。
在电-生物耦合水解阶段(16~135 d),染料废水氨氮的去除率随着电流密度的增加而缓慢提高。在16 ~45 d,反应器内电流密度为 0.024 mA/cm2,酸性红18原水氨氮平均值为11.95 mg/L,电-生物水解出水染料氨氮平均值为9.30 mg/L。此阶段氨氮去除效果较差且不稳定,还出现了出水氨氮超过进水的情况。这有两方面原因:电-生物水解反应降解染料分子而产生胺类化合物,再生成氨氮,导致废水中氨氮有所升高[9];反应器内的微生物,利用氮源进行同化作用形成细胞物质,电化学直接和间接氧化作用也能去除一部分氨氮,但总体来看去除的较少。在好氧接触氧化阶段,对染料废水氨氮有一定去除效果。氨氮去除率随电流密度增加而逐渐提高,从12.80%上升到20.07%。随着电流密度的升高,电-生物水解阶段对染料逐渐完全降解,有毒中间产物被降解,对接触氧化阶段的影响减弱;同时,随着温度的提高,电化学反应速率增大,对染料分子的去除效果也越好;随着运行时间增加,微生物的数量和种类也逐渐增加,对染料分子的去除降解的能力增强。
3 结论
(1)电-生物耦合系统对酸性红18染料废水的质量浓度、色度和COD有较好的处理效果。在一定的电流密度范围内,去除率随电流密度的增加而升高。当电流密度增加到0.095 mA/cm2时,处理效果最佳。此时电-生物系统对染料废水质量浓度、色度和COD的去除率分别为98.70%、95.67%和90.06%。
(2)电-生物系统对氨氮也有一定的处理效果,当电流密度分别为 0.024、0.048、0.071 和0.095 mA/cm2时,氨氮的去除率分别为31.33%、36.31%、45.14% 和 53.15%。
(3)电-生物耦合系统处理酸性红18染料废水染料质量浓度和色度,主要依靠电-生物耦合水解阶段,接触氧化阶段的去除率较小。
(4)电-生物耦合法处理酸性红18染料废水效能试验过程中,最佳处理工艺条件为水解反应器中电流密度为0.095 mA/cm2。
[1]黄春梅.偶氮染料的生物脱色及中间产物苯胺类的生物降解的特性研究[D].上海:华东理工大学,2012.
[2]宓益磊,樊金红,马鲁铭.电-生物耦合技术对偶氮染料的去除研究[J].环境工程学报,2009,3(8):1457-1461.
[3]金若菲.偶氮染料脱色工程菌的特性及强化作用研究[D].大连:大连理工大学,2007.
[4]王慧,周月霞,柏仕杰,等.染料废水生物法处理技术的研究进展[J].厦门大学学报,2008,12(47):286-290.
[5]黄玉.偶氮染料废水的处理方法及研究进展[J].宜宾学院学报,2007,29(6):54-57.
[6]张昌盛,薛安,赵华章.电-生物耦合技术在环境工程中的研究进展[J].工业水处理,2008,28(3):1-3.
[7]Peng She,BoSong,Xin-Hui Xing,et al.Electrolytic stimulation of bacteria Enterobacter by a direct current[J].Biochemical Engineering Journal,2006,28(12):23-29.
[8]何宝庆,吴灿灿.内电解-生化工艺处理染料废水研究[J].污染防治技术,2006,19(4):6-8.
[9]ZHAO Yuhua,DONG Ruijiao,CANG Xiaoyi,et al.Research on Removel of Azo Dye Wastewater by Bioelectrochemical Technology[M].Chengdu:Chengdu conference papers,2010.
