国产和进口荧光定量PCR试剂检测HBV-DNA的比对分析*
2015-03-15田文君刘义庆张炳昌刘春梅
张 玥,田文君,刘义庆,张炳昌,张 庆,渠 滕,刘春梅
(山东大学附属省立医院检验科,济南 250021)
·论 著·
国产和进口荧光定量PCR试剂检测HBV-DNA的比对分析*
张 玥,田文君,刘义庆,张炳昌,张 庆,渠 滕,刘春梅△
(山东大学附属省立医院检验科,济南 250021)
目的 分析国产和进口实时荧光定量聚合酶链反应(PCR)试剂检测乙型肝炎病毒(HBV)-DNA的相关性,探讨国产和进口试剂在临床应用中的差异。方法 使用国产和进口试剂平行检测262例乙型肝炎(乙肝)患者血浆当中的HBV-DNA水平,国产试剂采用手工提取标本,罗氏LightCycler480 Ⅱ(LC480 Ⅱ)进行核酸扩增;进口试剂则采用罗氏COBAS AmpliPrep(CAP)和COBAS Taqman48(CTM)进行标本提取和扩增;对HBV-DNA病毒载量数据进行对数转换(log10),并将两组数据进行相关分析。结果 国产和进口试剂检测结果,经线性拟合,R2=0.814 3。HBV-DNA浓度在10~103IU/mL的标本,R2=0.300 6;浓度在104~105IU/mL的标本,R2=0.411 8;浓度在106~108IU/mL的标本,R2=0.801 7。进口试剂阳性检出率为75.57%(198/262),明显高于国产试剂阳性检出率[65.65%(172/262)]。结论 国产试剂和进口试剂相比,相关性良好。HBV-DNA浓度在106~108IU/mL时,相关性最高;浓度在104~105IU/mL时,相关性一般;浓度在10~103IU/mL时相关性较差,国产试剂与进口试剂有明显差异,灵敏度有待进一步提高。
乙型肝炎病毒DNA; 实时荧光定量PCR; 试剂比对; 血浆
乙型肝炎(简称乙肝)是世界常见的传染病之一[1],全球感染乙肝的人群约有3.5亿[2],中国大约1.2亿人,占三分之一[3],占我国人口总数的8%~10%,是感染乙型肝炎病毒(HBV)人数最多的国家。HBV是属于嗜肝DNA病毒科,有较强的抵抗性、传染性和变异性,并且传播途径多样。乙肝极易发展为慢性肝炎和肝硬化,从而引发肝癌[3],所以预防和治疗乙肝已成为中国乃至全球尤为重要的研究课题之一。现今,在临床众多检测HBV感染的方法中,实时荧光定量PCR技术检测乙肝病毒核酸(HBV-DNA)是目前特异性较好、灵敏度较高的方法[4],HBV-DNA复制越高,传染性就越强。同时,结合乙肝五项[5]、肝功能和甲胎蛋白(AFP)等项目的测定,可以更好地反映出乙肝患者的病情和用药治疗情况,从而为临床医生对患者进行诊断和治疗提供可靠的理论依据。本文就收集的262例乙肝患者血液标本,采用两种不同的试剂进行检测并统计分析,现报道如下。
1 资料与方法
1.1 一般资料 收集2013年7月至2014年1月的期间在本院就诊做超敏乙肝病毒DNA(HS-HBV-DNA)检测时的乙二胺四乙酸二钾(EDTA-K2)抗凝血标本262例。将标本按3 000 r/min离心8 min,留取血浆冷冻于-80 ℃冰箱保存。
1.2 仪器与试剂 试剂A由凯杰生物工程(深圳)有限公司提供;试剂B由罗氏诊断产品有限公司提供。试剂A、B分别用罗氏LC480 Ⅱ扩增仪和罗氏CAPCTM检测系统,实验所用试剂在有效期内,仪器均已进行校准。
1.3 方法 将262例血浆标本分别用试剂A、B进行平行检测,试剂A采用人工提取核酸和实时荧光定量检测技术,最低检出限为5×102IU/mL,定量检测线性范围为(1×103)~(5×107)IU/mL;试剂B基于罗氏CAP提取仪标本制备过程和同时进行的靶DNA PCR扩增与靶序列特异性双标记寡核苷探针检测过程,最低检出限为12×10 IU/mL,定量检测线性范围为(5.45×10)~(1×108)IU/mL。
1.3.1 试剂A 离心管中加人100 μL待测血浆标本和100 μL的DNA提取液1,充分振荡混匀,13 000 r/min离心10 min;吸弃上清液;加入25 μL DNA提取液2,振荡混匀,完全将沉淀溶解,3 000 r/min离心10 s,然后100 ℃干浴10 min;13 000 r/min离心10 min,离心完毕后,取2 μL上清液加入PCR管内的反应液中。
1.3.2 试剂B 取待测血浆标本1 030 μL,加入带条码夹的样品管中,与配套专用试剂盒装入罗氏CAP提取仪内。
1.3.3 质量控制 试剂A每批次做阴性对照、空白对照及高中低三个不同水平的质控品;试剂B每批次均做阴性对照及一个低水平的质控品。
1.4 统计学处理 首先对HBV-DNA病毒载量数据进行对数转换(log10),采用SPSS21.0软件进行统计学分析。试剂比对用线性分析和χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 两种试剂检测结果相关分析 将试剂A、B的检测结果取对数值后做相关分析,通过分析曲线可以看出,线性良好,试剂A、B契合度一般,R2=0.814 3,线性曲线如表1所示。
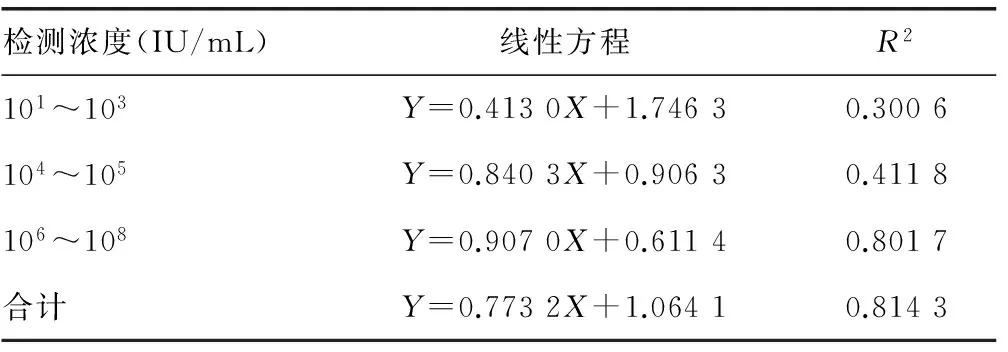
表1 两种试剂检测结果相关分析
2.2 两种试剂检测率比较 试剂B阳性检出率为75.57%(198/262),试剂A阳性检出率为65.65%(172/262),经检验,进口试剂阳性检出率明显高于国产试剂(χ2=20.833,P<0.01),结果详见表2。
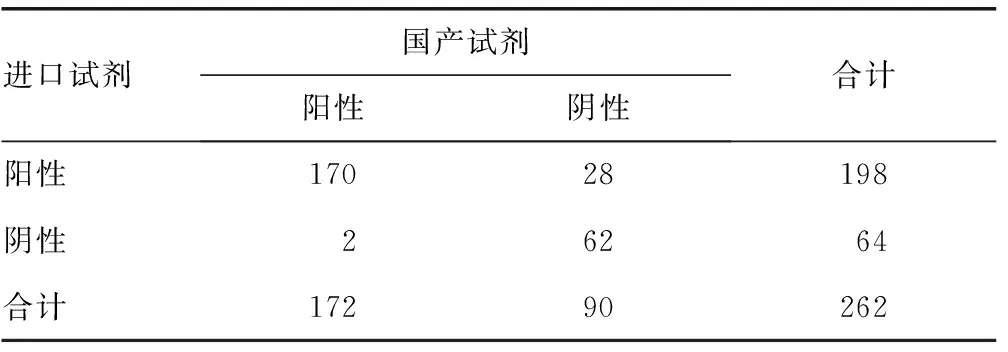
表2 两种试剂检测率比较(n)
3 讨 论
HBV-DNA定量可以精准地反映患者体内的病毒复制情况,目前检测HBV-DNA定量的方法和试剂种类繁多,国际公认进口罗氏试剂为检测HBV-DNA定量的参比试剂[6]。进口试剂灵敏度高、精密度好,但试剂成本较高,仪器价格昂贵,检测时间长,需要患者血浆量大,在大部分医院难以广泛使用。国产试剂基本为开放试剂,价格适中,检测快速,重复性较好,医院因为科室发展和经济水平等原因,使用国产试剂的单位比较普遍[7]。试剂A为煮沸法,手工提取核酸繁琐复杂,极易造成核酸的丢失,容易将检出限附近的低浓度标本漏检[8];试剂B采用磁珠分离技术,标本处理在罗氏CPA提取仪内进行,降低了因操作不当等原因产生的假阳性,且每个标本中加入内标来防止假阴性,监测整个提取和扩增过程,试剂前期准备也简单、便捷。
本组结果分析可以看出,两种试剂线性相关性良好,R2=0.814 3。HBV-DNA浓度在106~108IU/mL时,相关性最高;浓度在104~105IU/mL时,相关性一般;浓度在10~103IU/mL时相关性较差,较进口试剂差异有统计学意义,灵敏度有待进一步提高。在262例标本检测结果中,有28例经试剂A检测阴性而试剂B检测阳性,提示试剂B的灵敏度更高;有2例标本,试剂A检测阳性而试剂B检测阴性,说明在用试剂A提取过程存在污染的可能。两种试剂提取方法和对标本体积的需求量不同,所以试剂的灵敏度、精密度和操作过程等也不同。在262例标本当中,其中4例标本浓度大于5×107IU/mL,用罗氏CAPCTM检测系统第一次上机实验未得出数据,经10倍稀释得出结果。用试剂A做4例标本,不用稀释便可得出实验结果。使用试剂B做浓度大于5×107IU/mL的标本时,必须稀释。所以,在乙肝活动期或明确高浓度标本时,可以直接选择试剂A来检测HBV-DNA水平。
现在临床治疗乙肝以核苷类抗病毒药物为主,在长期的治疗过程当中,极易发生HBV的变异和耐药[9]。HBV变异和耐药的发生,不仅使患者治疗费用增加,如不及时发现,甚至会进一步恶化,使病情加重,影响后续治疗药物的选择。实时、准确地监测乙肝患者HBV-DNA的水平,不仅是临床医生用药的关键性指标,也是患者了解病情的直观数据[10]。虽然进口试剂价格较贵,但是灵敏度相比较高,可以在用药治疗后,进行随访检测,观察是否到达预期治疗效果。国产试剂在中、高浓度范围内,相关性良好,患者在初诊、乙肝活动期或HBV反跳时进行检测,不仅减少了患者看病时间和经济负担,还可以提高患者和医生对临床实验室的满意度。
综上所述,2种实时荧光定量PCR检测试剂,标本HBV-DNA浓度在10~103IU/mL时,国产试剂与进口试剂差异有统计学意义。进口试剂灵敏度较高,适用于乙肝患者耐药后选择新药治疗的疗效评估和患者治疗后期的病情监测。乙肝活动期或做高浓度标本时,可以直接选择试剂A。临床医生可根据患者的具体病情,选择适合的检测试剂。
[1]朱妍.137例病毒性肝炎的病原学分析[J].中国医药指南,2013,11(9):612-613.
[2]Tankivanich P,Sa-Nguanmoo P,Mahachai V,et al.A case-control study on sequence variations in the enhancer Ⅱ /core promoter /precore and X gens of hepatitis B virus in patients with hepatocellular carcinoma[J].Hepatol Int,2010,4(3):577-584.
[3]吴肖峰.PreS1Ag与HBV-DNA、乙肝病毒“两对半”的相关性分析[J].中国当代医药,2011,18(14):81-82.
[4]Caliendo AM,Valsamakis A,Bremer JW,et al.Multi-laboratory evaluation of real-time PCR tests for hepatitis B virus DNA quantification [J].J Clin Microbiol,2011,49(8):2854-2858.
[5]韩晓蓉.乙肝五项指标测定结果与HBV DNA的关系探析[J].中外医疗,2012,32(17):40-42.
[6]Allice T,Cerutti F,Pittaluga F,et al.Comparison of the Cobas Ampliprep/Cobas TaqMan HBV Test versus the Cobas Amplicor HBV monitor for HBV-DNA detection and quantification during antiviral therapy[J].New Micmbiol,2008,31(1):27-35.
[7]荆成宝,禹梅,刘婕.2种HBV-DNA荧光定量PCR检测试剂的比较[J].国际检验医学杂志,2013,34(2):206-207.
[8]陈小颖,赵荣平,应春妹.实时荧光定量PCR检测低含量HBV-DNA的分析[J].现代检验医学杂志,2009,24(5):85-87.
[9]Ghany MG,Doo EC.Antiviral resistance and hepatitis B therapy [J].Hepatology,2009,49(5 Suppl):S174-S184.
[10]蔡惠兴,吴英,梁鹏.乙肝血清标志物与HBV-DNA定量检测结果分析 [J].国际医药卫生导报,2010,16(2):227-229.
Comparative analysis on domestic and imported fluorescent quantitative PCR reagents for detecting HBV-DNA*
ZHANGYue,TIANWen-jun,LIUYi-qing,ZHANGBing-chang,ZHANGQing,QUTeng,LIUChun-mei△
(DepartmentofClinicalLaboratory,AffiliatedShandongProvincialHospital,ShandongUniversity,Jinan,Shandong250021,China)
Objective To analyze the correlation between the domestic and imported real-time fluorescent quantitative PCR reagents for detecting HBV-DNA and to explore their difference in clinical application.Methods The domestic and imported reagents were used to parallelly detect the plasma HBV-DNA content in 262 cases of hepatitis B.The domestic reagent adopted the sample extracting by adopting the manual method and the amplification for nucleic acid was performed by the Roche LightCycler480 Ⅱ(LC480 Ⅱ);the imported reagent used the Roche COBAS AmpliPrep (CAP) and COBAS Taqman48(CTM) for conducting the sample extracting and amplification;the HBV DNA viral load data (log10) was performed the logarithmic transformation and the 2 sets of data were conducted the correlation analysis.Results The detection results of the domestic and imported reagents were performed the linear fitting,R2=0.814 3.The sample with the concentration range of 10-103IU/mL,R2= 0.300 6;the sample with the concentration range of 104-105IU/mL,R2= 0.411 8;the sample with the concentration range of 106-108IU/mL,R2=0.801 7.The positive detection rate of the imported reagent was 75.57% (198/262),which was significantly higher than 65.65% (172/262) of the domestic reagent.Conclusion There is a good correlation between the domestic reagent and imported reagent.The correlation is the highest when the HBV-DNA concentration in the range of 106-108IU/mL;the correlation is general when the concentration in the range of 104-105IU/mL;the correlation is lowest when the concentration in the range of 10-103IU/mL,there is a significant difference between the domestic reagent and imported reagent and the sensitivity of the domestic reagent remains to be further improved.
HBV-DNA; real-time fluorescent quantitation PCR; reagent comparison; plasma
国家自然科学基金资助项目(81102220);山东省自然科学基金资助项目(ZR2011HM019); 山东省临床重点专科建设项目(鲁卫医字[2013]26号)。
张玥,女,技师,本科,主要从事肝病的分子诊断工作。△
,E-mail:lcm831011@163.com。
10.3969/j.issn.1672-9455.2015.02.002
A
1672-9455(2015)02-0147-02
2014-05-07
2014-08-28)
