食品中重金属铅、镉电化学检测的前处理技术
2015-03-11刘亚芹魏福祥
闫 珂,刘亚芹,魏福祥
(1.河北科技大学环境科学与工程学院,河北石家庄 050018;2.河北省污染防治生物技术实验室,河北石家庄 050018)
铅、镉是人体中不需要的重金属,而且在环境中铅、镉有蓄积性且不易消除,通过食物链一步步进入人体中,一旦积蓄过量将会对人体各机能造成极大的危害[1]。金属铅随食物进入人体后很难自然排泄出去,长期积累会造成人体免疫功能低下、智力受损、贫血、消化系统疾病、生殖系统疾病,甚至会引起癌变[2-4]。更为严重的是铅积聚在婴幼儿身体内,会有超过30%的铅保留在体内,这对婴幼儿的危害是致命的[5]。长期接触一定量的镉会导致肾脏的损伤、骨质软化和疏松,严重的极易发生病理性骨折和生殖毒性[6-7],还可引发心血管功能障碍、神经系统疾病、免疫系统疾病等严重病症[8-11]。因此,对于食品中金属铅、镉的检测极为重要。
食品中重金属检测方法多为原子吸收分光光度法,原子吸收分光光度计作为大型仪器,很难进行现场测定。而电化学检测仪器多为小型仪器,携带方便,适用于现场快速检测。用电化学方法检测食品样品中重金属,首先要对样品进行前处理。食品中重金属的含量属于痕量范围,样品前处理的好坏直接影响检测结果。所以,在食品中重金属检测中,样品前处理极为关键。目前样品前处理技术有干法灰化法、湿法消解法[12-13]、微波消解法[14-16]。干法灰化法耗时长,在反应过程中存在元素损失[17]。湿法消解法通用性强,所有食品均适用[18],可进行多样品操作。微波消解法多用于原子吸收分光光度法测定的前处理,成本高,不适于现场测定。基于此,本研究旨在选择适于电化学测定的湿法消解前处理技术,更好地为食品中重金属铅、镉的现场测定提供参考。
1 实验部分
1.1 仪器与试剂
1.1.1 实验仪器
FA2003型电子天平(上海良平仪器仪表有限公司提供),98-1-B型电子调温电热套(天津市泰斯特仪器有限公司提供),重金属检测仪(天津兰力科公司提供),三电极体系(检测用:工作电极为Φ3 mm玻碳电极,参比电极为银丝电极,对电极为铂丝电极;镀膜用:工作电极为Φ3 mm玻碳电极,参比电极和对电极均为黑色氯化银电极),40目(约0.42 mm)标准检验筛(浙江上虞市华丰五金仪器有限公司提供),SYZ-500型石英亚沸高纯水蒸馏器,玛瑙研钵,石棉网等。所有玻璃器皿要用质量分数为30%硝酸浸泡过夜后,用二次水清洗干净。
1.1.2 实验试剂
硝酸(优级纯),过氧化氢,硝酸铅[19](优级纯),氯化镉(优级纯),玉米面,小米,大米,二次水。
铅标准储备液:取0.159 8 g硝酸铅加1.0 mol/L硝酸10 mL全部溶解后,移入100 mL容量瓶中,加二次水定容至刻度,此溶液的铅质量浓度为1.0 mg/mL。
铅标液:铅标准储备液经过0.5 mol/L硝酸稀释后的各浓度标准使用液。
镉标准储备液:称取0.203 11 g氯化镉加二次水全部溶解后,移入100 mL容量瓶中,加二次水定容至刻度,此溶液中的镉质量浓度为1.0 mg/mL。
镉标液:镉标准储备液经过二次水稀释后的各浓度标准使用液。
1.2 实验方法
1.2.1 样品预处理
粮豆类等干样于玛瑙研钵内研磨成粉状,过40目(约0.42 mm)筛,储存在塑料瓶中,冷藏保存备用。蔬菜、水果等含水分高的鲜样要用不锈钢刀切碎或用匀浆机打成匀浆,储存在塑料瓶中,冷藏保存备用。
1.2.2 样品湿法消解
称取1 g过40目(约0.42mm)筛的样品放进锥形瓶中,采用硝酸-过氧化氢体系,加入一定量的硝酸,放在电热套上于一定温度下加热消解,等反应缓和即不再冒大量棕黄色烟后,加入1mL过氧化氢,当再次出现棕黄色烟时,随即加入1 mL过氧化氢,重复此过程,直至消解液颜色变浅、剩余2~3 mL时,不再加入过氧化氢,持续加热到剩余消解液为1~2 mL时,取下锥形瓶,加入二次水在140℃左右赶酸,剩余1 mL左右时取下,定容到10 mL或者25 mL比色管中。
1.2.3 样品电化学检测
1.2.3.1 玻碳电极预处理与镀汞
玻碳电极(Φ3 mm)在使用前需要进行抛光处理[20]。在麂皮上的三氧化二铝悬浊液中按照“8”字形垂直轻轻研磨2 min左右。保证每次研磨力度、时间相同。然后用二次水冲洗电极头,再用滤纸擦掉粘附的三氧化二铝粉。
将预处理后的玻碳电极在氯化汞溶液中镀汞,对电极、参比电极采用黑色氯化银电极,使电极表面形成一层均匀完整的浅灰色汞膜。镀汞图见图1。
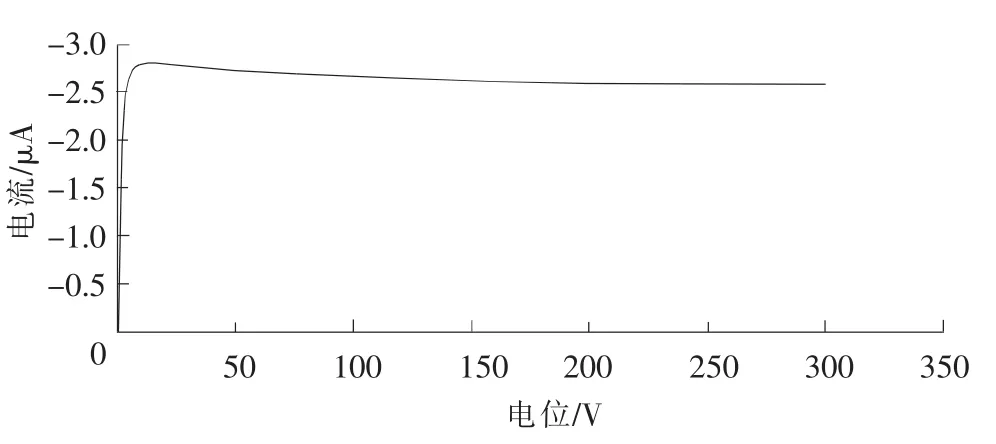
图1 玻碳电极镀汞Fig.1 Glassy carbon electrodemercury-plated
1.2.3.2 电化学工作程序
取一定浓度的铅、镉标液0.4 mL,置于1.6 mL体积分数为0.4%HCl底液中,按表1设置实验参数,测铅、镉含量所用参数一致。使用镀完汞膜的三电极系统,选择差分脉冲溶出伏安法,测定不同铅、镉标液在 -0.55 V,-0.75 V左右的峰电流。铅、镉标液出峰图见图2、图 3。

表1 电化学测定参数Tab.1 Electrochemicalmeasurement parameters

图2 1×10-5 mg/mL铅标液出峰图Fig.2 1 ×10 -5 mg/mL lead standard solution peak figure
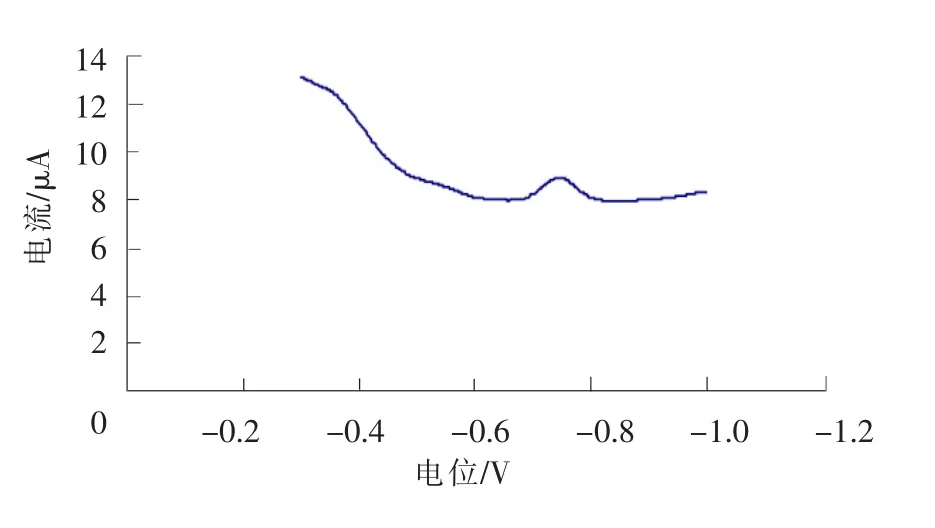
图3 4×10-5 mg/mL镉标液出峰图Fig.3 4 ×10 -5 mg/mL cadmium standard solution peak figure
测定消解液时,实验程序与铅、镉标液测定相同。测定消解液中铅、镉含量见图4、图5。图4中曲线a—曲线d表示在消解液中加入铅标液,标液浓度从低浓度到高浓度。图5中曲线e—曲线h表示在消解液中加入镉标液,标液浓度从低浓度到高浓度。图4、图5显示:随着在消解液中标液浓度增加,峰高也随之增高。图中表明:铅出峰位置在-0.55 V左右,镉出峰位置在-0.75 V左右。可根据峰高确定消解液中铅、镉含量,以此来确定最佳的湿法消解条件。

图4 测定消解液中铅含量Fig.4 Determination of lead in digestion solution
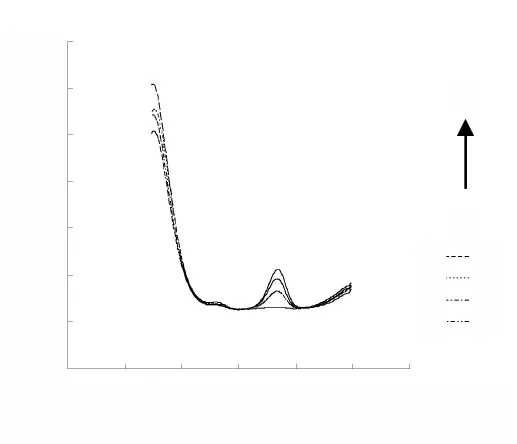
图5 测定消解液中镉含量Fig.5 Determination of cadmium in digestion solution
2 结果与讨论
2.1 预消解时间的影响
1 g过筛后的玉米面放入锥形瓶中,加入等量的硝酸,使用等量的过氧化氢,在电热套上加热消解之前,分别放置0,4,8,12 h进行预消解。消解液用电化学检测,根据电化学检测峰高算出样品中铅的含量,确定合适的预消解时间。放置时间越长,硝酸挥发越多,损失越多,在电热套上加热消解时达不到完全消解的目的。结果如图6所示,随着预消解时间的增长,同一样品消解液中的铅含量减少,在预消解时间为12 h时,则无法检测出铅含量。即加入硝酸后可直接放置在电热套上加热消解,不用进行预消解,消解效果最好,消解最完全。
2.2 消解温度的影响
取5份相同的等量过筛后的玉米面放入锥形瓶中,加入等量的硝酸,分别在100,120,140,160,180℃下加热消解,使用等量的过氧化氢,消解液用电化学检测,根据电化学检测峰高算出样品中铅的含量,确定合适的消解温度。结果见图7,在100~140℃范围内,随着温度增高,消解时间越短,消解越完全。在140~180℃范围内,随着温度增高,虽然消解时间缩短,但是挥发的硝酸增多,消解越来越不完全,而且在160℃之后样品回收率迅速降低,因为随着温度升高,消解速度加快,硝酸挥发速度也加快,硝酸量的减少,无法使消解完全。实验证明,湿法消解最佳温度应在120~140℃范围内。

图6 预消解时间的影响Fig.6 Influence of pre-digestion time

图7 消解温度的影响Fig.7 Influence of digestion temperature
2.3 硝酸-过氧化氢用量的影响
取5个锥形瓶,各放入1 g过筛后的玉米面,分别加入4,7,10,13,17 mL硝酸。放在电热套上于140℃下加热消解,使用等量的过氧化氢进行湿法消解,消解完成后的消解液用电化学检测,根据电化学检测出的峰高值计算出样品中铅的含量,继而确定合适的硝酸用量。硝酸量少时,湿法消解不完全,硝酸量多时,消解完全后还剩多余的硝酸,在继续消解后,铅、镉元素可能随着剩余硝酸的挥发造成损失。但因为硝酸含有少量铅、镉,当消解过程中用硝酸过多时,计算出来的样品中铅含量反而会增加。结果如图8所示,随着硝酸量的增加,样品中铅含量先增大后减小继而增大,在加入10 mL硝酸时达到最大。最终确定湿法消解硝酸用量为10 mL。

图8 硝酸用量的影响Fig.8 Influence of nitric acid dosage
根据实验操作步骤,由于实验过程中操作的不一致性,以及各食品特性不同,各食品含有的物质元素不同,以致各食品的消解难易程度不同,当食品消解困难时,则需要加入的过氧化氢次数多,用量就多,当食品消解容易时,则需要加入的过氧化氢次数少,用量就少。所以在湿法消解用10 mL硝酸时,过氧化氢用量在10~15 mL范围内。
2.4 湿法消解条件的确定
铅、镉属于低温重金属[21],而湿法消解过程的温度一般较低(<200℃),铅、镉离子可稳定存在于酸溶液中,在前处理过程中不易挥发损失,可以在同一个湿法消解体系中检测出来。因为铅、镉测定的底液环境为酸性环境,赶酸后的消解液为酸性,所以无需进一步地调节pH值,就可以同时用电化学检测铅、镉2种元素。测定消解液中铅浓度时所确定的湿法消解条件,亦可适用于测定镉。最终湿法消解条件见表2。

表2 湿法消解条件Tab.2 Wet digestion conditions
2.5 重复性
利用电化学方法对山楂干消解液进行重复测定11次,其铅含量检测结果的相对标准偏差为1.93%,镉含量检测结果的相对标准偏差为3.84%。表明电化学测定具有较好的重复性。
2.6 加标回收率
取2个相同的样品,其中一个加上8×10-3mg/mL铅(或镉)标液25μL,另一个则不加铅(或镉)标液。经过相同的湿法消解处理后,进行测定,计算回收率。
选用玉米面样品:1—3号为大米样品;4—6号为小米样品;7—9号为消解样品。具体数据见表3和表4。
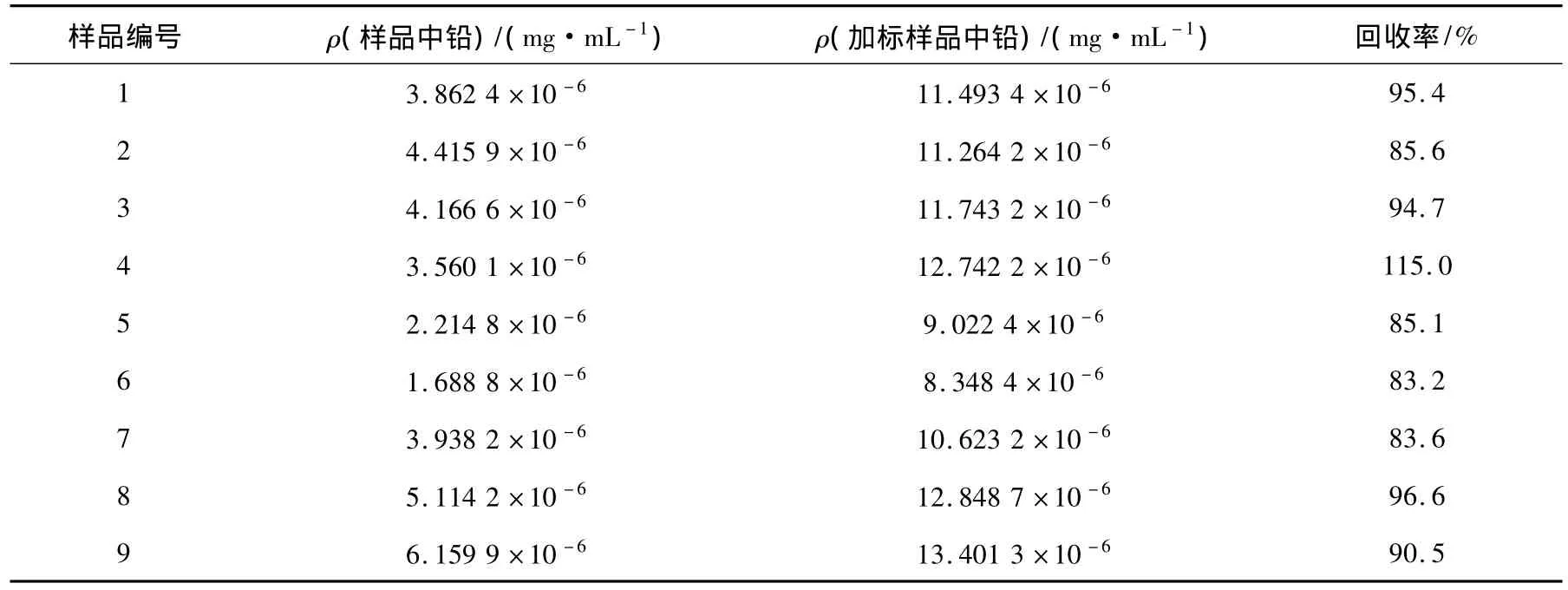
表3 样品中铅回收率Tab.3 Lead recovery of samples

表4 样品中镉回收率Tab.4 Cadmium recovery of samples
3 结论
对于检测食品中重金属铅、镉的前处理技术,采用湿法消解法确定使用10 mL硝酸-过氧化氢体系,在120~140℃温度范围内,无需放置预消解,可以消解完全,且硝酸和过氧化氢不会造成浪费和损失。样品加标回收率为82%~115%,此湿法消解法操作简便,通用性强,可同时进行多样品操作。通过对湿法消解过程中各实验参数的优化,该法作为电化学检测的前处理技术,可以消解完全,并满足电化学检测的要求。在操作过程中,要注意防止重金属铅、镉的污染,注意保障实验过程的安全性。
/References:
[1] 杨敬坡,罗建美,逯飞,等.石墨消解火焰原子吸收法测定土壤中重金属[J].河北科技大学学报,2014,35(4):392-396.YANG Jingpo,LUO Jianmei,LU Fei,et al.Determination of heavymetal contents in soil by flame atomic absorption spectrometry using graphite digestion device[J].Journal of Hebei University of Science and Technology,2014,35(4):392-396.
[2] TOPLAN S,OZCELIK D,GULYASAR T,et al.Changes in hemorheological parameters due to lead exposure in female rats[J].Journal of Trace Elements in Medicine and Biology:Organ of the Society for Minerals and Trace Elements(GMS),2004,18(2):179-182.
[3] 赵静,孙海娟,冯叙桥.食品中重金属铅污染状况及其检测技术研究进展[J].食品与发酵工业,2014,40(9):122-127.ZHAO Jing,SUN Haijuan,FENG Xuqiao.Research progress on the pollution of heavymetals lead and its detection technology in food[J].Food and Fermentation Industries,2014,40(9):122-127.
[4] HOU X,PARENTM,SAVARD M M,et al.Lead concentrations and isotope ratios in the exchangeable fraction:Tracing soil contamination near a copper smelter[J].Geochemistry:Exploration,Environment,Analysis,2006(6):229-236.
[5] BRUCE K R.Encyclopedia of Inorganic Chemistry[M].Hoboken:John Wiley& Sons Inc,2005.
[6] 杨永聪.食品重金属污染及其对策分析[J].轻工科技,2013(5):18-19.YANG Yongcong.Heavymetal contamination of food and countermeasures[J].Light Industry Science and Technology,2013(5):18-19.
[7] 赵静,孙海娟,冯叙桥.食品中重金属镉污染状况及其检测技术研究进展[J].食品工业科技,2014,35(16):371-376.ZHAO Jing,SUN Haijuan,FENG Xuqiao.Research progress in pollution of heavymetals cadmium and its detection technology in food[J].Science and Technology of Food Industry,2014,35(16):371-376.
[8] NORDBERG G,JIN T,BEMARD A,etal.Low bone density and renal dysfunction following environmental cadmium exposure in China[J].Ambio,2002,31(6):478-481.
[9] 吴思英,田俊,周天枢,等.镉污染区居民疾病死亡谱分析[J].中国公共卫生,2003,19(1):29-30.WU Siying,TIAN Jun,ZHOU Tianshu,et al.Cadmium polluted area residents died of disease spectrum analysis[J].China Public Health,2003,19(1):29-30.
[10] KAGAMIMORIS,WATANABEM,NAKAGAWA H,et al.Case control study on cardiovascular function in fem-aleswith a history of heavy exposure to cadmium[J].Bulletin of Environmental Contamination and Toxicology,1986,36(1):484-490.
[11] 韩磊,张恒东.铅、镉的毒性及其危害[J].职业卫生与病伤,2009,24(3):173-177.HAN Lei,ZHANG Hengdong.Lead,cadmium toxicity and hazards[J].Journal of Occupational Health and Damage,2009,24(3):173-177.
[12] GB 5009.12—2010,食品中铅的测定[S].GB 5009.12—2010,Determination of Lead in Foods[S].
[13] GB/T 5009.15—2003,食品中镉的测定[S].GB/T 5009.15—2003,Determination of Cadmium in Foods[S].
[14] 田龙.微波消解法快速测定大米中的痕量铅、镉[J].粮食加工,2008,33(1):97-100.TIAN Long.Determination of lead and cadmium in rice bymicrowavemicrowave-digestionmethod[J].Grain Processing,2008,33(1):97-100.
[15] 王永平,赖强,丁红梅,等.微波消解同时测定农产品中铅、镉、汞[J].中国卫生检验杂志,2012,22(2):214-215.WANG Yongping,LAIQiang,DING Hongmei,etal.Simultaneous determination of lead,cadmium and mercury in agricultural products bymicrowave digestion[J].Chinese Journal of Health Laboratory Technology,2012,22(2):214-215.
[16] 李军.微波消解-电化学法快速测定大米中的镉含量[J].化学传感器,2011,31(2):60-63.LIJun.Rapid determination of cadmium in rice bymicrowave digestion-electrochemical[J].Chemical Sensors,2011,31(2):60-63.
[17] 倪张林,汤富彬,屈明华.不同前处理方法测定植物油中重金属的研究[J].中国油脂,2012,37(7):85-87.NIZhanglin,TANG Fubin,QUMinghua.Determination of heavymetals content in vegetable oilswith different preprocessingmethods[J].China Oils and Fats,2012,37(7):85-87.
[18] 杨雪娇,黄伟,林涛,等.不同前处理方法检测食品中的重金属含量[J].现代食品科技,2008,24(10):1051-1054.YANG Xuejiao,HUANGWei,LIN Tao,et al.Determination of heavy metal contents in foodstuffs by three pretreatmentmethods[J].Modern Food Science and Technology,2008,24(10):1051-1054.
[19] 张宁,王俊菊.硝酸铅和金属铅作为对照品测定铅含量方法的探讨[J].中国农业科技导报,2009,11(sup1):32-34.ZHANG Ning,WANG Junju.Discussion onmethod of lead determination using lead nitrate andmetallic lead as reference substances[J].Journa l of Agrcultural Science and Technology,2009,11(sup1):32-34.
[20] 许嫔,魏福祥,张尚正,等.石墨烯/聚苯胺复合膜修饰玻碳电极测定多巴胺[J].河北科技大学学报,2014,35(2):139-143.XU Pin,WEIFuxiang,ZHANG Shangzheng,etal.Electrochemical detection of dopamine on the grapheme/polyaniline composite film modified electrode[J].Journal of Hebei University of Science and Technology,2014,35(2):139-143.
[21] 魏竟智,段妮.干、湿法消解-石墨炉原子吸收法测定茶叶中铅镉对比[J].广东微量元素科学,2014,21(3):7-12.WEI Jingzhi,DUAN Ni.Dry digestion and wet digestion-graphite furnace AAS tomeasure and compared the lead and cadmiun in tea leaves[J].Trace Elements Science,2014,21(3):7-12.
