无结扎技术与传统技术在胃癌根治术中的近期疗效比较
2015-03-11徐胜黄顺荣麦威钟晓刚李雷王晓通
徐胜 黄顺荣 麦威 钟晓刚 李雷 王晓通
[摘要] 目的 探讨无结扎外科技术在胃癌根治术中的临床价值和疗效。 方法 选择2011年1月~2013年12月广西壮族自治区人民医院行胃癌根治术病例60例,按照手术方式分为无结扎组和传统组,每组各30例。观察两组患者围术期临床疗效和外周血免疫功能变化。 结果 全部两组病例手术顺利,无术中、术后大出血。无结扎组与传统组手术时间分别为(82.67±17.05)、(93.80±14.55) min,术中出血量分别为(65.50±24.05)、(93.50±35.51)mL,术后平均引流量分别为(136.17±66.13)、(228.77±101.63)mL,两组比较差异均有统计学意义(P < 0.05);无结扎组与传统组清扫淋巴结个数分别为(19.16±9.12)、(20.13±7.43)个,平均肛门排气时间分别为(3.90±0.68)、(4.00±0.73)d,术后住院时间分别为(10.87±1.33)、(11.40±1.87)d,两组比较差异均无统计学意义(P > 0.05)。术后第1天、术后第7天无结扎组患者血球蛋白水平[(23.88±3.63)、(28.82±4.44)g/L]较传统组[(21.84±3.96)、(25.44±4.23)g/L]显著升高,差异均有统计学意义(P < 0.05)。术前、术后第1天、术后第7天两组外周血血红蛋白、红细胞比积、淋巴细胞计数、总蛋白、白蛋白及淋巴细胞计数比较,差异均无统计学意义(P > 0.05)。 结论 无结扎外科技术实施胃癌根治术可避免血管夹、缝线等异物体内存留,与传统胃癌根治术比较可达到相同的肿瘤根治效果,但具有手术时间短、术中出血及术后引流量少、手术创伤小、免疫功能损伤小的优点。
[关键词] 胃癌;胃癌根治术;无结扎外科技术;电外科
[中图分类号] R615 [文献标识码] A [文章编号] 1673-7210(2015)01(c)-0045-04
由于医学工具及技术的发展,诊治理念和外科手术也不断革新,为了达到肿瘤根治和外科微创化目的,手术方法推陈出新。尤其腔镜微创技术的快速兴起,Ligasure、超声刀等腔镜新工具被广泛应用到传统开腹手术中,给外科医生提出挑战的同时,也给广大患者带来新的机遇。其中,手术中的组织血管结扎材料(不吸收与可吸收缝线、塑料夹钛夹等)、结扎方式(丝线、血管夹、缝合器等)和止血方法(生物蛋白胶应用、电外科设备更新等)的不断进步也吸引了外科学者们的广泛关注[1-2]。本研究观察比较了广西壮族自治区人民医院(以下简称“我院”)2011年以来应用无结扎外科技术实施胃癌根治术病例的围术期临床疗效,现报道如下:
1 资料与方法
1.1 纳入及排除标准
本研究经我院伦理委员会审核通过,研究病例术前充分知情同意。入选标准:2011年1月~2013年12月我院住院患者;年龄30~80岁;术前经胃镜及病理组织检查确诊胃癌;术前凝血功能正常。排除标准:术前腹部CT提示胃癌外侵或远处转移者;近期大出血及感染者;严重心肺疾患者;有应用阿司匹林等药物抗凝病史者;既往有腹部大手术者;有乙肝肝硬化及门静脉高压症等严重慢性病史者。
1.2 一般资料
分组方法:按相同胃癌根治方式(近端胃切除术、远端胃切除术、全胃切除术)首选1例随机掷硬币入组(无结扎组或传统组),随后1例计入另一组;至全部手术病例分组完成。术中联合应用电刀、超声刀和Ligasure完成组织切割分离、止血或淋巴结清扫,即无结扎技术方法设为研究组(无结扎组);采用传统手术分离止血方法(术中不使用结扎速、超声刀,仅应用电刀、分离钳、解剖剪等手术器械)设为对照组(传统组)。其中,近端胃癌根治术毕Ⅰ式吻合2例,远端胃癌根治术Ⅱ式吻合21例,根治性全胃切除术ROU-Y吻合7例。两组各自入选30例,无结扎组:男22例,女8例;年龄36~76岁,平均(54.0±11.1)岁;其中Ⅰb期2例,Ⅱ期9例,Ⅲ期19例。传统组:男20例,女10例;年龄34~73岁,平均(56.3±11.0)岁;其中Ⅰb期1例,Ⅱ期8例,Ⅲ期21例。两组患者性别、年龄等一般资料比较差异无统计学意义(P > 0.05),具有可比性。
1.3 手术方法
体位:平卧位;麻醉方式:气管插管全麻、静脉复合麻醉;工具:电刀(威力)、超声刀(强生)或FORCE TM外科能量平台(威力)。所有患者均为同一组术者实施研究病例手术。
无结扎组(远端胃癌):第一步:入腹探查。上腹剑突至脐正中切口逐层切开入腹,探查盆腔、肝脾有无转移结节,明确肿瘤部位、大小、活动度等。第二步:处理横结肠系膜。大网膜中部开始,沿横结肠系膜前叶后方之疏松间隙电刀分离,沿胰腺被膜平面分离,清扫肠系膜上静脉淋巴结(No.14v),沿该平面分离、清扫幽门下淋巴结,显露胃网膜右动静脉,以Ligasure血管根部闭合离断,整块清扫幽门下淋巴结(No.6)。电刀结合ligasure向左分离大网膜,至胃短动脉第2支上方。第三步:处理十二指肠球部。将胃十二指肠交界部向上充分暴露,Ligasure自十二指肠后方分离处理与胰头间的细小分支血管。十二指肠上缘电刀切开小网膜,超声刀依次清扫肝固有动脉周围淋巴结(No.12a)。Ligasure切断胃右动脉、静脉,充分游离十二指肠,使上下方交通,远端分离达幽门下约4 cm。直线切割缝合器封闭、离断十二指肠。第四步:淋巴结清扫及血管骨骼化。胃十二指肠残端上提,联合电刀、超声刀从右向左清扫幽门上(No.5)、肝动脉旁(No.8a)淋巴结,整体切除小网膜及附属淋巴结。连续向左清扫分离到胃左动脉和腹腔动脉分支处,Ligasure闭合、离断胃左动脉,超声刀清扫胃左动脉干(No.7)和腹腔动脉周围淋巴结(No.9),沿胰上缘脾动脉分离、清扫周围淋巴结(No.11),向上游离肝胃韧带达贲门下,清扫贲门右淋巴结(No.1)。第五步:消化道重建及引流。距treitz韧带约12 cm空肠置放吻合器蘑菇头,胃空肠毕Ⅱ式吻合器吻合,距吻合口约4 cm以直线型缝合器TX60闭合胃壁、切除远端癌肿,移除标本。腹腔止血、冲洗、置放引流后手术完毕。注意要点主要包括:术中处理血管时,3 mm以下较细血管可运用超声刀、电刀直接离断,包含直径3~7 mm较粗血管的网膜、系膜可使用Ligasure多次闭合、形成闭合带后远端离断。清扫胃周淋巴结时,电刀、超声刀联合使用骨骼化血管,Ligasure双重钳夹、凝固确切后闭合带远端离断。一般非门静脉高压症者的胃左血管直径小于5 mm,因此,对于无需骨骼化者,直接以Ligasure闭合切断包含胃左、胃右动静脉的组织束。如术中出血,明确出血点后,可Ligasure刀头直接钳夹凝固止血。全胃切除或近端胃切除时,对部位较深或难以显露的脾门、膈肌脚,充分利用Ligasure刀头几乎无侧向热副损伤的优点,明确解剖结构后直接分离、闭合、离断。
传统组(远端胃癌):主要手术操作径路和步骤相同,不同点在于术中解剖、分离方法采用电刀、分离钳、解剖剪等手术器械,采用丝线结扎,而不使用超声刀或结扎术。如结肠系膜前后叶和网膜、胰腺被膜分离切除、全部胃周淋巴结清扫(包含No.14v、6、12a、5、8a、7、9、11、1)均使用解剖剪刀或电刀协助处理,十二指肠残端及消化道重建均同样方法使用直线缝合器或吻合器。全胃或近端胃切除时,对于部位深在的脾门和两侧膈肌脚,则需要小心保护脾脏、防止撕裂出血,分次血管钳钳夹、丝线结扎近脾门部胃短血管或两侧膈肌分支血管。
1.4 观察指标
观察两组患者的手术时间、术中出血量、术后引流量、淋巴结清扫个数、肛门排气时间、术后住院时间和并发症发生情况,观察术前及术后第1天、第7天患者外周血红细胞计数、血红蛋白、血细胞比容、淋巴细胞计数及总蛋白、白蛋白、免疫球蛋白。
1.5 统计学方法
采用SPSS 16.0统计学软件进行数据分析,符合正态分布计量资料的采用均数±标准差(x±s)表示,两组间比较采用t检验;不符合正态分布的改用中位数或四分位数间距表示,两组间比较采用非参数检验(秩和检验);计数资料用率表示,组间比较采用χ2检验,以P < 0.05为差异有统计学意义。
2 结果
2.1 两组围术期临床疗效
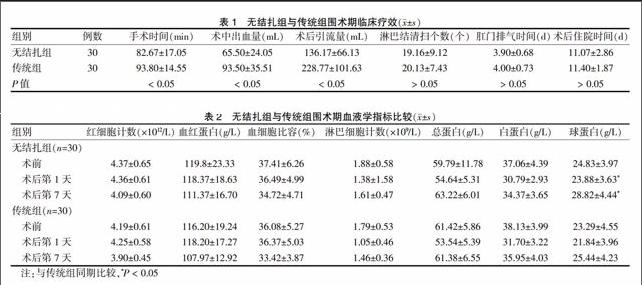
全部病例麻醉、手术过程顺利。两组比较,手术时间、手术术中出血、术后引流方面无结扎组均要少于传统组,差异有统计学意义(P < 0.05),而淋巴结清扫数目、肛门排气时间、术后住院时间方面两组之间差异无统计学意义(P > 0.05),见表1。无结扎组1例术后第7天出现十二指肠残端漏,经给予引流、抑酸等保守治疗治愈。两组病例均无术中、术后大出血等其他严重并发症,围术期恢复顺利。
2.2 两组围术期血液学指标
两组病例外周血血红蛋白、血细胞比容、总蛋白、白蛋白及淋巴细胞计数之间的差异均无统计学意义(P > 0.05),但是术后第1、7天无结扎组淋巴细胞计数要稍好于传统组。术后第1、7天无结扎组免疫球蛋白水平明显高于传统组,差异有统计学意义(P < 0.05),显示无结扎组术后免疫球蛋白恢复较传统组要快,见表2。上述结果显示,无结扎技术明显保护了胃癌患者围术期的免疫功能。
3 讨论
无论开腹或腹腔镜胃癌根治手术[3-4],步骤复杂,操作平面多,门静脉、胆管、肝总动脉、胃周血管等解剖管道多,血供丰富,良好的分离、切割、止血工具极为重要[5]。最初的传统胃癌切除手术,只有解剖剪、分离血管钳等实施组织分离,并使用丝线结扎血管,术中出血多,视野血液污染不清晰,麻醉和手术时间久,患者创伤极大,术后恢复很慢,体内永久异物存留。随着电刀、高频电刀、超声刀的临床应用、推广,极大降低了精细分离、切割、止血的繁杂程度,降低了外科创伤。Ligasure的临床应用则使相对粗大血管的处理进一步简化,对较粗大血管(非门脉高压症患者的胃左血管直径一般<5 mm)无需缝线、钛夹、缝合器等器械,也可安全进行血管闭合、离断。结合高频电刀、超声刀和Ligasure功能于一体的能量平台,使术者可根据实际手术需要自由转换分离、止血和切割器械,简化手术步骤,手术方式进一步改良。
我院于2004年最初开始应用Ligasure实施胃癌外科手术以来,积累了十年的临床经验认为[6-9]:无门静脉高压症病例的胃周血管,一般直径小于7 mm,Ligasure可安全、有效闭合包括胃左动静脉在内的较粗大血管。2008年即引进了Force Triad TM能量平台,应用于我院普外科临床,随后提出、逐步完善无结扎外科技术理论[8],即:根据组织结构、电外科设备特性和手术要求,手术中通过联合应用电刀、超声刀和Ligasure等电外科新工具,达到降低手术难度,缩短手术时间,减少缝线结扎和血管夹使用,尽可能避免体内异物存留的切割、分离、止血的手术技术,称之为无结扎外科技术。由于胃周解剖复杂,无结扎技术实施胃癌根治术优势较明显。而通过应用新的电外科设备、结合胃癌根治原则,进一步提出无结扎方法进行胃癌手术:①电刀:主要用于分离横结肠系膜前后叶、胰腺被膜的分离止血。②超声刀:主要用于肝十二指肠韧带及肝总动脉旁、腹腔动脉、胃左血管、脾动脉周围淋巴结清扫。可有效避免电刀操作导致的误损伤,减少分离钳、剪刀分离引起的出血,保持术野清洁无血液污染,增加分离安全性。③Ligasure:主要用于胃网膜及系膜、胃网膜右动脉、胃右血管、胰头与十二指肠间的小血管、胃左血管、胃小弯、胃短动脉、脾门、膈肌脚、贲门周围组织的闭合、离断止血,以及胃周淋巴结整块切除。但使用Ligasure处理前,必须明确周围重要组织结构,尤其是脉管样结构。简而言之,根据各种不同电外科设备的新特性,结合手术原则,选取不同的止血、结扎、分离方式,减少手术出血和时间、降低手术复杂性的技术即为无结扎外科技术。
本研究所有病例均采用电刀、超声刀、Ligasure闭合胃周血管,其中胃左血管、胃右血管、胃网膜血管均以Ligasure闭合、离断,均无术中、术后出血严重并发症的发生。由于避免了丝线结扎的繁复过程,无结扎技术也明显缩短了手术时间。从术后血红蛋白、红细胞计数及术中出血量、腹腔引流量两组的结果分析来看,两组之间机体循环整体的差异无统计学意义,但无结扎技术直接闭合了创面动静脉、毛细血管和淋巴管,术中出血、术后腹腔引流渗出也相对传统组较少。
本研究两组患者术后免疫球蛋白及淋巴细胞计数较术前均明显下降,提示胃癌术后免疫功能受到抑制。其中,术后第1、7天,淋巴细胞计数无结扎组较传统组稍高,尽管二者之间的差异无统计学意义。术后第1、7天,无结扎组免疫球蛋白水平明显高于传统组,显示术后免疫功能得到了一定保护,或术后免疫功能恢复速度较传统组较快。因此,本研究提示无结扎技术对胃癌根治术具备一定的免疫保护作用。胃癌患者往往合并免疫功能抑制,免疫治疗也是其综合治疗的重要部分[10-11]。围术期的麻醉和手术打击往往进一步导致机体免疫功能包括机体细胞免疫和体液免疫抑制,不利于术后感染和肿瘤的控制,因此,通过无结扎技术保护胃癌患者围术期免疫功能也显得极为重要。
在胃癌手术中联合运用电刀、超声刀和Ligasure等电外科新设备,结合胃周解剖特点以及胃癌根治要求,有效组合不同止血方式,尽量避免金属夹、丝线等异物材料存留和繁复操作,改良传统胃癌手术,程序化建立无结扎胃癌根治的手术方式,达到降低手术难度和减轻手术创伤、促进患者机体免疫保护以及术后快速恢复的目的,均具有重要的临床意义。
[参考文献]
[1] Rajbabu K,Barber NJ,Choi W,et al. To knot or not to knot? Sutureless haemostasis compared to the surgeon's knot [J]. Ann R Coll Surg Engl,2007,89(4):359-362.
[2] Landman J,Kerbl K,Rehman J,et al. Evaluation of a vessel sealing system,bipolar electrosurgery,harmonic scalpel,titanium clips,endoscopic gastrointestinal anastomosis vascular staples and sutures for arterial and venous ligation in a porcine model [J]. J Urol,2003,169(2):697-700.
[3] 赵庆洪,鲁明,张弛,等.腹腔镜胃癌根治术与开放性胃癌根治术的对比研究[J].临床肿瘤学杂志,2010,(5):438-440.
[4] 郑民华.腹腔镜胃肠手术中消化道重建方式的选择和技术难点[J].中华胃肠外科杂志,2011,14(6):399-402.
[5] Asao T,Kuwano H,Mochiki E,et al. A novel ligation forceps can be used as a ligature carrier and knot pusher during laparoscopic surgery [J]. Surgical Endoscopy,2001,15(5):524-527.
[6] 徐胜,黄顺荣.无结扎技术在胃癌外科的应用进展[J].中国临床新医学,2012,5(5):467-470
[7] 黄顺荣,徐胜,冯泽荣,等.LigaSure 在腹腔镜胃癌根治术中的应用[J].中国微创外科杂志,2008,8(12):1076-1078.
[8] 徐胜,麦威,黄顺荣.无结扎技术在胃癌根治术中的应用探讨[J].实用医学杂志,2013,29(13):2172-2174.
[9] 黄前堂.胃癌D2根治术中医源性胰腺损伤的防治对策[J].临床误诊误治,2013,26(6):74-75.
[10] 顾玮,胡梅洁.胃癌免疫治疗研究进展[J].上海交通大学学报,2009,29(5):594-597.
[11] 陈香梅,李金运,刘太锋,等.甲地孕酮联合DCF方案化疗对进展期胃癌患者生活质量的影响[J].中国医药,2013,8(9):1259-1261.
(收稿日期:2014-10-28 本文编辑:任 念)
