微粒作用观视角下“离子反应及其发生条件”教学设计*
2015-03-07张志杰
张志杰
(北京市通州区永乐店中学 北京 101105)
化学基本观念的研究和实践已成为当前中学化学教育研究的热点,成为中学化学教学的一个基本价值取向和实践追求。[1]要实施观念教学,其中最关键的是要对教材内容的本体知识有深入的理解,充分挖掘本体知识中所蕴含的化学观念,让具体的知识服务于观念建构,同时围绕观念建构采取行之有效的教学策略[2]。从教材内容的特点来看,“离子反应及其发生条件”是高中阶段初步构建和发展学生微粒观很好的素材,因此,本节课的教学设计不能只局限于讲授具体的化学知识,而应该体现知识的功能和价值,对教学内容应该整体把握并建构化学观念,促进学生的可持续发展。
一、“离子反应及其发生条件”的知识分析及其教学价值
“离子反应”是人教版高中化学必修(1)第二章“化学物质及其变化”的内容,这一节共分成三个课时:第一课时讲酸碱盐在水溶液中的电离;第二课时讲离子反应及其发生条件;第三课时是离子反应的具体应用。从整体单元教学的视角来看,本单元的研究对象是水溶液体系,其中第一课时研究的是单一电解质在水溶液中的行为,是从微观角度对物质的认识,而第二课时则是在此基础上进一步认识两种电解质混合后在水溶液中的行为,是从微观的角度对酸、碱、盐在水溶液中反应的认识。(见图1)。其中第二课时“离子反应及其发生条件”的主要内容包括:离子反应的实质、离子反应发生的条件、离子方程式的书写和离子反应的简单应用。通过本节课的学习,让学生从微观角度认识酸、碱、盐在水溶液中反应的实质,深化从微观角度认识和分析离子反应的思路和方法,并从宏观事实进入微观分析,形成高度概括的深层理解,逐渐建构和发展微粒作用观的内涵。下图表示“离子反应”一节的知识层级关系。(见图2)

图1 “离子反应”单元知识结构图

图2 “离子反应及其发生条件”的知识层级图
“离子反应及其发生的条件”的教学价值:首先离子反应的学习,发展了学生对酸、碱、盐水溶液中物质的存在状态和它们之间反应的再认识,使学生对溶液的认识从宏观进入微观,建立了从微观角度看溶液中化学反应的新视角[3],发展了学生的微粒作用观,运用微粒作用观的观点有助于学生从微观角度认识两种电解质在水溶液中的行为,分析电解质在水溶液中存在哪些离子,这些微粒之间存在哪些作用,它们之间如何转化,在转化过程中微粒的数量发生了什么变化,学会从溶液中微粒的来源、数量和微粒间的相互作用认识化学反应,深化了学生对化学反应的认识,建立起研究水溶液的新思路和新视角;此外,以“微粒作用观”作为“离子反应及其发生的条件”内容的基本思想和处理问题的价值取向,有助于学生对化学反应的深层次理解,并将具体知识中所蕴含的化学观念提炼出来,促进学生的可持续发展。
二、学生学习情况分析
在“离子反应”第一课时,学习了电解质与非电解质,能区分哪些物质是电解质,哪些物质是非电解质,已了解电解质在溶液中能发生电离,以离子形式存在于溶液中,会书写简单的电离方程式。对于酸碱盐在水溶液中的反应,学生的前知识是复分解反应,知道复分解反应的条件是生成沉淀、气体和水,这是对水溶液中复分解反应的宏观认识,但是,学生对电解质在水溶液中的存在状态及行为还缺乏足够的理解和认识,对水溶液中物质的认识还没有深入到微观这一层面,对复分解反应的微观实质还不太清楚,不能从微观的角度分析离子的存在以及离子之间的相互作用,欠缺研究微观问题的方法和思路。为此,在“离子反应及其发生条件”的教学中,很重要的一点就是促进学生认识角度的转变,从微粒作用观的角度剖析复分解反应的实质,从微粒的存在到离子之间的相互作用再到离子之间相互作用的结果,深刻理解水溶液中物质反应的微观实质,建立研究水溶液中物质反应的新思路和新视角。
三、促进观念建构的教学设计
1.教学整体思路
按照“离子反应”单元整体教学的设计,本单元的研究对象是水溶液体系,其中第一课时研究单一电解质在水溶液中的行为,第二课时“离子反应及其发生条件”研究两种电解质混合后在水溶液中的行为,从蕴含的化学观念而言,确定微粒观为本单元的观念教学目标,其中第二课时是从微观的角度对溶液中反应的研究,进而确定微粒作用观为本节课的观念目标,并以微粒作用观为统领构建教学内容,围绕“电解质在水中能电离出自由移动的离子复分解反应的实质是离子反应离子反应是有条件离子反应可用离子方程式表示 ”四个环节展开教学(见表1)。在具体的教学过程中,以化学实验为支持,并通过一系列核心问题和学生活动将教学活动串联起来,从微粒作用观的角度出发设置启发性问题,从而实现学生对复分解反应的深层次理解。
2.关键教学环节
环节一:再认识单一电解质在水溶液中的行为,关注微粒的来源和种类。

表1 教学整体思路
[演示实验]演示CuSO4溶液、BaCl2溶液的导电性实验。
[问题]请从微观角度分析以上溶液导电的原因?如果把两种物质的水溶液相互混合,溶液中的离子之间会有何影响?
设计意图:通过导电性实验,将微观问题宏观化,借助溶液的导电性引导学生进一步巩固单一电解质在水溶液中的行为,关注电解质溶液中微粒的来源和种类,使学生的认识角度从物质到离子再到离子之间的相互反应。
环节二:分析溶液中微粒间的相互作用,探讨复分解反应的微观实质。
[学生实验]
(1) 向 2mL 1mol·L-1的 CuSO4溶液中加入等体积 1mol·L-1的 BaCl2溶液,观察现象。取反应后的上层清液置于两只试管中,向一只试管中加少量硝酸银,有何现象 ? 向另一只试管中加少量氢氧化钠,又有何现象?
[问题]通过以上实验,你认为是不是所有离子都参加了反应?反应后离子数量发生了什么变化?你认为复分解反应的实质是什么?
设计意图:通过实验手段,借助宏观实验现象,让学生认识复分解反应的微观实质。在实验(1)中,学生观察到反应生成了白色沉淀,由此可以判断和Ba2+反应生成了BaSO4沉淀,溶液的颜色仍为蓝色,说明Cu2+并没有参加反应。在第二步实验中,加少量硝酸银也观察到有白色沉淀产生,该沉淀为AgCl,该实验证明了硫酸铜和氯化钡发生反应的时候Cl-并没有参加反应;同样在第三步反应中,加少量氢氧化钠生成了蓝色的氢氧化铜沉淀也进一步证明了Cu2+也没有参加反应。通过一系列宏观实验可以证明:CuSO4和BaCl2溶液之间的反应其实质是和Ba2+之间的反应,而Cl-和Cu2+并没有参加反应。该环节从微观层面分析了两种电解质混合后的行为,让学生感受到复分解反应其实质就是离子之间的反应,而在发生反应时并不是所有的离子都参与反应,然后归纳出离子反应的概念,通过和Ba2+之间反应也让学生意识到电解质溶液中微粒之间存在着相互作用,作用过程是通过微粒的解离和再结合完成的,微粒间发生化学反应的实质是强的相互作用代替弱的相互作用,相互作用的结果会导致微粒种类、数量和溶液性质的变化。此外,通过探究两种电解质溶液混合时离子数目的变化,使学生对反应的认识由定性到定量,从宏观到微观,从而更深刻的理解离子反应的实质,提升了学生的思维深度。
环节三:从微粒间相互作用的结果归纳离子反应发生的条件。
[学生实验]
(2)向 2mL 1mol·L-1盐酸溶液中加几滴石蕊,再加入1mol·L-1碳酸钠溶液使其恰好完全反应,观察现象;
(3)向滴有酚酞的 2mL 1mol·L-1氢氧化钠溶液中滴加等体积1mol·L-1的硫酸使其恰好完全反应,观察现象。
[问题]根据以上三个反应的宏观现象和微观实质,你认为离子反应发生的条件是什么?
[总结]酸、碱、盐之间发生离子反应的条件:
微观角度:离子数量减少
宏观角度:生成沉淀、气体和水
[问题]根据离子反应发生的条件,你认为那些物质在水溶液中以离子形式存在?哪些以分子形式存在?
[总结]沉淀、气体、水在水溶液中以分子形式存在,钠盐、钾盐等可溶盐以离子形式存在。
设计意图:从微观的角度理解离子反应发生的条件,即离子之间相互作用的结果是是反应向着生成沉淀、气体、水等离子浓度减小的方向移动。第二个问题的设计意图是从复分解反发生的条件再看单一电解质在水溶液中的行为,深刻理解微粒间的相互作用及其结果是物质在水溶液中存在形式和离子反应发生条件的微观实质。
环节四:用化学用语表征离子之间的相互作用及其结果。
[问题]根据复分解反应的实质,如何用化学用语来表达CuSO4和BaCl2溶液之间的反应?
[学生活动]基于对反应(1)的分析,小组讨论,汇报交流如何用化学用语来表达 CuSO4和BaCl2溶液之间的反应。[教师引导]在师生互动中总结出书写离子方程式的一般方法:
书写电离方程式(微粒的来源):
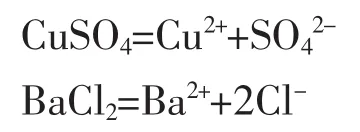
找出参加反应的离子(微粒间的相互作用)
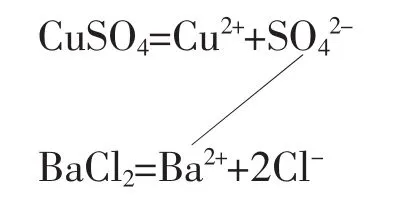
书写离子方程式(微粒间相互作用的结果)
检查离子方程式:质量守恒、电荷守恒。
[学生活动]根据以上书写规则,完成盐酸和碳酸钠溶液、氢氧化钠和硫酸反应的离子方程式。
[问题]你认为H++OH-=H2O除可以表示氢氧化钠和硫酸溶液之间的反应外,还可以表示哪些物质之间的反应?你认为能表示硫酸和氢氧化钡之间的反应吗?
设计意图:通过归纳总结,从微粒的来源和微粒间相互作用及其结果的角度梳理书写离子方程式的一般方法和分析水溶液中离子反应的一般思路,并借助离子反应来表示酸、碱、盐在水溶液中的反应实质。此外,用硫酸替代盐酸和氢氧化钠的反应,进一步培养学生“量”的意识。对于H++OH-=H2O还可以表示哪些离子反应,其设计意图是让学生进一步认识离子反应的本质,一个离子反应不仅可以表示一个反应还可以表示一类反应,让学生养成见到物质会想到它在水溶液中的存在形式,见到离子会想到哪些物质含有这些离子的思维习惯,进一步构建和发展了学生的微粒观。该离子反应能否表示硫酸和氢氧化钡的反应?其目的是让学生从微粒的来源、微粒间的相互作用及其结果进行判断,并通过该离子方程式的书写,进一步巩固学生对离子反应的定量认识,从而更深刻的理解离子反应的实质,提升了学生的思维深度。
环节五:归纳小结。
[问题]通过本节课的学习,你对溶液中的复分解反应有哪些新的认识?你认为分析离子反应的思路是什么?
设计意图:通过学生的归纳总结,再次强化了学生从微观角度对复分解反应的深层理解,形成从微粒的来源、微粒间的相互作用及其结果去分析溶液中离子反应的基本思路和方法。
总之,实施促进化学观念的教学是为了学生的可持续发展,以化学观念统领的课堂教学,更有助于学生对知识的深层次理解,当然要实现从从“知识为本”到“观念构建”,必须要充分挖掘具体知识所蕴含的化学观念,让具体的知识服务于观念建构,重视化学实验提供的感性认识,在围绕观念建构问题的驱动下,引导学生经历知识的形成、应用和反思,不断发展对化学观念的认识。[2]
[感谢王钦忠老师、何彩霞老师在课题研究和论文写作过程中的悉心指导。]
[1] 毕华林,万延岚.化学基本观念:内涵分析与教学建构[J].课程·教材·教法,2014,(4) :76-77
[2] 何彩霞.以化学观念为统领设计教学活动[J].化学教育,2013,34(1):16-18
[3] 何彩霞,张琦,王钦忠.促进学生认识角度转变的化学教学[J].教学仪器与实验,2014,30(1) :7-10
