半胱氨酸抑制二氧化铈纳米颗粒化学发光
2015-03-07石文兵戚景南万邦江
石文兵,戚景南,贺 薇,万邦江
(1.无机特种功能材料重庆市重点实验室,长江师范学院化学化工学院,重庆 408100;2.唐山科技职业技术学院,唐山 063001)
半胱氨酸抑制二氧化铈纳米颗粒化学发光
石文兵1,戚景南2,贺 薇1,万邦江1
(1.无机特种功能材料重庆市重点实验室,长江师范学院化学化工学院,重庆 408100;2.唐山科技职业技术学院,唐山 063001)
在碱性条件下,二氧化铈纳米颗粒能够有效催化过氧化氢-鲁米诺体系的化学发光。然而,当加入半胱氨酸,该体系的化学发光强度得到极大抑制。该文详细讨论发光条件,如二氧化铈纳米颗粒、过氧化氢、鲁米诺等质量浓度及鲁米诺pH对发光强度的影响。在最佳试验条件下,探讨半胱氨酸的抑制特性,在一定范围内抑制强度与半胱氨酸的质量浓度成正比。线性范围为0.01~1.8μg/mL,(r=0.994 6),检出限(3σ)为1.6ng/mL,对质量浓度为1.0μg/mL的半胱氨酸进行11次平行测定,RSD为0.72%。该法有望用于测定实际样品中半胱氨酸的含量。
半光氨酸;抑制;二氧化铈纳米颗粒;化学发光
0 引 言
L-半胱氨酸属于蛋白质氨基酸,在临床医学和医药产业中发挥着重要的生物学作用。L-半胱氨酸参与多种重要的细胞功能,如蛋白质合成、解毒和新陈代谢等;因此,灵敏、快速和廉价检测半胱氨酸的含量具有重要意义。近几年,越来越多的方法已用于测定药物、尿液、血清和血浆中L-半胱氨酸含量,如高效液相色谱法(HPLC)[1-2]、分光光度法[3-4]、固相微萃取[5]、比色法[6-7]、电化学法[8]、荧光法[9]。 虽然这些方法大多数具有灵敏度高和选择性好的优点,但它们要么仪器昂贵,要么步骤繁复耗时。化学发光法(LC)因其灵敏度高、线性范围宽、仪器设备便宜简单、容易实现自动化,广泛应用于不同领域。由于传统的化学发光体系发光强度较弱,因此利用一些新兴材料来提高化学发光法的灵敏度是近年来的研究热点。
功能纳米材料在化学催化、分子识别、生化标记等领域具有诱人的应用前景[10-11],但多数纳米粒子的水溶性不好,传统的发光体系研究都集中在分子水平。近年来,纳米粒子催化液相化学发光得到了蓬勃发展[12-13]。然而,制备具有水溶性好、催化效率高的纳米材料仍是该领域的研究热点和难题。本文合成了一种水溶性好、化学发光催化效率高的二氧化铈纳米颗粒,并根据半胱氨酸能够有效抑制二氧化铈纳米颗粒-H2O2-鲁米诺发光体系,详细研究了各种发光条件,得出了体系对半胱氨酸的响应特性,该体系有望用于半胱氨酸的实际样品分析。
1 实验部分
1.1 仪器与试剂
发光信号用RFL-1型超微弱化学发光/生物发光检测仪(西安瑞迈电子科技有限公司)检测;利用蠕动泵(15r/min,30 r/min,上海仪表电机厂)泵送溶液;流动注射系统各部件利用聚四氟乙烯管(内径0.8 mm)连接;二氧化铈纳米颗粒的浓度利用TPS-7000型ICP单道扫描光谱仪(北京谱析通用仪器有限责任公司)测定;二氧化铈纳米颗粒的红外光谱用Tensor27型红外光谱仪(BRUKER公司,德国)测定;85-2型恒温磁力搅拌器(上海司乐仪器有限公司)用于合成二氧化铈纳米颗粒时磁力搅拌;800型离心沉淀器(上海手术机械厂)用于离心二氧化铈纳米颗粒。
鲁米诺储备液:准确称取1.772 g鲁米诺,用1.0 mmol/L NaOH溶解并定容至 1 000 mL,即得0.01 mol/L储备液,需用时取适量用0.8 mol/L碳酸钠溶液稀释至所需浓度;过氧化氢溶液:用水稀释30%过氧化氢(重庆东方试剂厂)至所需浓度;二氧化铈纳米颗粒(CeO2NPs):其合成和表征参照前期工作[14],需用时用水稀释2.633 g/L二氧化铈纳米颗粒储备液至所需浓度;六水硝酸铈购于国药集团化学试剂有限公司;浓氨水(30%)购自重庆川东化工集团有限公司试剂厂;聚丙烯酸(PAA)购自上海晶纯试剂有限公司;半胱氨酸购自国药集团化学试剂有限公司。其他试剂均为分析纯,实验用水为去离子超纯水。
1.2 实验方法
化学发光的测定:如图1所示,超纯水作为载流将半胱氨酸带入三通(T)点与鲁米诺-H2O2-二氧化铈纳米颗粒溶液汇合,混合后进入反应盘管进而抑制化学发光,实验参数由IFFM-D型流动注射分析仪设定。
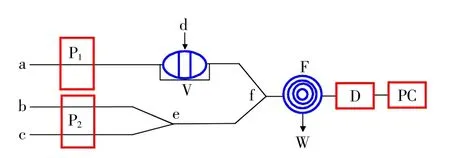
图1 半胱氨酸抑制化学发光流动注射示意图
2 结果与讨论
2.1 二氧化铈纳米颗粒对制备与表征
二氧化铈纳米颗粒的合成和表征参照前期工作完成[14],由于其粒径极小,反衬度不高,不适合利用TEM来表征,动态光散射的表征结果见图2,二氧化铈纳米颗粒的水合粒子半径为2.6~4.2nm。

图2 二氧化铈纳米颗粒的动态光散射图
2.2 二氧化铈纳米颗粒对发光体系的增敏作用
为证明纳米颗粒对发光强度的影响,考察了加入CeO2NPs前后H2O2-鲁米诺发光体系的发光强度变化情况,试验结果如图3所示,当有CeO2NPs存在时,H2O2-鲁米诺体系的发光强度得到极大增强(见图3中的1)。为验证该增敏效果非游离的Ce3+所致,用0.5mol/L的盐酸将CeO2NPs沉淀下来,于15000r/min转速离心后,用Na2CO3将离心液调至中性,再将其作为催化剂,于相同的实验条件(与未处理的CeO2NPs溶液相同)下测定其催化效果。试验结果表明(见图3中的2),滤液的催化效果与CeO2NPs相比,其增强的发光信号可忽略不记,说明催化效果来源于CeO2NPs。
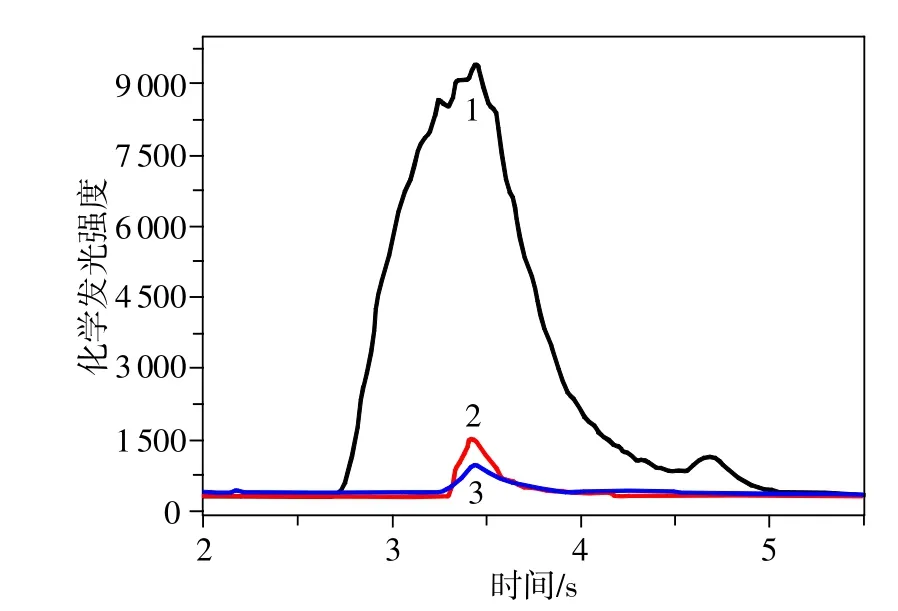
图3 二氧化铈纳米颗粒对H2O2-鲁米诺发光体系的影响
2.3 半胱氨酸对发光体系的抑制作用
为考察半胱氨酸对该发光体系的影响,选择3个半胱氨酸质量浓度0.1,1.0,10μg/mL,实验结果表明(见图4),半胱氨酸能够有效抑制该发光体系,而且随着半胱氨酸质量浓度的增高,化学发光强度逐渐降低,当半胱氨酸质量浓度降低到0.1 μg/mL时,仍有显著的抑制效果,这使得该法在检测半胱氨酸是可获得较高的灵敏度。
2.4 其他发光条件对发光强度的影响
鲁米诺与过氧化氢的质量浓度、二氧化铈纳米颗粒和鲁米诺中的pH对该体系的影响尤为显著,详细考察了这些条件对发光强度的影响。在鲁米诺为1.0×10-6~5.0×10-4mol/L范围内,发光强度随其物质量浓度的增加而增强,当达到1.0×10-5mol/L时,发光强度骤降,故选择鲁米诺的最佳物质量浓度为1.0× 10-5mol/L。当H2O2物质量浓度小于1.0×10-4mol/L时,发光强度随其升高而升高,然而当H2O2物质量浓度超过该值时化学发光信号反而降低,故本实验选择H2O2最佳物质量浓度为1.0×10-4mol/L。二氧化铈纳米颗粒为本实验的催化剂,其用量直接影响着发光强度。考察了5.3~1316.5μg/mL范围内二氧化铈纳米颗粒对发光强度的影响,实验发现,当其质量浓度为132μg/mL时发光信号达最大值,故本实验选择该值为最佳质量浓度。考察鲁米诺溶液中的pH对发光强度的影响,包括氢氧化钠、碳酸钠及碳酸氢钠缓冲溶液以及单独的碳酸钠对发光强度的影响。实验发现,单独的碳酸钠溶液更有利于该体系的发光,而且当碳酸钠为1.0mol/L(pH 11.73)时体系的发光强度最强。其他实验参数对发光强度也具有一定的影响,如流量太小峰型很宽,影响测试效率,太大则发光信号会降低,当流速为3.6mL/min时,既有较好的信号强度又有较快的分析速度,故选择3.6mL/min作为最佳流量。温度发光信号也有一定的影响,温度越高发光强度越高,但是在室温(25℃)时,发光信号就达到分析要求,为了简化操作程序,选择室温为分析温度。另外,进样体积为150μL,混合管与三通管之间的管长为7.5cm,负高压为-650V,增益为×2时,体系具有最佳的信号轻度。
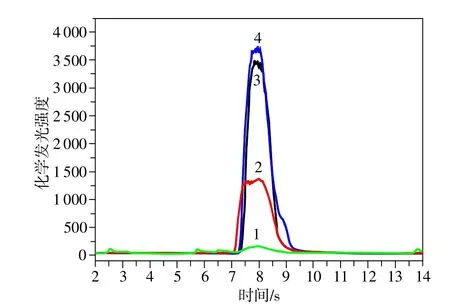
图4 半胱氨酸对二氧化铈纳米颗粒-过氧化氢-鲁米诺发光体系的影响 (1.0×10-5mol/L鲁米诺;1.0×10-4mol/LH2O2)
2.5 发光体系对半胱氨酸的响应特性
在上述优化试验条件下,在0.01~1.8μg/mL范围内半胱氨酸质量浓度与化学发光强度呈良好的线性关系,lgΔI=0.532 97lgc+3.779 23(r=0.9946)(n=9)(ΔI为化学发光强度,c为半胱氨酸质量浓度(μg/mL),r为相关系数)。根据IUPAC的建议算出的检出限(3σ)为1.6 ng/mL,对1.0 μg/mL的半胱氨酸平行测定11次,得RSD为0.72%。
2.6 化学发光机理探讨
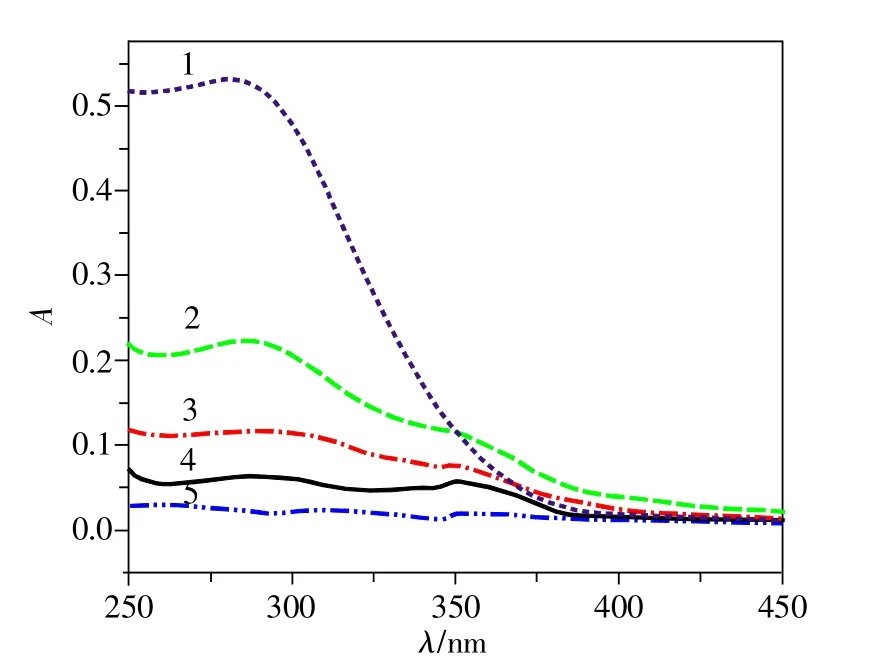
图5 化学发光体系的紫外吸收光谱
为探讨二氧化铈纳米颗粒对鲁米诺-H2O2体系增强作用的反应机理,采用紫外-可见吸收光谱进行研究,实验发现,鲁米诺-H2O2体系在298,358nm处有两个吸收峰(图5曲线4);发现二氧化铈纳米颗粒在299nm处有1个吸收峰(图5曲线1);二氧化铈纳米颗粒-鲁米诺-H2O2体系在298,358nm处有2个特征吸收峰,二氧化铈纳米颗粒的特征吸收峰消失是因为其吸收峰在298nm处与鲁米诺-H2O2体系的吸收峰重叠,故它们的吸收峰位置并没有改变(图5曲线2),也没有新峰生成,说明将二氧化铈纳米颗粒加入鲁米诺-H2O2体系后,没有生成新的物质,可以推断二氧化铈纳米颗粒在鲁米诺-H2O2体系中仅起到催化作用。半胱氨酸的吸收(图5曲线5)可以忽略不计,但将半胱氨酸加入二氧化铈纳米颗粒-鲁米诺-H2O2体系后,在298,358nm的吸收峰明显降低(图5曲线3),说明半胱氨酸明显抑制了二氧化铈纳米颗粒催化鲁米诺-H2O2体系产生的中间产物,从而起到抑制发光的作用。
3 结束语
本文采用二氧化铈纳米颗粒作为催化剂催化H2O2-鲁米诺发光体系可获得很强的化学发光强度。当加入半胱氨酸后该发光体系的发光强度得到极大抑制。基于此,我们优化了各种发光条件,在优化的实验条件下,根据抑制的发光强度与半胱氨酸浓度呈良好的线性关系构建了测定半胱氨酸的方法。
[1]Chwatko G,Kuzniak E,Kubalczyk P,et al.Determination of cysteine and glutathione in cucumber leaves by HPLC with UV detection[J].Analytical Methods,2014,6(19):8039-8044.
[2]Yoshitake M,Nohta H,Sejima N,et al.Selective determination of cysteines through precolumn double-labeling and liquid chromatography followed by detection of intramolecular FRET[J].Analytical and Bioanalytical Chemistry,2011,399(4):1665-1675.
[3]Montaseri H,Yousefinejad S.Design of an optical sensor forthe determination ofcysteine based on the spectrophotometric method in a triacetylcellulose film:PC-ANN application[J].Analytical Methods,2014,6(21):8482-8487.
[4]Khajehsharifi H,Shenini A.A selective naked-eye detection and determination of cysteine using an indicator-displacement assay in urine sample[J].Sensors and Actuators B-Chemical,2014(199):457-462.
[5]Liu X C,Zhu Y C,Zhu Z Q,et al.Solid phase microextraction and selective determination of cysteine in whole blood by cyclic voltammetry with silver nanoparticles modified clustered carbon fiber electrodes[J]. Analytical Methods,2012,4(10):3256-3260.
[6]Farhadi K,Forough M,Pourhossein A,et al.Highly sensitive and selective colorimetric probe for determination of L-cysteine in aqueous media based on Ag/Pd bimetallic nanoparticles[J].Sensors and Actuators BChemical,2014(202):993-1001.
[7]Wei X Y,Qi L,Tan J J,et al.A colorimetric sensor fordetermination ofcysteine by carboxymethylcellu lose-functionalized gold nanoparticles[J].Analytica Chimica Acta,2010,671(1-2):80-84.
[8]Nezamzadeh-ejhieh A,Hashemi H S.Voltammetric determination of cysteine using carbon paste electrode mo dified with Co(II)-Y zeolite[J].Talanta,2012(88):201-208.
[9]Chen S,Fan Y,Yang Y,et al.Determination of cysteine based on fluorescence enhancement of CdS quantum dots with Cd2+rich surface[J].Chinese Journal of Analytical Chemistry,2012,40(1):173-176.
[10]Chen S,Hai X,Chen X W,et al.In situ growth of silver nanoparticles on graphene quantum dots for ultrasensitive colorimetric detection of H2O2and glucose[J]. Analytical Chemistry,2014,86(13):6689-6694.
[11]Abdukayum A,Yang C X,Zhao Q,et al.Gadolinium complexes functionalized persistent luminescent nanoparticles as a multimodal probe for near-infrared luminescence and magnetic resonance imaging in vivo[J].Analytical Chemistry,2014,86(9):4096-4101.
[12]Iranifam M.Analytical applications of chemiluminescence-detection systems assisted by magnetic micropar ticles and nanoparticles[J].Trac-Trends in Analytical Chemistry,2013(51):51-70.
[13]He Y,He X,Liu X Y,et al.Dynamically tunable chemiluminescence of luminol-functionalized silver nanoparticles and Its application to protein sensing arrays[J].Analytical Chemistry,2014,86(24):12166-12171.
[14]石文兵,刘希东,张小丹,等.二氧化铈纳米微粒过氧化物酶活性及其在葡萄糖检测中的应用[J].中国科学:化学,2014,44(10):1633-1640.
The chemiluminescence inhibition of cysteine on ceria nanoparticles
SHI Wenbing1,QI Jingnan2,HE Wei1,WAN Bangjiang1
(1.Chongqing Key Laboratory of Inorganic Special Functional Materials,College of Chemistry and Chemical Engineering,Yangtze Normal University,Chongqing 408100,China;2.Tangshan Vocational College of Science and Technology,Tangshan 063001,China)
In basic conditions,the luminol-H2O2chemiluminescence system can be effectively catalyzed by ceria nanoparticles,however,the chemiluminescence intensity wastremendously inhibited when the cysteine was added into this system.In this paper,the effects of the chemiluminescence conditions such as ceria nanoparticles concentration,luminuol concentration,H2O2concentration and the pH in luminol solution were investigated in detail.Under optimal conditions,the inhibition properties of cysteine have been investigated,in certain concentration range,the inhibition intensities were proportional to the concentrations of cysteine.The linear range was 0.01-1.8μg/mL(r=0.994 6),and the detection limit(3σ)was 1.6 ng/mL.The relative standard deviation(RSD)was 0.72%for 1.0μg/mL cysteine(n=11).The method can be expected to used to determine cysteine in real samples.
cysteine;inhibition;ceria nanoparticles;chemiluminescence
A
:1674-5124(2015)07-0037-04
10.11857/j.issn.1674-5124.2015.07.009
2015-02-07;
:2015-03-24
国家自然科学基金项目(21275021)重庆市教委科学研究项目(KJ1401201,KJ1401220)
石文兵(1976-),男,湖南凤凰县人,副教授,博士,主要从事药物分析。
