杨木废弃物湿氧化预处理提高酶解效率的工艺研究
2015-03-05房桂干刘姗姗沈葵忠
房桂干 刘姗姗 沈葵忠
(1.中国林业科学研究院林产化学工业研究所,国家林业局林产化学工程重点开放性实验室,
生物质化学利用国家工程实验室,江苏省生物质能源与材料重点实验室,江苏南京,210042;
2.中国林业科学研究院林业新技术所,北京,100091;3. 齐鲁工业大学,山东济南,250353)
·杨木废弃物·
杨木废弃物湿氧化预处理提高酶解效率的工艺研究
房桂干1, 2刘姗姗3沈葵忠1, 2
(1.中国林业科学研究院林产化学工业研究所,国家林业局林产化学工程重点开放性实验室,
生物质化学利用国家工程实验室,江苏省生物质能源与材料重点实验室,江苏南京,210042;
2.中国林业科学研究院林业新技术所,北京,100091;3. 齐鲁工业大学,山东济南,250353)
摘要:对杨木废弃物制生物燃料的湿氧化预处理条件进行优化实验。研究表明,湿氧化预处理杨木废弃物的最佳工艺为:初始pH值10,温度195℃,最佳保温时间15 min,氧压1.2 MPa。所得物料得率为51.7%。酶解优化工艺条件为:酶解温度49℃,酶解时间56 h,酶用量38 FPU/g。其他条件为:pH值4.8,固液比1∶50,酶解纤维素转化率为96.4%。湿氧化预处理过程使原料中的半纤维素含量由18.7%降到1.43%,Klasson木素含量由23.6%降到13.5%;木素溶出率为43%,半纤维素溶出率为 92%。X射线衍射分析显示原料的结晶度从57.4%降到了54.8%;扫描电镜显示湿氧化预处理后纤维的细纤维化程度增强;高效液相色谱显示预处理分离液中木糖含量较高,并含有单糖降解产物如乙酸、甲酸和糠醛等单糖降解产物。湿氧化预处理可以较大幅度地降解或脱除原料中的木素和半纤维素,改变原料的结晶结构,增加了可酶解性,提高了物料中纤维素转化率。
关键词:杨木废弃物;湿氧化预处理;预处理条件;可酶解性
Pretreatment of Poplar Wood Residues Using Wet Oxidation to Enhance Enzymatic Digestibility
由木质纤维素生物质生产生物液化燃油或生物乙醇,是当今世界生物质高值化利用的主要途径。开发经济高效的木质纤维素类生物质预处理技术,是这一利用过程中的重点和难点,预处理的目标是打破纤维素的致密结构以及木素和半纤维素对纤维素的包裹,破坏纤维素的结晶结构,或使纤维素、半纤维素与木素相对分离,从而提高后续液化的适应性和催化效率,或酶解剂对纤维素的可及度,使碳水化合物易于转变成可发酵糖。常用的生物质预处理技术一般可以分为物理法、化学法、物理化学法和生物法或其组合方法。本实验探讨的湿氧化预处理技术,属于物理化学法预处理技术范畴。湿氧化法[1-2]是通过加热、高压、碱性环境、水和氧气的共同作用处理纤维原料,降解木素和半纤维素,膨化纤维素,有利于提高水解效率或增加生物质液化的适应性。通常采用Na2CO3等弱碱性化学品来调节湿氧化预处理分离液的pH值呈碱性,在这种环境中可以防止纤维素的降解,还可以限制产生糠醛等副产物。有研究表明[3],在预处理温度195℃、预处理时间15 min、Na2CO3含量2 g/L、氧压1.2 MPa的条件下,对浓度为60 g/L的麦草进行预处理,可以较大程度地提高纤维素酶解率。而且与其他预处理方法相比,湿氧化预处理过程中产生的糠醛、羟甲基糠醛及乙酸等抑制酶活性的物质较少,因此有利于后续的生化处理[4]。但是在湿氧化预处理过程中,高温高压导致了投资和成本较高。本研究重点对杨木废弃物湿氧化预处理条件进行优化,为开发生物乙醇或生物质液化油工业生产技术提供参考。
1实验
1.1实验原料
杨木废弃物(以下统称原料)取自山东晨鸣纸业P-RC APMP制浆生产线备料工段,含木屑、木节和木针,不含树皮。风干后密封保存,按相应的国家标准分析原料的化学成分含量为: 水分9.63%,硝酸乙醇纤维素44.8%,聚戊糖18.7%,Klasson木素23.6%,灰分2.63%,苯-醇抽出物1.10%。
纤维素酶L-10(青岛康地恩生物集团); 氧气(工业级); Na2CO3, 固体、 H2SO4, 配制成质量分数为36.5%的H2SO4溶液、 3, 5-二硝基水杨酸、 酒石酸钾钠、 无水亚硫酸钠、 苯酚、 葡萄糖,以上均为分析纯。
1.2实验方法
1.2.1实验设计
湿氧化预处理禾本科原料的研究表明[3,5-6],影响湿氧化预处理效果的主要因素为初始pH值、温度、保温时间和氧压。本实验设计也选择这4个因素对原料进行单因素预处理实验,各因素的变化范围为:①初始pH值为3~10;②保温时间为5~30 min;③氧压为0.4~1.2 MPa;④温度为165~205℃。
1.2.2湿氧化预处理
湿氧化预处理在6罐空气浴蒸煮器(型号6×3L,AG Brown机械公司,Australia)中进行。每罐加入60 g绝干原料,与1 L蒸馏水混合,用固体Na2CO3或质量分数为36.5%的H2SO4溶液调节初始pH值。混匀后装罐,通过盖顶进气口通氧,密封后放入蒸煮器中进行升温和保温处理。反应结束后取出钢罐,迅速用流水冷却至室温。开罐,过滤,分离固液,所得液体装瓶留样备测。所得固体(以下统称物料)洗净后放入聚乙烯袋中,密封、平衡和测定水分、备用。
1.2.3湿氧化预处理后物料的纤维素酶水解
在进行预处理单因素条件优化实验时,采用如下酶水解方法:将湿氧化预处理所得的物料用纤维素酶进行水解,首先称取2.00 g(绝干质量)物料放入容积为250 mL的锥形瓶中,加入纤维素酶溶液,纤维素酶用量35 FPU/g,固液比1∶50,用1 mol/L的乙酸-乙酸钠缓冲溶液调节pH值为4.8,酶解实验在恒温培养振荡器(ZH WY-200B型,上海智城分析仪器公司)中进行。水解时间72 h,反应完毕后经过滤分离酶解液和残渣,分别供后续测试分析使用。取酶解液,测定其还原糖含量,从而计算出还原糖得率(Reducing Sugar Yield,RSY),计算公式见式(1)。
(1)
式中,RSY为还原糖得率,%;m0为绝干原料质量,g;m为还原糖质量,g;V为水解液总体积,L;n为测定还原糖浓度时稀释的倍数;c为还原糖浓度,g/L。
1.2.4还原糖含量的测定
酶解液中的还原糖含量采用Miller G. L介绍的DNS法测定.[7]。主要包括DNS的配置,葡萄糖标准溶液的配制,显色实验,还原糖含量的计算见公式(2)。吸光度测定使用紫外分光光度计(T6新世纪,北京普析通用仪器公司)。
测量液体中的还原糖浓度时,将液体稀释一定的倍数,取0.5 mL放入25.0 mL带刻度的具塞试管中,加入0.5 mL蒸馏水,并加入DNS试剂3.0 mL,于沸水浴中进行显色反应,用紫外分光光度计在波长550 nm处测量其吸光度。同时用0.5 mL蒸馏水做相应的显色实验,作为空白调零点。根据液体在550 nm处的吸光度计算待测液的还原糖浓度,计算公式见式(2)。
(2)
式中,c为还原糖浓度,g/L;A为液体显色后在波长550 nm处的吸光度;n为液体稀释的倍数;0.0757和0.9744分别为本研究通过实验方法确定的葡萄糖标准曲线的截距和斜率。
1.2.5纤维素转化率的计算
用响应面实验设计对酶水解的工艺条件进行了优化,采用的因素和水平为:酶水解温度45℃、50℃和55℃,酶水解时间24 h、48 h和72 h,酶用量25 FPU/g、35 FPU/g和45 FPU/g,以纤维素转化率为考核指标,实验结果用设计软件Design Expert 7.1分析计算。采用DNS法测定其中的还原糖质量。按照式(3)计算纤维素转化率。
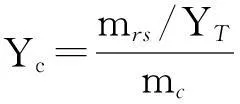
(3)
式中,Yc为纤维素转化率,%;mrs为预处理分离液的还原糖质量,g;YT为还原糖的理论产率,%;纤维水解得到葡萄糖时,YT=111.1%,半纤维素水解得到木糖时,YT=113.6%,计算时YT根据物料和水解液纤维素和半纤维素的比例进行取值;mc为物料中纤维素和半纤维素的质量,g;
1.2.6高效液相色谱(HPLC)测定糖及单糖降解产物
将待测液体稀释至一定的倍数,用带有0.45 μm孔径聚四氟乙烯微孔滤膜的注射过滤器进行过滤后,进行HPLC检测。测试条件为:采用Agilent 1100色谱仪,Aminex HPX-87H色谱柱进行分离,柱温63℃,流量0.6 mL/min,进样量10 μL,4 mmol/L的H2SO4作为流动相,示差折光检测器(RI)进行检测。根据各种单糖和单糖降解产物在HPLC图谱中的峰面积计算液体中各种单糖和单糖降解产物的浓度。
1.2.7纤维素酶活的测定
纤维素酶活按照Ghose T介绍的方法进行测试[8]。本实验所用纤维素酶活为149.73 FPU/mL。
1.2.8物料的分析
(1)化学成分分析:物料纤维素、半纤维素、Klasson木素、灰分和苯-醇抽出物的含量按相应的国家标准进行分析。
(2)X射线衍射(XRD)分析:物料首先采用梯度乙醇(乙醇质量分数30%、50%、70%、80%、90%)逐级脱水,每级脱水时间15 min,再用100%的乙醇脱水两次,每次15 min,然后再进行低温真空干燥和研磨。所得样品的结晶度用X射线衍射仪(D8-FOCUS,德国布鲁克公司)采用分峰法测定。利用Cu,Ka,Ni,λ=15.4×10-2nm,电压10 kV,测角仪的移动速度2°/min,固定时间3 s。结晶度计算由X光衍射图上002晶面产生的衍射强度与非结晶区背景的散射强度相除获得,见式(4)。在XRD衍射曲线上2θ=22°附近的极大峰值即为002晶面的衍射强度,在2θ=18°附近存在一个峰谷,为非结晶背景的散射强度。
(4)
式中,Icr为结晶度指数,%;I002为002晶面的最大衍射强度;Iam为非结晶背景衍射的散射强度。
(3)扫描电镜(SEM)分析:物料进行梯度乙醇逐级脱水后,由扫描电镜(S-3400,日本东芝公司)观察表面形貌并照相,加速电压15.2 kV。
1.2.9湿氧化预处理分离液的分析
湿氧化预处理后所得的液体部分稀释一定的倍数后,采用HPLC进行分析,测定其单糖组分及含量,以及单糖降解物的成分及含量。
2结果与讨论
2.1湿氧化预处理条件的优化
2.1.1初始pH值

图1 初始pH值对湿氧化预处理的影响
对湿氧化预处理的初始pH值进行了优化。实验条件为:温度195℃,保温时间15 min,氧压1.2 MPa,设定初始pH值的变化范围为3~10。实验结果显示(见图1),在酸性和碱性条件下,物料的得率较低;中性预处理条件的物料得率较高,初始pH值为7时,物料得率最高为52.0%,高于酸性和碱性条件。原料在酸性或碱性条件下的湿氧化预处理反应更加剧烈,溶出的物质较多,而在近中性条件原料的降解溶出较少。但从不同初始pH值条件下所得物料酶解还原糖得率可以看出,在酸性或碱性条件下物料的酶解还原糖得率较高。由图1可知,预处理初始pH值为3时,还原糖得率为42.0%;初始pH值为10时,还原糖得率为43.6%;而当初始pH值为7时,还原糖得率仅为38.4%。可能的原因是,在酸性或碱性环境下的湿氧化预处理可以更剧烈地破坏纤维结构,提高纤维素酶对物料的可及度,从而改善酶解效率,提高还原糖得率;而近中性条件下的湿氧化处理虽然也溶出了半纤维素和木素,但对物料的纤维素酶解可及度改善并不多。
2.1.2保温时间
固定初始pH值10,温度195℃,氧压1.2 MPa,保温时间的变化范围为5~30 min,对保温时间进行了优化,实验结果见图2。从图2可以看出,保温时间是影响湿氧化预处理的一个重要因素,对物料得率和还原糖得率的影响结果不相同,存在一个适宜的保温时间。随着保温时间的延长,物料得率呈逐渐降低的趋势,特别是在保温5~15 min内下降速度最快,然后趋于缓和。从物料得率来看,保温时间为15 min时物料得率为52.1%,进一步延长保温时间至30 min,物料得率降低为49.8%。从物料酶解还原糖得率来看,在保温时间5~15 min范围内还原糖得率迅速升高,进一步延长时间后还原糖得率增加趋缓;保温时间为5 min时还原糖得率为33.6%,延长保温时间到15 min时还原糖得率增加到39.0%,但延长保温时间到30 min时还原糖得率为40.3%,仅比15 min时的得率提高了1.3个百分点。综合考虑物料得率和物料酶解还原糖得率的变化规律,湿氧化预处理适宜的保温时间为15 min,此时有接近1/2的物质溶出,纤维的致密结构已经被破坏,物料的酶解率较高。
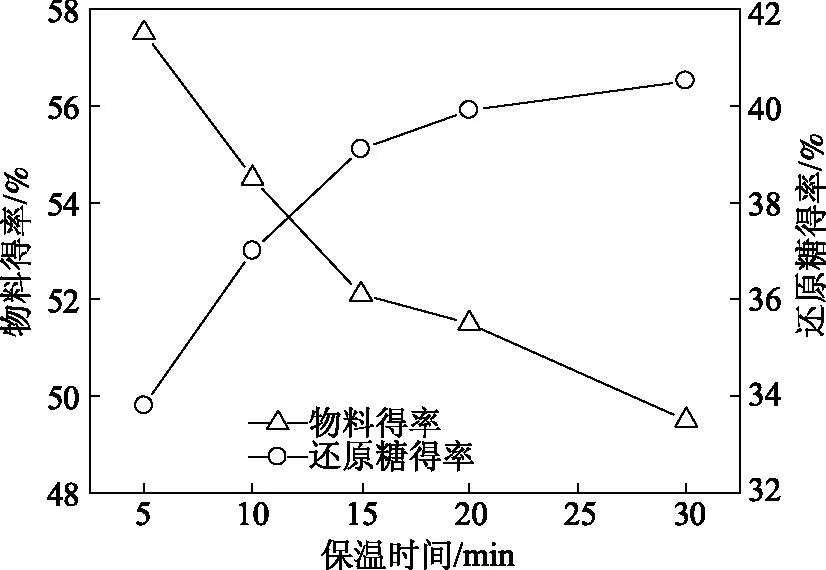
图2 保温时间对湿氧化预处理的影响
2.1.3氧压
氧气在碱性条件下可以产生较好的脱木素作用,但在一定碱度和较高的温度作用下,原料中半纤维素及部分纤维素也会发生较强的降解反应。本实验预处理条件选择为:固定初始pH值10、温度195℃、保温时间15 min,氧压变化范围为0.4~1.2 MPa,实验结果如图3所示。

图3 氧压对湿氧化预处理的影响
从图3可知,随着氧压在0.4~1.2 MPa范围内增加,物料得率几乎呈线性降低。氧压为0.4 MPa时物料得率为57.0%,升高氧压至0.8 MPa时物料得率降低为55.1%,进一步升高为1.2 MPa时物料得率降低为49.4%,较0.4 MPa时降低7.6个百分点。可以看出随着氧压的提高,湿氧化预处理的效果逐渐增强,原料中溶出的物质也逐渐增多。从物料的酶解还原糖得率来看,随着氧压的升高,得率也几乎呈线性升高趋势。氧压为0.4 MPa时还原糖得率为34.5%,升高氧压到0.8 MPa时还原糖得率为37.4%,进一步升高氧压到1.2 MPa时得率增至42.1%,较0.4 MPa时提高了7.6个百分点。这说明随着氧压的升高,溶出的物质增多,使得纤维的结构变得松散,增加了纤维素酶对物料的可及性,改善了酶解效率,提高了酶解还原糖的产率。
2.1.4温度
固定初始pH值10,保温时间15 min,氧压1.2 MPa,温度的变化范围为165~205℃,探讨了不同温度对湿氧化预处理的影响,实验结果如图4所示。
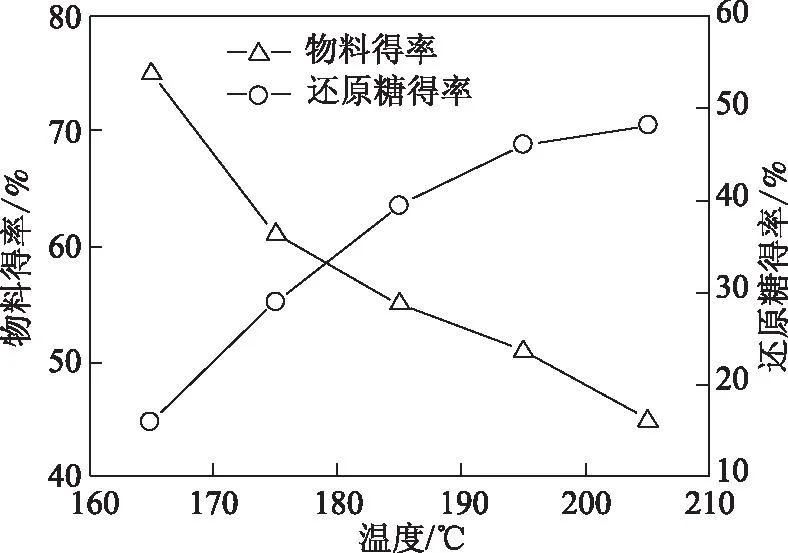
图4 温度对湿氧化预处理的影响
从图4可以看出,随着预处理温度的升高,物料得率迅速降低。在温度为165℃时物料得率为74.9%,升高温度到185℃时物料得率降低至54.9%,195℃时物料得率为51.7%,进一步升高温度到205℃时物料得率降低为42.7%,较165℃时降低了32.2个百分点,在温度由165℃升高到205℃时物料得率下降幅度较大。可以看出温度对物料得率有重要影响。较低温度时物质溶出量有限,当升高至较高温度后,原料中碳水化合物发生大量降解而溶出。从物料酶解的还原糖得率也可以看出,随着温度的升高,还原糖得率呈逐渐上升的趋势。预处理温度为165℃时还原糖得率为15.9%,升高温度至185℃时得率为39.1%,进一步升高温度到195℃时得率增加到46.8%,再继续升高温度还原糖得率增加幅度较小。经分析可以得出,随着温度的升高,纤维原料得到更好的破解,阻碍酶解反应的木素和半纤维素组分大量溶出,使得纤维素的酶解效率大幅升高,湿氧化预处理适宜的预处理温度为195℃。
依据单因素实验结果,较优的湿氧化预处理工艺条件为:初始pH值10,保温时间15 min,氧压1.2 MPa,温度195℃,此时物料得率为51.7%,还原糖得率为46.8%。
2.2湿氧化预处理后物料的分析
采用优化工艺条件对原料进行预处理,对预处理后物料的化学组成分进行分析,并采用XRD分析手段比较预处理前后结晶度的变化。
2.2.1组分分析
湿氧化预处理前后化学组分变化见表1。由表1数据可以发现,湿氧化预处理显著改变了原料化学组分所占的比例。预处理过程纤维素发生了一定程度的降解,经过预处理后由纤维素含量原来的44.3%降到32.7%。聚戊糖含量由原料的18.7%降到1.43%,约92%的半纤维素降解溶出,说明在湿氧化预处理过程中,原料中大部分半纤维素经过溶解除去,与文献[9]中的结论一致。从表1木素的含量可以看出,物料中的木素含量相当于原料中的13.5%,说明溶出了近43%的木素,还有相当一部分的木素保留在物料中。物料的灰分及苯-醇抽出物含量都有所降低。通过对预处理前后原料的化学成分分析可以得出结论:湿氧化预处理过程中,半纤维素成分大量溶出,并溶出了部分木素,这些化学组分的溶出,大大改善了物料酶解时物理空间阻隔效应,有利于纤维素酶解反应的顺利进行。

表1 原料湿氧化预处理前后化学组分变化 %
2.2.2XRD分析
为了研究经过湿氧化预处理后物料纤维结晶区的变化情况,采用XRD对原料和物料进行了分析,所得XRD图谱如图5所示。
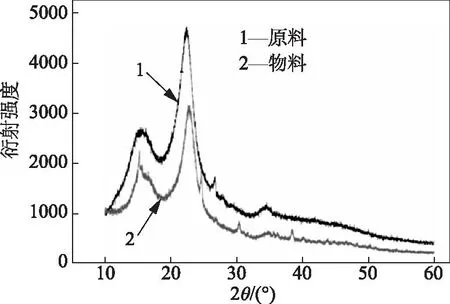
图5 原料和物料的XRD图谱
由图5可以看出,原料的XRD谱图呈现典型的纤维结构特征。使用式(3)对物料的结晶度指数进行计算,原料的结晶度为57.4%,物料的结晶度为54.8%,降低了2.7%,表明原料经过湿氧化预处理后结晶结构发生一定程度的改变,有利于增加纤维物料的酶与纤维素分子的接触程度,从而提高酶解反应效率。
2.3湿氧化预处理分离液的特征
对优化条件下得到的湿氧化预处理分离液进行了HPLC液相色谱分析,对预处理分离液中的糖组分和单糖降解成分进行了分析,结果如表2所示。
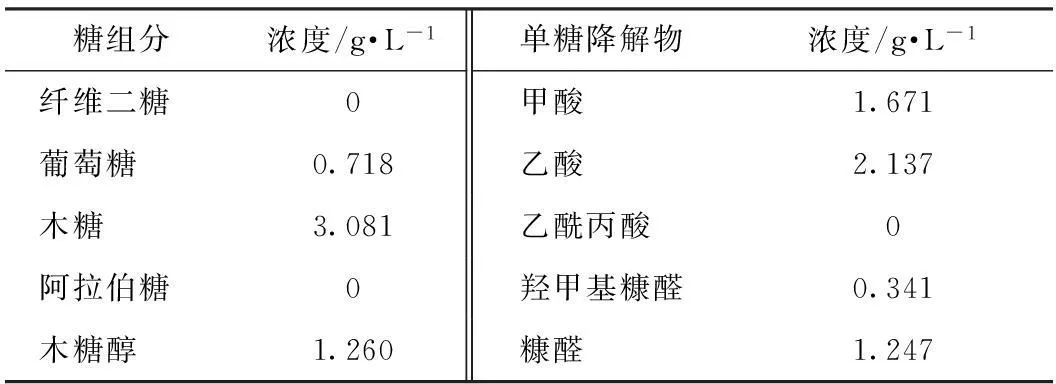
表2 湿氧化预处理分离液的HPLC谱分析
由表2可以看出,在湿氧化预处理分离液中,木糖含量最高,浓度为3.081 g/L,其次为木糖醇,浓度为1.260 g/L,两者均来自原料中戊糖组分,为葡萄糖含量的6.05倍;预处理分离液中基本不含纤维二糖和阿拉伯糖。在预处理分离液中的单糖降解物中,乙酸和糠醛降解物主要由木糖降解得到,来自原料中的戊糖组分;甲酸和羟甲基糠醛,主要由葡萄糖降解得到,来自原料中纤维素组分。表2结果表明,湿氧化预处理过程中半纤维素降解溶出较多,纤维素降解溶出较少,与表1中预处理前后原料化学组分分析结果一致。
2.4湿氧化预处理后物料的酶解反应
2.4.1酶水解工艺的优化


表3 酶水解响应面法实验设计方案及结果
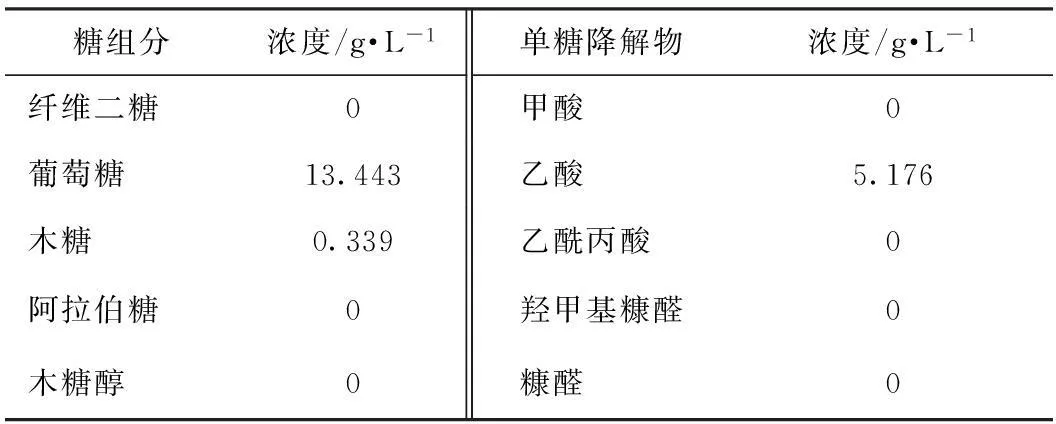
表4 纤维素酶水解液的HPLC分析
2.4.2物料酶水解液的特征
对优化酶水解条件下得到的纤维素酶水解液进行了HPLC分析,测定其单糖及单糖降解物的组分及含量,分析结果如表4所示。
由表4可以看出,纤维素酶水解液中只检测出了葡萄糖和木糖两种单糖组分,其中葡萄糖含量最多,浓度为13.443 g/L,占到了总糖量的97.54%,木糖含量较少,浓度仅为0.339 g/L。表明所采用的纤维素酶L-10的选择性很强,只针对纤维素进行有效地水解。单糖降解物中仅有乙酸这一种物质,而且含量较高,为5.176 g/L,从浓度上看,水解液中的乙酸不是由纤维素降解产生的,而是在调节水解液pH值时加入的乙酸-乙酸钠缓冲液引入的;酶水解液中未检出糠醛、羟甲基糠醛等抑制酶活性的物质。
2.4.3酶解前后SEM的形貌观察
采用SEM对酶水解前物料和酶解后残渣的表面形貌进行观察,如图6所示。由图6(a)可以看出,原料经湿氧化预处理后,物料的细纤维化程度明显增加,单根纤维或纤维束表面出现了大量的凹陷和裂痕,这在一定程度上可以增加物料的比表面积,有助于纤维素酶与物料的接触,改善酶解环境,从而提高酶解效率。物料与酶解后残渣的SEM照片进行比较可以看出,经过纤维素酶水解处理,纤维结构变化明显,纤维表面和内部出现了许多孔洞和缝隙,表明有较多的碳水化合物在水解中降解溶出(见图6(b))。
2.5讨论
Schmidt A. S.等人[3]在使用湿氧化预处理麦草原料时,30%的木素和60%的半纤维素降解溶出,原料的组织结构发生变化,其酶解转化率达到85%。本实验使用优化的湿氧化预处理条件,木素溶出43%,半纤维素溶出 92%,酶解转化率达到了96.4%。湿氧化预处理由于大部分的半纤维素组分及部分木素的溶出,增加了酶水解时酶与纤维素大分子的接触,提高了物料的酶解反应效率。但湿氧化预处理也造成了大约相当于原料中约26%纤维素组分的溶出,有待今后进一步优化,以降低预处理过程纤维素的损失。湿氧化预处理液中含有大量的半纤维素和部分纤维素溶出组分(见表2),对这部分糖组分的综合利用将有助于改善整个预处理工艺的经济性。

图6 物料和酶水解后残渣的SEM照片
杨木废弃物湿氧化预处理条件为:初始pH值10,保温时间15 min,氧压1.2 MPa,温度195℃,此时预处理物料得率为51.7%,所使用的预处理条件需要较高的温度和压力,这将导致较高的投资和使用成本,需要进一步探讨降低预处理温度的可能性,以便能够利用制浆工厂闲置的蒸煮设备,提高其工程适应性且降低投资成本。
3结论
3.1通过湿氧化预处理杨木废弃物,可以较高程度地溶出木素,降解半纤维素,从而提高预处理后物料的酶解性,得到较高的还原糖得率。湿氧化预处理杨木废弃物的最佳工艺条件为:初始pH值10,保温时间15 min,氧压1.2 MPa,温度195℃。在此条件下,物料得率为51.7%,还原糖得率为46.8%。
3.2在最佳工艺条件下得到的物料纤维含量为63.26%。原料经处理后木素溶出43%,半纤维素溶出 92%。湿氧化预处理过程中大部分半纤维素和部分木素被降解溶出,大大改善了物料酶解时物理空间阻隔效应。湿氧化预处理后物料结晶度由原料的57.4%降低到54.8%,且纤维细纤维化程度较明显。
3.3对杨木废弃物湿氧化预处理后物料采用响应面实验设计进行了酶水解工艺优化实验。酶解优化工艺条件为:酶解温度49℃,酶解时间56 h,酶用量38 FPU/g,其他条件为:pH值4.8,固液比1∶50,此时酶解转化率达到96.4%。湿氧化预处理方法在提高物料的酶解效率方面具有一定的优势。如果能够在提高物料得率、降低投资成本和生产成本等方面取得突破,湿氧化预处理工艺将具有一定产业化应用前景。
参考文献
[1]Homsen Annebet. Pretreatment of Corn Stover Using Wet Oxidation to Enhance Enzymatic Digestibility[J]. Applied Biochemistry And Biotechnology, 2003, 104: 37.
[2]Mart C, Klinke H B, Belinda A. Wet oxidation as a pretreatment method for enhancing the enzymatic convertibility of sugarcane bagasse[J]. Enzyme and Microbial Technology, 2007, 40: 426.
[3]Schmidt A S, Thomsen A B. Optimization of wet oxidation pretreatment of wheat straw[J]. Bioresource Technology, 1998, 64(2): 139.
[4]Chang J, Cheng W, Yin Q, et al. Effect of steam explosion and microbial fermentation on cellulose and lignin degradation of corn stover[J]. Bioresource Technology, 2012, 104: 587.
[5]Bjerre A B, Schmidt A S, Ris F. Development of chemical and biological processes for production of bioethanol: Optimization of the wet oxidation process and characterization of products[M]. Risø National Laboratory, 1997, 32.
[6]Varga E, Schmidt A S, Rczey K, et al. Pretreatment of corn stover using wet oxidation to enhance enzymatic digestibility[J]. Applied Biochemistry and Biotechnology, 2003, 104(1): 37.
[7]Miller G L. Use of dinitrophenyl acid reagent for the determination of reducing sugar[J]. Anal Chem., 1959, 31: 420.
[8]Ghose T. Measurement of cellulase activities[J]. Pure Appl. Chem., 1987, 59(2): 257.
[9]Zhu W, Zhu J, Gleisner R, et al. On energy consumption for size-reduction and yields from subsequent enzymatic saccharification of pretreated lodgepole pine[J]. Bioresource Technology, 2010, 101(8): 2782.
[10]LV Jian, ZHAN Huai-yu, FU Shi-yu. Optimization of enzymatic hydrolysis of bleached pulp by response surface methodology[J]. Transactions of China Pulp and Paper, 2010, 25(2): 16.

(责任编辑:常青)
推进林业生态建设加快发展林纸循环经济
FANG Gui-gan1,2,*LIU Shan-shan3SHEN Kui-zhong1,2
(1.InstituteofChemicalIndustryofForestryProducts,CAF;NationalEngineeringLabforBiomassChemicalUtilization;KeyLab
onForestChemicalEngineering,SFA,KeyLabofBiomassEnergyandMaterial,Nanjing,JiangsuProvince, 210042;
2.InstituteofNewTechnologyofForestry,CAF,Beijing,100091; 3.QiluUniversityofTechnology,Ji′nan,ShandongProvince, 250353)
(*E-mail: fangquigang@icifp.cn)
Abstract:Nowadays production of renewable fuels, especially boil-oil or bio-ethanol,is the main way for efficient utilization of lingo cellulosic biomass in the world. This paper carried out the study to optimize wet oxidation pretreatment conditions for utilizing poplar residues from the preparation sector of paper mill, to produce bioethanol. The research results showed that the optimal conditions of wet oxidation pretreatment for poplar residues were as follows: initial pH value 10, temperature 195℃, time at 195℃ 15 min, oxygen pressure 1.2 MPa. The yield of the obtained material of wet oxidation pretreatment was 51.7%. The optimal enzymatic hydrolysis conditions were: temperature 49℃, time 56 h, enzyme charges 38 FPU/g at the pH of 4.8 and the ratio of substance to liquor was 1∶50. The cellulose conversion rate was 96.4% on the pretreated substance. After wet oxidation pretreatment, hemicelluloses content of the substance decreased from 18.7% to 1.43%, Klasson lignin content decreased from 23.6%% to 13.5%, which mean that almost 43% of lignin and 92% hemicelluloses were degraded and solved from the raw material. XRD analysis indicated that the crystallinity decreased from 57.4% to 54.8%. The obvious fibrilization of the pretreated fiber was found by SEM. HPLC analysis results showed that pretreatment liquid contained higher content of xylose, and monosaccharide degradation products, such as acetic acid, formic acid and furfural. Wet oxidation pretreatment was able to greatly degrade or remove lignin and hemicellulose significantly, reduce the crystallinity of
the lingo cellulosic material, which could improve enzymatic degradability and increase reduce sugar yield and cellulose conversion rate.
Key words:poplar wood residues; wet oxidation pretreatment; pretreatment conditions; enzymatic degradability
项目基金:国家十二五科技支撑项目“栎类淀粉与秸秆生物质炼制生物柴油及其综合利用产业化示范(项目编号:2014BAD02B02)”。
收稿日期:2014- 09- 17(修改稿)
中图分类号:TQ35
文献标识码:A
文章编号:0254- 508X(2015)01- 0006- 07
作者简介:房桂干先生,研究员;主要从事制浆造纸、环境保护及生物质高值化利用技术研究。
