乳腺癌患者血清HER-2/neu浓度与组织HER-2表达水平的相关性
2015-03-02周爱清陈志军孙正魁黄传生
周爱清 陈志军 孙正魁 黄传生
乳腺癌患者血清HER-2/neu浓度与组织HER-2表达水平的相关性
周爱清陈志军孙正魁黄传生
作者单位:330029 江西省肿瘤医院
【摘要】目的探讨化学发光法检测可手术乳腺癌患者血清HER-2/neu ECD浓度与组织HER-2表达水平的相关性。方法采用西门子化学发光仪检测2012年12月至2013年12月收治的84例可手术乳腺癌患者血清HER-2/neu ECD水平,并采用同期的58例乳腺良性病变患者及56例健康体检女性作为对照;同时对84例可手术乳腺癌患者进行组织HER-2表达的检测。结果可手术乳腺癌患者血清HER-2/neu ECD水平及阳性率分别为(15.56±6.79)ng/ml、19.05%,明显高于乳腺良性病变患者的(6.21±3.21)ng/ml、0.00%,及健康体检者的(5.13±2.25)ng/ml、0.00%,P均<0.05。34例组织HER-2表达阳性的可手术乳腺癌中有14例血清HER-2/neu阳性,阳性符合率为41.2%;50例组织HER-2表达阴性的可手术乳腺癌中有48例血清HER-2/neu阴性,阴性符合率为96.0%;血清HER-2/neu水平与组织HER-2表达状态具有较好的一致性,(kappa=0.406,P<0.05)。结论化学发光法检测可手术乳腺癌患者血清HER-2/neu浓度与组织HER-2表达水平具有较好的一致性。因此,乳腺癌患者在系统治疗期间,可通过化学发光法动态监测患者血清HER-2/neu ECD水平,可弥补组织HER-2检测的不足,在乳腺癌随访、疗效监测尤其是用Herceptin治疗后的疗效监测中发挥其独到作用。
【关键词】乳腺癌;化学发光法;血清;HER-2/neu;免疫组化;荧光原位杂交
(ThePracticalJournalofCancer,2015,30:479~481)
人类表皮生长因子受体-2(human epidermal growth factor receptor 2,HER-2)基因是一种原癌基因,由具有酪氨酸激酶活性的胞质区、跨膜区及胞外域(extracellular domain,ECD)组成。目前临床多采用免疫组化(IHC)和荧光原位杂交(FISH)判断组织HER-2表达水平,但这些方法有流程繁琐复杂、灵敏度及特异性较差等缺点,且对于晚期无法取得实体瘤样本的患者,IHC和FISH均无法检测。有研究表明,HER-2/neu的细胞外区(ECD)可脱离进入血清,形成游离的HER-2/neu蛋白,称血清HER-2/neu[1]。血清HER-2/neu检测具有简单、方便、定量及动态观察等优点,可以监控治疗效果、预测复发或提供乳腺癌转移时HER-2状态的实时评估[2]。本研究通过化学发光法检测可手术乳腺癌患者血清HER-2/neu ECD水平,对其与组织HER-2表达水平的相关性进行探讨,现报告如下。
1材料与方法
1.1一般资料
收集我院2012年12月至2013年12月可手术乳腺癌患者84例,所有病例均经病理检查证实为浸润性导管癌,均为女性;年龄26~71岁,平均年龄52岁。另外收集健康体检女性56例作为正常对照组,年龄21~53岁,平均年龄37岁。手术证实为乳腺良性病变患者58例,其中乳腺纤维瘤31例,小叶增生27例,年龄31~65岁,平均年龄39岁。受检者抽空腹血3~5 ml,不抗凝,待血液凝固后分离血清置于无菌有盖试管中,置于-25 ℃低温冰箱保存备用。
1.2仪器与方法
测量仪为西门子centaur XP化学发光仪,HER-2/neu试剂由西门子公司提供。
1.3结果判断
血清HER-2/neu>15.2 ng/ml为阳性。组织HER-2阳性的判断标准:IHC计分3+或IHC计分2+再经荧光原位杂交(FISH)验证阳性者视为阳性;组织HER-2阴性的判断标准:IHC计分0+~1+或IHC计分2+再经荧光原位杂交(FISH)验证阴性者视为阴性。
1.4统计学处理
两样本均数比较用t检验,阳性率的比较采用χ2检验,采用Kappa检验来判断2种检测方法结果是否具有一致性,Kappa值的判断[3]:k>0.75一致性好,0.40≤k≤0.75一致性较好,k<0.4一致性差。
2结果
2.1血清HER-2/neu ECD的水平和阳性率
可手术乳腺癌患者血清HER-2/neu ECD水平均高于乳腺良性病变患者及健康体检者(P均<0.05),乳腺良性病变患者血清HER-2/neu ECD水平高于健康体检者(P<0.05);可手术乳腺癌血清HER-2/neu ECD阳性率均高于乳腺良性病变患者及健康体检者(P均<0.05),乳腺良性病变患者血清HER-2/neu ECD阳性率与正常对照组相比无统计学意义(P>0.05);见表1。
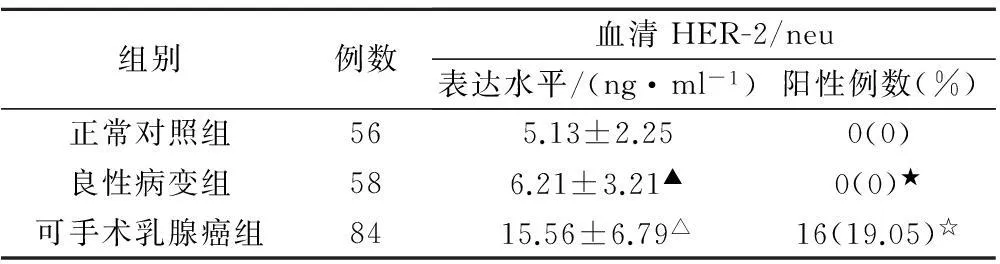
表1 不同组别血清HER-2/neu水平及阳性率
注:△为乳腺癌患者血清HER-2/neu水平与乳腺良性病变及正常对照组相比,P均<0.05;▲为乳腺良性病变患者血清HER-2/neu水平与正常对照组相比,P<0.05。☆为乳腺癌患者血清HER-2/neu阳性率与乳腺良性病变及正常对照组相比,P均<0.05;★为乳腺良性病变患者血清HER-2/neu阳性率与正常对照组相比,P>0.05。
2.2血清HER-2/neu浓度与组织HER-2表达水平的关系
34例组织HER-2表达阳性的可手术乳腺癌中有14例血清HER-2/neu阳性,阳性符合率为41.2%;50例组织HER-2表达阴性的可手术乳腺癌中有48例血清HER-2/neu阴性,阴性符合率为96.0%。化学发光法检测结果显示血清HER-2/neu水平与组织HER-2表达水平差异无统计学意义,2种检查方法具有较好的一致性,(kappa=0.406,P<0.05);见表2。
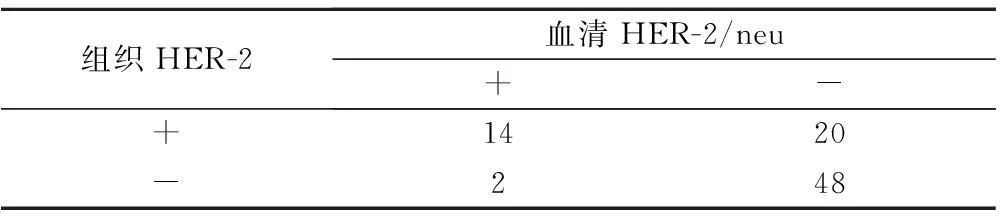
表2 乳腺癌患者HER-2/neu水平与组织HER-2
3讨论
乳腺癌是女性发病率最高的恶性肿瘤,且发病率呈逐年上升的趋势。20%~30%的乳腺癌患者呈HER-2过度表达或基因扩增,HER-2基因的扩增和蛋白的过度表达预示肿瘤的生物学行为恶性程度高,侵袭力强,无病生存期短,预后差[4]。组织HER-2和激素受体的表达是乳腺癌的内分泌治疗和靶向治疗的唯一选择依据,目前大多数乳腺癌患者的临床治疗仍然是根据初始评估,但HER-2的表达状态随疾病的进展会发生改变[5]。
目前国际上认可的筛选HER-2表达阳性乳腺癌的方法有免疫组化(immunohistochem istry,IHC)法和荧光原位杂交(fluorescence in situ hybridization,FISH)法。IHC法由于蛋白在标本固定和处理过程中容易变形破坏,以及抗体不同批号产生的差异和结果判断的主观差异等,使假阳性和假阴性无法避免[6];FISH技术是一种基因技术,具有敏感性高、稳定性和重复性好等优点,但检测费用高,且两者均需要实体瘤样本;对于晚期乳腺癌或治疗过程中出现肝、骨等转移不能取得实体标本的患者,均不能做IHC和FISH检测。因此,仅仅根据以往组织学检测结果来判断HER-2状态并不科学,需要及时监测HER-2表达状态,否则可能会使部分组织HER-2假阴性的患者失去靶向治疗和临床获益的机会。国家综合癌症网(NCCN)建议尽可能进行转移灶的活检,但很少得到关注,尤其当转移灶难以活检时。
在这种情况下,血清HER-2/neu胞外段(extracellular domain,ECD)可能可以作为乳腺癌患者治疗的一个重要的依据。袁芃等[7]采用ELISA方法检测可手术乳腺癌血清HER-2/neu ECD阳性率为19%,组织HER-2/neu阳性率为47%。而采用化学发光法检测乳腺癌患者血清HER-2/neu水平的文献至今还未见报道,本研究采用化学发光法检测可手术乳腺癌患者血清HER-2/neu ECD阳性率为19.05%(16/84),组织HER-2/neu阳性率为40.5%(34/84);可手术乳腺癌患者血清HER-2/neu ECD水平和阳性率均高于乳腺良性病变患者及健康体检者(P均<0.05),与袁芃等报道一致。
总之,目前被广泛采用的HIC和FISH存在诸多问题:由于活检的创伤性和标本的局限性,HER-2的检测无法动态随访,实时监测;而且部分患者无法提供检测所需的组织切片;肿瘤异质性会导致假阴性结果,有些患者的HER-2表达水平在疾病的发展过程中可能发生转变,有些可由阴性表达转为阳性表达。因此,临床需要持续了解患者机体HER-2的表达水平,而血清HER-2/neu ECD检测作为“液体活检”可随时进行,做到量化、实时、动态监测,从而有助于临床医生根据HER-2表达情况制定治疗方案,以实现个体化治疗。本研究显示化学发光法检测可手术乳腺癌患者血清HER-2/neu浓度与组织HER-2表达水平具有较好的一致性(kappa=0.406,P<0.05);化学发光法检测可手术乳腺癌患者血清HER-2/neu ECD的敏感性不高(41.2%),但特异性很好(96.0%)。因此,乳腺癌患者在系统治疗期间,可通过化学发光法动态监测患者血清HER-2/neu ECD水平,弥补组织HER-2检测的不足,在乳腺癌随访、疗效监测尤其是用Herceptin治疗后的疗效监测中发挥其独到作用。
参考文献
[1]Cook GB,Neaman IE,Goldblatt JL,et al.Clinical utility of serum HER-2/neu testing on the Bayer Immuno 1 automated system in breast cancer〔J〕.Anticancer Res,2001,21(2B):1465-1470.
[2]Leary AF,Hanna WM,van de Vijver MJ,et al.Value and limitations of measuring HER-2 extracellular domain in the serum of breast cancer patienta〔J〕.J Clin Oncol,2009,27(10):1694-1705.
[3]孙振球主编.医学统计学(第三版)〔M〕.北京:人民卫生出版社,2011:662-663.
[4]步宏,陈杰,丁华野,等.乳腺癌HER2检测指南〔J〕.中华病理学杂志,2006,35(10):631.
[5]臧爱华,冉凤鸣,张菁,等.乳腺癌生物标志物表达状态的时间变异性〔J〕.肿瘤防治研究,2010,37(9):1031-1034,1039.
[6]万美珍,凌扬,徐志毅,等.荧光原位杂交与免疫组化检测乳腺癌组织HER-2基因扩增或蛋白表达情况的比较分析〔J〕.肿瘤基础与临床,2010,23(1):16-18.
[7]袁芃,徐兵河,齐军.乳腺癌患者血清与肿瘤组织中Her-2/neu表达的相关性研究〔J〕.临床肿瘤学杂志,2004,9(5):449-451.
(编辑:甘艳)
Correlation between Serum HER-2/neu Concentration of Breast Cancer Patients and HER-2 Expression Level
ZHOUAiqing,CHENZhijun,SUNZhengkui,etal.JiangxiCancerHospital,Nanchang,330029
【Abstract】ObjectiveTo explore the correlation between concentration of HER-2/neu ECD and HER-2 expression level in tissues by chemiluminescence.MethodsSiemens chemiluminescence apparatus was used to detect the serum HER-2/neu ECD level in 84 operable breast cancer patients.58 patients with breast benign lesions over the same period and 56 cases of healthy patients were selected as contrast.HER-2 expression level in tissues of 84 cases of breast cancer patients were detected.ResultsHER-2/neu ECD levels and serum positive rate of the breast cancer patients were 15.56±6.79 ng/ml and 19.05%,which were significantly higher than patients with breast benign lesions (6.21±3.21 ng/ml,0.00%) and healthy patients (5.13±2.25 ng/ml,0.00%),P<0.05.There were 14 cases of positive serum HER-2/neu in 34 operable breast cancer patients with positive expression of HER-2,positive coincidence rate was 41.2%.There were 48 cases of negative serum HER-2/neu in 50 operable breast cancer patients with negative expression of HER-2,negative coincidence rate was 96%.The serum HER-2/neu level had good consistency with expression of HER-2(kappa=0.406,P<0.05).ConclusionSerum Her-2/neu concentration in operable breast cancer patients has good consistency with expression of HER-2 by chemiluminescence.During the system treatment for breast cancer patients,dynamic monitoring of serum HER-2/neu ECD level by chemiluminescence can make up for the insufficiency of HER-2 detection.It plays an unique role in the follow-up of breast cancer patients and monitoring of efficacy,especially monitoring of efficacy after treatment with Herceptin.
【Key words】Breast cancer;Chemiluminescence method;Serum;HER-2/neu;Lmmunohistochemical;Fluorescence in situ hybridization(FISH)
(收稿日期2014-12-04修回日期 2015-01-14)
中图分类号:R737.9
文献标识码:A
文章编号:1001-5930(2015)04-0479-03
DOI:10.3969/j.issn.1001-5930.2015.04.002
基金项目:江西省卫生厅科技计划(编号:20123106)
