抗丙型肝炎病毒药物研究进展
2015-02-24吴晓明王国成
吴晓明,王国成,刘 斌
(1. 内蒙古医科大学药学院,呼和浩特 010110; 2.天士力控股集团有限公司研究院化学药物研究所,天津 300410)
抗丙型肝炎病毒药物研究进展
吴晓明1,2,王国成2*,刘 斌2
(1. 内蒙古医科大学药学院,呼和浩特 010110; 2.天士力控股集团有限公司研究院化学药物研究所,天津 300410)
丙型肝炎病毒(HCV)是导致慢性肝病和肝细胞癌的主要原因,越来越多的人感染HCV已成为严重的社会和公共卫生问题。由于HCV具有很强的变异性,目前尚无有效的疫苗。虽然新上市的telaprevir和boceprevir联合peg-IFN(聚乙二醇-干扰素)和ribavirin治疗方法具有较强的抗HCV能力,可以有效的治疗部分HCV患者,但是仍具有较大的副作用和较差的药物耐受性,而二代直接抗病毒药物和宿主靶向药物的发现为治愈HCV患者提供了新的方向。
丙型肝炎,丙型肝炎病毒,抗病毒治疗
1989年美国的Chiron公司应用分子克隆技术率先将丙肝病毒(HCV) cDNA克隆成功,使得HCV成为人类用分子生物学技术发现的第一个病毒,该病毒被确认为是导致慢性肝病的主要病因。世界大约有1.7亿人感染了HCV,每年新增病例300~400万人[1],同时造成约47万人死于与丙肝相关的晚期肝病及丙肝并发症[2]。HCV的持续性感染可造成被感染者发展为肝硬化和肝细胞癌[3]。每年全球肝癌新发病例的22%是由于感染HCV引起的[4]。
我国HCV感染发病率较高,一般人群抗HCV阳性率为3.2 %,总数超过4 000万,多数演变成慢性感染。因HCV具有高突变性,目前对HCV感染尚无有效疫苗预防[5]。慢性肝炎患者早期一般没有明显的临床症状,但随病情的进展会出现肝功能受损、肝肿大和肝硬化的临床症状。HCV的主要传播方式为血液传播,在我国输血后患丙型肝炎者占1/3[6]。近年来,丙型肝炎的发病率呈上升趋势,已成为严重的社会和公共卫生问题。
1 HCV的生物学特征
HCV属披膜病毒科,其生物性状、基因结构与黄病毒、瘟病毒近似。目前已确认HCV为含有脂质外壳的球形颗粒,直径30~60 nm。HCV基因组是一长的正链、单股RNA,长约9.6 kb,可以分为三个区域,其中5′和3′非编码区(NCR)分别有319~341 bp和27~55 bp,含有几个顺向和反向重复序列,与基因复制有关。在5′非编码区下游紧接一开放的阅读框(ORF), 基因排列顺序为5′-C-E1-E2-p7-NS2-NS3-NS4-NS5-3′,可以编码3010或3011个氨基酸的蛋白体。编码的蛋白体与黄病毒有明显的类似结构:含结构蛋白(包膜蛋白E1和E2、核心蛋白)和非结构蛋白( p7、NS2、NS3、NS4A、NS4B、NS5A和NS5B)[7]。参考其他黄病毒中类似位置的蛋白质功能来看,结构蛋白用来合成HCV的核衣壳和包膜,非结构蛋白在病毒复制周期中起到调控的作用。
HCV可分为7个基因型67个不同亚型[8],且呈明显的地域分布。其中1、2、3型呈全球性分布,4型主要分布在非洲中部、中东地区和地中海区域。我国主要的HCV基因型为基因1b、2a和6型[9]。
2 抗HCV病毒治疗的发展
20世纪90年代初治疗HCV感染患者的方法是单一使用干扰素(IFN),取得的SVR(持续性病毒应答)率为14%~78%。其中高剂量的使用干扰素(5~6 MU×3/周)12个月取得了最高的SVR率。在20世纪90年代后期,peg-IFN由于每周用药1次且疗效更高代替了传统的IFN用来治疗HCV患者。在21世纪早期,peg-IFN和ribavirin联合用药成为治疗HCV患者的标准治疗方法,此后十多年间仍然如此。然而,这种治疗周期长,且价格昂贵,在治疗期间,患者还要承受身体疲劳、头疼、贫血和精神沮丧等不良反应[10]。而且治疗过程中约50%患者不能产生SVR,其中基因HCV 1型感染患者 SVR 率最低。有基因研究表明,19号基因组IL28B区上的单核苷酸多态性与该疗法有关[11]。
2011年,美国食品和药品监督管理局(FDA)通过了两种治疗1型丙肝的蛋白酶抑制剂,分别是Telaprevir和Boceprevir。作为NS3蛋白酶抑制剂,Telaprevir能直接攻击HCV,迅速阻断HCV的RNA复制[12]。但单一使用该药物HCV易发生变异,须与peg-INF联合使用[13]。Telaprevir与peg-INF/ribavirin联合用药,患者的SVR率可以提高到70%以上[14]。而Boceprevir与peg-INF/ribavirin联合用药可以使SVR率提高到66%[15]。而且该疗法大大缩短了患者的用药时间。然而,使用三联疗法仅限于感染HCV基因1型的患者,且治疗的成本进一步上升,同时约40%的病人在治疗时存在不良反应,如皮疹和贫血。在未来,不依靠IFN和ribavirin的小剂量、高依从性和高SVR率的药物将会被发现。
3 HCV疗法新领域
尽管Telaprevir和Boceprevir的使用给HCV感染患者的治疗带来了很大进展,但还是不能作为单药治疗。此外,其仅仅被批准用来治疗HCV 1型感染患者。研发抗HCV药物的最终目的是研究一类用药周期短、疗效高、副作用小的口服药物。这类新型药物包括二代直接抗病毒药物和宿主靶点药物。
3.1 二代直接抗病毒药物 目前已研发大量的直接抗病毒药物(DAA),见表1。在接下来的临床实验中,一些DAAs药物将联合peg-IFN和ribavirin使用,其目的是在以后可以实现使用单药治疗丙肝患者。
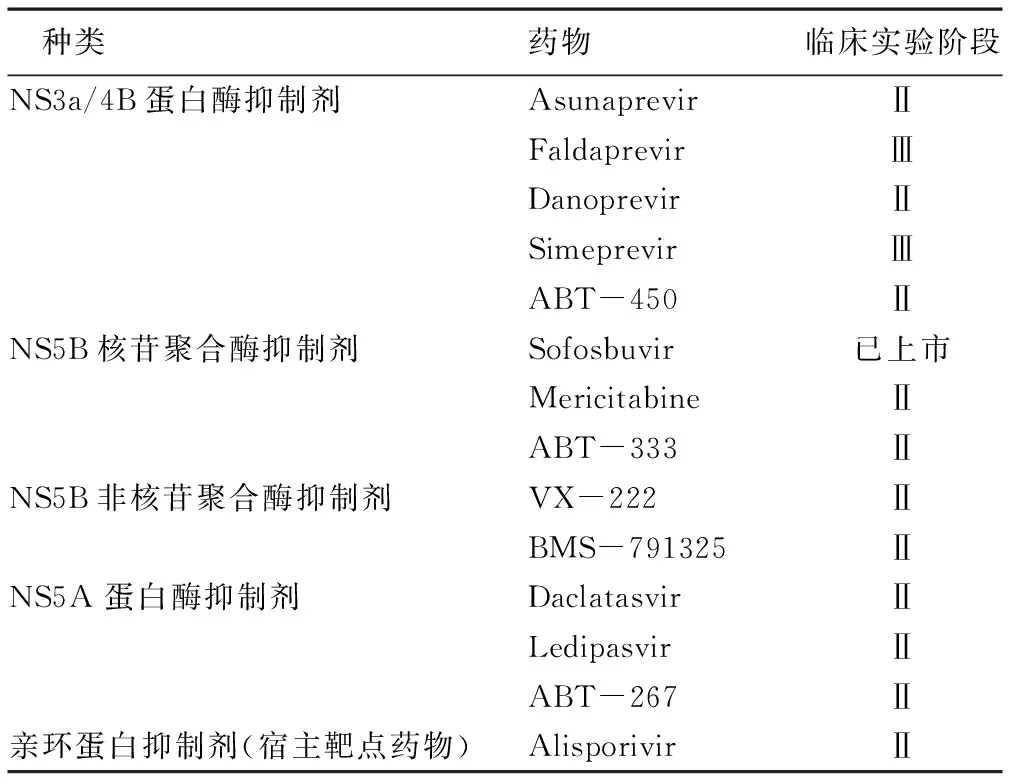
表1 直接抗病毒药物和宿主靶点药物的种类及其临床实验阶段
3.1.1 Faldaprevir Faldaprevir是NS3/4A蛋白酶抑制剂。Ferenci[16]等使用Faldaprevir加peg-IFN/ribavirin分别对三组共656个基因1型HCV患者的疗效进行了研究:①faldaprevir 120 mg加peg-IFN/ribavirin治疗12周,再用相同的组合或者安慰剂继续治疗12周。最后24~48周用peg-IFN/ribavirin治疗。②faldaprevir 240 mg加peg-IFN/ribavirin治疗12周,之后用peg-IFN/ribavirin 治疗至48周。③peg-IFN/ribavirin 治疗48周。研究发现,在①和②中非合并肝硬化的HCV 1a型患者的SVR率均为69%,HCV 1b型患者的SVR率均为 84%。在患有肝硬化的HCV患者中,SVR率降到了56%。在符合缩短治疗周期标准(在第4周HCV RNA<25 IU/ml)的患者的SVR率为86%~89%,同时存在可能与剂量有关的副作用,包括贫血、皮疹、光敏性和胃肠道反应。
3.1.2 Simeprevir Simeprevir是另外一种的NS3/4A 蛋白酶抑制剂。通过让病人随机接受两种治疗方案来研究Simeprevir对于首次治疗的1型HCV患者的功效评价[17,18]。①Simeprevir加peg-IFN/ribavirin治疗12周,继续使用peg-IFN/ribavirin 12周或者根据患者的情况至36周,患者的SVR率高达80%。②使用peg-IFN/ribavirin 12周,患者SVR率为50%。两项研究中,在持续治疗48周患者的SVR 率有所降低(21%~32%)。研究还发现,并发肝硬化的患者SVR率较低为65%,非肝硬化的患者SVR率为85%。在使用simeprevir药物的过程中,患者的胆红素有短暂性的增加。
3.2 宿主靶点药物 丙肝病毒在其整个生命周期都依赖于不同的宿主因素,如亲环蛋白。Alisporivir是一种口服的亲环蛋白A抑制剂,通过抑制丙肝病毒复制从而发挥抗病毒作用[19]。Alisporivir的特点是对所有的HCV基因型都具有相对较高的抗病毒活性[20]。首次治疗HCV基因型1患者,Alisporivir联合peg-IFN-α-2a和ribavirin治疗24~48周,结果显示SVR率为69%~76%,对照组的SVR率为55%[21]。由于该药物Ⅱ期临床表现优秀,诺华制药于2010年2月申请了专利权。
实验结果表明,Alisporivir具有较全面的基因活性和低耐药性的特点,证明了宿主靶向药物在非依赖干扰素治疗方案中具有巨大的潜力。
4 非干扰素治疗HCV的初步研究
在治疗HCV患者过程中,患者是否对干扰素过敏是影响三联法治疗方案是否成功的主要因素[22]。在用三联法治疗过程中,有相当数量的患者对使用的peg-IFN-a 和ribavirin只有部分应答或没有应答,HCV病毒数量减少有限,或者由于患有晚期肝硬化而导致了病毒耐药性变异。为了解决这个问题,有效的直接抗病毒药物或是基于peg-IFN和ribavirin加两个不同类型的直接抗病毒药物的四联法治疗方案可能会适用。采用四联法治疗,之前对peg-IFN和ribavirin治疗没有病毒应答的患者也取得了显著的SVR 率[23,24]。但是,这些临床实验对HCV患者的选择具有很高的要求,三联法和四联法治疗都选择对peg-IFN或者ribavirin没有不良反应的患者。因此,对于大多数不耐受IFN-a的HCV病人还急需新的抗病毒疗法。为了得到比干扰素更为有效的治疗方案,人们加快了对具有潜力的非干扰素药物的研究。下面总结目前一些安全有效的非干扰素治疗方法,以说明非干扰素治疗方法的前景。
4.1 Daclatasvir+Sofosbuvir+/-ribavirin联合治疗 Daclatasvir(NS5A抑制剂)、Sofosbuvir(NS5B 抑制剂)和ribavirin联合用药24周,得到了很好的结果[25]。在大约90名首次治疗的患者中,HCV 1型患者的快速病毒学应答(RVR)和SVR率都为100%,在HCV 2型和HCV 3型的患者中SVR率分别为100%和91%。在实验过程中,加入ribavirin并没有提高病毒学应答率,反而导致了相当一部分患者的出现贫血症状。此外,在这个研究中发现,不利基因型IL28B并没有减少治愈的几率。但是,由于在研究过程中Bristol-Myers Squibb 和Gilead的策略不同,导致了这个很有发展前景的项目被停止。
4.2 多种DAAs +ribavirin联合治疗 最近一个正在研究中的治疗方案-QUAD(即NS5A抑制剂gs-5885,NS3-4A抑制剂gs - 9451,NNI tegobuvir,和ribavirin联合治疗),这是第一个包含多个DAAs的治疗方案[26]。在QUAD研究中,对首次接受治疗的HCV1型患者进行为期12~24周的口服四联药物治疗。在进行到第二周治疗时,如果患者HCV的RNA值没有降到检测限以下,将被转换为基于peg-IFN-a的治疗方案。在这个研究中大约有70%的患者适合这种口服四联药物治疗,在这些HCV 1a和HCV 1b的患者SVR率分别为77%和89%。
4.3 Faldaprevir和BI 207127+/-ribavirin联合治疗 Zeuzem等[27]进行的二期临床实验研究,对首次接受治疗的HCV 1型患者使用Faldaprevir(蛋白酶抑制剂)和BI 207127(聚合酶抑制剂),在加或不加利巴韦林的治疗方法中,分别对其安全性和有效性进行了评估。研究结果显示,治疗28周以上有85%的HCV 1b型感染患者和43%的HCV 1a基因型感染患者达到了一定的SVR率。
5 总结
近年来,丙肝病毒治疗领域的发展迅速。目前,三联疗法是治疗HCV 1型的标准疗法,SVR率高,也是唯一被批准用来治疗HCV 1型患者的疗法。但该疗法有严重的副作用,同时存在药物相互作用和病毒的耐药性等问题。 多种直接抗病毒药物(DAA)联用治疗方法和亲环素抑制剂的出现,为抗HCV治疗打开了一个新的领域,其具有高的SVR率、低耐受性和良好的安全性等特点,将有可能成为治疗没有并发肝硬化的HCV患者的单一用药治疗方案。对于这类患者,与peg-IFN/ribavirin的治疗方案相比,使用联合两种或三种直接抗病毒药物治疗方案更加具有吸引力。
1 Manns M P, Fost er G R, Rockst roh J K,etal.The way of forward in HCV treatment- finding the right path[J].Nat Rev Drug Dis Cov,2007, 6 (12):991-1000
2 Colin w shepard,Lyn Finelli,Miriam J Alter.Global epidemiology of hepatitis C virus infection.[J].The Lancet Infectious Diseases,2005,5(9):558-567
3 Christina Schlecker, Alfred Ultsch, Gerd Geisslinger,etal.The pharmacogenetic background of hepatitis C treatment[J].Mutation Research,2012, 751(1):36-48
4 T R Lim, B H Tan, D J Mutimer.Evolution and emergence fo a new era of antiviral treatment for chronic hepatitis C infection[J].International Journal of Antimicrobial Agents .2014,43(1):17-25
5 徐东平,周先志.丙型肝炎抗病毒治疗药物研究进展[J].传染病信息,2008,21(4):210-213
6 王莹莹,龚莉,王成港,等.丙型肝炎治疗新药替拉瑞韦[J].药物评价研究,2011,34(6):482-486
7 Penin F, Dubuisson J, Rey F A,etal. Structural biology of hepatitis C virus[J]. Hepatology, 2004, 39(1):5-19
8 Donald B Smith, Jens Bukh,A Scott,etal.Expanded classification of hepatitis C virus into 7 genotypes and 67subtypes, updated criteria and assignment web resource[J].Hepatology,2014,59(1):318-327
9 霍霏霏, 刘晓清, 周宝桐,等.慢性丙型肝炎抗病毒治疗进展[J].中华实验和临床感染病杂志,2009,3 (2) : 55-57
10 Muir A J, Hu K Q, Gordon S C,etal. Hepatitis C treatment among racial and ethnic groups in the IDEAL trial[J]. J Viral Hepat,2011,18(4):134-143
11 Ge D, Fellay J,Thompson A J,etal. Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance[J]. Nature,2009,461(7262):399-401
12 闫书山,徐栋花,张鹏军,等.Telaprevir联合聚乙二醇干扰素a及利巴韦林治疗慢性丙型肝炎疗效的荟萃分析[J].中国肝脏病杂志,2013,21(7):506-509
13 曾庆磊,李元元,王福生.抗HCV新药sofosbuvir和ABT-450研究进展[J].传染病信息,2013,26(2):85-88
14 Jacobson I M, McHutchison J G, Dusheiko G,etal. Telaprevir for previously untreated chronic hepatitis C virus infection[J]. N Engl J Med,2011,364(25):2405-2416
15 Poordad F, McCone Jr J, Bacon B R,etal. Boceprevir for untreated chronic HCV genotype 1 infection[J]. N Engl J Med,2011,364(13):1195-1206
16 Ferenci P, Asselah T, Foster G R,etal. Faldaprevir plus pegylated interferon alfa-2a and ribavirin in chronic HCV genotype-1 treatment-naive patients: final results from STARTVerso1, a randomised,double-blind, placebo controlled phase Ⅲtria[J]. J Hepatology,2013,58(s1):S569-S570
17 Manns M, Marcellin P,Poordad F,etal. Simeprevir (TMC435) with peginterferon/ribavirin for chronic HCV genotype-1 infection in treatment-naive patients: results from QUEST-2,a phase ⅡI trial[J].J Hepatology,2013,58(s1):568
18 Jacobson I, Dore G J, Foster G R,etal. Simeprevir(TMC435) with peginterferon/ribavirin for chronic HCV genotype-1 infection in treatment-naive patients: results from QUEST-1, a phase ⅡI trial[J]. J Hepatology,2013,58(s1):574
19 Giovanni Quarato,Annamaria D’Aprile,Bruno Gavillet,etal.The Cyclophilin Inhibitor Alisporivir Prevents Hepatitis C Virus-Mediated Mitochondrial Dysfunction[J].Hepatology,2012,55(5):1333-1343
20 Coelmont L, Kaptein S, Paeshuyse J,etal.Debio 025, a cyclophilin binding molecule, is highly efficient in clearing hepatitis C virus (HCV) replicon-containing cells when used alone or in combination with specifically targeted antiviral therapy for HCV (STAT-C)inhibitors[J]. Antimicrob Agents Chemother,2009,53(3):967-976
21 Flisiak R, Feinman S V, Jablkowski M,etal. The cyclophilin inhibitor Debio 025 combined with PEG IFN alpha 2a significantly reduces viral load in treatment-naive hepatitis C patients[J].Hepatology,2009,49(5):1460-1468
22 Lange C M, Sarrazin C, Zeuzem S. Review article: specifically targeted antiviral therapy for hepatitis C-a new era in therapy[J]. Aliment Pharmacol Ther,2010,32(1):14-28
23 Lok A S, Gardiner D F, Lawitz E,etal.Preliminary study of two antiviral agents for hepatitis C genotype 1[J]. N Engl J Med,2012,366(3):216-224
24 Chayama K, Takahashi S, Toyota J,etal. Dual therapy with the nonstructural protein 5A inhibitor, daclatasvir, and the nonstructural protein 3 protease inhibitor, asunaprevir, in hepatitis C virus genotype 1b-infected null responders[J]. Hepatology,2012.55(3):742-748
25 Sulkowski M S, Gardiner D F, Lawitz E,etal. Potent viral suppression with all-oral combination of daclatasvir (NS5A inhibitor) and GS-7977 (NS5B inhibitor), +/-ribavirin, in treatment-naive patients with chronic HCV GT 1, 2, or 3[J]. J Hepatology,2012,56(s2):560
26 Sulkowski M S, Rodriguez-Torres M, Lawitz E,etal. High sustained virologic response rate in treatment-naive HCV genotype 1a and 1b patients treated for 12 weeks with an interferon-free all-oral quad regimen: interim results[J]. J Hepatology,2012,56(s2):560
27 Zeuzem S, Asselah T, Soriano V,etal. Interferon (IFN)-free combination treatment with the HCV NS3/4A protease inhibitor BI 201335 and the non-nucleoside NS 5B inhibitor BI207127±ribavirin (R): final results of SOUND-C2 and predictors of response[J]. J Hepatology,2012,56(s4):308A-309A
Research advances in anti-hepatitis C virus drugs
Wu Xiaoming1, 2, Wang Guocheng2,Liu Bin2
(1. College of Pharmacy, Inner Mongolia Medical University, Hohhot 010110; 2. Chemical Medicine Department of Tasly R&D Institute, Tasly Holding Group Co Ltd,Tianjin 300410)
Hepatitis c virus (HCV) is a primary cause of chronic liver disease and hepatocellular carcinoma (HCC), and it becomes a major public health burden associated with significant morbidity and mortality. Because of HCV’s variability, there is no effective vaccine.The approval of telaprevir and boceprevir for use with interferon and ribavirin in chronic HCV infection significantly increased viral eradication but has been accompanied by increased adverse events and therefore inferior clinical tolerance. Newer antiviral agents of directly acting antiviral and host-targeting agents can achieve better response rates with a shorter duration of treatment. This offers an exciting prospect in the new era of antiviral treatment for HCV infection.
hepatitis c, hepatitis c virus, antiviral treatment
2014-09-18
R975+.5
A
1006-5687(2015)01-0069-04
*通讯作者:王国成,E-mail:wanggc@tasly.com。
