HPLC法测定土霉素二水物的有关物质的方法研究*
2015-02-23曹晓云
顾 云,曹晓云
(天津市药品检验所,天津 300070)
HPLC法测定土霉素二水物的有关物质的方法研究*
顾 云,曹晓云
(天津市药品检验所,天津 300070)
目的:建立HPLC法测定土霉素二水物的有关物质。方法:色谱柱为XDB-C18(250 mm×4.6 mm,5 μm),流动相为醋酸铵溶液[0.25 mol/L醋酸铵溶液-0.05 mol/L乙二胺四醋酸二钠溶液-三乙胺(100∶10∶1),用醋酸调节pH至7.5]-乙腈(88∶12),流速:1.0 ml/min,紫外检测波长:280 nm,柱温:30 ℃,进样量:10 μl。 结果:土霉素在0.25~15 μg/ml范围内线性关系良好(r=0.999 95),最低检出限为 0.1 μg/ml。结论:本方法专属性强、灵敏度高、准确度和重复性好、方法简便,可作为土霉素有关物质的检测方法。
HPLC,有关物质,土霉素二水物
土霉素二水物[1]属四环素类抗生素药,对革兰阴性菌和革兰阳性菌均有抑制作用,同时对立克次体、螺旋体及某些原虫等也具有抑制作用。为更好地控制土霉素二水物的质量,采用HPLC法测定土霉素二水物有关物质,该方法专属性强、灵敏度高、准确度和重复性好、方法简便,可作为土霉素有关物质的检测方法。
1 仪器与试药
LC-2010 cLass-vp型高效液相色谱仪(日本岛津公司),AG245型电子天平,PB-10型精密pH计(塞多利斯公司),恒温干燥箱DN64(日本Uamato),紫外线杀菌车DZS3型(上海科凌医疗器械有限公司)。土霉素样品(河北圣雪大诚制药有限公司,批号T3-11314417-3、T3-11301416-3、T3-11319424-3),土霉素对照品( 批号130487-200302,中国药品生物制品检定所提供,88.2%)。4-差向四环素对照品(批号130401-200209,中国药品生物制品检定所提供)。乙腈、甲醇为色谱纯,水为净化水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件 色谱柱:XDB-C18(250 mm×4.6 mm,5 μm),流动相:醋酸铵溶液[0.25 mol/L醋酸铵溶液-0.05 mol/L乙二胺四醋酸二钠溶液-三乙胺(100∶10∶1),用醋酸调节pH至7.5]-乙腈(88∶12),流速:1.0 ml/min,柱温:30 ℃,紫外检测波长:280 nm,进样量:10 μl。
2.2 溶液制备
2.2.1 供试品溶液 取本品适量,用0.01 mol/L盐酸溶解并定量稀释制成每1 ml中约含0.5 mg的溶液,作为供试品溶液。
2.2.2 对照溶液 精密量取供试品溶液2 ml,置100 ml量瓶中,用0.01 mol/L盐酸溶解并定量稀释至刻度,作为对照溶液。
2.3 系统适用性试验 取4-差向四环素对照品适量,加0.01 mol/L盐酸溶解并定量稀释制成每1 ml中约含0.5 mg的溶液;取土霉素素对照品适量,加0.01 mol/L盐酸溶解并定量稀释制成每1 ml中约含0.5 mg的溶液;取上述两种溶液(1∶24)混合,作为分离度测试溶液。取该溶液10 μl注入液相色谱仪,记录色谱图,按4-差向四环素峰(与土霉素色谱峰相对保留时间约为0.9)、土霉素峰、2-乙酰-2-去酰胺土霉素峰(与土霉素色谱峰相对保留时间约为1.1)的顺序出峰。4-差向四环素与土霉素峰分离度应不小于2.0,土霉素峰与2-乙酰-2-去酰胺土霉素峰的分离度应不小于2.5[2]。见图1。
2.4 专属性试验 取样品约25 mg,置50 ml量瓶中,共6份,分别按以下条件操作。①酸破坏:加1 mol/L盐酸溶液2 ml,于60 ℃水浴中加热20 min,取出,立即加1 mol/L氢氧化钠溶液调pH值至中性;②碱破坏:加1 mol/L氢氧化钠溶液2 ml,室温放置20 min,取出,立即加1 mol/L盐酸溶液调pH值至中性;③氧化破坏:加30%过氧化氢溶液0.5 ml,室温放置20 min;④加热破坏:置105 ℃烤箱中加热2 h;⑤光照破坏:强光4 000 lx照射48 h(距光源约5 cm高度);⑥紫外光照破坏:紫外灯(254 nm)照射6 h(距光源约15 cm高度)。取上述样品依法操作,加0.01 mol/L HCl溶液稀释至刻度,摇匀,精密量取10 μl注入液相色谱仪,记录色谱图(见图2)。结果表明:杂质峰之间、杂质与主峰之间均能分离良好,本方法专属性较好。
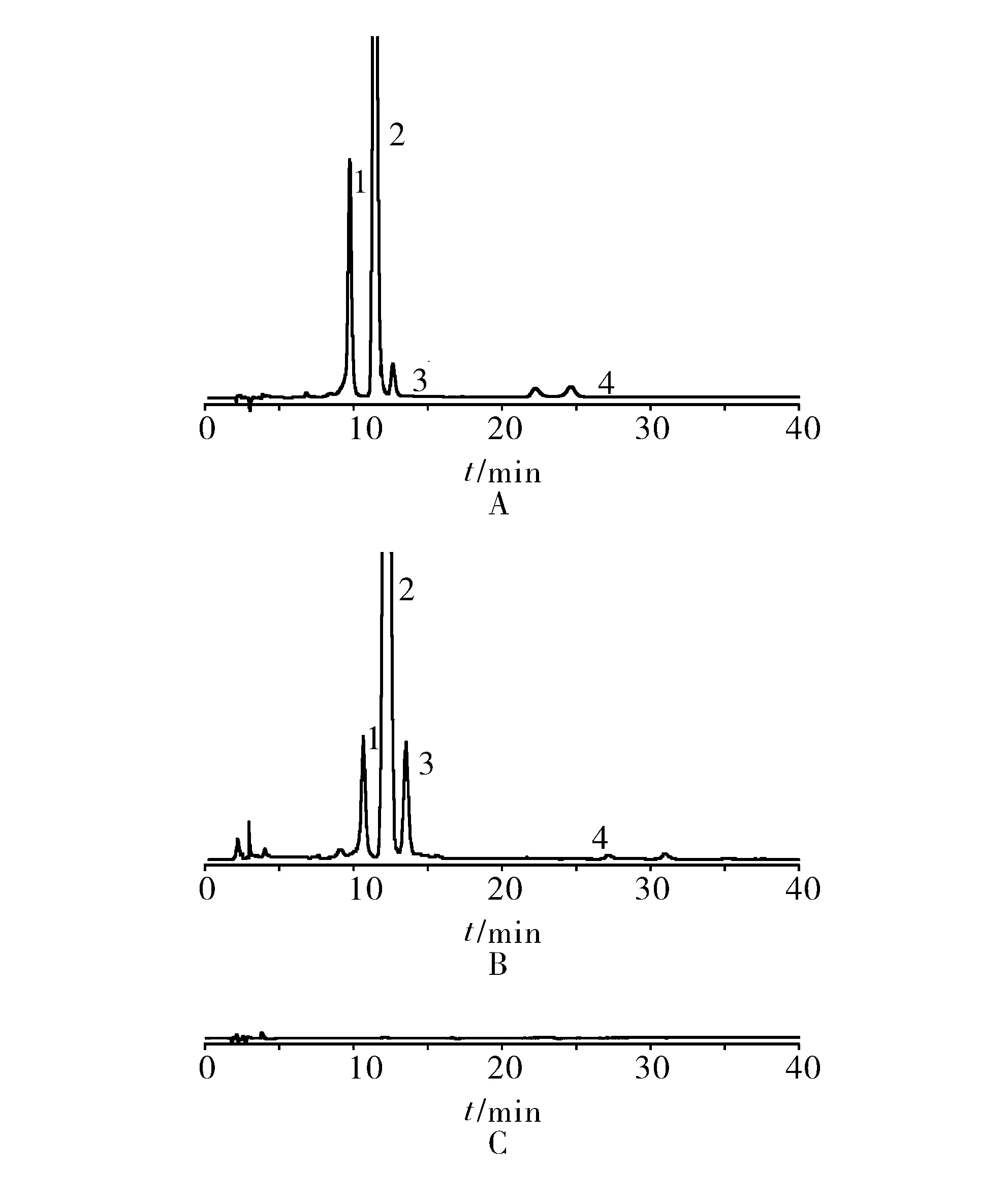
1. 4-差向四环素 2. 土霉素
2.5 最小检出限 用逐步稀释法,按信噪比3∶1计算,该方法的最小检测限为0.1 μg/ml,最小定量限为
0.2 μg/ml。
2.6 线性范围 取土霉素供试品(批号T3-11314417-3)加0.01 mol/L的盐酸溶液定量制成每1 ml中含50 μg的溶液,分别精密量取适量,加0.01 mol/L的盐酸溶液定量制成每1 ml中含0.25、2.5、5、10和15 μg的溶液。依法测定,以峰面积对浓度进行线性回归,回归方程为:Y=12 444X-494.26(r=0.999 95),结果在0.25~15 μg/ml范围内线性关系良好。
2.7 稳定性试验 取样品测定项下供试品溶液(批号T3-11314417-3)分别于室温放置0、1、2、4、6、8和24 h后进行测定,结果RSD为1.61%,表明供试品溶液室温放置24 h稳定。
2.8 有关物质的相关性 本方法进行了相关性考查试验,供试品溶液配制的称重在25~75 mg时,与有关物质测定之间有良好的相关性。
2.9 方法的粗放度 本方法用不同型号色谱柱测定同批样品(批号T3-11314417-3)有关物质,① Agilent XDB-C18柱(250 mm×4.6 mm,5 μm)、②Ultimate XB-C18柱(250 mm×4.6 mm,5 μm)、③Syncronis C18柱(250 mm×4.6 mm,5 μm),在相同的色谱条件下,测定结果基本一致,本方法耐用性良好,可以作为控制土霉素质量的有效手段。见表1和表2。
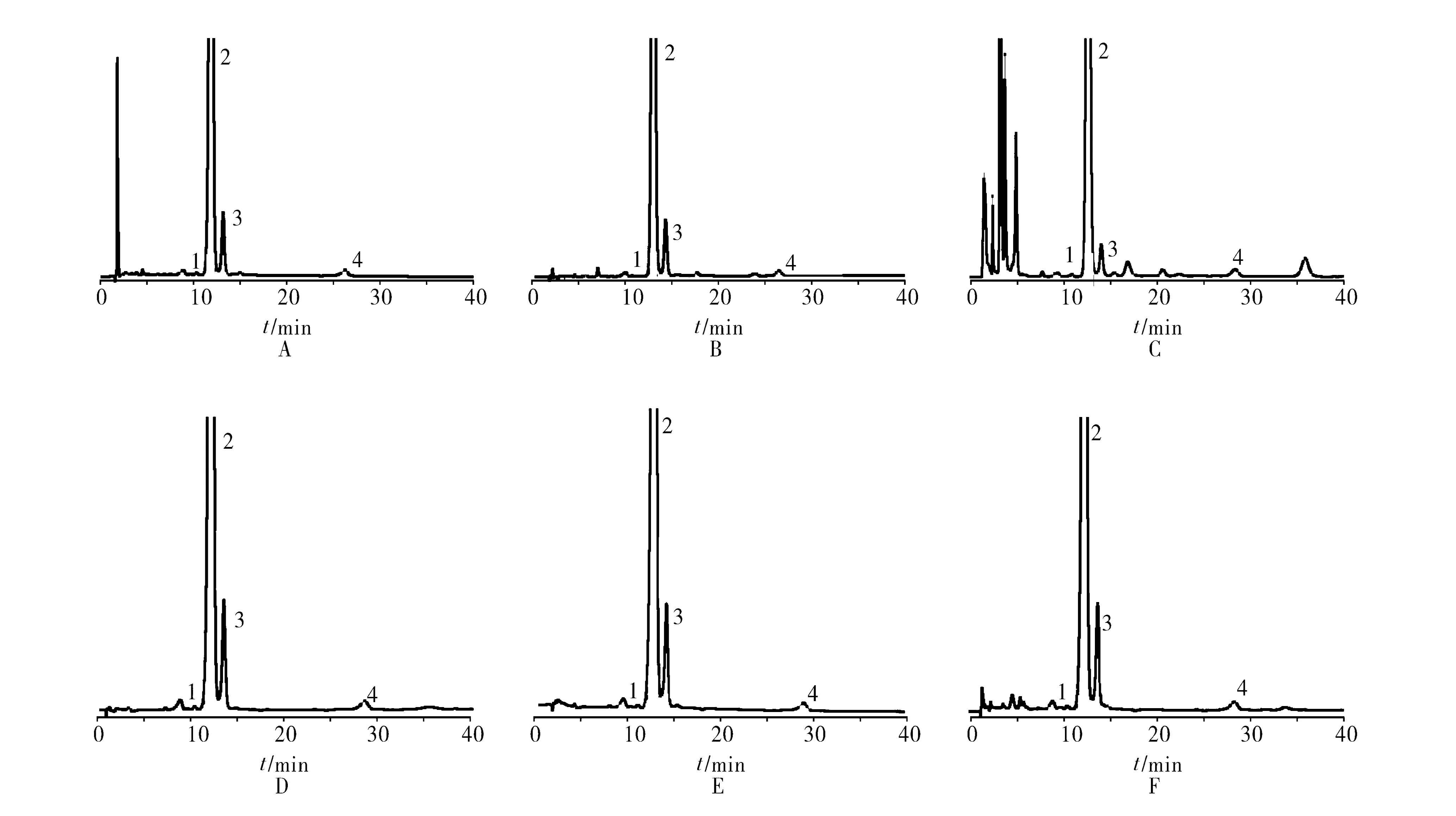
1. 4-差向四环素 2. 土霉素 3. 2-乙酰-2-去酰胺土霉素 4. 四环素
2.10 有关物质的测定 取“2.2.1”和“2.2.2”项下的供试品溶液和对照溶液、 “2.3” 项下系统适用性试验溶液。取对照溶液10 μl注入液相色谱仪,其峰能检出(即信噪比大于10)。再精密量取供试品溶液和对照溶液各10 μl分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍,供试品溶液色谱图中如有杂质峰, 2-乙酰-2-去酰胺土霉素杂质峰面积不得大于对照溶液主峰面积的1.75倍(3.5%),其他各杂质峰峰面积的和不得大于对照溶液主峰面积(2.0%)。三批样品测定结果见表3。
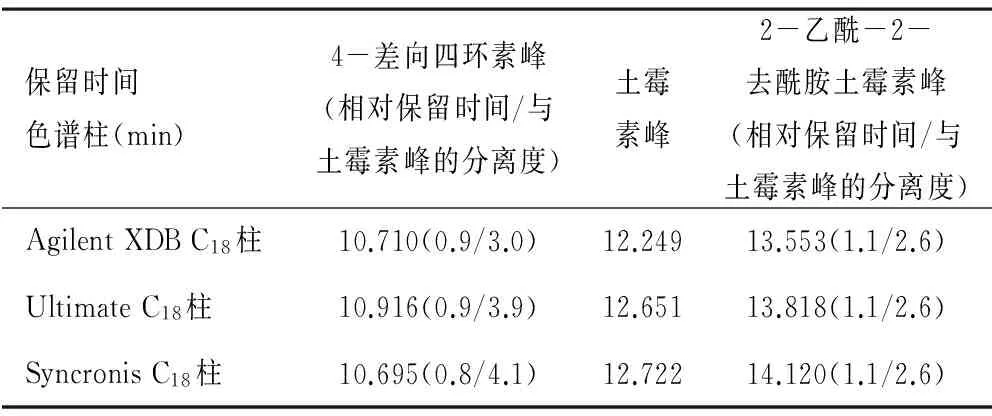
表1 分离度测试溶液
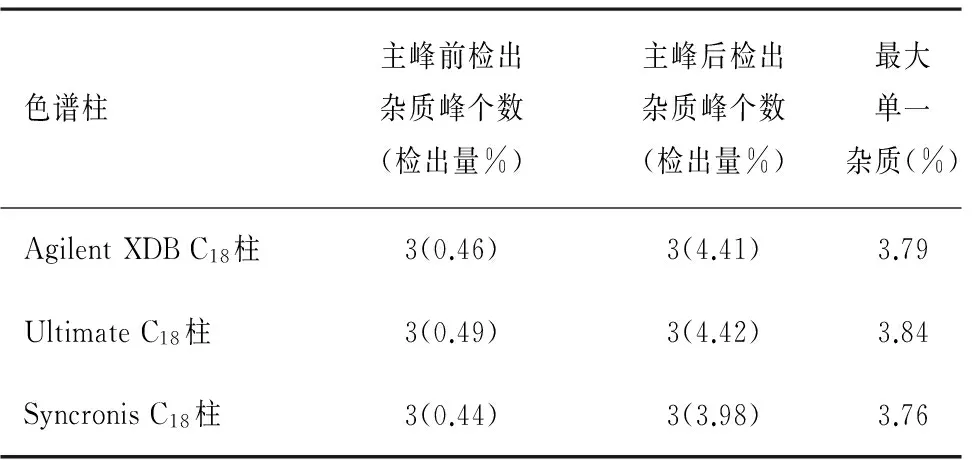
表2 样品测定

表3 有关物质检查测定结果
3 讨论
3.1 因土霉素破坏性试验难以控制,参考国内外相关资料[3],土霉素的有关物质采用主要杂质对照品定位来控制。现已定位的杂质有:4-差向土霉素、4-差向四环素、四环素和2-乙酰-2-去酰胺土霉素(土霉素自身含的杂质成分)。四环素和4-差向四环素的杂质对照品均由中国药品生物制品检定所提供。4-差向土霉素杂质对照品由厂家提供。而2-乙酰-2-去酰胺土霉素的杂质,就是土霉素中的最大单一杂质(参照《中国药典》2010版二部盐酸土霉素标准而定),2-乙酰-2-去酰胺土霉素与土霉素主峰的相对保留时间约为1.1。未定位的杂质有:α和β-阿扑土霉素。因为目前尚无纯的α和β-阿扑土霉素杂质对照品提供;且以厂家提供的α和β-阿扑土霉素的杂质溶液,在分析条件下显现微量、峰形差且重现性不好而不能确定,既然α和β-阿扑土霉素杂质无法定位且微量,因此,如果检品中出现α和β-阿扑土霉素的杂质峰就按一般杂质检查,不另外再做其他研究。
3.2 由相关资料得出,各杂质校正因子为:2-乙酰-2-去酰胺土霉素斜率/盐酸土霉素=0.92;盐酸四环素斜率/盐酸土霉素=1.01;其校正系数均在0.8~1.1之间,因此,无需采用杂质校正因子。所以,土霉素也采用不加杂质校正因子,以自身对照作为有关物质检查的方法。
3.3 本方法是采用高效液相色谱法来测定有关物质,其结果可靠,经方法学验证,此方法专属性强、灵敏度高、准确度和重复性好,可作为土霉素的有关物质的检测方法。
1 国际药典[S].2011:1-3
2 中国药典[S]. 二部.2010:635-636
3 英国药典[S].2011:1635-1636,3078-3079
2014-09-19
R927.11
A
1006-5687(2015)02-0014-03
