乳腺粒细胞肉瘤1例报告并文献复习
2015-02-15高宇哲贾琦陈华建
高宇哲 贾琦 陈华建
(贵州省人民医院医院乳腺外科,贵州 贵阳550002)
粒细胞肉瘤(granulocytic sarcoma,GS)是发生于髓外由未成熟髓系细胞构成的局限性恶性肿瘤。自1970年起共报道乳腺粒细胞肉瘤30余例[1],易误诊。本文总结我院收治的1例乳腺粒细胞肉瘤临床资料,并复习相关文献,旨在提高临床医师对本病的认识。
1 资料与方法
1.1 临床资料 患者女性,24岁,因“发现右乳包块1个月”于2013年10月23日入院。患者于1个月前无意间发现右乳外下方有一包块,约鸽蛋大小,不伴疼痛,无乳头溢血、溢液,无发热、乏力、盗汗。自发病以来包块未见明显变化。既往1年前曾行剖腹产术。月经规律,经量中等,无痛经,G2P1,流产1次。体检示双乳对称,未见乳头偏斜、内陷,乳房皮肤无红肿及破溃,右乳外下象限8点距乳晕1cm处可扪及一约2.5cm×2.0cm大小包块,质地较硬,类圆形,界清,表面光滑,活动度一般,无触痛及波动感,与皮肤及胸大肌无粘连,无乳头溢液,右腋下未扪及肿大淋巴结。左乳及左腋下未见异常。辅助检查:B超示右乳外下象限探及一实性包块,约2.3cm×1.4cm大小,椭圆形,未见包膜,边界清,低回声,不均质,CDFI示条状血流信号,腋窝未探及肿大淋巴结。乳腺钼靶示右乳外侧皮下肿块,考虑良性病变可能性大,BI-RADS分级为2级。血常规未见异常。于2013年10月24日在局麻下行右乳包块切除活检术,术中见包块与周围腺体分界不清,无包膜,其外侧可扪及一稍小包块,性质相似,遂行两包块及周围腺体切除术。术中快速冰冻病理右乳A处及右乳B处均提示乳腺小细胞肿瘤,倾向恶性。
1.2 方法 手术切除标本经10%甲醛固定,常规脱水、包埋、切片。免疫组化采用EnVision法,按说明书操作,EnVision试剂盒及 MPO、CD34、CD68等抗体购于福建迈新生物有限公司。
2 结 果
2.1 巨检 右乳包块 A,大小2.5cm×2.5cm×1.5cm,切面呈灰绿色,与周围分界清。右乳包块B,直径约1cm,切面呈灰绿色,与周围组织分界清。
2.2 镜检 HE染色光镜下观察两块组织来源的切片均见肿瘤细胞呈片状、索条状列兵样排列,弥漫分布,中等大小,形态单一,弥漫片状分布,细胞间可见较多嗜酸性粒细胞(见图1)。

图1 瘤细胞中等大小,形态一致(HE,×100)
2.3 免疫组化染色 瘤细胞抗髓过氧化物酶(MPO)、CD68、CD34、CD117、Vimentin均(+)(见图2~4),LCA(±)、Ki-67(40%+),EMA、Mammaglobin、CD7、Lysozyme、CD3、CD20、CD235a、CD61、CK8/18、CD79a、CDl9均(-)。病理诊断:右侧乳腺粒细胞肉瘤。

图2 瘤细胞MPO阳性表达(免疫组化,×400)
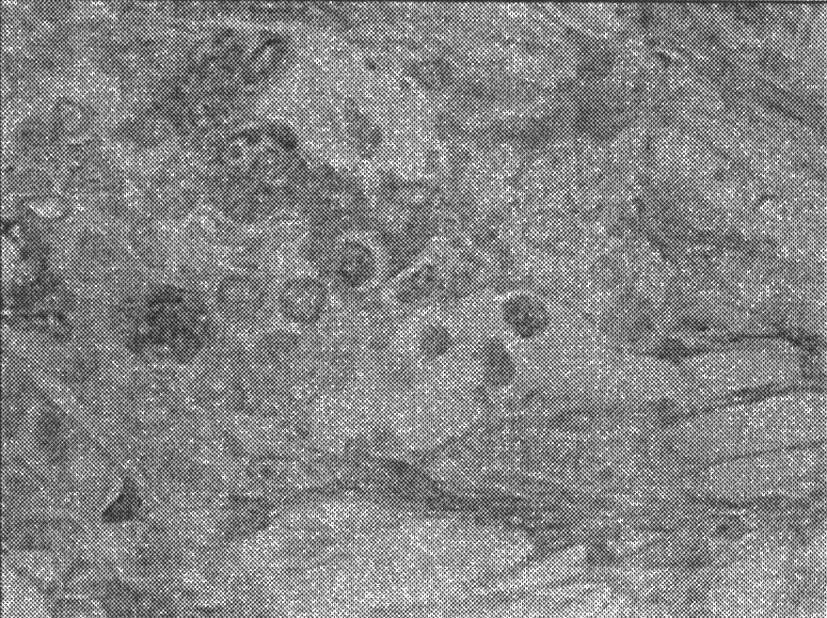
图3 瘤细胞CD68阳性表达(免疫组化,×400)

图4 瘤细胞CD34阳性表达(免疫组化,×400)
2.4 骨髓检查 术后据病理诊断完善骨髓检查,提示骨髓增生明显活跃,粒系高度增生,原始阶段比例轻度增高(原始粒细胞2%,早幼粒细胞4%),少数异常幼粒细胞,少数异常嗜酸粒细胞,红系百分率重度减少,形态正常,淋巴、单核、组织细胞、浆细胞正常,血小板易见。临床诊断:粒细胞白血病。
2.5 治疗及随访 局部乳腺包块切除后接受全身化疗DA方案(柔红霉素+阿糖胞苷)。随访6个月,乳腺未发现肿块,外周血及骨髓检查正常。
3 讨 论
GS是最常见的髓系肉瘤(myeloid sarcoma,MS),由原始粒细胞或不成熟粒细胞组成的髓细胞在髓外增生和浸润形成,因瘤组织呈绿色故又称绿色瘤。GS包括局部孤立性GS即非白血病性GS和白血病髓外浸润GS即白血病性GS。GS可累及任何部位,常见部位是淋巴结、皮肤,其它好发部位是骨、中枢神经系统、子宫和卵巢等,累及乳腺者少见。3.1 临床特点 乳腺GS发病年龄16~72岁,平均年龄38.4岁,好发于青壮年,大部分患者因偶然发现乳腺无痛性肿块就诊,一般无乳头溢液和乳头凹陷等表现,临床表现缺乏特异性。诊断前多无急性髓性白血病(acute myeloid leukemia,AML)病史。本例患者就是无意间发现乳腺肿块就诊,影像学检测无特征性表现,与文献报道一致。乳腺的GS大多伴发AML,也可发生于慢性粒细胞白血病急变前期或骨髓增生异常综合征转化期,少数乳腺孤立性GS可先于髓系肿瘤发生[2]。本例患者外周血检测未见异常,因病理提示乳腺GS后进一步行骨髓检查发现粒细胞白血病。总结经验,对于粒细胞肉瘤以乳腺包块为首发症状者,若外周血涂片未提示急性髓细胞白血病,需进一步行骨髓涂片,必要时完善染色体及融合基因检测,以明确是否存在AML。
3.2 病理特点 乳腺GS临床表现缺乏特异性,镜下形态易和其它小细胞肿瘤混淆,易误诊。诊断及鉴别诊断主要依靠病理组织学检查。病理组织学诊断依据包括形态学改变和免疫组织化学检测。形态学改变主要表现为:(1)局部占位性病变,大体标本切面呈绿色;(2)光镜下观察见瘤细胞中等大小,形态单一,大小一致,呈弥漫性增生和浸润。免疫组织化学检测是诊断和鉴别诊断的重要手段。乳腺GS至少表达一种以上髓系相关抗原,如MPO、溶菌酶(1ysozyme)、CD34、CD43、CD68、CD45、CD117等,其中MPO、CD68、lysozyme的敏感性和特异性均较高。因MPO对髓系细胞的高敏感性和特异性,故被认为是诊断GS的特异性抗原标记物。CD68可表达于粒系和单核细胞系中,是单核细胞的特异性标记,在 MS中的阳性率为72.5%~93%。lysozyme主要表达于粒系和单核系细胞浆,是髓细胞最敏感的标志物之一,阳性率达60%~93%,是鉴别GS和淋巴瘤的一个重要指标,但由于人体内很多组织都含有溶菌酶,故其特异性低于MPO。CD34是造血干细胞、血管内皮细胞和树突状细胞的标记,可特异性标志造血干细胞,但仅1/3的GS患者呈阳性表达[3],其它辅助诊断的指标有CD117、CD13等。目前普遍认为,一组抗体的联合检测更有助于诊断。本例患者术中快速冰冻切片曾考虑乳腺小细胞恶性肿瘤可能,但术后免疫组化明确诊断为粒细胞肉瘤,故对于乳腺GS的诊断和鉴别诊断应结合形态学与免疫表型结果进行综合分析。
3.3 治疗和预后 乳腺GS主要治疗措施包括手术切除、化疗、局部放疗和干细胞移植。研究认为即使临床上仅有局部乳腺肿块,无白血病表现,仍应按AML进行全身化疗和/或放疗[3]。联合化疗方案治疗GS优于单纯手术切除及局部放疗[4]。首选的化疗方案是蒽环类联合阿糖胞苷为基础的方案。虽然放疗对部分患者有效,但不能延缓孤立性GS向AML转化,也不能提高长期缓解率。从1991年首次应用异基因干细胞移植治疗回肠GS开始,近年来不断有文献报道干细胞移植技术在GS中的应用。Chevallier等[5]的研究提示接受异基因造血干细胞移植的GS患者5年生存率为48%,无白血病生存率为36%,高于非干细胞移植者。但另一个回顾性分析[6]却发现干细胞移植患者生存期无明显延长。因此,干细胞移植是否能延长GS患者生存期有待大样本多中心研究。
GS预后差,平均生存期为2.5~22个月,但也有部分患者通过化疗可以得到长时间缓解。Garcia等[7]报道2例完全缓解达10年之久,其中1例还曾2次复发,通过化疗完全缓解,长达31年仍存活。本例患者确诊后除进行局部乳腺肿块切除外,还按AML采用DA方案进行全身化疗,随访6个月,乳腺无肿块,外周血及骨髓涂片未见异常。
总之,乳腺GS临床表现缺乏特异性,易误诊,病理组织形态改变和免疫组化染色是确诊的主要手段,早期确诊和早期全身化疗是提高生存率的关键。
[1] 郭庆,王彩霞,陆珍凤,等.乳腺粒细胞肉瘤3例临床病理分析[J].诊断病理学杂志,2013,20(1):13-16.
[2] Cui Y,Zhou JL,Wu JH,et al.Synchronous granulocytic sarcoma of the breast and spine:a case report and review of the literature[J].Chin Med J,2008,121(18):1854-1856.
[3] Dohner H,Estey EH,Amadori S,et al.Diagnosis and management of acute myeloid leukemia in adults:recommendations from an international expert panel on behalf of the European Leukemia Net[J].Blood,2010,115(3):53-474.
[4] Delporte F,Voorhoopf LJ,Lodewyck T,et al.Primary granulocytic sarcoma of the breast:a case report and review of the literature[J].Eur J Gynaecol Oncol,2011,32(4):425-438.
[5] Chevallier P,Mohty M,Lioure B.Allogeneic hematopoietic stem-cell transplantation for myeloid sarcoma,a retrospective study from the SFGM-TC[J].J Clin Oncol,2008,26(30):4940-4943.
[6] Tsung-Yu Lan,Dong-Tsamn Lin,Hwei-Fang Tien,et al.Prognostic factors of treatment outcomes in patients with granulocytic sarcoma[J].Acta Haematol,2009,122(4):238-246.
[7] Garcia MG,Deavers MT,Knoblock RJ,et al.Myeloid sarcoma involving the gynecologic tract[J].Am J Clin Pathol,2006,125(5):783-790.
