黄芪浸膏质量标准的研究
2015-01-16李雯婷毛秀红
聂 晶, 苗 水, 李雯婷, 毛秀红, 季 申*
(1.上海医药工业研究院,上海200040;2.上海食品药品检验所,上海201203)
[质量]
黄芪浸膏质量标准的研究
聂 晶1,2, 苗 水2, 李雯婷2, 毛秀红2, 季 申2*
(1.上海医药工业研究院,上海200040;2.上海食品药品检验所,上海201203)
目的建立黄芪浸膏的质量标准。方法采用薄层色谱 (TLC)法对黄芪浸膏中的黄芪甲苷进行定性鉴别,应用HPLC法对黄芪甲苷和毛蕊异黄酮葡萄糖苷进行定量测定。结果薄层色谱斑点清晰,分离度良好;黄芪甲苷及毛蕊异黄酮葡萄糖苷在测定范围内均表现出良好的线性 (r>0.999),方法的平均回收率在97.5%~100.5%之间。结论定量的方法在Pheomenex Luna C18(0.46 cm×25 cm,5μm),Agilent Eclipse XDB-C18(0.46 cm×25 cm,5μm),Waters XBridgeShieldrp18(0.46 cm×15 cm,5μm)和Welch Xtimate C18(0.46 cm×15 cm,5μm)4根色谱柱具有良好的精密度和重现性,结果准确可靠。
黄芪浸膏;黄芪甲苷;毛蕊异黄酮葡萄糖苷;薄层色谱;高效液相色谱
药用黄芪为多年生草本植物豆科植物蒙古黄芪Astragalusmembranaceus(Fisch.)Bge.Var,mongholicus(Bge.)Hsiao或膜荚黄芪Astragalusmembranaceus(Fisch.)Bge.的干燥根,性温味甘,具有补气固表、敛汗固脱、托疮生肌、利水消肿之功效[1-5]。脑络通胶囊收载于卫生部药品标准中药成方制剂19册 (标准号:WS3-B-3667-98)[6],由黄芪浸膏、丹参浸膏、川芎浸膏等药味组成,主要用于补气活血,通经活络[7-8];其中黄芪浸膏是处方中的主要药味,是由黄芪经水提而制成的黄棕色至黑褐色的粉末或块状物。卫生部标准对脑络通胶囊中黄芪浸膏仅规定了制法[6],缺少具体质量标准控制方法,不能有效保证投料用黄芪浸膏的质量。黄芪化学成分众多,其中黄芪甲苷和毛蕊异黄酮葡萄糖苷对细胞免疫功能具有促进作用,是目前质量标准控制较多的指标性成分[9]。现有文献中关于这两种成分定量测定研究较多,其测定方法主要有高效液相色谱法、薄层色谱扫描法,鉴别方法一般采用传统的薄层分析方法[10-15]。《中国药典》2010年版对黄芪质量进行了全面的控制,采用对照药材和黄芪甲苷对照品制订了薄层鉴别方法,采用HPLC法对黄芪甲苷和毛蕊异黄酮葡萄糖苷进行了含量测定,此外还规定了水分、灰分等检查项[16]。为了更好地保障脑络通胶囊的质量,本实验参照黄芪的质量控制方法,对脑络通胶囊中的黄芪浸膏进行了系统的研究,制订了黄芪浸膏的质量标准。相较于 《中国药典》2010年版黄芪质量标准,本方法新增订了特征指纹图谱质量控制方法[17-19],更好地控制了黄芪浸膏中黄酮醇苷类化合物。
1 仪器与试药
1.1 仪器 Agilent 1100高效液相色谱仪(美国Agilent公司);蒸发光散射检测器(Varian 385-LC);Agilent1260型高效液相色谱仪(美国Agilent公司),DAD检测器;Sartorius BS 2202S电子天平。
1.2 药品及试剂 黄芪甲苷对照品 (批号0781-200210,供含量测定用)、毛蕊异黄酮葡萄糖苷对照品 (批号877-200001,供含量测定用)、黄芪对照药材 (批号120974-201311,供薄层鉴别用)均购自中国药品生物制品检定所。芒柄花苷、毛蕊异黄酮、芒柄花素供特征图谱定位用;乙腈为色谱纯(MERCK公司);其余均为分析纯,由中国医药(集团)上海化学试剂公司提供。
2 方法与结果
2.1 定性鉴别 (黄芪浸膏的TLC鉴别) 参照《中国药典》2010年版 “黄芪” 项下的规定[16],取黄芪对照药材2 g,置圆底烧瓶中,加入80%甲醇50 mL,加热回流2 h,放冷,滤过,滤液蒸干,残渣加水20mL使溶解,用水饱和的正丁醇振摇提取2次,每次20 mL,合并正丁醇液,用氨试液30 mL洗涤,弃去氨液,正丁醇液蒸干,残渣加甲醇1 mL使溶解,作为对照药材溶液。另取黄芪甲苷对照品,加甲醇制成每1 mL含0.5 mg的溶液,作为对照品溶液。照薄层色谱法 (《中国药典》2010年版一部附录ⅥB)试验,吸取 “2.2.3”项下的供试品溶液及上述对照药材、对照品溶液各5~10 μL,分别点于同一硅胶G薄层板上,以二氯甲烷-甲醇-水 (13∶7∶2)的下层溶液为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105°C加热至斑点显色清晰,分别置日光和紫外光灯(365 nm)下检视。结果显示供试品色谱中,在与黄芪对照药材色谱相应的位置上,日光下显相同颜色的主斑点,紫外光灯 (365 nm)下显相同颜色的荧光斑点;与黄芪甲苷对照品色谱相应的位置上,日光下显相同颜色的斑点,紫外光灯 (365 nm)下显相同颜色的荧光斑点。结果表明TLC分离效果良好 (见图1)。

图1 黄芪提取物的薄层色谱图(T:20℃RH:50%)Fig.1 TLC of Astragalus extract(T:20℃RH:50%)
2.2 黄芪甲苷测定
2.2.1 色谱条件 Pheomenex Luna C18色谱柱(0.46 cm×25 cm,5μm);以乙腈-水(32∶68)为流动相;蒸发光散射检测器;柱温30°C;体积流量1.0 mL/min;进样量为对照品溶液5μL,15 μL,供试品溶液20μL。
2.2.2 对照品溶液的制备 精密称取黄芪甲苷对照品适量,加甲醇制成每1mL含500μg的对照品溶液。
2.2.3 供试品溶液的制备 取本品约1.0 g,精密称定,置于圆底烧瓶中,精密加入80%甲醇50 mL,称定质量,加热回流2 h,放冷,再称定质量,用80%甲醇补足减失的质量,摇匀,滤过,精密量取续滤液25 mL,回收溶剂至干,残渣加水20 mL,微热使溶解,用水饱和的正丁醇振摇提取4次,每次20 mL,合并正丁醇液,用正丁醇饱和的氨试液充分洗涤2次,每次40 mL,弃去氨液,正丁醇液蒸干,残渣用甲醇溶解并转移至5 mL量瓶中,加甲醇至刻度,摇匀,即得。
2.2.4 测定方法 精密吸取对照品溶液5μL、15 μL,供试品溶液10~20μL,注入液相色谱仪,测定,以外标两点法对数方程计算,记录色谱图,见图2。

图2 黄芪提取物中黄芪甲苷对照品 (A)、供试品 (B)、空白样品 (C)测定的高效液相色谱图Fig.2 HPLC chromatogram s of astragaloside IV(A),sam p le(B),and blank sam p le(C)
2.2.5 线性关系的考察 精密吸取对照品溶液1、2、5、10、15、20μL注入液相色谱仪,记录峰面积,以ln进样量 (μg)为横坐标 (X),ln峰面积为纵坐标 (Y),绘制标准曲线,进行回归分析,得回归方程为Y=1.722 7X+2.155 6(r= 0.999 6)。结果表明,黄芪甲苷在 0.544μg~10.880μg范围内进样量的对数与峰面积的对数呈良好的线性关系。
2.2.6 精密度试验 精密吸取黄芪甲苷对照品溶液10μL,连续进样6次,记录峰面积,计算得RSD为2.3%。结果表明,仪器精密度良好。
2.2.7 重复性试验 取同一批样品 (批号13030)6份,分别按 “2.2.3”项下供试品溶液的制备方法处理后进样测定,计算得黄芪甲苷的RSD为3.6%,表明本方法的重复性良好。
2.2.8 稳定性试验 将 “2.2.7”项下第一份供试品溶液分别于0、4、8、12、16、20、24 h进样,记录峰面积,计算得对照品溶液和供试品溶液RSD分别为3.0%和2.6%。结果表明对照品溶液和供试品溶液在24 h内基本稳定。
2.2.9 加样回收率试验 取已测定含有量的供试品 (广州白云山光华制药股份有限公司,批号13030,含黄芪甲苷2.90 mg/g)0.5 g,精密称定,一式9份,置圆底烧瓶中,再按 “2.2.3”项下供试品溶液的制备方法处理,以3份为一组,各组分别精密加入黄芪甲苷对照品溶液 (质量浓度为3 mg/mL)0.4 m L、0.5 mL、0.6 mL,分别制得低、中、高3个质量浓度水平的加样供试品溶液各3份,进样测定。计算得平均回收率为99.7%,RSD为1.7% (n=9)。结果见表1。

表1 黄芪甲苷加样回收率试验结果(n=9)Tab.1 Results of recovery tests for astragaloside IV(n=9)
2.3 毛蕊异黄酮葡萄糖苷测定
2.3.1 色谱条件 ZOBAX C18色谱柱(Agilent公司,0.46 cm×15 cm,5μm);以乙腈为流动相A,水为流动相B,梯度洗脱 (0~25 min,5%→35%A,25~30 min,35%→80%A,30~35 min,80%A);柱温30°C;体积流量1.0 m L/min;检测波长为260 nm;进样量5μL。
2.3.2 对照品溶液的制备 精密称取毛蕊异黄酮葡萄糖苷对照品适量,加甲醇制成每1 mL含20 μg的对照品溶液。
2.3.3 供试品溶液的制备 取本品约1.0 g,精密称定,置于圆底烧瓶中,精密加入 50%甲醇50 m L,称定质量,加热回流1 h,放冷,再称定质量,用50%甲醇补足减失的质量,摇匀,用0.45μm微孔滤膜滤过,取续滤液,即得。
2.3.4 测定方法 精密吸取对照品溶液和供试品溶液各5μL,注入液相色谱仪,记录色谱图,见图3。

图3 黄芪提取物中毛蕊异黄酮葡萄糖苷对照品 (A)、供试品 (B)、空白样品 (C)测定的高效液相色谱图Fig.3 HPLC chromatogram s of calycosin-7-glucoside(A),test sam p le(B),and blank sam p le(C)
2.3.5 线性关系的考察 取毛蕊异黄酮葡萄糖苷对照品适量,加甲醇分别制成质量浓度为2.507 5 μg/mL、5.015μg/mL、10.03μg/mL、20.06 μg/mL、50.15μg/mL、100.30μg/mL、200.60 μg/mL的系列溶液,精密吸取系列溶液各5μL注入液相色谱仪,记录峰面积,以质量浓度 (μg/mL)为横坐标,峰面积为纵坐标,绘制标准曲线,进行回归分析,得回归方程为Y=18.254 5X+1.629 7(r=0.999 8)。结果表明,毛蕊异黄酮葡萄糖苷在2.507 5~200.60μg/mL范围内进样量与峰面积的对数呈良好的线性关系。
2.3.6 精密度试验 精密吸取毛蕊异黄酮葡萄糖苷对照品溶液 (含毛蕊异黄酮葡萄糖苷20.06 μg/mL)5μL,连续进样6次,记录峰面积,计算得RSD为0.3%。结果表明,仪器精密度良好。
2.3.7 重复性试验 取同一批样品 (批号:13030)6份,分别按 “2.3.3”项下供试品溶液的制备方法处理后进样测定,计算得毛蕊异黄酮葡萄糖苷含有量的RSD为1.8%,表明本方法的重复性良好。
2.3.8 稳定性试验 将 “2.3.7”项下第一份供试品溶液分别于0、2、4、8、12、16、20、24 h进样,记录峰面积,计算得对照品溶液和供试品溶液RSD均为1.3%。结果表明毛蕊异黄酮葡萄糖苷在24 h内基本稳定。
2.3.9 加样回收率试验 取已测定含有量的供试品 (广州白云山光华制药股份有限公司,批号13030,含毛蕊异黄酮葡萄糖苷0.84 mg/g)0.5 g,精密称定,一式9份,置圆底烧瓶中,再按“2.3.3”项下供试品溶液的制备方法处理,以3份为一组,各组分别精密加入毛蕊异黄酮葡萄糖苷对照品溶液(质量浓度为1.003 mg/m L)0.4 m L、0.5mL、0.6mL,分别制得低、中、高3个质量浓度水平的加样供试品溶液各3份,进样测定。计算得平均回收率为98.0%,RSD为1.1% (n=9)。结果见表2。

表2 毛蕊异黄酮葡萄糖苷加样回收率试验结果 (n=9)Tab.2 Results of recovery tests for calycosin-7-glucoside (n=9)
2.4 特征图谱 记录 “2.3.4”项下35 min内的色谱图。供试品特征图谱中应呈现4个特征峰,与毛蕊异黄酮葡萄糖苷参照物对应的峰为S峰,计算各特征峰与S峰的相对保留时间,应在规定值的± 10%范围之内。相对保留时间规定值为:1.35(峰1)、1.54(峰2)和1.72(峰3)。见图4。
2.4.1 色谱条件 同“2.3.1”项。
2.4.2 对照品溶液的制备 取毛蕊异黄酮葡萄糖苷、芒柄花苷、毛蕊异黄酮和芒柄花素对照品适量,加甲醇制成每1 mL含20μg的对照品溶液。
2.4.3 供试品溶液的制备 取 “2.3.3”项下的供试品溶液,即得。

图4 HPLC对照特征图谱Fig.4 HPLC matched chromatography for the reference fingerprint
2.4.4 重复性试验 取 “2.3.7”项下重复性考察的样品,进样分析,记录特征图谱,结果表明各供试品溶液特征图谱中均呈现4个特征峰,以毛蕊异黄酮葡萄糖苷为参照物S峰,计算各特征峰与S峰的相对保留时间,结果表明各特征峰均在规定值的±10%范围之内。
2.4.5 稳定性试验 取供试品溶液 (批号13030)分别于0、2、7、9、12、16、20、25 h进样,记录峰面积,计算得毛蕊异黄酮葡萄糖苷、芒柄花苷、毛蕊异黄酮和芒柄花素的RSD分别为1.8%、2.9%、0.5%和0.5%。结果表明供试品溶液在25 h内基本稳定。
2.4.6 耐用性试验 由于不同厂家不同牌号的色谱柱存在填料及性能上的差异,为考察拟订方法的可行性及通用性,对(1)Pheomenex Luna C18(Pheomenex,0.46 cm×25 cm,5μm)(2)Agilent Eclipse XDB-C18(Agilent,0.46 cm×25 cm,5 μm)(3)Waters XBridgeShieldrp18(Waters,0.46 cm×15 cm,5μm)(4)Welch Xtimate C18(月旭,0.46 cm×15 cm,5μm)4根色谱柱进行了考察,计算相对保留时间与质量标准正文规定值的偏差。结果表明,不同色谱柱得到的供试品特征色谱基本一致,相对保留时间与规定偏差均小于10%,表明拟定方法通用性较广。
2.4.7 特征峰保留时间测定 取8批供试品溶液进样分析,记录特征峰的保留时间,计算相对保留时间及平均值,结果见表3。
2.5 样品测定 取8批样品,按供试品溶液制备方法进行制备,按上述色谱条件测定峰面积,计算,结果见表4。
3 讨论
3.1 特征图谱 黄芪中主要含有氨基酸、黄芪皂苷类与黄酮醇苷类等化合物,由于氨基酸测定方法需要衍生,步骤繁琐、重复性差,黄芪皂苷类化合物测定需要采用蒸发光散射检测器、灵敏度低,反应的信息量少,故上述二类化合物暂不考虑订入特征图谱,故本研究重点在于黄酮醇苷类化合物的特征图谱研究,主要针对报道中的几种化合物,建立特征图谱。除文中提到的几种化合物外,8批样品在4~10 min保留时间内有部分共有峰,但此类化合物由于极性较低,在不同品牌色谱柱上峰形不一致,保留时间差别也较大,另外此部分色谱峰峰面积较小,考虑暂不将此类色谱峰订入质量标准,有待进行进一步的物质基础研究,明确物质基础后,再行将相关化合物订入特征图谱。
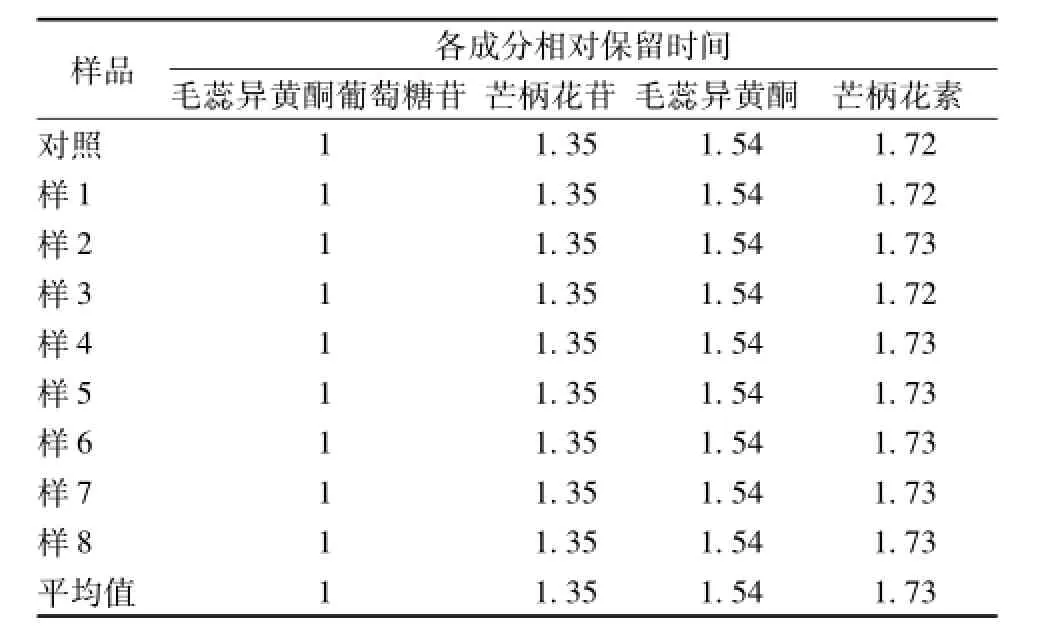
表3 特征图谱中4种成分相对保留时间Tab.3 Relative retention time of 4 components in characteristic spectria

表4 样品测定结果Tab.4 Test results of sam p les
3.2 黄芪甲苷测定研究
3.2.1 黄芪甲苷提取方式的考察 本实验考察了50%甲醇、甲醇超声30 min或加热回流30 min时的提取效率,结果表明采用不同溶剂时,加热回流的提取效率均高于超声提取,故选择回流提取作为供试品的提取方式。
3.2.2 黄芪甲苷提取溶剂的考察 本实验考察了采用水、30%甲醇、50%甲醇、80%甲醇及甲醇等不同溶剂的回流提取,结果表明以80%甲醇作为提取溶剂时,黄芪甲苷的提取效率最高,故选择80%甲醇作为提取溶剂。
3.2.3 黄芪甲苷回流时间的考察 本实验考察了0.5、1、2、3、4 h不同加热回流时间下,黄芪甲苷的提取效率。结果表明随回流时间的延长,黄芪甲苷的提取效率呈增加趋势,增大至一定数值后基本稳定,回流2 h可基本提取完全,故确定加热回流时间为2 h。
3.2.4 黄芪甲苷提取和洗涤次数的考察 本实验考察了正丁醇提取次数及氨试液洗涤次数对测定的影响,结果表明采用水饱和正丁醇提取4次、氨试液洗涤2次时,即可达到理想的提取净化效果。
3.3 毛蕊异黄酮葡萄糖苷测定研究
3.3.1 毛蕊异黄酮葡萄糖苷提取溶剂的考察 本实验考察了采用水、30%甲醇、50%甲醇、80%甲醇等不同溶剂的回流提取,结果表明以50%甲醇作为提取溶剂时,毛蕊异黄酮葡萄糖苷的提取效率最高,故选择50%甲醇作为提取溶剂。
3.3.2 毛蕊异黄酮葡萄糖苷回流时间的考察 本实验考察了0.5、1、1.5、2 h不同加热回流时间下,毛蕊异黄酮葡萄糖苷的提取效率。结果表明随回流1 h即可完全提取出毛蕊异黄酮葡萄糖苷,故确定提取时间为1 h。
[1]张 蔷,高文远,满淑丽.黄芪中有效成分药理活性的研究进展[J].中国中药杂志,2012,37(21):3203-3207.
[2]王春怡,叶雪兰,李卫民,等.黄芪总皂苷提取物的质量标准研究[J].时珍国医国药,2012,23(1):94-96.
[3]陈国辉,黄文凤.黄芪的化学成分及药理作用研究进展[J].中国新药杂志,2008,17(17):1482-1485.
[4]刘浩文,刘嘉仪,杨妙荣,等.黄芪药材中黄芪甲苷含量测定的两种方法的比较研究[J].中国新药与临床药理,2011,22(6):659-662.
[5]何 娟,何秀英.黄芪四物汤颗粒的质量标准研究[J].中国中医药科技,2009,16(3):217-219.
[6]WS3-B-3667-98,卫生部药品标准:中药成方制剂第19册[S].
[7]何选林,王群英.RP-HPLC测定脑络通胶囊中原儿茶醛、阿魏酸、丹参酮IIA和盐酸托哌酮的含量[J].中成药,2011,33(1):61-65.
[8]黄 松,陶 艳,蒋东旭,等.脑络通胶囊质量标准的完善[J].中国药师,2008,11(2):142-145.
[9]姚雪莲,裴彩云,王宗权.不同产地、不同采收期黄芪药材及饮片中毛蕊异黄酮葡萄糖苷及芒柄花素含量测定[J].药物分析杂志,2012,32(5):797-805.
[10]覃洁萍,姚 蓉,李 芸,等.HPLC-ELSD同时测定复方扶芳藤胶囊中卫矛醇和黄芪甲苷的含量[J].中成药,2008,30(10):1468-1471.
[11]胡芳弟,赵健雄,封士兰,等.黄芪的高效液相色谱指纹图谱及主成分含量测定[J].中药材,2004,27(11):831-834.
[12]查建蓬,张嫡群,王云志.黄芪及其制剂质量控制方法研究进展[J].中成药,2006,28(6):875-878.
[13]熊泽,徐红霞,伟邵,等.养荣丸 (浓缩丸)质量标准研究[J].中成药,2010,32(6):1070-1073.
[14]宋成英,封加福.HPLC同时测定黄芪药材中毛蕊异黄酮葡萄糖苷和黄芪甲苷[J].中国实验方剂学杂志,2013,19(11):115-117.
[15]黄志勤,李洪亮,程齐来.HPLC测定黄芪药材中的毛蕊异黄酮葡萄糖苷[J].光谱实验室,2012,29(5):2736-2738.
[16]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:283.
[17]梁 瑾,刘小花,远 任,等.黄芪药材的HPLC-DADELSD指纹图谱研究[J].中国实验方剂学杂志,2012,18(7):70-74.
[18]黄月纯,尹 雪,魏 刚.玉屏风汤剂的HPLC指纹图谱研究[J].中成药,2008,30(10):1405-1408.
[19]张庆芝,吴晓俊,刘 涤,等.黄芪及其民间习用品DNA指纹图谱和有效成分含量的比较[J].中国药学杂志,2005,40(6):457-459.
Quality standard for Astragali Radix aqueous extract
NIE Jing1,2, MIAO Shui2, LIWen-ting2, MAO Xiu-hong2, JIShen2*
(1.Shanghai Institute of Pharmaceutical Industry,Shanghai200040,China;2.Shanghai Institute for Food and Drug Control,Shanghai 201203,China)
AIMTo establish the quality standard for Astragali Radix aqueous extract.M ETHODSTLC was adopted for the qualitative identification of astragaloside IV.HPLCwas used to determine the contents of astragaloside IV and calycosin-7-glucoside.RESULTSTLC spotswere clear and well separated without interference. The compounds showed a good linearity(r>0.999)in a determination range.The average recovery was between 97.5%-100.5%.CONCLUSIONThe method can repeat itself on four columns,including Pheomenex Luna C18(0.46 cm×25 cm,5μm),Agilent Eclipse XDB-C18(0.46 cm×25 cm,5μm),Waters XBridgeShieldrp18(0.46 cm×15 cm,5μm),and Welch Xtimate C18(0.46 cm×15 cm,5μm)with good precision and accuracy.
Astragali Radix aqueous extract;astragaloside IV;calycosin-7-glucoside;TLC;HPLC
R927.2
:A
:1001-1528(2015)07-1471-06
10.3969/j.issn.1001-1528.2015.07.017
2015-02-09
聂 晶(1989—),女,硕士生。E-mail:jingxin1205@126.com
*通信作者:季 申 (1968—),女,博士生导师,从事中药质量标准及中药安全性研究。Tel:(021)50798196,E-mail:jishen2013 @163.com
