快速响应大孔聚(N-异丙基丙烯酰胺-co-甲基丙烯酸)水凝胶的制备及性能研究
2015-01-12郑丝柳周颖梅
徐 阳,郑丝柳,王 帅,周颖梅
(徐州工程学院化学化工学院,江苏 徐州 221018)
快速响应大孔聚(N-异丙基丙烯酰胺-co-甲基丙烯酸)水凝胶的制备及性能研究
徐 阳,郑丝柳,王 帅,周颖梅
(徐州工程学院化学化工学院,江苏 徐州 221018)
在不同浓度的氯化钠水溶液中,成功制备了聚(N-异丙基丙烯酰胺-co-甲基丙烯酸)[P(NIPAM -co-MAA)]水凝胶,用红外光谱仪(FT-IR)、扫描电镜(SEM)、测溶胀比对凝胶性能进行了表征,讨论了凝胶内部微观结构的形成机理,以及它们对凝胶性能的影响。发现当氯化钠浓度大于0.3 mol·L-1时凝胶内部形成孔洞网络结构,随着其浓度的增加孔洞网络结构越来越明显,同时凝胶表现出较快的响应速率。
N-异丙基丙烯酰胺;甲基丙烯酸;微观结构;响应速率
敏感性水凝胶(又称智能水凝胶)是一种亲水性高分子交联网络,它能够感知外界环境的细微变化与刺激(如温度、pH、离子强度、光、电场和磁场等),并通过自身体积的膨胀和收缩而发生不连续的体积相转变来响应外界刺激,并具有可逆性[1-2]。根据需要,近年来开发了多重敏感性水凝胶,而研究最多的是双重敏感性水凝胶。因温度和pH值是生理、生物和化学系统中的两个重要因素[3],所以pH/温度敏感水凝胶的研究最为活跃。它在药物缓释[4]、酶反应控制[5]、物质分离提纯等领域有广泛的潜在应用价值。但是常规水凝胶存在一些缺点,如响应速率慢、机械性能差等,大大限制了水凝胶的应用,因此解决水凝胶的响应速率成为当前高分子凝胶研究和开发的一个重要课题。研究发现凝胶内部微观结构对于其响应性有着显著的影响[6]。通常是使凝胶的内部形成孔状结构,以此来提高它的相应速率。Zhang[7]和Cheng等[8]分别以水与四氢呋喃的混合溶剂、NaCl水溶液为反应介质,合成了大孔PNIPAM水凝胶,研究了反应介质的组成对凝胶性能的影响。Tuncer Caykara等[9]以不同分子量的聚乙二醇(PEG)为成孔剂,采用辐射聚合的方法制备了大孔的聚丙烯酰胺水凝胶,发现PEG分子量和浓度越大,制备的凝胶的溶胀速率越快。Liu等[10]以不同浓度的NaCl水溶液为聚合介质,采用紫外辐射的方法合成了一系列聚甲基丙烯酸羟乙酯[p(HEMA)]水凝胶,发现随着聚合介质中NaCl浓度的增加,p(HEMA)水凝胶的孔隙率和在蒸馏水中的平衡溶胀比依次增加。
本文采用不同浓度的氯化钠溶液作为反应介质,以N,N’-亚甲基双丙烯酰胺(BIS)为交联剂,以过硫酸钾作为引发剂,室温下反应使NIPAM与单体MAA共聚。制备了温度与pH快速响应性聚(N-异丙基丙烯酰胺-co-甲基丙烯酸)[P(NIPAM-co-MAA)]水凝胶,考察不同浓度的氯化钠溶液对凝胶内部结构的影响。通过考察水凝胶的溶胀动力学、温敏性、pH敏感性,研究内部结构和凝胶响应性之间的关系,为制备快速响应性智能型凝胶提供依据。
1 实验
1.1 主要试剂与仪器
N-异丙基丙烯酰胺(NIPAM,AR),甲基丙烯酸(MAA,AR),过硫酸钾(KPS, AR),N,N’-亚甲基双丙烯酰胺(BIS,AR),其余试剂均为分析纯。实验用水为自制蒸馏水。
DZF6020型真空干燥箱,FA1004型电子天平,SYP-Ⅲ型玻璃恒温水浴,JSM-840型扫描电镜(SEM),AVATAR-360型傅里叶变换红外谱仪。
1.2 实验方法
1.2.1 P(NIPAM-co-MAA)水凝胶的制备
准确称取N-异丙基丙烯酰胺(NIPAM)0.625 g于5mL玻璃试管中,接着分别称取0.005g N,N’-亚甲基双丙烯酰胺(BIS)和0.0038g过硫酸钾(KPS)加入试管中,加1.5mL蒸馏水在25℃下完全溶解,加入配置好的氯化钠水溶液1.5mL,使溶液中总的氯化钠分别为0 mol·L-1、0.1 mol·L-1、0.3 mol·L-1、0.5 mol·L-1、0.6 mol·L-1、0.7 mol·L-1以及0.9 mol·L-1,分别标记为Gel 0、Gel 0.1、Gel 0.3、Gel 0.5、Gel 0.6、Gel 0.7、Gel 0.9,用微量进样器吸取丙烯酸(MAA)10μL,促进剂7.5μL 混合均匀并通入氮气大概5min充分除氧后,在室温下放置24h。取出凝胶,先用去离子水反复冲洗数遍,然后再将凝胶置于去离子水中浸泡,每隔24h换水1次,以除去未反应的杂质、氯化钠单体。4d后将凝胶切片,真空烘干,编号,置于干燥器中待用。
1.2.2 P(NIPAM-co-MAA)水凝胶的红外分析
取少量凝胶,在70℃的真空烘箱中充分干燥并研磨,用KBr压片,测定其在400~4000cm-1的FT-IR谱。
1.2.3 P(NIPAM-co-MAA)水凝胶的形态观察
为了防止凝胶样品在干燥过程中孔洞结构遭到破坏,观察不到其真实的形态,本文将凝胶于液氮中冷冻24h,然后低温真空干燥6h,最后取凝胶新鲜的断面喷金通SEM在20kV下观察其微观形貌。
1.2.4 P(NIPAM-co-MAA)水凝胶溶胀率测试
将恒温水浴设定为初始温度12℃,将切片溶胀平衡后的凝胶置于恒温水浴中,每隔60min升温1次,刚开始每次升高2℃,在接近33℃时,每次升高1℃。用滤纸拭干凝胶表面的水后称重,分别记下凝胶的质量。重复上述过程,直至凝胶质量变化很小为止。水凝胶的溶胀率SR由式(1)求得。
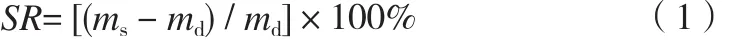
式中ms是不同温度下充分溶胀的水凝胶的质量,md是真空干燥后干凝胶的质量。
1.2.5 P(NIPAM-co-MAA)水凝胶退胀率测试
将在室温下达到溶胀平衡的样品投入温度60℃的恒温水中,每隔一定时间用滤纸拭干凝胶表面的水后称重1次,直至样品质量基本不变为止。水凝胶的退胀率WU由式(2)求得。
式中mt是时间t时水凝胶的质量,md是真空干燥后干凝胶的质量。
1.2.6 P(NIPAM-co-MAA)水凝胶pH敏感性测试
首先,用盐酸、冰乙酸、乙酸钠、氨水和氯化铵配置pH分别为2.0、4.0、9.0、12.0的缓冲溶液,其pH用pHS-25C数显酸度计测定并校准,用NaCl溶液将其离子强度统一调至0.10mol·kg-1,然后,取在20℃蒸馏水中溶胀平衡后体积大致相同的小块凝胶,分别放入上述pH缓冲溶液中,每隔12h取出,用湿的滤纸快速擦去其表面的水分并称重,直到恒重为止;最后,将其放入80℃真空烘箱中,干燥12h至恒重,并按照公式(1)计算其平衡溶胀比(SR)。
2 结果与讨论
2.1 P(NIPAM-co-MAA)水凝胶的制备
实验表明,P(NIPAM-co-MAA)水凝胶很容易生成,在室温下放置大概0.5h就能聚合成功。生成的凝胶颜色有差异,其中Gel 0、Gel 0.1、Gel 0.3凝胶是无色透明的,而Gel 0.5、Gel 0.6、Gel 0.7、Gel 0.9凝胶为白色不透明状。当以氯化钠水溶液作为反应介质时,氯化钠的浓度会使NIPA和MAA在溶液中的溶解度发生变化。虽然单体NlPA、MAA以及线形的p(NIPAM-co-MAA)都是水溶性的,但随着氯化钠浓度的增大,它们的溶解度降低,从而导致沉淀或盐析,形成了非均相。当氯化钠浓度小于0.3mol·L-1时,高分子链可以自由伸展,形成的凝胶能充分吸收水溶胀,所以呈现透明状。当氯化钠浓度大于0.3mol·L-1时,凝胶内高分子链得不到充分的伸展,被迫发生蜷曲,相互缠绕在一起,形成一个核。随着聚合与交联的进行,相分离持续发生,新核不断地出现,这些核的聚集导致凝胶变为白色不透明状,同时在凝胶内部生成不均匀的大孔网络结构[11]。
2.2 P(NIPAM-co-MAA)水凝胶的红外光谱分析
从图1可以看出,7个样品的红外图基本相同,表明它们具有相同的结构。1637.61cm-1处为酰胺Ⅰ带,是C=O的吸收峰;1560.28 cm-1是酰胺Ⅱ带-NH-的面内弯曲振动峰;2973 cm-1左右的峰是甲基和次甲基的C-H振动峰;1417 cm-1附近为C-H的不对称弯曲振动峰。1346 cm-1附近为-CH(CH3)2中双甲基的对称振动耦合分裂峰,再加上1130.75cm-1处的C-C骨架振动吸收峰,可以证明-CH(CH3)2的存在。1271.46 cm-1处为C-O的伸缩振动峰。由此说明该聚合物为N-异丙基丙稀酰胺与甲基丙稀酸的共聚物。

图1 P(NIPAM-co-MAA)水凝胶的红外光谱Fig. 1 FT-IR spectra of the P(NIPAM-co-MAA) hydrogels
2.3 P(NIPAM-co-MAA)水凝胶的微观形态
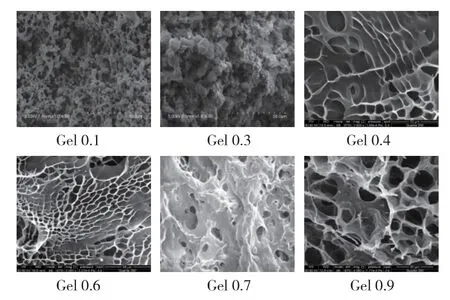
图2 P(NIPAM-co-MAA)水凝胶的电镜扫描照片Fig. 2 SEM images of the P(NIPAM-co-MAA) hydrogels
凝胶的微观形态如图2所示,Gel 0.1内部具有蜂窝状的微孔结构,这是因为,在常温下聚合时,自由水可以停留在凝胶的网络中,从而形成这种细密的蜂窝状结构[12]。Gel 0.3凝胶内部分子链发生蜷曲,相互缠绕在一起,形成突出的核。Gel 0.4内部表面开始出现不平的凹坑,孔洞开始形成;Gel 0.6内部出现的孔洞比较明显。Gel 0.8内部孔洞变大,Gel 0.9内部已经形成相互贯穿的孔洞网络结构。由此可以看出氯化钠溶液浓度对于凝胶分子的内部结构有着非常明显的影响,并且这种孔洞网络的形成为水分子提供了较大的接触面积和进出的通道,很大程度上减小了水分子在水凝胶中的扩散阻力,同时也为水分子提供了巨大的容纳空间,使凝胶的响应速率大大增加。
2.4 P(NIPAM-co-MAA)水凝胶的溶胀性能测试
图3是P(NIPAM-co-MAA)水凝胶的溶胀率曲线。由图3可知,以不同浓度的氯化钠溶液为聚合介质所制得的凝胶溶胀性能不同,但是它们都在43℃时发生体积突变。这是因为凝胶的LCST由化学组成决定,而NaCl水溶液仅充当反应介质,当凝胶形成后NaCl被洗掉,所以它们的化学组成相同因而具有相同的LCST。这与红外光谱分析的结果也是一致的。同时可以看出随着氯化钠溶液浓度增大,凝胶的SR也相应增大。结合凝胶的电镜扫描图可以得知,氯化钠的浓度增加使凝胶内部形成的孔洞结构越来越明显,更加有利于水分子的快速进出,所以溶胀速率也逐渐升高。

图3 P(NIPAM-co-MAA)水凝胶的溶胀率曲线Fig. 3 Swelling curves of the P(NIPAM-co-MAA) hydrogels
2.5 P(NIPAM-co-MAA)水凝胶的退胀性能测试
将在20℃蒸馏水中充分溶胀的凝胶转移到60℃的热水中,凝胶开始收缩并开始失水。随着溶剂浓度的增加凝胶的退溶胀速率加快,退溶胀率升高。当温度高于凝胶的LCST时,高分子链之间的氢键遭到破坏,疏水作用占主导,使凝胶网络收缩而发生退胀。对于大孔水凝胶来说因为其孔洞结构有利于内部自由水的快速失去,表现出很高的退胀率。
2.5 P(NIPAM-co-MAA)水凝胶的pH敏感性研究
图5是不同浓度下制得的凝胶在不同pH的缓冲溶液中浸泡24h后的溶胀情况。由图5可以看出,该类水凝胶具有较高的pH敏感性,在pH=2.0的缓冲溶液中凝胶的溶胀率很小,甚至不溶胀。这是因为在酸性缓冲溶液中,由于H+浓度较高,抑制了亲水基团-COOH和酰胺基(-CONH)的解离,所以水凝胶的亲水性变弱。当缓冲溶液pH值升高时,凝胶的溶胀率也逐渐升高。随着聚合介质中NaCl浓度的增加,凝胶对pH敏感性也逐渐增加。这是因为在溶胀时,具有大孔结构的水凝胶在同一pH值溶液中能表现出较大的平衡溶胀比。

图4 P(NIPAM-co-MAA)水凝胶在60℃下的退胀率曲线Fig. 4 Deswelling curves of the P(NIPAM-co-MAA) hydrogels at 60℃
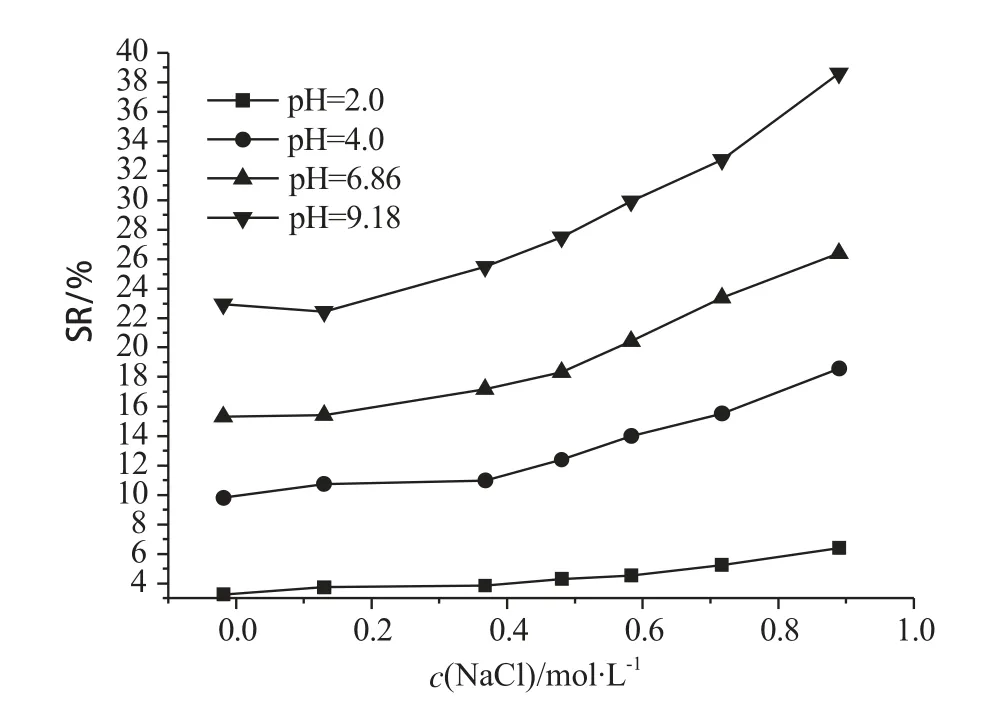
图5 P(NIPAM-co-MAA)水凝胶在20℃下的pH敏感性Fig. 5 pH sensitivity of the P(NIPAM-co-MAA)hydrogels in buffer solutions at 20℃
3 结论
在不同浓度的氯化钠水溶液中,成功制备了P(NIPAM-co-MAA)水凝胶,氯化钠溶液浓度对于凝胶内部结构有着明显影响。当反应介质中c(NaCl)≤0.3mol·L-1时,凝胶内部结构为细密的蜂窝状小孔,凝胶表现为无色透明状;当反应介质的浓度大于0.3mol·L-1时,凝胶内部发生盐析,高分子链发生蜷曲,凝胶表现为白色不透明状。随着氯化钠浓度的增大,孔状结构逐渐明显且相互贯通。这种相互贯通的孔状结构的形成,使得凝胶具有较快的响应速率。
[1] 毕曼,郝红,李涛,等.智能水凝胶研究最新进展[J].离子交换与吸附,2008,24(2):188-192.
[2] Sehmaljoharm D. Thermo-and-pH-responsive polymers in drug deliery[J]. Advanced Drug Delivews, 2006(58): 1655-1670.
[3] 凌有道,吕满庚.温度和pH双重敏感性水凝胶的制备及表征[J].精细化工,2008,25(6):545-549.
[4] Zhuo R X, Li W. Preparation and characterization of macroporous poly(N-isopropylacrylamide) hydrogels for the controlled release of proteins[J]. J Polym Sci: Polym Chem., 2003(41): 152-159.
[5] Park T G, Hoffman A S. Immobilization of Arthrobacter simplex cellsin thermally reversible hydrogel: Effect of gel hydrophobicity on steroid conversion[J]. Biotechnol Prog, 1991(7): 383-390.
[6] 褚良银,谢锐,巨晓洁,等.Smart Hydrogel Functional Materials[M].北京:化学工业出版社,2014:4-6.
[7] Zhang X Z, Yang Y Y, Chung T S. Effect of mixed solvents on characteristics of poly(N-isopropylacry-lamide) gels[J]. Langmuir, 2002, 18(7): 2538-2542.
[8] Cheng S X, Zhang J T, Zhuo R X. Macroporous poly(N-isopropylacrylamide) hydrogels with fast response rates and improved protein release properties[J]. Journal of Biomedical Materials Research A, 2003(67): 96-103.
[9] Caykara T, Bulut M, Demirei S. Preparation of macroporous poly(acrylamide) hydroges by radiation induced polymerization technique[J]. Nuelear Instruments and Methods in Physics Research-B, 2007(265): 366-369.
[10] Liu Q, Hedberg E L, Liu Z W, etal. PreParation of macroporous Poly(2-hydro-xyethylmethacrylate) hydrogels by enhanced phase separation[J]. Biomaterials, 2000(21): 2163-2169.
[11] Ling Y D, Lu M G. Thermo and pH dual responsive Poly(N-isopropylaerylamide-co-itaconic acid) hydrogels prepared in aqueous NaCI solutions and their characterization[J]. J Polym Res, 2009(16): 29-37.
Preparation and Characterization of Fast-responsive Porous Poly(NIPA-co-MAA) Hydrogels
XU Yang, ZHENG Si-liu, WANG Shuai, ZHOU Ying-mei
(School of Chemistry and Chemical Engineering, Xuzhou Institute of Technology, Xuzhou 221018, China)
The poly (N-isopropylacrylamide-co-acrylic acid) [P(NIPAM-co-AAc)] hydrogels were successfully prepared in aqueous NaCl solutions with different concentration. The characteristics of the resulting hydrogels was investigated with Fourier trans-form infrared spectroscopy (FT-IR), scanning electron microscopy(SEM) and measuring swelling ratio.The inf uence of internal microstructure on the characteristics of the resulting hydrogels and their formation mechanism were studied. The results showed that the pore network was informed when NaCl concentration raised to 0.3 mol/L.With the NaCl concentration increased in the polymerization medium, the pores in the hydrogels were informed more obviously. The hydrogels exhibited fast response rates.
N-isopropylacrylamide; methyl acrylic acid; microstructure; response rates
TQ 317.3
A
1670-9905(2015)05-0025-04
周颖梅(1975-),女,江苏徐州人,实验师,主要研究方向为功能高分子材料合成。E-mail:hgzym2012@163.com
2015-03-16
