IL-35在宫颈癌根治术后复发和转移中的预测价值
2015-01-08王镇南林琼燕李淑慧
王镇南 黄 颢 林琼燕 邹 琳 唐 志 李淑慧
(广东医学院附属医院肿瘤中心,广东湛江524001)
宫颈癌又称宫颈浸润癌,是最常见的妇科恶性肿瘤,严重威胁女性生命健康,发病率和死亡率呈逐年升高的趋势。全世界每年大约有新发病例50万,其中80%以上发生在发展中国家[1,2]。细胞因子在介导机体针对病原微生物的免疫反应、自身免疫耐受以及维持机体内环境平衡等过程中起了重要作用[3-5]。白介素35(interleukin-35,IL-35)是 IL-12 家族的新成员,被认为是一种具有潜在治疗前景的新型抗炎因子[6]。目前认为IL-35可能广泛参与了体内的免疫应答过程,不仅在细胞内感染及炎症过程中起着重要的调节作用,而且与自身免疫病和肿瘤等多种临床疾病的发生、发展密切相关,成为细胞因子研究的新热点,为感染性疾病、自身免疫性疾病和肿瘤的生物治疗提供了新思路[7]。然而,关于IL-35在宫颈癌手术前后血液标本中的表达及其与临床预后的关系目前国内外尚未见相关报道。本研究通过检测73例宫颈癌患者手术前后血清中IL-35的表达水平,探究其对患者临床预后的影响。
1 资料和方法
1.1 一般资料
73例宫颈癌患者手术前后外周血液标本取自2009年1月至2014年1月就诊于我院行宫颈癌手术切除的患者,所有标本均为经病理学检查确诊的宫颈癌,全部病例获取前均未行化疗和放疗,临床资料完整。73例宫颈癌患者中,年龄18~86岁,中位年龄55岁,55岁以下患者32例,55岁以上患者41例;Ia期20例,Ib期29例,IIa期24例;鳞癌41例,腺癌23例,腺鳞癌9例;淋巴结转移28例,无淋巴结转移 45例;人乳头瘤病毒(human papilloma virusr,HPV)(+)63例,HPV(-)10例;35例正常血液标本取自正常女性体检血液标本,体检证实未患肿瘤及其他疾病。所有患者均签署知情同意书。随访:全部73例患者出院后均随访,随访方式为电话随访,随访内容包括一般情况、临床症状及影像学检查。随访起点为手术日期,末次随访时间为2014年7月31日,至随访截止日,依然生存35例,死亡38例,无失访病例。
1.2 分组情况
患者入组标准如下:①组织学明确诊断的宫颈癌,包括鳞状细胞癌,腺癌,腺鳞癌;②FIGO分期为临床分期为 Ia-IIa期;③年龄18~86岁;④既往无并发症;⑤美国东部肿瘤协作组(ECOG)体能评分0~2分;⑥ 肝肾功能正常,血清转氨酶(AST,ALT)≤60 IU/mL,总胆红素≤1.5 mg/dL,肌酐≤1.5 mg/dL,尿素氮≤20 mg/dL;⑦ 骨髓功能正常:中性粒细胞≥1 500/mm且血小板≥100 000/mm。排除标准如下:① 既往放疗史或化疗史;② 既往肿瘤病史;③妊娠;④精神障碍。
1.3 ELISA分析血清IL-35的表达
使用不含热原和内毒素的试管收集血液后,1000×g离心10 min将血清和红细胞迅速小心地分离(操作过程中避免任何细胞刺激),将收集到的血清分成小部分 -70℃保存,避免反复冷冻。行ELISA检测时将所有样品及试剂解冻,充分混匀。不要使液体产生大量的泡沫,以免加样时加入大量的气泡,产生加样上的误差。加入稀释好后的标准品50μL于反应孔、加入待测样品50μL于反应孔内;立即加入50μL的生物素标记的抗体;盖上膜板,轻轻振荡混匀,37℃温育1 h。甩去孔内液体,每孔加满洗涤液,振荡30 s,甩去洗涤液,用吸水纸拍干。重复此操作3次;每孔加入80μL的亲和链酶素-HRP,轻轻振荡混匀,37℃温育30 min;甩去孔内液体,每孔加满洗涤液,振荡30 s,甩去洗涤液,用吸水纸拍干;每孔加入底物A、B各50μL,轻轻振荡混匀,37℃温育10 min。避免光照;取出酶标板,迅速加入50μL终止液,加入终止液后应立即测定结果;在450 nm波长处测定各孔的OD值。
1.4 统计方法
采用SPSS 13.0统计学软件进行数据分析。血液标本中IL-35 mRNA的表达差异采用One way ANOVA分析。IL-35的表达与各临床病理参数之间的关系使用Chi-Square检验;生存分析用Kaplan-Meier法。组间生存曲线差别用对数秩检验(logrank test);应用Cox比例风险模型分析影响宫颈癌预后的因素,以P<0.05为差异具有统计学意义。
2 结果
2.1 宫颈癌患者临床病理特征
73例宫颈癌患者年龄18~86岁,具体临床病理特征见表1。

表1 宫颈癌患者的临床病理特征(n=73)
2.2 IL-35在宫颈癌患者手术前后外周血液中的表达
通过ELISA分别检测宫颈癌患者手术前后外周血液标本及正常人外周血液标本中IL-35的差异表达,与正常对照组比较,IL-35在手术前后患者血清中的表达升高(P<0.001)。术后患者血清中的表达(213.79±23.89)pg/mL 较术前(398.71±31.09)pg/mL明显降低,50例术后复发和转移患者血清IL-35的表达(374.25±27.74)pg/mL较23例稳定期患者(183.65±34.51)pg/mL 明显增高(P <0.001),见图 1。
2.3 宫颈癌患者生存分析
采用Kaplan-Meier法估计患者生存时间,结果发现高表达IL-35的患者的中位无病生存时间(DFS)为9.115月,较低表达者17.476月明显缩短,差异具有统计学意义(χ2=36.24,P <0.001)。高表达IL-35的患者的总生存时间(OS)为18.031,低表达者为34.254月,差异具有统计学意义(χ2=35.7,P <0.001),见图2。
本研究同时分析IL-35的表达与患者年龄、疾病分期、组织来源、生存时间、复发及转移的关系,结果发现,IL-35的表达与患者的年龄及组织来源无相关性,差异无统计学意义(均P>0.05);与疾病分期、是否合并HPV感染、是否手术及术后的复发和转移密切相关,差异具有统计学意义(均P<0.05),见表2。
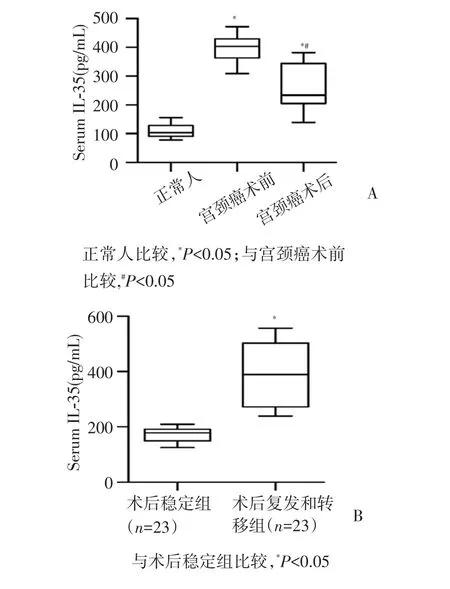
图1 不同组别患者血清IL-35的表达

图2 IL-35的表达与宫颈癌患者无进展生存时间(DFS)及总生存时间(OS)的关系

表2 宫颈癌患者血液标本中IL-35的表达与临床参数的关系
Cox回归分析患者的IL-35的表达可作为独立的预后因子,如表3所示,IL-35高表达的相对危险度为7.083,95%相对危险度的可信区间为(2.366-21.200),差异具有统计学意义(W=12.248,P=0.000),高表达 IL35的患者的总生存时间(HR,0.861;95%CI,0.788 -0.941;P=0.001)和无病生存时间(HR,0.774;95%CI,0.689 -0.870;P=0.000)较低表达者缩短。

表3 Cox回归分析IL-35的表达与宫颈癌预后的关系
3 讨论
IL-35是最近几年新发现的细胞因子,由调节性T细胞分泌,属于IL-12细胞因子家族,它的主要功能是抑制效应性T细胞的活性,对免疫系统和免疫反应有负向抑制作用[8,9]。调节性T细胞是体内存在的一类抑制免疫应答的T细胞亚群,分为天然调节性T细胞(即CD4+CD25+Treg)和诱导型调节性T细胞(iTreg),通过细胞-细胞互相接触、分泌细胞因子(IL-10、TGF-β1)等途径抑制B细胞、效应性T细胞的增殖、活化和免疫效应,在抑制自身免疫性疾病发展、移植耐受、肿瘤免疫逃逸等方面发挥重要作用。最近发现,白介素35(IL-35)的产生及功能与Treg密切关系,而且可能为Treg发挥最大免疫抑制功能所需的关键细胞因子。Nicholl等[10]研究发现IL-35通过增加细胞增殖、抑制细胞凋亡,促进前列腺癌细胞的生长;Pan等[11]研究发现树突状细胞减少调节性T细胞的扩增及调节性T细胞相关IL-35诱导的细胞杀伤作用增加细胞毒性药物治疗白血病的作用;循环IL-35在胰腺导管腺癌中高表达,尤其是可手术切除的患者中明显增高[12];血清IL-35作为评估结直肠癌疾病进展和预后的肿瘤标志物[13];Wang等[14]研究发现,IL-35 通过增加髓性细胞的聚集、肿瘤形成,抑制肿瘤免疫反应促进肿瘤细胞的生长;然而,Long等[15]的研究发现 IL-35通过调节基因相关的细胞周期和凋亡抑制癌症细胞的活性,抑制其生长,增加肿瘤细胞的凋亡敏感性,此项研究提示IL-35可能作为一个癌基因。本研究发现宫颈癌患者手术前后血液标本中IL-35的表达高于正常人,而术后患者IL-35的表达较术前明显降低,但仍高于正常人,差异具有统计学意义。进一步采用Kaplan-Meier法估计患者生存时间,结果发现高表达IL-35的患者的总生存时间(OS)及无病生存时间(DFS)较低表达者明显缩短,差异具有统计学意义。IL-35的表达与患者的年龄及组织来源无相关性,差异无统计学意义,与疾病分期、HPV感染、是否手术及术后是否复发和转移密切相关,差异具有统计学意义。Cox回归分析发现IL-35可作为独立的预后因子。以上结果提示IL-35在宫颈癌中也可能作为一种癌基因,影响宫颈癌的发生、发展及预后。为进一步研究宫颈癌的机制及治疗提供一定的理论基础和临床指导。
[1]Hu CJ,Zhou L,Cai Y.Dihydroartemisinin induces apoptosis of cervical cancer cells via upregulation of RKIP and downregulation of bcl-2[J].Cancer Biol Ther,2014,15(3):279-288.
[2]Marchetti C,Manci N,Pernice M,et al.Multiple Bulky Lymph Nodal Metastasis in Microinvasive Cervical Cancer:A Case Report and Literature Review[J].Case Rep Oncol,2010,3(2):176-181.
[3] Ghaemi A,Soleimanjahi H,Razeghi S,et al.Genistein induces a protective immunomodulatory effect in a mouse model of cervical cancer[J].Iran J Immunol,2012,9(2):119-127.
[4]Hafidh RR,Abdulamir AS,Bakar FA,et al.Novel molecular,cytotoxical,and immunological study on promising and selective anticancer activity of mung bean sprouts[J].BMCComplement Altern Med,2012,12:208.
[5]Roy S,Barik S,Banerjee S,et al.Neem leaf glycoprotein overcomes indoleamine 2,3 dioxygenase mediated tolerance in dendritic cells by attenuating hyperactive regulatory T cells in cervical cancer stage IIIB patients[J].Hum Immunol,2013,74(8):1015-1023.
[6]Shi M,Wei J,Dong J,et al.Function of interleukin17 and 35 in the blood of patients with hepatitis Brelated liver cirrhosis[J].Mol Med Rep,2015,11(1):121-126.
[7]Bettini M,Castellaw AH,Lennon GP,et al.Prevention of autoimmune diabetes by ectopic pancreatic beta-cell expression of interleukin-35[J].Diabetes,2012,61(6):1519-1526.
[8]Tedder TF,Leonard WJ.Leonard,Autoimmunity:Regulatory B cells-IL-35 and IL-21 regulate the regulators[J].Nat Rev Rheumatol,2014.10(8):452-453.
[9]Tedder TF,Leonard WJ.Autoimmunity:regulatory B cells-IL-35 and IL-21 regulate the regulators[J].Nat Rev Rheumatol,2014,10(8):452-453.
[10]Nicholl MB,Ledgewood CL,Chen X,et al.IL-35 promotes pancreas cancer growth through enhancement of proliferation and inhibition of apoptosis:Evidence for a role as an autocrine growth factor[J].Cytokine,2014,70(2):126-133.
[11]Pan Y,Tao Q,Wang H,et al.Dendritic cells decreased the concomitant expanded Tregs and Tregs related IL-35 in cytokine-induced killer cells and increased their cytotoxicity against leukemia cells[J].PLoS One,2014,9(4):e93591.
[12]Jin P,Ren H,Sun W,et al.Circulating IL-35 in pancreatic ductal adenocarcinoma patients.Hum Immunol[J],2014,75(1):29-33.
[13]Zeng JC,Zhang Z,Li TY,et al.Assessing the role of IL-35 in colorectal cancer progression and prognosis[J].Int J Clin Exp Pathol,2013,6(9):1806-1816.
[14]Wang Z,Liu JQ,Liu Z,et al.Tumor-derived IL-35 promotes tumor growth by enhancing myeloid cell accumulation and angiogenesis[J].JImmunol,2013,190(5):2415-2423.
[15]Long J,Zhang X,Wen M,et al.IL-35 over-expression increases apoptosis sensitivity and suppresses cell growth in human cancer cells[J].Biochem Biophys Res Commun,2013,430(1):364-369.
