槲皮素铋的合成及其生物活性研究
2015-01-08翟广玉渠文涛马海英樊卫华
翟广玉,渠文涛,马海英,韩 冰,樊卫华*
1郑州大学护理学院;2 郑州大学药学院,郑州 450052
铋是人和生物体非必需的微量元素。铋及其化合物在医药上广泛应用,临床上主要治疗各种微生物感染,包括梅毒、腹泻、胃炎和结肠炎等[1]。现在人们又发现铋及其化合物可以抑制癌细胞生长,具有抗癌活性,起辅助抗癌的作用[2]。
槲皮素(quercetin,图1)属于黄酮类,含有酚类结构的天然化合物,广泛存在于水果(苹果、草莓)、蔬菜(洋葱、蕃茄)、饮料(茶叶、咖啡、红酒)中[3],它显示出多方面的生物活性,是天然的抗氧化剂,特别是具有清除体内自由基的性能,保护细胞氧化造成的损伤,能够调整细胞内信号,促进细胞的存活[5],还具有抗炎[4]、抗病毒[5]、降血压[6]、预防心脑血管疾病[7]、防癌抗癌作用[8]。
槲皮素对金属离子具有强烈的螯合作用,可生成稳定的环状配合物。研究发现,槲皮素与不同金属离子形成配合物,其生物活性得到了不同程度的改善。Ferrer EG 等[9]合成了槲皮素钒配合物,研究发现槲皮素钒可以刺激I 型骨生长,对磷酸酯酶有抑制作用,可促进骨细胞的分裂、增殖,具有抗骨癌的作用。Zhou J 等[10]合成了槲皮素铜,研究表明槲皮素铜能够插入DNA 的碱基对中,从而影响DNA分子的构型,抑制了DNA 分子的进一步复制与转录,最终达到抗癌效果。Tabassum S 等[11]合成了槲皮素-CuⅡ-SnⅣ2配合物,可改变DNA 单链和双螺旋结构的空间结构,可以激活SOD 酶活性,清除活性氧,具有显著的抗癌活性。近年来,对槲皮素金属配合物的研究逐年增多,这对槲皮素的开发利用及寻找新药开辟了新的途径[12]。这提示经常食用一些含有槲皮素的黄酮类的食物,如苹果、洋葱、茶叶、银杏、荞麦等,可清除体内的自由基,使机体免受自由基的损伤,对降低人体内重金属离子的含量起着重要的作用。本文介绍了合成槲皮素铋的方法,并对其结构进行了表征,研究了清除自由基的能力。

图1 槲皮素的结构Fig.1 Chemical structure of quercetin
1 材料与方法
1.1 材料与仪器
槲皮素(自制),氯化铋(分析纯),其他试剂均为分析纯。
FTS-3000 型红外光谱仪(KBr 压片);德国耐驰(Netzsch)STA 409 PC/PG 差热分析仪;UV-240 型紫外-可见分光光度计(日本岛津公司);400 MHz 核磁共振仪(Bruker);RE-52AA 型旋转蒸发仪(上海亚荣生化仪器厂)。
1.2 槲皮素铋的制备
将文献[13]方法适当改进,在三颈烧瓶中,取1 mmol(302 mg)槲皮素,加入25 mL 甲醇,搅拌使完全溶解,加入甲醇钠调pH=8.5。加入预先溶于25 mL 甲醇中的1 mmol(315.34 mg)无水氯化铋溶液。在可加热的磁力搅拌器上加热回流6 h。用硅胶G板监控反应进程,待反应完成时停止回流。过滤,滤液在旋转蒸发仪上蒸干,得棕黄色固体,用甲醇冲洗三次,真空干燥器中干燥,得深棕黄色固体。
槲皮素铋为深棕黄色粉末,溶于甲醇、乙醇、DMSO,微溶于丙酮,乙酸乙酯,不溶于苯和甲苯。
1.3 清除自由基实验
溶液的配制:1 ×10-4mol/L 的DPPH 溶液的配制:精密称取10 mg DPPH,置于250 mL 容量瓶中,加入少量无水乙醇,待溶解后再用无水乙醇定容至刻度,混匀,避光,置于冰箱保存。供试液的配制:精密取各样品适量,以乙醇为溶剂,分别配制100、80、60、40、20 mg/L 的待测溶液。精确吸取不同浓度的样品溶液1 mL,分别与3 mL 1 ×10-4mol/L 的DPPH溶液混合,避光放置30 min,在517 nm 处测吸光度Ay。以相应溶剂代替样品作为空白对照,吸光度为As,相应样品溶液的吸光度为A0。DPPH 自由基清除活性按下式计算:

式中,Ay为1 mL 样品溶液与3 mL DPPH 溶液混匀后的吸光度值;As为1 mL 乙醇溶液与3 mL DPPH 溶液混匀后的吸光度值;A0为1 mL 样品溶液与3 mL 乙醇溶液混匀后的吸光度值;参考文献[13]计算自由基半数清除率。
2 结果与讨论
2.1 紫外光谱分析
槲皮素在258 nm 和360 nm 有两个吸收峰,分别属于n→π* (A 环)电子跃迁和π→π* (B 环)电子跃迁,分别对应两个生色团组成:258 nm 吸收带由苯甲酰生色团产生,为带Ⅱ;360 nm 吸收带由肉桂酰生色团产生,为带Ⅰ。
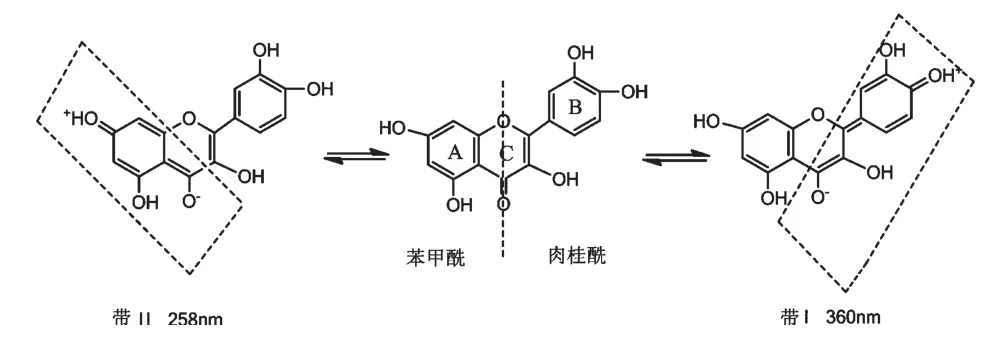
图2 槲皮素的结构及其紫外光谱特征Fig.2 Structure and UV-Visible absorption characteristics of quercetin
槲皮素铋的UV 吸收带Ⅱ由258 nm 红移至265 nm,红移7 nm;带Ⅰ由360 nm 红移至465 nm,红移95 nm(图2、3)。这是由于形成配合物后,共轭体系增大,能量降低,最大吸收向长波方向移动引起的。带Ⅰ红移远远大于带Ⅱ,这说明Bi3+是在带Ⅰ区域内与槲皮素配位形成配合物的。

图3 槲皮素和槲皮素铋的紫外光谱重叠图Fig.3 UV-Visble spectra of quercetin and quercetin-Bi complexes
2.2 红外光谱分析
槲皮素分子主要官能团红外吸收归属:υC=O1663.10 cm-1;苯环骨架振动频率υC=C1610.89 cm-1,1449.49 cm-1;δC3-OH1382.03 cm-1;υC-O酚1319.41 cm-1;υ-OH3408.74 cm-1。
槲皮素铋的红外光谱显示,羰基吸收峰υC=O1663.10 cm-1,红移至1648.48 cm-1,这是因为羰基形成了配合物引起的。槲皮素的特征吸收峰υ-OH3408.74 cm-1吸收,在槲皮素铋中是3420.34 cm-1几乎没有发生变化,这说明槲皮素的基本骨架没有发生变化。

图4 槲皮素(A)和槲皮素铋(B)的红外光谱Fig.4 IR spectrum of quercetin (A)and quercetin-Bi complexes (B)
槲皮素和槲皮素铋的红外图谱特征吸收峰比较结果显示:①槲皮素的υC=O1663.10 cm-1羰基振动频率移至1648.48 cm-1,向红移了14.62 cm-1,可见槲皮素的4-羰基参与了槲皮素铋配合物的形成[13]。②槲皮素铋配合物在613.52 cm-1出现了υM-O,说明有金属配位键生成。③苯环骨架振动频率υC=C1610.89 cm-1,和υC-O-C1262.46cm-1,分别移至1597.45 cm-1和1269.60 cm-1,说明在形成配合物后,苯环骨架的存在,只是向红移动了约几个—几十个波数[13]。
2.3 槲皮素铋的氢谱
1H NMR 谱是鉴定黄酮化合物的结构类型、确定取代基的位置和进行结构研究的有效方法。氢谱可以提供有关分子中不同种类氢原子的情况,如根据化学位移和偶合常数可以判断有关氢原子的化学环境,每种不同环境下氢原子的数目以及每个氢原子相邻的基团的结构等。槲皮素和槲皮素铋1HNMR 谱中每个氢原子的归属(400 MHz;DMSO-d6ppm)见表1。

表1 槲皮素和槲皮素铋1H-NMR 谱Table 1 1H-NMR data for quercetin and quercetin-Bi complexes (ppm)
由上述氢谱数据可知,槲皮素铋中的3'-OH 上的氢消失,而其它4 个羟基(7-OH,5-OH,3-OH,4'-OH)上的氢依然存在,这说明槲皮素的3'位羟基与铋离子结合。这与紫外光谱和红外光谱数据是一致的[14]。
2.4 热差分析
加热可引起物质的物理、化学变化,同时伴随放热和吸热的产生,以及质量的变化。通过热重分析,可以了解配合物的稳定性,及其结构特征。在静态空气气氛,升温速度为10 ℃/min,差热量程为100 μV,测定温度范围从室温到784 ℃。
对槲皮素铋的热分析显示出裂解分解过程[15]。配合物的DSC 曲线上呈现出吸热和放热峰与热重分析一致。

图5 示差热重分析图Fig.5 Thermogravimetric analysis of quercetin-Bi complexes
在151 ℃附近的放热峰对应于槲皮素铋的第一步分解,主要是失去结晶水,4 个H2O,对应质量损失为13.37%。在397 ℃附近的放热峰对应于残余有机物的氧化分解,对应质量损失为48.14%。在749 ℃附近,失去CHO,对应质量损失为4.90%。最后剩余的残渣是三氧化二铋。
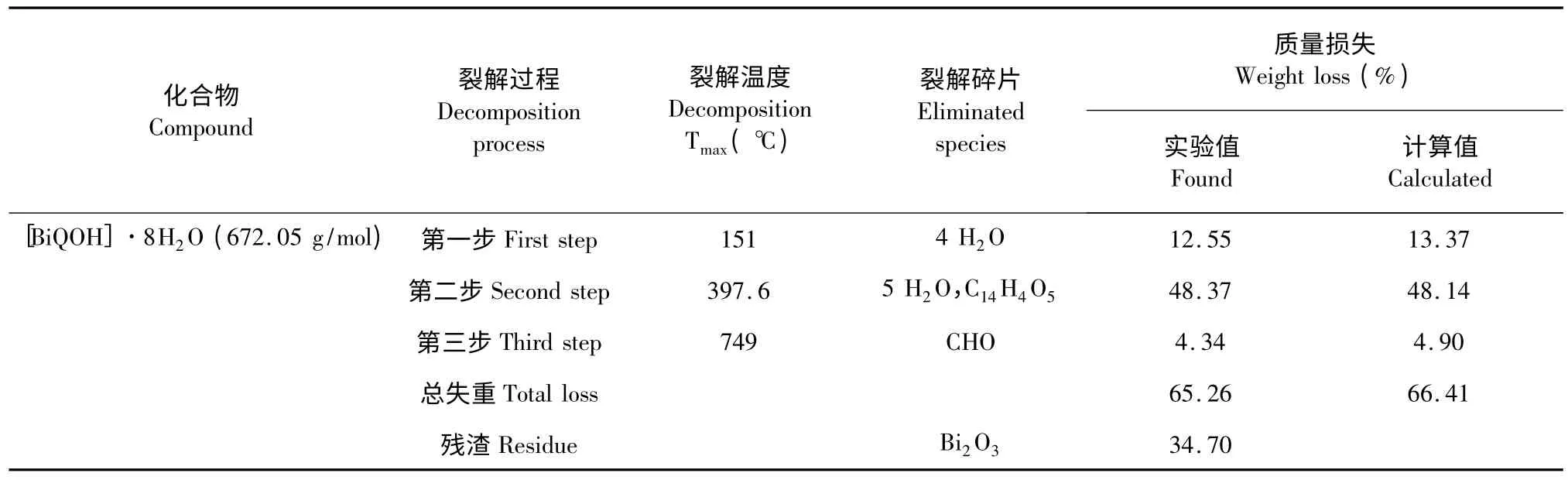
表1 槲皮素铋分解与失重的最大温度Table 1 The Tmax(℃)and weight loss values of the decomposition stages for the quercetin-Bi complexes
由上述槲皮素铋的热分解实验,根据残渣的重量,可以计算出氧化铋中铋的含量(实验值):

槲皮素铋中铋的含量(理论值):
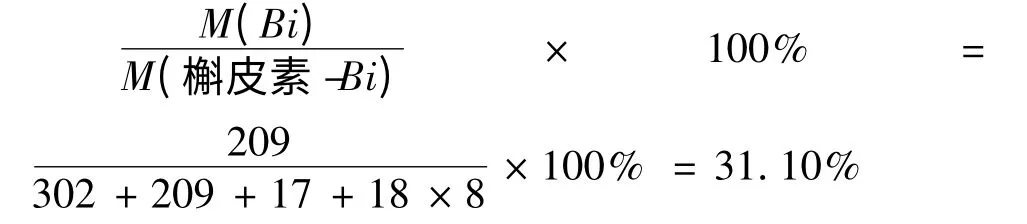
由上述计算结果可以看出,实验值与理论值误差很小。结合紫外光谱、红外光谱、氢谱和热分析图谱可以写出槲皮素铋配合物的结构为:

图6 槲皮素铋的结构Fig.6 Chemical structure of quercetin-Bi complexes
2.5 槲皮素铋清除DPPH 自由基的作用
DPPH 在有机溶剂中是一种稳定的自由基,其乙醇溶液在517 nm 处有最大吸收,当有自由基清除剂存在时,由于DPPH 自由基的单电子被配对,从而使得在517 nm 处的吸光度减小,因此该法常被用来评价样品的抗氧化能力[12]。

图7 槲皮素和槲皮素铋对DPPH 自由基的清除作用Fig.7 The scavenging effect of quercetin and quercetin-Bi complexes on on DPPH free radical
从图7 可见,槲皮素和槲皮素铋都随着浓度的增大,对DPPH 自由基的清除率也增大,但是很明显槲皮素与铋离子形成配合物后,其对DPPH 自由基的清除能力略有降低。根据实验结果,槲皮素铋与槲皮素的EC50分别是8.17 mg/L 和14.07 mg/L,进一步说明槲皮素在与铋配位后,其清除DPPH 自由基能力降低,这可能是形成配合物后,邻二酚结构的羟基与铋离子配位,使其接受质子的能力降低引起的。
3 结论
槲皮素与氯化铋在碱性条件下,可生成槲皮素铋配合物。通过紫外、红外、核磁、热分析等手段对槲皮素铋进行了结构表征。光谱数据阐明了配位的位点:槲皮素的3'位羟基与铋离子结合。通过DPPH 法测定了槲皮素铋清除自由基的能力,通过实验显示,槲皮素铋清除DPPH 自由基的能力弱于槲皮素。
1 Yang N(杨楠),Sun HZ(孙红哲).Application of arsenic,Antimony and Bismuth in Medicine.Prog Chem,2009,21:856-865.
2 Zhang H(张辉),Yu LP(喻莉萍),Peng GJ(彭国茳),et al.Optimization of preparation technology for binary complexes of rutin and bismuth microcapsules and its quality evaluation.Chin J Exp Tradit Med Form,2012,18(13):31-33.
3 Lee JH,Mitchell AE.Pharmacokinetics of quercetin absorption from apples and onions in healthy humans.J Agric Food Chem,2012,60:3874-3881.
4 Wang L,Wang B,Li H,et al.Quercetin,a flavonoid with anti-inflammatory activity,suppresses the development of abdominal aortic aneurysms in mice.Eur J Pharmacol,2012,690:133-141.
5 Ganesan S,Faris AN,Comstock AT,et al.Quercetin inhibits rhinovirus replication in vitro and in vivo.Antivir Res,2012,94:258-271.
6 Larson AJ,Symons JD,Jalili T.Quercetin:A treatment for hypertension?-A review of efficacy and mechanisms.Pharmaceuticals,2010,3:237-250.
7 Khoo NKH,White CR,Pozzo-Miller L.Dietary flavonoid quercetin stimulates vasorelaxation in aortic vessels.Free Radical Bio Med,2010,49:339-347.
8 Dajas F.Life or death:Neuroprotective and anticancer effects of quercetin.J Ethnopharmacol,2012,143:383-396.
9 Ferrer EG,Salinas MV,Correa MJ,et al.Synthesis,charac-terization,antitumoral and osteogenic activities of quercetin vanadyl(IV)complexes.J Biol Inorg Chem,2006,11:791-801.
10 Zhou J,Wang LF,Wang JY,et al.Synthesis,characterization,antioxidative and antitumor activities of solid quercetin rare earth(III)complexes.J Biol Inorg Chem,2001,83:41-48.
11 Tabassum S,Zaki M,Afzal M,et al.New modulated design and synthesis of quercetin-Cu(II)/Zn(II)-Sn2(IV)scaffold as anticancer agents:in vitro DNA binding profile,DNA cleavage pathway and Topo-I activity.Dalton Trans,2013,27:10029-10041.
12 Zhai GY(翟广玉),Qu WT(渠文涛),Ma HY(马海英),et al.Progress in the study of quercetin complexes.Chem Reag(化学试剂),2013,35:140-146.
13 Dehghan G,Khoshkam Z.Tin (II)-quercetin complexes:synthesis,spectral characterization and antioxidant activity.Food Chem,2012,131:422-426.
14 Ahmedova A,Paradowska K,Wawer I.1H,13C MAS NMR and DFT GIAO study of quercetin and its complexes with Al(III)in solid state.J Inorg Biochem,2012,110:27-35.
15 Ravichandran R,Rajendran M,Devapiriam D.Structural characterization and physicochemical properties of quercetin-Pb complexes.J Coordinat Chem,2014,67:1449-1462.
