兼具磁共振响应的碳量子点光致发光材料的构筑和性能
2015-01-06任先艳刘丽华
任先艳,刘丽华,李 瑜
(1.西安交通大学理学院,陕西西安 710049; 2.西南科技大学材料科学与工程学院,四川绵阳 621010; 3.西安交通大学第一附属医院,陕西西安 710061)
兼具磁共振响应的碳量子点光致发光材料的构筑和性能
任先艳1,2*,刘丽华3,李 瑜1
(1.西安交通大学理学院,陕西西安 710049; 2.西南科技大学材料科学与工程学院,四川绵阳 621010; 3.西安交通大学第一附属医院,陕西西安 710061)
碳量子点作为光功能组分和纳米载体用于构筑磁共振-荧光双模态分子探针的研究才刚刚开始。本文首次以兼作Gd3+源和碳源的钆喷酸单葡甲胺为前驱体,研究了热裂解温度、保温时间和加热速率对前驱体碳化程度、所得产物量子产率和Gd3+掺杂量的影响。结果显示,前驱体在经历合理的热裂解条件(热裂解温度不高于350℃)后,可简便地制得Gd3+螯合物掺杂的碳量子点。该碳量子点除了具有优异的发光能力外(量子产率~7.6%),还表现出磁共振响应(纵向弛豫率~6.5 mmol-1·L·s-1),可用作磁共振-荧光双模态分子影像探针。
碳量子点;Gd3+螯合物;荧光;磁共振;分子影像探针
1 引 言
自从克莱姆森大学的孙亚平等在2006年第一次应用激光刻蚀方法合成出一种新型的低维碳纳米材料——零维碳量子点之后[1],其作为生物相容的光致发光材料代替半导体量子点用于荧光分子影像探针的研究备受关注[2-3]。近年来,人们已开发出众多制备碳量子的碳源。例如:由最早的天然气燃烧灰、蜡烛灰、石墨[4],发展至石墨烯、碳纳米管等;由葡萄糖、柠檬酸、蔗糖类含碳有机物发展至有机聚合物(如酚醛树脂[5])和生物质(如鸡蛋清[6]、橘子汁[7]、蛋白质[8])等。然而,碳量子点纳米载体的作用却被忽视。应用碳量子点作为具备超顺磁性Gd3+的纳米平台构筑兼具磁共振响应和光致发光性能的阳性磁共振-荧光双模态分子影像探针的研究具有极高的现实价值和学术意义。
生物相容的磁共振-荧光双模态分子影像探针的问世,可以使癌症病灶得到早期、准确的诊断,治愈率提高。近年来,由于癌症发病比较隐匿,早期诊断比较困难,癌症的发病率及死亡率均有逐渐升高的趋势。而癌症治疗的成功在很大程度上依赖于癌症的早期诊断。可以在分子或细胞水平反映生物体生理、病理变化的分子影像技术,包括磁共振、光学和核医学分子影像技术则应运而生。然而,截至目前,每种分子影像技术都存在限制其应用的缺陷。例如,磁共振分子影像技术具有无创、分辨率高、能同时提供解剖与生理信息等优点,但其敏感度低,难以准确判断早期小的病灶;光学分子影像技术具有敏感度高、可进行连续实时监测的优点,但其穿透力有限(数毫米至数厘米)。因此,研发一种同时具备高敏感度和高分辨率的分子影像技术,即兼具磁共振响应的荧光分子影像技术(磁共振-荧光双模态分子影像技术),显得极为重要和迫切。这种双模态分子影像技术的成功开发和应用很大程度上依赖于双模态探针的开发和高性能化。
本文以兼作钆源和碳源的钆喷酸单葡胺(GdPM)为前驱体,采用由下而上的方法,通过将前驱体热裂解,简便地制备了牢固负载Gd3+的碳量子点纳米颗粒(记为Gd3+/CQDs)。在该纳米颗粒中,碳量子点既表现出作为Gd3+的纳米载体的作用,又具有荧光功能性。Gd3+/CQDs可以用作生物相容的磁共振-荧光双模态分子影像探针,可望实现恶性肿瘤的早期精确诊断,并有利于实现临床精确治疗。
2 实 验
2.1 Gd3+/CQDs的制备
将GdPM置于氧化铝坩埚中,在连续通入N2的高温电阻炉中加热并保温一定时间。自然冷却至室温后,得到棕褐色粉末状热解产物(Py-Gd-PM)。将Py-GdPM分散入去离子水中,并经过孔径为0.22μm的水性微孔滤膜抽滤,收集黄褐色的透明滤液。用NaOH水溶液将滤液的pH值调节至9左右后,将该滤液在8 000 r/min的转速下离心并收集上清液。上清液经过旋转蒸发仪浓缩后,在50℃的真空烘箱中干燥至恒重,即得到纯净的Gd3+/CQDs纳米粒子。通过调节热裂解温度和保温时间,优化Gd3+/CQDs的制备条件。
2.2 表征
采用热重分析(TGA)对比不同升温速率下Gd-PM的热行为,N2气氛保护,温度范围为300~450℃。采用X射线光电子能谱(XPS)确认Gd3+/CQDs纳米粒子中Gd3+的结合形式,X射线源为Al Kα (1 486.7 eV)。采用电感耦合等离子体发射光谱(ICP-OES)测定Gd3+/CQDs纳米粒子中Gd3+的含量。
2.3 Gd3+@CQDs的性能测试
采用GE公司的医用3.0TMR仪扫描Gd3+/ CQDs纳米粒子的T1W1加权图像、计算纵向弛豫效率r1,并与含等浓度Gd3+(0.5 mmol/L)的临床用马根维显磁共振探针进行比较。详细的测试方法见文献[9]。
采用FLsp920型荧光光谱仪扫描Gd3+/CQDs纳米粒子的光致激发光谱和发射光谱(不同激发波长下测试),并根据365 nm激发波长下的发射光谱计算量子产率(Q)。以硫酸奎宁的0.1 mol/ L的H2SO4溶液为参比物(365 nm波长下激发时,Q=0.55),通过公式(1)计算Gd3+/CQDs纳米粒子的量子产率,具体步骤见文献[10]。
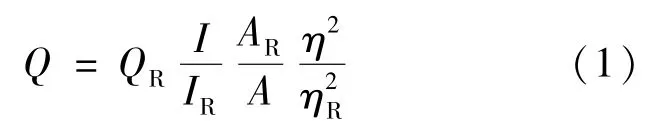
式中:Q为量子产率,I为光致发光强度,A为激发波长下经UV-Vis测得的碳量子点的吸光度,η为溶剂的反射系数,R代表参比物。
3 结果与讨论
3.1 GdPM的热裂解条件的选择
考虑到GdPM的结构特点,即其分子由热稳定性迥异的葡甲胺(Meg)和钆喷酸(GdPA)两种结构单元构成,并基于前期的工作基础,GdPM可以作为制备Gd3+掺杂的碳量子点的碳源和钆源[9]。在很宽的升温速率范围内,Meg结构单元皆表现出较GdPA结构单元中的Gd3+—N—O螯环结构优先分解的现象。比较不同升温速率下GdPM的DTG曲线不难看出,当升温速率为5℃· min-1时,Meg结构单元的热分解较快,此时它的起始分解温度最低,为190℃;当升温速率提高到25℃·min-1时,直至加热到220℃之后,Meg结构单元才开始分解(图1)。Meg结构单元的起始分解温度位于190~220℃之间。然而,同样的道理,升温速率的变化会在一定范围内影响GdPA结构单元的分解。升温速率在5~25℃·min-1时, GdPA结构单元的起始分解温度在350~380℃之间。可见,Meg和GdPA结构单元的起始分解温度之间保持有较大的差距。这点足以保证在一定范围内的热裂解条件下,前驱体GdPM碳化物中仍保留有Gd3+螯合物。根据GdPM的热重曲线,本文初步选取GdPM的热分解温度为250~400℃。

图1 不同升温速率下GdPM的DTG曲线Fig.1 DTG curves of GdPM heating at different rates
3.2 GdPM碳化程度的影响因素
GdPM的碳化是制备碳量子点的前提。碳化程度不仅决定碳量子点的结构、尺寸和性能,而且决定碳量子点中掺杂的Gd3+的含量。因此,热裂解条件(温度、升温速率、保温时间)的优选和控制,对于实现GdPM碳化程度的调控,进而实现性能可调、可控的碳量子点的制备至关重要。易溶于水的白色粉末状GdPM在管式炉中热裂解后会因为小分子(H2O、CO和CO2)的释放而发生体积膨胀和质量损失,且经历浅黄色、黄色、黄褐色等一系列由浅至深的颜色变化,最终变为可部分溶解于水的褐色粉末状,这一过程说明GdPM被碳化。
3.2.1 温度对碳化程度的影响
分别在250,300,330,350,365,380,400℃下对GdPM进行热裂解(升温速率10℃·min-1,保温2 h)。热裂解温度越高,则GdPM的碳化产物(Py-GdPM)的颜色就越深,含有的不可溶物就越多,且残余质量就越少(图2(a))。将不同温度下热裂解后GdPM的残余质量对热裂解温度作图,GdPM的残余质量随热裂解温度的变化曲线在350℃处出现转折,说明GdPM在350℃之上和之下分别表现出不同的热裂解过程。这种现象同TGA分析结果一致,说明在低于350℃时主要发生Meg结构单元的热裂解碳化,在高于350℃时才发生Gd3+螯环结构的热裂解。
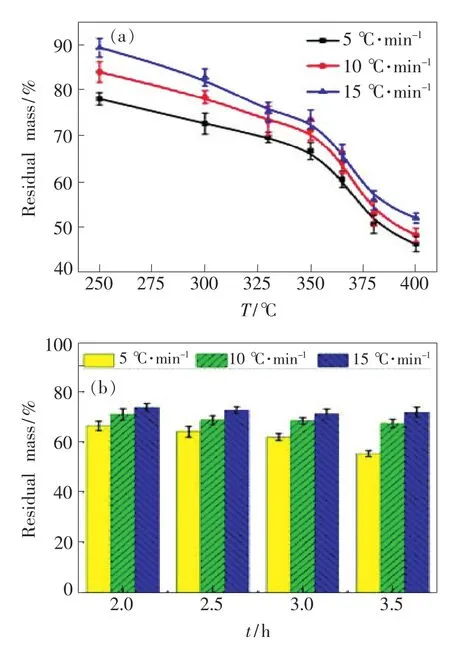
图2 GdPM热裂解后的残余质量。(a)在不同温度下保温2 h后;(b)在350℃下分别保温2,2.5,3,3.5 h后。升温速率分别为5,10,15℃·min-1。Fig.2 Residual mass of GdPMafter pyrolysis at different temperatures for2 h(a),and at350℃for2,2.5, 3,3.5 h with heating rate of 5,10,15℃·min-1(b),respectively.
3.2.2 升温速率和保温时间
除了高的热裂解温度会提高GdPM的碳化程度外,减慢升温速率亦会使GdPM的受热更充分、碳化程度增加。如图2(a)所示,当以5℃· min-1的速率将GdPM由室温加热至250~400℃中的某一温度并保温2 h后,GdPM的残余质量依次低于升温速率为10℃·min-1和15℃·min-1时的残余质量。尤其对于GdPM中的Meg结构单元而言,升温速率对其分解程度的影响更为显著。
延长保温时间对增加GdPM的碳化程度也有一定的积极作用,并且该作用在低升温速率时表现更突出。由不同升温速率下将GdPM加热至350℃并保温不同时间后GdPM的残余质量(图2(b))可以看出,GdPM的残余质量随保温时间的延长而减少。尤其是在慢速升温的情况下,减少幅度更为显著。例如,当以5℃·min-1的速率将GdPM加热至350℃时,保温2 h后的GdPM残余质量为66.5%;继续保温至3.5 h时,GdPM的残余质量已经减少至55.5%。
总而言之,就对于提高GdPM的碳化程度而言,高的裂解温度、长的保温时间和低的升温速率皆是有利的。其中,慢速升温甚至表现出高于延长保温时间所带来的效果。
3.3 碳化程度对碳量子点光致发光能力的影响
从250~400℃下热裂解得到的GdPM的碳化产物Py-GdPM中均可以提取碳量子点(CQDs),在一定范围内CQDs的光致发光能力(量子产率Q)可以随GdPM的碳化程度的增加而增强。根据公式(1)计算由不同热裂解条件下得到的Py-GdPM中提取出的碳量子点的量子产率,列于表1。由高碳化程度的Py-GdPM中提取出的CQDs的Q值亦较高。例如,以5℃·min-1的速度由室温升至380℃并保温2 h后制得的CQDs的Q值为12.4%,高于在较快的10℃·min-1和15℃·min-1升温速率下达到380℃并保温2 h后制得的CQDs的9.3%和6.6%,亦高于在较低温度下保温2 h后制得的CQDs的3.6%~11.2%。

表1 由不同热裂解条件下的Py-GdPM中提取的CQDs的量子产率Table 1 Quantum yield of CQDs collected from Py-GdPM prepared under different pyrolysis condition
延长保温时间对增加CQDs的Q值也有一定的效果。GdPM在350℃保温2 h后制得的CQDs 的Q值为8.84%,继续保温至3.5 h后制得的CQDs的Q值增加至10.3%。然而,碳化程度对Q值的影响并非线性的,碳化程度过高的Py-Gd-PM中提取的CQDs的Q值反而会降低,这是由碳量子点的发光机理所决定的[11]。
总之,通过改变热裂解条件实施的对GdPM碳化程度的调整,可以实现CQDs的光致发光性能,尤其是量子产率的可调。在获得较高碳化程度时,CQDs的量子产率甚至高于经过表面钝化后的碳量子点的平均水平。基于碳量子点的发光机理,即激子的辐射重组理论,对碳量子点表面进行钝化(例如聚乙二醇修饰)可以提高其量子产率[12-14]。据文献[15]报道,表面钝化后的碳量子点的量子产率可提高4%~15%。本方法在高热裂解温度下可将CQDs的量子产率调至12.5%。
3.4 碳化程度对碳量子点弛豫性能的影响
CQDs虽然可以在较宽的热裂解温度范围内获得,但是为了得到Gd3+掺杂的CQDs(Gd3+/ CQDs),GdPM的碳化程度不宜过高。表2为采用ICP-OES检测的不同条件下热裂解得到的CQDs中的Gd3+含量。高的热裂解温度、长的保温时间和低的加热速度对提高CQDs的量子产率是有利的,然而却降低了CQDs中的Gd3+含量。在不高于350℃的温度下热裂解得到的CQDs中的Gd3+含量随热裂解温度的升高而缓慢降低,其值与GdPM中的Gd3+含量(质量分数21.4%)相比减小不明显。这也进一步印证了上文的TGA结果和管式炉内恒温热处理后的热失重结果,即GdPM在不高于350℃的温度下恒温热裂解时,其中的Gd3+螯环结构基本不会分解,Gd3+含量不会发生显著变化。而碳化程度过高的Py-GdPM中提取的CQDs中的Gd3+含量急剧下降;热裂解温度至400℃时,Gd3+含量仅为0.4%~2.3%。

表2 由不同热裂解条件下的Py-GdPM中提取的CQDs中的Gd3+含量Table 2 Gd3+contents in CQDs collected from Py-GdPM prepared under different pyrolysis condition
因此,只有在适当范围内提高的热裂解温度,才能既有利于提高CQDs的量子产率,又不显著影响Gd3+掺杂量,且保证Gd3+以螯合物形式掺杂。众所周知,Gd3+被螯合后可以降低游离Gd3+的毒性,而低毒性是成功应用于临床的首要条件。通过Gd4d和Gd3d的高分辨率谱图可以清晰地发现,适当提高热裂解温度至350℃时,制得的CQDs中Gd4d和Gd3d的结合能与300℃时Gd-PM中的一致,分别为 142.4 eV和 1 187.0 eV[16];而当热裂解温度为 400℃时,CQDs中Gd3+的结合能明显降低,谱带强度大幅减弱(图3)。因此,可以确定适当调节热裂解温度至不高于350℃时,GdPM中的螯环结构尚未分解,Gd3+仍以螯合物的形式掺杂于CQDs中。
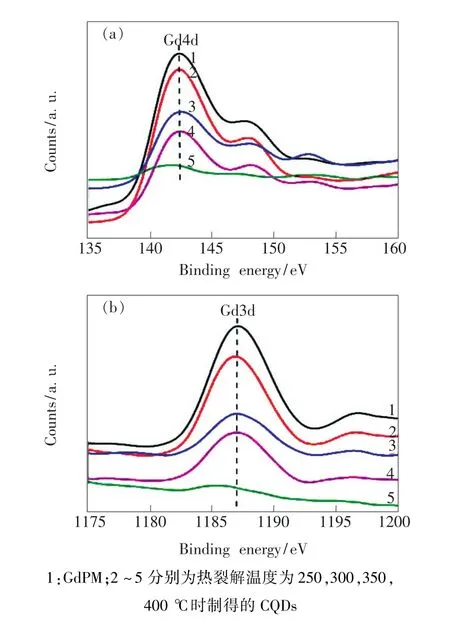
图3 Gd4d和Gd3d的高分辨谱图Fig.3 High-resolution XPS spectra of Gd4d and Gd3d
Gd3+/CQDs的弛豫性能与其中含有的Gd3+的掺杂量正相关。热裂解温度在250~350℃之间时,降低热裂解温度可以保持Gd3+/CQDs中较高的Gd3+含量,进而使Gd3+/CQDs的阳性对比亮度增加,其周围水质子的纵向弛豫率r1增大。如图4(a)所示,当热裂解温度为250℃时,Gd3+/CQDs的T1W1冠状和轴状扫描图的亮度明显最大,说明其可以表现出最大的MRI对比强度。随着热裂解温度的升高,制得的 Gd3+/CQDs的T1W1图像亮度依次减弱。通过反转恢复序列测试热裂解温度分别为250,300,350℃时制得的Gd3+/CQDs周围水质子的纵向弛豫时间T1(图4(b)),并计算r1。热裂解温度为300℃时,Gd3+/ CQDs周围水质子的r1值约为6.1 mmol-1·L· s-1;升高热裂解温度至350℃时,其r1值降低为5.5 mmol-1·L·s-1;而降低热裂解温度至250℃时,其r1值增加至6.5 mmol-1·L·s-1。该结果进一步说明,热裂解温度过高会影响制备高MRI对比强度的Gd3+/CQDs。然而,在250~350℃温度范围内制得的Gd3+/CQDs的r1值均高于含等度Gd3+的临床用马根维显磁共振造影剂的r1值(4.7 mmol-1·L·s-1),表现出优异的弛豫性能。

图4 (a)T1W1加权图像;(b)纵向弛豫时间(Ⅰ~Ⅲ:热裂解温度分别为250,300,350℃下制得的Gd3+/CQDs;Ⅳ:马根维显;Ⅴ:前驱体GdPM;Ⅵ: H2O,[Gd3+=0.5 mmol/L])。Fig.4 (a)T1-weighted MR images.(b)Longitudinal relaxation time.(Ⅰ-Ⅲ:Gd3+/CQDs prepared at250,300, 350℃,respectively;Ⅳ:Magnevist;Ⅴ:Precusor GdPM;Ⅵ:H2O,[Gd3+=0.5 mmol/L]).
4 结 论
选用钆喷酸单葡甲胺为前驱体,基于其可同时提供钆源和碳源的优势,提出了一种一步法制备兼有弛豫性能的碳量子点发光材料的方法。通过调节热裂解温度和保温时间,调整前驱体的碳化程度,研究了碳化程度对该发光材料(Gd3+/ CQDs)的发光能力和弛豫性能的影响,并优选出最佳制备温度为250~350℃。在该温度范围内,前驱体碳化程度的增加仅微弱地影响 Gd3+/ CQDs中的Gd3+掺杂量,同时可显著提高Gd3+/ CQDs的发光能力。当升温速率为10℃·min-1、保温时间为2 h、热裂解温度为250~350℃时, Gd3+/CQDs的弛豫性能为2.6%~7.6%,纵向弛豫率为6.5~5.5 mmol-1·L·s-1。掌握前驱体碳化程度与Gd3+/CQDs性能的关系,可以指导合成高钆离子掺杂的具有高发光强度的碳量子点类发光材料,用作高性能的磁共振-荧光双模态分子影像探针。
[1]Sun Y P,Zhou B,Lin Y,et al.Quantum-sized carbon dots for bright and colorful photoluminescence[J].J.Am. Chem.Soc.,2006,128(24)∶7756-7757.
[2]Yang ST,Wang X,Wang H,et al.Carbon dots as nontoxic and high-performance fluorescence imaging agents[J].J. Phys.Chem.C,2009,113(42)∶18110-18114.
[3]Zheng X T,Ananthanarayanan A,Luo K Q,et al.Glowing graphene quantum dots and carbon dots∶Properties,syntheses,and biological applications[J].Small,2014,11(14)∶1620-1636.
[4]Hu S L,Niu K Y,Sun J,etal.One-step synthesis of fluorescent carbon nanoparticles by laser irradiation[J].J.Mater. Chem.,2009,19(4)∶484-488.
[5]Liu R,Wu D,Liu S,et al.An aqueous route tomulticolor photoluminescent carbon dots using silica spheres as carriers [J].Angew.Chem.,2009,121(25)∶4668-4671.
[6]Wang J,Wang C F,Chen S.Amphiphilic egg-derived carbon dots∶Rapid plasma fabrication,pyrolysis process,andmulticolor printing patterns[J].Angew.Chem.,2012,124(37)∶9431-9435.
[7]Sahu S,Behera B,Maiti T K,et al.Simple one-step synthesis of highly luminescent carbon dots from orange juice∶Application as excellent bio-imaging agents[J].Chem.Commun.,2012,48(70)∶8835-8837.
[8]Sun Y P,Wang J,Sahu S,et al.Versatility with carbon dots-from overcooked BBQ to brightly fluorescent agents andphotocatalysts[J].RSC Adv.,2013,3∶15604-15607.
[9]Ren X,Liu L,Li Y,et al.Facile preparation of gadolinium(ш)chelates functionalized carbon quantum dot-based contrast agent formagnetic resonance/fluorescencemultimodal imaging[J].J.Mater.Chem.B,2014,2(34)∶5541-5549.
[10]Kundu A,Layek R K,Kuila A,et al.Highly fluorescentgraphene oxide-poly(vinyl alcohol)hybrid∶An effectivematerial for specific Eu3+ion sensors[J].ACSAppl.Mater.Interf.,2012,4(10)∶5576-5582.
[11]Cao L,Meziani M J,Sahu S,et al.Photoluminescence properties of graphene versus other carbon nanomaterials[J]. Acc.Chem.Res.,2012,46(1)∶171-180.
[12]Peng H,Travassejdic J.Simple aqueous solution route to luminescent carbogenic dots from carbohydrates[J].Chem. Mater.,2009,21(23)∶5563-5565.
[13]Yang Y,Cui J,Zheng M,etal.One-step synthesis of amino-functionalized fluorescent carbon nanoparticles by hydrothermal carbonization of chitosan[J].Chem.Commun.,2012,48(3)∶380-382.
[14]Cao L,Wang X,MezianiM J,etal.Carbon dots formultiphoton bioimaging[J].J.Am.Chem.Soc.,2007,129(37)∶11318-11319.
[15]LiQ,Ohulchanskyy T Y,Liu R,et al.Photoluminescent carbon dots as biocompatible nanoprobes for targeting cancer cells in vitro[J].J.Phys.Chem.C,2010,114(28)∶12062-12068.
[16]Bourlinos A B,Bakandritsos A,Kouloumpis A,et al.Gd(ш)-doped carbon dots as a dual fluorescent-MRIprobe[J]. J.Mater.Chem.,2012,22(44)∶23327-23330.

任先艳(1982-),女,陕西西安人,讲师,博士研究生,2009年于西南科技大学获得硕士学位,主要从事碳纳米材料的功能化及应用开发方面的研究。
E-mail:rxy2002com@163.com
Preparation and Properties of Carbon Quantum Dots-photolum inescence Materials with Magnetic Resonance Response
REN Xian-yan1,2*,LIU Li-hua3,LIYu1
(1.School of Science,Xi'an Jiaotong University,Xi'an 710049,China; 2.School ofMaterials Science and Engineering,Southwest University ofScience and Technology,Mianyang 621010,China; 3.First Affiliated Hospital of Xi'an Jiaotong University,Xi'an 710061,China)
*Corresponding Author,E-mail:rxy2002com@163.com
The study of carbon quantum dots used as either photoluminescence functional components or nano carriers for magnetic resonance-fluorescence multimodal molecular imaging probe is just beginning.In the paper,the gadopentetatemonomeglumine was used as a precursor which provides simultaneously carbon sources and Gd3+sources.The influences of pyrolysis temperature, holding time and heating rate on the carbonization degree of the precursor,the quantum yield and the Gd3+content of the products were studied.When the precursor was pyrolized under reasonable condition(the pyrolysis temperature was not higher than 350℃),Gd3+chelates dopped carbon quantum dots were facilely prepared.The carbon quantum dots not only possessing high luminous power(quantum yield~7.6%),but also showing good magnetic resonance response(longitudinal relaxation rate~6.5 mmol-1·L·s-1)can be used as a magnetic resonance/fluorescence multimodalmolecular imaging probe.
carbon quantum dots;Gd3+chelates;fluorescence;magnetic resonance;molecular imaging probe
O482.31
:A
10.3788/fgxb20153608.0861
1000-7032(2015)08-0861-07
2015-05-16;
:2015-07-11
国家自然科学基金(81171318)资助项目
